新型二硫杂环戊烯硫酮化合物的合成及其对谷氨酸诱导损伤HT22细胞的保护作用
2017-05-17李玉姚孙银星敖桂珍
李玉姚, 孙银星, 程 坚, 敖桂珍*
(1. 苏州大学 a. 药学院; b. 神经科学研究所,江苏 苏州 215123)
新型二硫杂环戊烯硫酮化合物的合成及其对谷氨酸诱导损伤HT22细胞的保护作用
李玉姚1a, 孙银星1a, 程 坚1b, 敖桂珍1a*
(1. 苏州大学 a. 药学院; b. 神经科学研究所,江苏 苏州 215123)
在保留ADT- OH的3H- 1,2- 二硫杂环戊烯- 3- 硫酮结构的基础上,用芳乙烯基替换4- 羟基苯环,设计并合成了6个二硫杂环戊烯硫酮化合物(L1~L6,其中L2, L3, L5和L6为新化合物),其结构经1H NMR,13C NMR和HR- MS(ESI)表征。采用MTT法研究了L1~L6对谷氨酸诱导损伤的海马神经元HT22细胞的影响。药理初筛结果表明:给药浓度为10~100 μmol·L-1时,L1, L2, L4和L6均能提高受损HT22细胞的存活率(P<0.01);给药浓度为1 μmol·L-1时,L3和L5均可提高损伤HT22细胞的存活率(P<0.01)。
5- 对羟基苯基- 3H- 1,2- 二硫杂环戊烯- 3- 硫酮; H2S供体; 二硫杂环戊烯硫酮化合物; 合成; 神经保护作用
1996年,Kimmura发现内源性H2S在大脑中扮演了神经调质的角色[1]。此后,诸多研究结果表明H2S对神经调节具有多方面的生物效应,如血管松弛[2]、心肌缺血损伤保护[3-4]及氧化应激细胞保护等[5]。新型H2S供体的研究已成为化学与神经学交叉学科的热点之一[6]。H2S供体释放H2S的机制多样,其对神经系统的影响也不同。选择合适的H2S供体对准确开展药理机制的研究具有重要意义。

Scheme 1
5- 对羟基苯基- 3H- 1,2- 二硫杂环戊烯- 3- 硫酮(ADT- OH)为一种重要的硫化氢缓释供体。本课题组前期研究发现,ADT- OH能够保护谷氨酸损伤的HT22海马神经元细胞[7];抑制脂多糖诱导的BV2小胶质细胞的炎症应答[8];ADT- OH衍生物ADT在小鼠脑中动脉堵塞模型上能减少脑梗死体积,保护血脑屏障[9]。在此基础上,本文在保留ADT- OH的3H- 1,2- 二硫杂环戊烯- 3- 硫酮结构的基础上,用芳乙烯基替换ADT- OH的4- 羟基苯环,设计并合成了6个二硫杂环戊烯硫酮化合物(L1~L6, Scheme 1),其中L2, L3, L5和L6为新化合物,其结构经1H NMR,13C NMR和HR- MS(ESI)表征。采用MTT法研究了L1~L6对谷氨酸诱导损伤的海马神经元HT22细胞的影响。
1 实验部分
1.1 仪器与试剂
XT- 5型显微熔点仪(温度未校正);ABI Varian UNTIY INOVA 400 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);ALT Micromass TOF- MS型质谱仪;Bio- Tek型酶标仪。
5- 硫代- 5H- 1,2- 二硫杂环戊二烯- 3- 甲醛(5)按文献[10]方法合成;RPMI- 1640培养基,MTT,Sigma公司;胰蛋白酶,吉诺生物医药技术有限公司;其余所用试剂均为分析纯。
1.2 合成
(1) 三苯基膦盐(7)的合成
将6 4 mmol和三苯基膦1.049 g(4 mmol)加至乙腈(50 mL)中,回流反应24~48 h。旋干得白色或淡黄色粉末状固体7。
(2) L1~L6的合成(以L1为例)
将7 325 mg(0.75 mmol)和氢化钠17 mg(0.7 mmol)加至无水THF(15 mL)中,氮气保护,搅拌下于0 ℃反应1 h。加入5 80 mg(0.5 mmol)的无水THF(15 mL)溶液,反应2 h。加水15 mL,用乙酸乙酯(3×30 mL)萃取,有机相减压蒸干,残余物经硅胶柱层析(洗脱剂:石油醚/乙酸乙酯=10/1,V/V)纯化得5- (2- 苯乙烯基)- 3H- 1,2- 二硫杂环戊二烯- 3- 硫酮(L1)。
用类似的方法合成L2~L6。
L1: 黄色固体,收率45%, m.p.117~120 ℃;1H NMRδ: 7.54(d,J=6.5 Hz, 2H, ArH), 7.45~7.40(m, 3H, ArH), 7.32(d,J=16.1 Hz, 1H, C=CH), 7.16(s, 1H, C=CH), 7.13(d,J=16.2 Hz, 1H, C=CH);13C NMRδ: 215.02, 169.78, 138.31, 137.61, 134.54, 130.45, 129.14, 127.76, 120.06; HR- MS(ESI)m/z: Calcd for C11H8S3{[M+H]+}236.986 6, found 236.986 9。
L2: 黄褐色固体,收率47%, m.p.207~210 ℃;1H NMRδ: 8.28(d,J=8.7 Hz, 2H, ArH), 7.70(d,J=8.8 Hz, 2H, ArH), 7.34(d,J=16.2 Hz, 1H, C=CH), 7.28(s, 1H, C=CH), 7.20(s, 1H, C=CH);13C NMRδ: 215.12, 167.58, 148.32, 140.59, 138.88, 134.92, 128.24, 124.42, 124.16; HR- MS(ESI)m/z: Calcd for C11H7NO2S3{[M+H]+}281.971 7, found 281.971 4。
L3: 黄色固体,收率51%, m.p.150~153 ℃;1H NMRδ: 7.48(d,J=8.5 Hz, 2H, ArH), 7.43(d,J=8.5 Hz, 2H, ArH), 7.30(d,J=16.1 Hz, 1H, C=CH), 7.15(s, 1H, C=CH), 7.10(d,J=16.1 Hz, 1H, C=CH), 1.34(s, 9H, CH3);13C NMRδ: 214.85, 170.22, 154.21, 138.29, 137.30, 131.80, 127.64, 126.12, 119.21, 34.96, 31.08; HR- MS(ESI)m/z: Calcd for C15H16S3{[M+H]+}293.049 2, found 293.048 6。
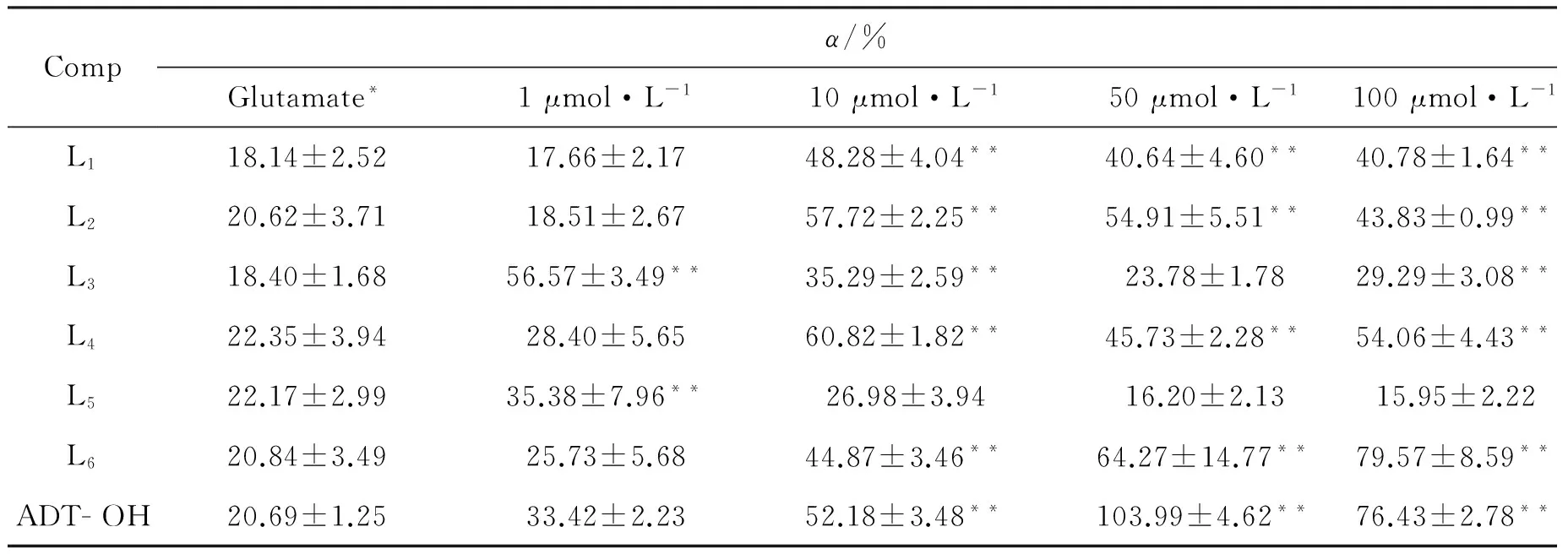
表1 L1~L6对谷氨酸诱导损伤的小鼠海马神经元HT22细胞的保护作用
*10 mmol·L-1;**P<0.01vsglutamate group。
L4: 黄褐色固体,收率46%, m.p.126~128 ℃;1H NMRδ: 7.44(d,J=8.1 Hz, 2H, ArH), 7.29(d,J=16.1 Hz, 1H, C=CH), 7.22(d,J=8.0 Hz, 2H, ArH), 7.15(s, 1H, C=CH), 7.09(d,J=16.1 Hz, 1H, C=CH), 2.39(s, 3H, CH3);13C NMRδ: 214.91, 170.20, 141.08, 138.43, 137.29, 131.85, 129.89, 127.78, 119.06, 29.69; HR- MS(ESI)m/z: Calcd for C12H10S3{[M+H]+}250.978 8, found 250.978 5。
L5: 黄色固体,收率42%, m.p.195~198 ℃;1H NMRδ: 8.10(d,J=8.2 Hz, 1H, ArH), 7.87(d,J=16.0 Hz, 1H, C=CH), 7.73~7.68(m, 2H, ArH), 7.61~7.56(m, 1H, ArH), 7.19(s, 1H, C=CH), 7.07(d,J=16.0 Hz, 1H, C=CH);13C NMRδ: 215.26, 168.02, 138.76, 133.78, 133.19, 130.69, 130.36, 128.84, 125.32, 124.65; HR- MS(ESI)m/z: Calcd for C11H7NO2S3{[M+H]+}281.971 7, found 281.972 1。
L6: 黄色固体,收率55%, m.p.178~181 ℃;1H NMRδ: 7.80(d,J=15.4 Hz, 1H, C=CH), 7.45(d,J=15.4 Hz, 1H, C=CH), 7.24(s, 1H, C=CH), 2.62(s, 3H, CH3), 2.55(s, 3H, CH3), 2.54(s, 3H, CH3);13C NMRδ: 215.17, 169.09, 152.65, 150.16, 148.65, 142.47, 138.44, 131.86, 124.61, 22.07, 21.74, 20.70; HR- MS(ESI)m/z: Calcd for C12H12N2S3{[M+H]+}281.024 1, found 281.024 2。
1.3 化合物对谷氨酸诱导的HT22细胞损伤的保护作用测定[7]
空白组只加培养基。谷氨酸组HT22细胞用10 mmol·L-1谷氨酸处理;样品测试组用10 mmol·L-1谷氨酸和终浓度分别为1, 10, 50和100 μmol·L-1的受试化合物处理。用酶联测试仪测定波长570 nm处每孔的吸收度(OD值),计算细胞存活率α(α=实验组平均OD值/空白组OD值×100%)。实验重复3次,采用SPSS进行统计。
2 结果与讨论
2.1 合成
合成L2时,最开始采用的是Knoevenagel缩合法,即2与对硝基苯甲醛在哌啶催化下,回流进行缩合反应。化合物经1H NMR鉴定为L2顺反异构体的混合物,M(反式) ∶M(顺式)=3 ∶1,反应产率也较低(<20%)。采用该方法合成其他目标化合物时,立体选择性也较差。最后改用Wittig缩合法,5与7反应所得产物均为反式,立体选择性较好。
2.2 化合物对谷氨酸诱导损伤的HT- 22细胞保护作用
表1为L1~L6对谷氨酸诱导损伤的小鼠海马神经元HT22细胞的保护作用。由表1可见,空白对照组的细胞存活率为100%。 glutamate组的HT- 22细胞单独经10 mmol·L-1谷氨酸处理后,存活率<25%,说明10 mmol·L-1谷氨酸已对HT- 22细胞造成了损伤。样品组的HT- 22细胞经10 mmol·L-1谷氨酸和不同浓度的目标化合物处理后,细胞存活率均能够明显提高,说明L1~L6可以保护谷氨酸诱导损伤的HT- 22神经细胞。其中,L1, L2, L4和L6的给药浓度为10~100 μmol·L-1时,均可提高受损HT22细胞的存活率(40.64%~79.57%)(P<0.01),具有较好的神经保护作用,但低于ADT- OH。 L5只在低浓度(1 μmol·L-1)时才表现出神经保护作用,细胞存活率为35.38%(P<0.01)。 L3在用药浓度为1 μmol·L-1时,HT22细胞存活率为56.57%,高于ADT- OH(33.42%),P<0.05,神经保护作用较强。
合成了6个二硫杂环戊烯硫酮化合物(L1~L6,其中L2, L3, L5和L6为新化合物)。采用MTT法研究了L1~L6对谷氨酸诱导损伤的海马神经元HT22细胞的影响。药理初筛结果表明:给药浓度为10~100 μmol·L-1时,L1, L2, L4和L6均能提高受损HT22细胞的存活率(P<0.01);给药浓度为1 μmol·L-1时,L3和L5均可提高损伤HT22细胞的存活率(P<0.01)。 L1~L6具有较好的神经保护作用,对神经保护作用的研究具有一定意义。
[1] Abe K, Kimura H. The possible role of hydrogen sulfide as an endogenous neuromodulator[J].Journal Of Neuroscience,1996,16(3):1066-1071.
[2] Kohn C, Dubrovska G, Huang Y,etal. Hydrogen sulfide:Potent regulator of vascular tone and stimulator of angiogenesis[J].International Journal of Biomedical Science,2012,8(2):81-86.
[3] Lee Predmore B, Joseph L D, Gojon G. Hydrogen sulfide in biochemistry and medicine[J].Antioxidants & Redox Signaling,2012,17(1):119-140.
[4] King A L, Lefer D J. Cytoprotective actions of hydrogen sulfide in ischaemia- reperfusion injury[J].Experimental Physiology,2011,96(9):840-846.
[5] Kimura Y, Goto Y I, Kimura H. Hydrogen sulfide increases glutathione production and suppresses oxidative stress in mitochondria[J].Antioxidants & Redox Signaling,2010,12(1):1-13.
[6] Martelli A, Testai L, Marino A,etal. Hydrogen sulphide:Biopharmacological roles in the cardiovascular system and pharmaceutical perspectives[J].Current Medicinal Chemistry,2012,19(20):3325-3336.
[7] Cheng J, Ao G Z, Jia J,etal. Differential mechanisms underlying neuroprotection of hydrogen sulfide donors against oxidative stress[J].Neurochemistry International,2013,62(8):1072-1078.
[8] Ao G Z, Jia J, Cheng J,etal. CaMKKβ- dependent activation of AMP- activated protein kinase is critical to suppressive effects of hydrogen sulfide on neuroinflammation[J].Antioxid Redox Signal,2014,21(12):1741-1758.
[9] Wang Y, Jia J, Ao G Z,etal. Hydrogen sulfide protects blood- brain barrier integrity following cerebral ischemia[J].Journal Neurochemistry,2014,129(5):827-838.
[10] Abazid M, Bertrand H O, Christen M O,etal. A general synthesis of new dithiolethione derivatives 5- (1- hydroxyimino alkyl)- 1,2- dithiole- 3- thiones and 5- acyl- 1,2- dithiole- 3- thiones[J].Phosphorus Sulfur And Silicon And The Related Elements,1994,88(1-4):195-206.
Synthesis of Novel 3H- 1,2- dithiole- 3- thione Compounds and Their Protective Effects on Glutamic Acid- induced Damage of HT22 Cells
LI Yu- yao1a, SUN Yin- xing1a, CHENG Jian1b, AO Gui- zhen1a*
(a. College of Pharmaceutical Science; b. Institute of Neuroscience, 1. Soochow University, Suzhou 215123, China)
The structure of ADT- OH was modified by replacing 4- OH phenyl with aryl vinyl, based on retaining its 3H- 1,2- dithiocyclopentene- 3- thione. Six 3H- 1,2- dithiole- 3- thione compounds(L1~L6) were designed and synthesized. Among them, L2, L3, L5and L6were novel compounds. The structures were characterized by1H NMR,13C NMR and HR- MS(ESI). Effects of L1~L6on glutamic acid- induced damage of HT22 cells were investigated by MTT method. The primary pharmacological results displayed that L1, L2, L4and L6significantly improved the survival rates of damaged HT22 cells at the concentration of 10~100 μmol·L-1(P<0.01), L3and L5increased the survival rates of damaged HT22 cells at the concentration of 1 μmol·L-1(P<0.01).
ADT- OH; hydrogen sulfide donor; 3H- 1,2- dithiole- 3- thione compound; synthesis; neuroprotection
2016- 11- 01;
2017- 01- 16
苏州市科技计划项目(N313202713)
李玉姚(1989-),男,汉族,山东潍坊人,硕士研究生,主要从事药物合成的研究。 E- mail: 18896587664@163.com
敖桂珍,副教授, E- mail: aoguizhen2007@sohu.com
O626.2
A
10.15952/j.cnki.cjsc.1005- 1511.2017.05.16278
