新型含卤噻唑类酰腙化合物的合成及其与小牛胸腺DNA的相互作用
2017-05-17刘向荣杨再文代爱萍赵顺省
刘 萌, 刘向荣, 王 鲁, 杨再文, 代爱萍, 赵顺省
(西安科技大学 化学与化工学院,陕西 西安 710054)
新型含卤噻唑类酰腙化合物的合成及其与小牛胸腺DNA的相互作用
刘 萌, 刘向荣*, 王 鲁, 杨再文, 代爱萍, 赵顺省
(西安科技大学 化学与化工学院,陕西 西安 710054)
以2- 氨基噻唑- 4- 甲酸乙酯和水合肼为原料,制得2- 氨基噻唑- 4- 甲酰肼(2); 2与卤代(F, Cl, Br)对苯甲醛反应,合成了3种新型的含卤噻唑类酰腙化合物[C11H9N4OSF(3a), C11H9N4OSCl(3b)和C11H9N4OSBr(3c)],其结构和性能经元素分析,XRD和TG- DTG表征。结果表明:3a和3c属于三斜晶系,Pī空间群;3b属于单斜晶系,P2(1)/c空间群。3a~3c的热稳定性均较好,最大热分解过程的表观活化能均大于100 kJ·mol-1。采用UV- Vis研究了3a~3c与小牛胸腺DNA(CT- DNA)的相互作用。结果表明:3a~3c与CT- DNA均以插入方式相互作用。
2- 氨基噻唑- 4- 甲酸乙酯; 酰腙化合物; 合成; 晶体结构; 相互作用
酰腙化合物含有酰腙基团,具有较强的生物活性和配位能力[1]。若再引入具有生物活性的杂原子,不仅可以产生生物活性叠加效果,还能显著提高配位能力。噻唑环是一种含硫、氮两种杂原子的杂环,具有良好的药理活性,热稳定性、耐酸、耐碱和耐氧化等化学稳定性。含噻唑环的酰腙化合物被广泛应用于抗菌、抗癌、抗病毒药物和除草剂的合成[2-12]。

Scheme 1
含卤素原子的酰腙具有较强的抑菌活性,如对氟苯甲醛水杨酰腙镍(Ⅱ)配合物具有多种生物活性[13]。5- 氯水杨醛水杨酰腙及其配合物对辣椒疫霉菌、烟草赤星菌和棉花枯萎菌均有抑制作用[14]。5- 溴水杨醛烟酰腙的镁配合物具有抗癌、抗炎、杀菌等活性[15]。
本文以2- 氨基噻唑- 4- 甲酸乙酯(1)和水合肼为原料,制得2- 氨基噻唑- 4- 甲酰肼(2); 2与卤代(F, Cl, Br)对苯甲醛反应,合成了3种新型的含卤噻唑类酰腙化合物[C11H9N4OSF(3a), C11H9N4OSCl(3b)和C11H9N4OSBr(3c), Scheme 1],其结构和性能经元素分析,XRD和TG- DTG表征。采用UV- Vis研究了3a~3c与小牛胸腺DNA(CT- DNA)的相互作用[16-19]。
1 实验部分
1.1 仪器与试剂
WRS- 2型熔点仪;TU- 1900型紫外- 可见分光光度计;PE- 2400- II型元素分析仪;Bruker Smart APEXⅡ CCD型X- 射线单晶衍射仪;Mettler- Toledo TG- DSC HT型热重分析仪(N2氛围,升温速率依次为5.00 ℃·min-1, 10.00 ℃·min-1和15.00 ℃·min-1)。
CT- DNA,生物试剂,Sigma公司;其余所用试剂均为分析纯。
1.2 合成
(1) 2的合成
在圆底烧瓶中加入1 1.722 0 g(10 mmol)和甲醇20.0 mL,搅拌使其溶解;加入80%水合肼10.0 mL,回流(65 ℃)反应3 h。冷却至室温,滤除不溶物,用保鲜膜罩住烧杯口并扎孔,静置1 d,出现白色针状晶体,抽滤,滤饼用甲醇重结晶后烘干得白色固体2,产率72.36%, m.p.194~196 ℃; Anal. calcd for C11H9N4OSF: C 30.37, H 3.82, N 35.42; found C 31.68, H 3.75, N 35.74。
(2) 3a~3c的合成(以3a为例)
在圆底烧瓶中加入2 0.079 1 g(0.5 mmol)和甲醇10.0 mL,搅拌使其溶解;缓慢加入4- 氟苯甲醛54.0 μL(0.5 mmol),加毕,回流(65 ℃)反应4 h。冷却至室温,滤除不溶物,用保鲜膜罩住烧杯口并扎孔,静置3 d,析出淡黄色针状晶体3a,产率71.23%, m.p.218~219 ℃; Anal. calcd for C11H9N4OSCl: C 49.99, H 3.43, N 21.20; found C 47.02, H 3.94, N 19.20。
用类似的方法合成3b和3c。
3b: 无色透明针状晶体,产率71.55%, m.p.237~238 ℃; Anal. calcd for C11H9N4OSCl: C 47.06, H 3.23, N 19.96; found C 47.19, H 3.26, N 19.67。
3c: 淡黄色块状晶体,产率68.43%, m.p.240~241 ℃; Anal. calcd for C11H9N4OSBr: C 40.63, H 2.79, N 17.42; found C 41.33, H 2.95, N 17.42。
1.3 晶体结构测试
选取尺寸分别为:0.37 mm×0.30 mm×0.23 mm(3a), 0.36 mm×0.30 mm×0.23 mm(3b)和0.37 mm×0.31 mm×0.21 mm(3c)的单晶样品,于296(2) K用经石墨单色器单色化的MoKα射线(λ=0.071 073 nm),以ω/2θ扫描方式,分别在1.49~25.10°(3a), 2.72~25.10°(3b)和1.56~25.10°(3c)测试晶体数据,用SADABS程序进行经验吸收校正,SHELXS程序[20]对晶体结构进行解析,对所有非氢原子进行全矩阵最小二乘法精修[21],所有氢原子用理论加氢法获得。
1.4 与CT- DNA的相互作用方式测定
量取新配制的0.01 mol·L-1Tris- HCl缓冲溶液3.0 mL(pH 7.9),加入参比比色皿中。量取等体积新配制的3溶液(c=1×10-4mol·L-1),加入样品比色皿中。在扫描波长250~500 nm,每隔5 min分别向参比比色皿和样品比色皿中加入100.0 mg·L-1CT- DNA溶液50.0 μL,连续加5次,测定UV- Vis谱图。
2 结果与讨论
2.1 晶体结构
图1~图3为3a~3c的分子结构图,图4~图6为3a~3c的空间堆积图,图7~图9为3a~3c的氢键作用图。由图1~图9可见,3种化合物具有相似的晶体结构。化合物分子间以氢键方式相互作用,交错排列堆积。
表1为3a~3c的晶体数据,表2和表3为3a~3c的主要键长、键角及氢键参数。计算发现,3a~3c中的苯环和噻唑环的二面角分别为6.7°, 2.94°和9.53°,表明两个环不在同一平面上,结构上均有一定扭曲[22]。3a分子中的S1—C11和N3—C11的键长分别为1.737(4) Å和1.299(4) Å,与理论值[23]接近(微小差异为环扭曲所致)。3a的噻唑环中的扭转角C11—S1—C10—C9和C11—N3—C9—C10分别为0.5(3)°和-0.4(5)°, C22—S2—C21—C20和C20—N7—C22—S2分别为-0.6(3)°和-0.8(4)°,说明C11—S1和C22—S2并不在相应的噻唑环平面内,而是与噻唑环平面存在一定夹角,这也说明该噻唑环的结构存在扭曲。3a中N1—C7的键长为1.271(4) Å,小于典型的N—C单键键长[23],所以该键为N=C双键。O1—C8的键长为1.230(4) Å,为典型的C=O双键键长,说明3a中存在酰腙基团,并以酮式结构存在。3a~3c的酰腙键C7—N1—N2—C8, C4—N3—N4—C5和C4—N3—N4—C5的扭转角分别为-179.9(4)°, 179.1(2)°和-177.0(7)°。 3a~3c的分子间是通过氢键交错排列堆积而成。3a中的弱氢键为N2—H2B┈O4i, N4—H4A┈N3ii和N4—H4B┈F2iii。 3a~3c的区分键F1—C1,Cl1—C9和Br1—C9的键长分别为1.366(4) Å, 1.734(3) Å和1.893(7) Å,与文献值[24]接近。

图1 3a的分子结构图

图2 3b的分子结构图

图3 3c的分子结构图Figure 3 Molecular structure of 3c

图4 3a的堆积图

图5 3b的堆积图Figure 5 Packingdiagram of 3b

图6 3c的堆积图Figure 6 Packingdiagram of 3c

图7 3a的氢键图Figure 7 View of the hydrogen bonds of 3a

图8 3b的氢键图Figure 8 View of the hydrogen bonds of 3b
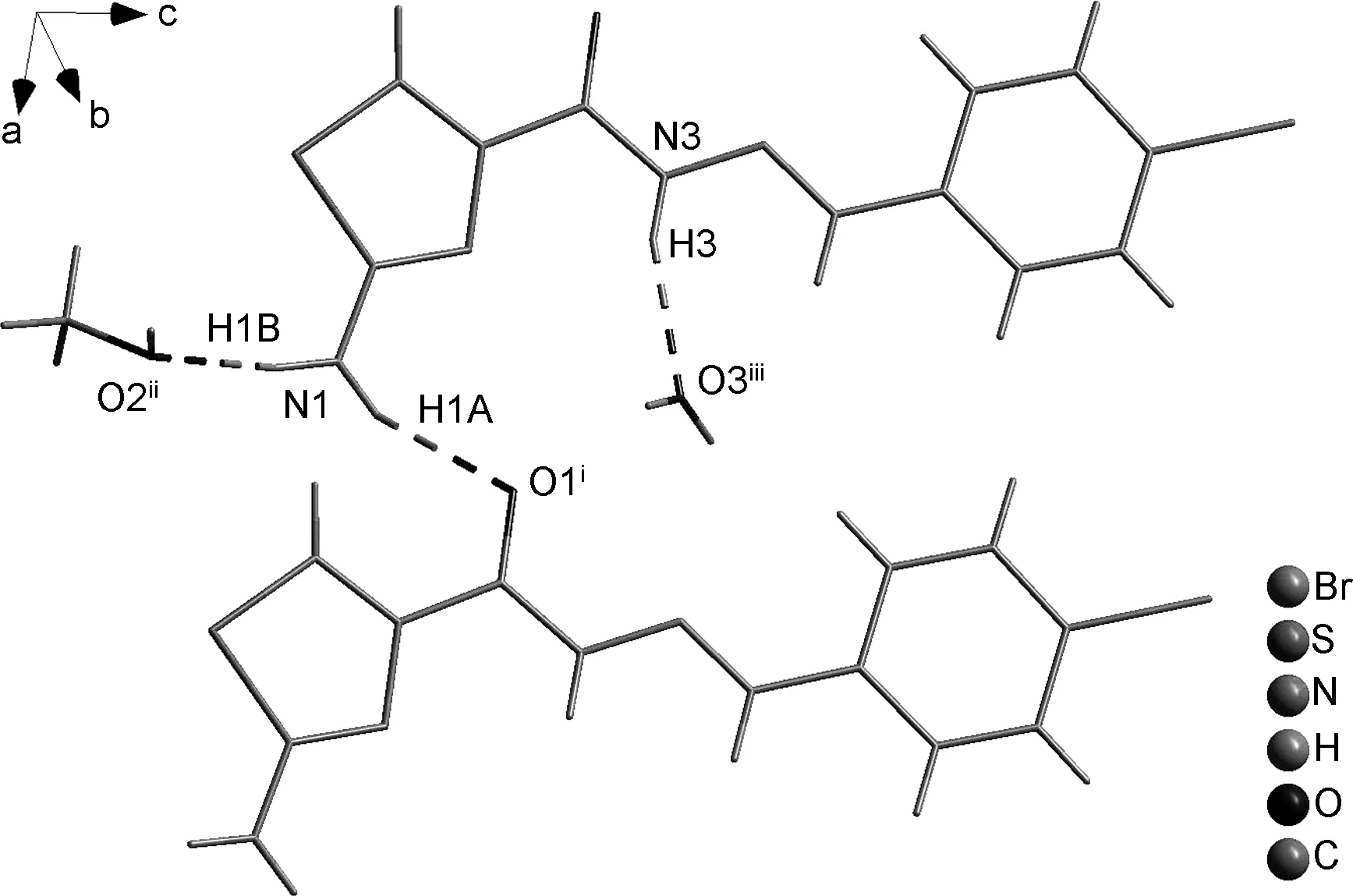
图9 3c的氢键图Figure 9 View of the hydrogen bonds of 3c

Temperature/℃
Temperature/℃

表1 3a~3c的晶体学参数

表2 3a~3c的主要键长(Å)和键角(°)
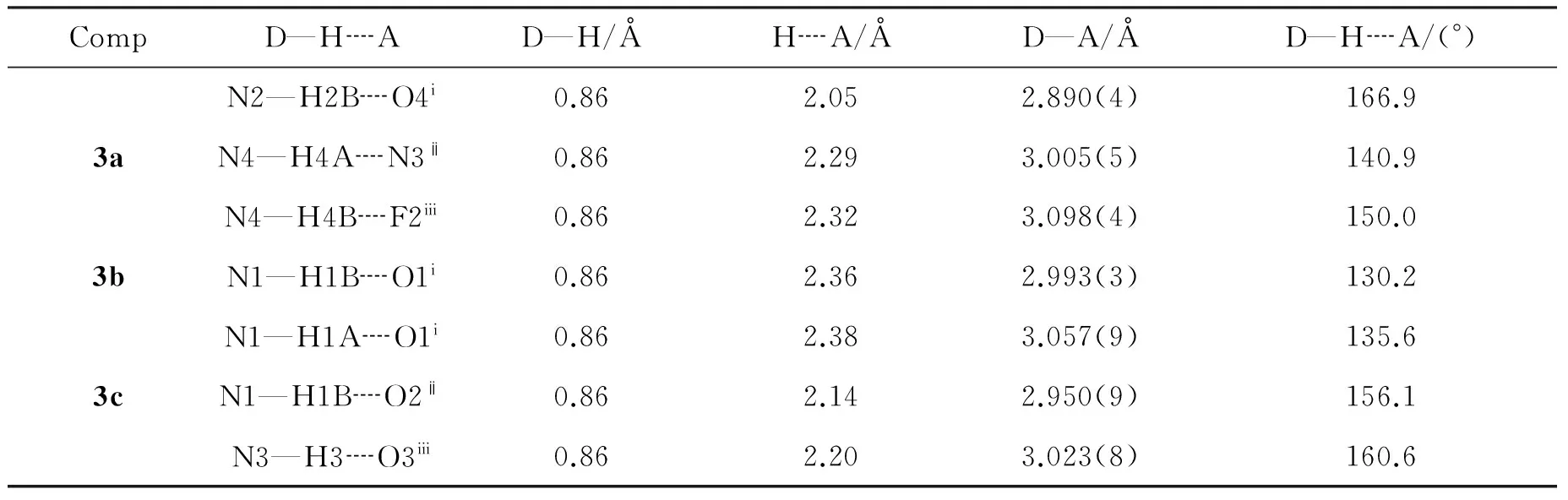
表3 3a~3c的氢键参数*
*3a:i-1+x, 1+y, 1+z;ii1-x, 1-y, 2-z;iii1-x, 1-y, 1-z;iv1-x, 1-y, 1-z; 3b:ix, 0.5-y, 0.5+z;iix, 1+y,z; 3c:i1-x, 1-y, -z;ii2-x, -y, -z;iii1+x,y,z;iv1+x,y,z。
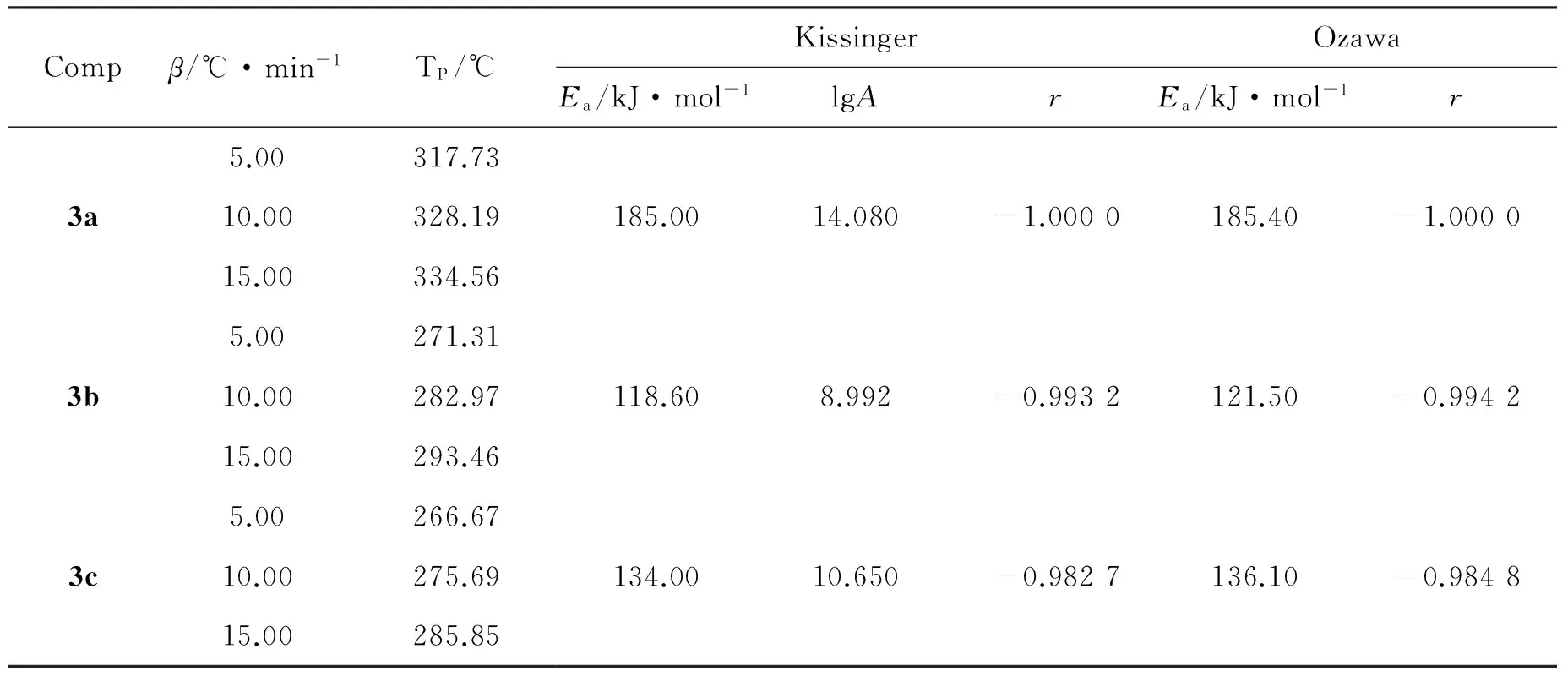
表4 3a~3c的热分解动力学参数*
*TP为化合物的分解峰温值,A为指前因子,Ea为表观活化能,R为气体摩尔常数,β为恒定升温速率。
Temperature/℃

Temperature/℃

Temperature/℃

Temperature/℃

λ/nm
2.2 3a~3c的热重分析
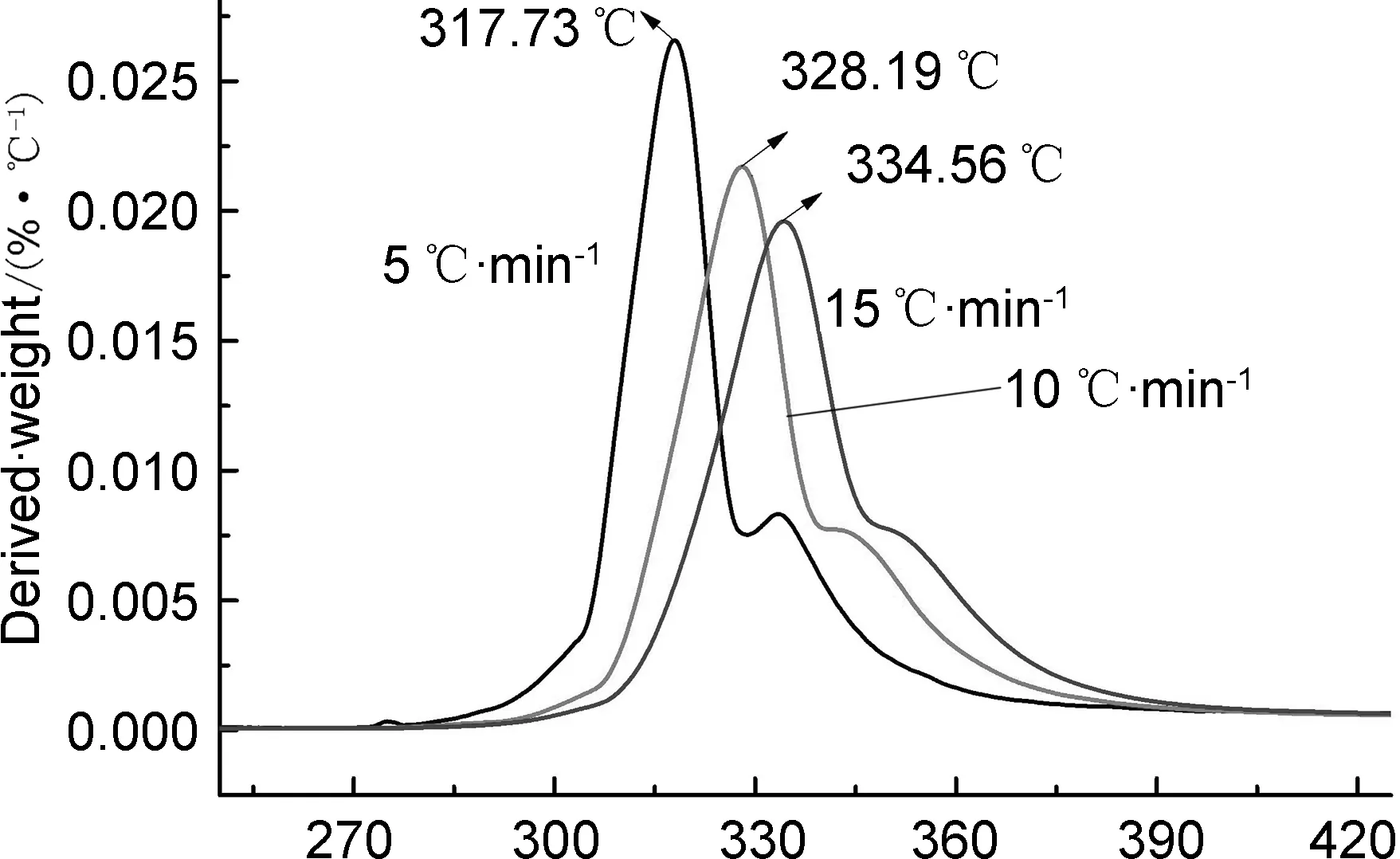
图10,图12和图14为3a~3c的TG- DTG曲线;图11,图13和图15为3a~3c的DTG曲线。采用Kissinger和Ozawa公式分别计算出3种化合物热分解过程的表观活化能(Ea)[25],结果见表4。
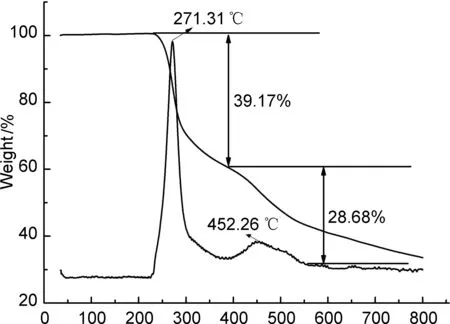
由图10,图12和图14可见,3a~3c的最大热分解吸收峰对应的温度分别为318.18 ℃, 271.67 ℃和266.70 ℃。 10.00 ℃·min-1和15.00 ℃·min-1的升温速率曲线与5.00 ℃·min-1图相似。从图中还可以看出,3a仅有一个热分解阶段,失重率为71.26%; 3b和3c均有两个热分解阶段。3b在第一阶段失重率为39.17%,在第二阶段失重率为28.68%。 3c在第一阶段失重率为31.62%,第二阶段失重率为34.47%。 3a~3c的Ea分别为185.00 kJ·mol-1,118.60 kJ·mol-1和134.00 kJ·mol-1。由此可知,3种化合物的热稳定性均较好。
2.3 与CT- DNA的相互作用
以3a为例,由3a~3c与CT- DNA相互作用的UV- Vis谱图(图16)可知,3a~3c的最大吸收峰分别位于308.62 nm, 313.85 nm和315.23 nm。未加入CT- DNA时,化合物的紫外吸收峰为噻唑环、芳香环和亚氨基的π┈π*跃迁及亚氨基的n┈π*跃迁[26]。加入CT- DNA后,随着浓度梯度的逐渐增加,化合物的吸光度相应减小,这是由于CT- DNA碱基对π电子轨道与化合物本身存在的空π*轨道发生耦合而填充部分电子,导致π┈π*跃迁几率减小所致。因此,化合物的最大吸收峰产生明显的减色效应和微弱的红移现象[27]。由此可知,化合物与CT- DNA发生了插入作用。为进一步了解化合物与CT- DNA的结合能力,可以计算化合物与CT- DNA的结合常数Kb[28]。由拟合图(图略)可知,3种化合物的Kb分别为7.970×106L·mol-1, 7.064×105L·mol-1和1.076 4×107L·mol-1。 3种化合物的Kb的数量级均≥105,说明化合物与CT- DNA的插入作用较强[29-32],大小依次为:3c>3a>3b。
合成了3种新型的含卤原子的噻唑类酰腙化合物[C11H9N4OSF(3a), C11H9N4OSCl(3b)和C11H9N4OSBr(3c)]。3a~3c的热稳定性均较好,最大热分解过程的表观活化能均>100 kJ·mol-1。采用UV- Vis研究了3a~3c与小牛胸腺DNA(CT- DNA)的相互作用。结果表明:3a~3c与CT- DNA均以插入方式相互作用。
[1] Agarwal A, Srivastava K, Puri S K,etal. Synthesis substituted indole derivatives as a new class of antimalarial agents[J].Bioorganic & Medicinal Chemistry Letters,2005,15(12):3133-3136.
[2] 陶艳,孙晓红,刘源发,等. 三唑类席夫碱衍生物的研究新进展[J].应用化工,2009,38(5):722-728.
[3] 胡卫兵,冯驸,刘红霞. 2,4,7- 三氨基席夫碱的合成及抗菌活性研究[J].化学试剂,2008,30(6):449-450.
[4] 王飞利,王伯明,聂万利,等. 钌(Ⅱ)异烟酰腙配合物的合成、表征及生物活性研究[J].化学通报,2013,76(9):838-842.
[5] Nouri H, Cadiou C, Henry A,etal. 1- (2- Methyl- 5H- chromeno[2,3-b]pyridin- 5- ylidene) hydrazone as fluorescent probes for selective zinc sensing in DMSO[J].Journal of Luminescence,2014,148:202-206.
[6] Krishnamoorthy P, Sathyadevi P, Cowley A H,etal. Syntheses,structure,and luminescence of two new 1D Cd(II) complexes[J].European Journal of Medicinal Chemistry,2011,46:3376-3387.
[7] 杨清翠,孙晓红,刘源发,等. 3- 甲基- 4- 氨基- 5- 乙氧羰基甲硫基三唑席夫碱的合成及生物活性[J].化学通报,2013,76(8):758-761.
[8] Williams D R. Metals,ligands and cancer[J].Chemical Reviews,1972,72(3):203-213.
[9] 杨欢春,杨天林,王丽娟. 2- 羟基- 1- 萘酚醛缩2- 氨基苯并噻唑铜配合物的合成及其与DNA作用的光谱研究[J].光谱实验室,2010,27(6):2124-2129.
[10] 章明,陈振锋,梁宏. 几种噻唑类席夫碱及其配合物的研究进展[J].广西师范大学学报(自然科学版),2002,20(3):42-46.
[11] 孙国锋,孙晓红,陈邦,等. 4- 氨基- 1,2,4- 三唑- 3- 酮席夫碱合成及毒性[J].西北大学学报,2002,32(6):647-650.
[12] Li L Z, Zhao C, Xu T,etal. Synthesis,crystal structure and nuclease activity of a Schiff base copper(II) complex[J].Journal of Inorganic Biochemistry,2005,99(5):1076-1082.
[13] 张淑萍,刘昭第,陈水生,等. 对氟苯甲醛水杨酰腙镍(Ⅱ)配合物的合成、表征及其晶体结构[J].无机化学学报,2007,06:1069-1071.
[14] Purser S, Moore P R, Swallow S,etal. Fluorine in medicinal chemistry[J].Chemical Society Reviews,2008,37:320-330.
[15] 孟铁宏,李春荣,刘仕云. 5- 溴水杨醛烟酰腙与镁金属配合物的合成与表征[J].化工生产与技术,2012,4(19):17-19.
[16] 夏金虹,刘峥,王松梅,等. 3,5- 二氯水杨醛氨基硫脲酰腙钴(Ⅱ)配合物的合成及其晶体结构[J].合成化学,2010,4(18):446-450.
[17] 杨颖,宋宇飞. 金属配合物键合DNA的研究进展[J].化学进展,2000,12(1):32-40.
[18] 侯林荣. 几种席夫碱和金属配合物的合成、表征、荧光活性及与CT- DNA相互作用的研究[D].银川:宁夏大学,2008.
[19] 张晓威,赵风林,李克安. 环丙沙星与牛血清蛋白相互作用的研究[J].高等学校化学学报,1999,20(7):231-238.
[20] Sheldrick G M. SHELXS- 97,Program for the solution of crystal structures[P].University of Göttingen,Germany,1997.
[21] Sheldrick G M. SHELXL- 97,Program for the refinement of crystal structure[P].University of Göttingen,Germany,1997.
[22] 杨滋渊,宋斌,徐守卫,等. 呋喃酰腙及其镍、锰配合物的合成与晶体结构及抑菌活性[J].无机化学学报,2014,30(3):585-590.
[23] 邵菊香,程新路,杨向东,等. C—H,C—N,C—O,N—N的键离解能和键长的计算[J].原子与分子物理学报,2006,01:80-84.
[24] 孙二平. 三原子卤代卡宾自由基电子态的理论研究[D].长春:吉林大学,2013.
[25] 胡荣祖,高胜利,赵凤起,等. 热分析动力学(第二版)[M].北京:科学出版社,2008.
[26] 高敏,杨天林,李慧,等. 3,5- 二碘水杨醛缩2,6- 二氨基吡啶席夫碱及其金属配合物的制备及与ct- DNA 的作用研究[J].化学通报,2011,74(6):562-568.
[27] Raman N, Sobha S. [Zn(phen)(O,N,O)(H2O)] and [Zn(phen)(O,N)(H2O)] with O,N,O is 2,6- dipicolinate and N,O is l- threoninate:Synthesis,characterization,and biomedical properties[J].Biological Inorganic Chemistry,2012,17:120-123.
[28] 朱莉,彭斌,凌友,等. 配合物[Co2(EGTB)Cl2]·(BF4)2·5H2O与DNA相互作用的研究[J].化学学报,2008,66(24):2704-2711.
[29] 杨莉宁,黑嘉慧,成昭,等. 联咪唑镍、镉配合物的合成、晶体结构及其与DNA相互作用[J].应用化学,2016,33(6):710-718.
[30] 简勇,李刚,杨鹏,等. 新型咔唑类衍生物的合成、光谱性质及其与ct- DNA作用的研究[J].有机化学,2014,34:809-816.
[31] 刘延成,王海璐,梁炜乾,等. 2- 羟基苯乙酮铜(Ⅱ)配合物与ct- DNA的键合作用研究[J].分析测试学报,2011,30(12):1400-1405.
[32] 史蕾,杨文聪,曾淑莹,等. 咔咯钴(Ⅲ)配合物与DNA的相互作用及抗肿瘤活性[J].高等学校化学学报,2016,37:1059-1068.
Synthesis of Novel Thiazole Acylhydrazone Compounds Containing Halogen Atoms and Their Interaction with CT- DNA
LIU Meng, LIU Xiang- rong*, WANG Lu, YANG Zai- wen, DAI Ai- ping, ZHAO Shun- sheng
(College of Chemistry and Chemical Engineering, Xi’an University of Science and Technology, Xi’an 710054, China)
2- Aminothiazole- 4- formylhydrazine(2)was obtained by the reaction of 2- aminothiazole- 4- methylformate with hydrazine hydrate.Three novel thiazole acylhydrazone compounds containing halogen atoms[C11H9N4OSF(3a), C11H9N4OSCl(3b) and C11H9N4OSBr(3c)] were synthesized by the reaction of 2 with halogenated benzaldehydes(F, Cl, Br). The structures and properties were characterized by elemental analysis, XRD and TG- DTG. The results showed that 3a and 3c belong to triclinic, space groupPī, and 3b belongs to monoclinic, space groupP2(1)/c. 3a~3c exhibited good thermal stabilities with apparent activation energies above 100 kJ·mol-1during the maximum thermal decomposition processes. The interaction of 3a~3c with CT- DNA were investigated by UV- Vis. The results indicated that 3a~3c interact with CT- DNA by the mode of insert.
2- aminothiazole- 4- methylformate; acyl hydrazone; synthesis; crystal structure; interaction
2016- 09- 12;
2017- 03- 10
国家自然科学基金资助项目(21073139, 21103135, 21301139)
刘萌(1992-),女,汉族,陕西富平人,硕士研究生,主要从事功能配合物的合成与性能研究。 E- mail: 958744395@qq.com
刘向荣,教授, E- mail: liuxiangrongxk@163.com
O626.2; O623.7
A
10.15952/j.cnki.cjsc.1005- 1511.2017.05.16231
