黑斑息肉病1例报告并文献复习
2017-05-15管丽芳张晓宇刘同亭
管丽芳,张晓宇,刘同亭
黑斑息肉病1例报告并文献复习
管丽芳,张晓宇,刘同亭*
黑斑息肉综合征;消化道息肉;家族遗传;致病基因;恶变;诊断;治疗
黑斑息肉病(Peutz-Jeghers syndrome,PJS,即黑斑息肉综合征)临床十分少见,是一种常染色体显性遗传病。临床具有胃肠道多发错构瘤性息肉、皮肤黏膜色素沉及阳性家族史三大特征。黑斑息肉病患者临床面临消化道恶性肿瘤的风险较高,还有胃肠道外其他系统恶性肿瘤的可能。文章对1例患儿进行了长达7年的随访,并通过回顾性分析和文献复习,总结治疗经验,为临床诊治黑斑息肉病提供参考。
1 病例资料
患者,女,15岁。患者2003年出现口唇黑斑,直径约0.1~0.2 cm,后逐渐增多,涉及口、唇及口腔两颊黏膜等多处,无其他不适。自2006年起,时有大便带血,用力排便后肛门处可见直径0.5 cm大小肿物,可回纳。2007年4月就诊原济南军区总医院,行电子结肠镜检查结肠黏膜未见异常,患者及其家属拒绝胃镜检查。自2008年开始反复出现腹痛伴呕吐,为阵发性绞痛,持续约2~3 min,呕吐后腹痛减轻,每于当地诊所输液(具体药物及剂量不详)治疗后缓解。2009年12月无明显诱因腹痛症状加重,呕吐频繁,就诊于该院完善检查后诊断为“Peutz-Jeghers综合征”,并行“剖腹探查,空肠息肉切除术,经胃镜胃息肉切除术,经小肠切口小肠镜检查,小肠息肉切除术,经肛门直肠息肉切除术”,病理示:“多发性错构瘤性息肉(Peutz-Jeghers型)”(图1),术后恢复良好。2014年7月28日行无痛胃镜检查示:胃多发息肉,并行内镜下治疗,术后恢复顺利。为复查入院。查体:口、唇及口腔两颊黏膜直径约0.1~0.2 cm(图2),余无阳性体征,胃镜检查示:胃体散在直径约0.3~0.5 cm黏膜样增生,部分呈绒毛样,内镜下用圈套器息肉,高频电凝除较大者3个胃内散在黏膜隆起(图3),胶囊内镜检查示:十二指肠、空肠、回肠散在大小不等黏膜隆起,表面光滑,部分呈分叶状(图4)。
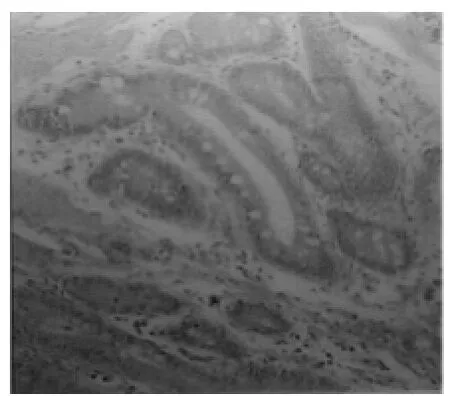
图1 黑斑息肉的病理类型

图2 口唇黑斑

图3 胃镜下胃息肉切除

图4 胶囊内镜下小肠隆起
2 讨论
PJS是一种十分罕见的常染色体显性遗传病,以黏膜黑斑和胃肠道多发息肉为主要临床表现。1921年荷兰学者Peutz[1]首次报道了一家三代7人同时发病的病例,随后Heghers等[2,3]学者进一步研究发现PJS患者多数有口唇、黏膜等处黑斑及胃肠道多发息肉等共同表现,此外患者胃肠外肿瘤发生的概率明显高于正常人。研究[4]发现仅1995年—2004年间,我国大陆地区共报道黑斑息肉综合征1133例,并呈逐年增长的趋势。
2.1 临床特征
2.1.1 黏膜黑斑黏膜色素沉着是黑斑息肉病最具特色的临床特征。黑色素斑以口唇黏膜最为常见。黑色素斑直径通常<5 mm,黑斑的大小、数目、颜色随年龄而变化,随着儿童的成长发育的过程,色素沉着颜色加深,成年后部分患者颜色逐渐变淡甚至消失,但颊黏膜色素斑可伴随终生。外形上色素斑一般不高出皮肤,无毛发生长,部分可融合成斑片状,多呈黑褐色。黏膜色素斑沉着的位置、范围大小及颜色的深浅与胃肠道息肉的多少、部位极其病情的严重程度之间并无必然的联系。
2.1.2 胃肠道息肉胃肠道多发息肉是PJS的重要特征。可分布于消化道的任何部位,其中小肠息肉最为多见,其次结肠和胃。息肉常多发,数目在数个至上百个不等,有蒂或无蒂,表面光滑,呈桑椹状、分叶状,呈分批、间歇性生长,多发引起的消化道出血,腹痛,肠梗阻,肠套叠等临床症状。
2.1.3 家族遗传性PJS是一种常染色体显性遗传性疾病,有家族聚集现象。近年来研究[4,5]发现PJS发病多与19号染色体短臂(19p13.3)的STK11/ LKB1(丝氨酸/苏氨酸激酶)基因相关。
2.2 黑斑息肉病的癌变息肉病理类型主要为错构瘤。有恶变的风险,恶性肿瘤的发生率可高达20%[6]。中国PJS患者的恶性肿瘤发生率,与国外的临床报道一致。更有研究[7]发现PJS患者发生恶性肿瘤的概率是正常人的9~18倍,不仅消化道恶性肿瘤的风险大幅度增加,非胃肠系统的其他部位发生肿瘤的风险也明显增加。研究[8]发现PJS多通过错构瘤-腺瘤-腺癌途经和denovo的恶变途经,引起癌变。而且息肉恶变的概率与息肉的大小与病程的长短呈正相关,但与息肉的数目多少之间并没有必然的联系。王振军等[9]也认为是PJS患者胃肠息肉有癌变倾向,其中结直肠癌的发生率最高,预后不良。因此对黑斑息肉病的患者进行及时的随访是十分必要的。做到早期干预,改善患者预后。
2.3 临床诊断PJS临床表现的三大特征:皮肤黏膜色素沉着斑,多发胃肠道息肉,家族遗传史,其息肉的病理类型常为错构瘤。2002年张卫等[10]提出PJS的诊断标准:(1)有3个或3个以上、经组织学证实为PJ息肉;(2)任何数目的PJ息肉合并有黑斑息肉病家族史;(3)典型的皮肤黏膜黑斑合并有黑斑息肉病家族史;(4)任何数目的PJ息肉合并典型的皮肤黏膜黑斑;(5)STK1胚系突变合并任何数目PJ息肉或典型的皮肤黏膜黑斑。
2.4 治疗目前黑斑息肉病仍无法根治。只能对症处理。对于皮肤黏膜色素沉着斑,影响外观,有美容要求者,激光治疗等。目前PJS的治疗以主切除胃肠道息肉及由胃肠道息肉导致的并发症的处理。由于胃肠道息肉有癌变的倾向,当前切除胃肠道息肉,防止恶性肿瘤的发生对于PJS的治疗至关重要。通过胃十二指肠镜、小肠镜、结肠镜等手段进行息肉的切除具有低风险、损伤小特点,成为临床息肉切除的首选治疗方法。
临床若出现肠套叠、出血等内镜下无法处理的并发症时,应考虑外科手术治疗。手术治疗的适应证是:(1)出现肠套叠或肠梗阻等并发症者;(2)引起消化道出血者;(3)内镜下无法摘除的较大的息肉,如小肠息肉在2 cm以上,大肠息肉息在1.5 cm以上;(4)小肠息肉广泛密集存在者;(5)疑有癌变者。
无论是内镜治疗还是外科手术治疗,并没有达到根治的目的。药物治疗仍有很大的机遇。国外Udd等[11]研究发现,并给予实验老鼠模型服用塞来昔布3.5~10个月后发现小鼠的息肉生长明显减缓,并指出黑斑息肉病患者息肉的生长与氧合酶2(COX-2)的作用密切相关,并提出可以使用COX-2抑制剂来控制PJS息肉的生长。在国内,顾国利等[12]也进行相关的临床研究,研究纳入71例PJS患者,应用塞来昔布治疗消化道息肉。研究发现6例坚持服用口服塞来昔布6个月,200 mg,2次/d的患者中2例患者息肉的数量及大小逐渐减少。虽然因为样本量小,无统计学意义,但仍能为塞来昔布治疗黑斑息肉的研究带来思考。Wei等[13]研究发现,雷帕霉素可通过特异性抑制哺乳动物中mTOR靶信号而达到有效抑制实验鼠的PJS息肉的作用。靶向药物治疗具有精准、有效的特点,但存在其费用昂贵、不良反应大的缺点。而近些年随着中医中药具有价格低廉、不良反应少等优势,中医治疗黑斑息肉病也得到越来越多人关注。研究发现[14]五倍子乌梅汤(五倍子10 g、乌梅15 g、黄连10 g、金银花10 g、紫草15 g、白芨15 g、薄荷10 g、丹参10 g、僵蚕10 g),具有清热解毒,祛腐化瘀等作用,煎汤保留灌肠可以起到抑制消化道息肉生长的作用。但关于此方面的研究数据不足,仍需要进一步研究,也为治疗黑斑息肉病提供了新思路、新方法。
3 小结
PJS以黏膜黑斑、胃肠道多发息肉及家族遗传性为主要临床表现。其息肉主要的病理类型是错构瘤,有恶变的风险。因此临床多以摘除息肉为治疗的关键,尚无根治的办法。研究发现黑斑息肉病较常人发生恶性肿瘤的概率更大,因此做好随访工作,早期发现肿瘤,改善预后极为重要。此外有研究表明雷帕霉素可以一直息肉的生长,这为药物治疗黑斑息肉病带来了曙光,但仍需要大量的研究。
[1]Girvin F,Glancy S,Dunlop M.Peutz-Jeghers syndrome:a case report and discussion of surveillance recommendations[J].Eur J Radiol,2007,62(3):81-84.
[2]Giardiello FM,Brensinger JD,Tersmette AC.Very high risk of cancer infamilial Peutz-Jeghers syndrome[J].Gastroenterology,2000,119(6):1447-1453.
[3]董科,李波,李本海,等.黑斑息肉综合征六例临床分析[J].中华胃肠外科杂志,2005,7(8):336-338.
[4]Hemminki A,MarKie D,Tomlinson I,et al.A serine/threonine kinase gene defective in Peutz-Jeghers syndrome[J].Nature,1998,391(2):184.
[5]Jenne DE,Reimann H,Nezu J,et al.Peutz-Jeghers syndrome is caused by mutations in a novel serine threonine kinase[J]. Nature Genetics,1998,18(1):38-43.
[6]戴益琛,谢军培,曾伟,等.中国大陆黑斑息肉综合征临床荟萃分析[J].临床内科杂志,2008(5):526-527.
[7]王辉,孟松,李超,等.黑斑息肉综合征的诊治分析[J].中国普通外科杂志,2015,24(3):449-451.
[8]Ben Brahim E,Jouini R,Khayat O,et al.Adenomatous transformation in hamartomatous polyps cases of two patients with Peutz-Jeghers syndrome[J].Int J Colorectal Dis,2009,24(11):1361-1363.
[9]王振军,刘玉村,毕郭龙,等.黑斑息肉病病人的恶性肿瘤易感性研究[J].中国实用外科杂志,1999,19(11):655-656.
[10]张卫,孟荣贵,傅传刚,等.黑斑息肉综合征27例的诊治分析[J].中华普通外科杂志,2002,17(6):349-351.
[11]Udd L,Katajisto P,Rossi DJ,et al.Suppression of Peutz-Jeghers polyposis by inhibition of cyclooxygenase-2[J].Gastroenterology,2004,127(4):1030-1037.
[12]顾国利,魏学明.Peutz-Jeghers综合征预防性治疗的研究[J].胃肠病学和肝病学杂志,2012,21(4):380-383.
[13]Wei C,Amos CI,Zhang N,et al.Suppression of Peutz-Jeghers polyposis by targeting mammalian target of rapamycin signaling[J].Clin Cancer Res,2008,14(4):1167-1171.
[14]Zhang FQ,Fang J.The curative effect observation and nurse of enema with Traditional Chinese Medicine preventing intestinal polys recur-rence after extirpating operation J[J].Journal of Nurses Training,2002,17(3):200-201.
[2016-09-15收稿,2016-10-12修回][本文编辑:吴蓉]
R596
B
250355山东济南,山东中医药大学[管丽芳(2014级研究生),张晓宇];250031山东济南,原济南军区总医院医务部(刘同亭)
刘同亭,Email:liutongting@163.com
