表面改性的类水滑石催化醇的选择性氧化
2017-04-07王晓丽商丛笑吴功德
王晓丽, 商丛笑, 吴功德, 刘 浩
(1.南京工程学院 环境工程学院,江苏 南京 211167;2.英国东英吉利大学 环境科学学院, 诺维奇 NR4 7TJ, UK)
表面改性的类水滑石催化醇的选择性氧化
王晓丽1, 商丛笑2, 吴功德1, 刘 浩1
(1.南京工程学院 环境工程学院,江苏 南京 211167;2.英国东英吉利大学 环境科学学院, 诺维奇 NR4 7TJ, UK)
制备了一系列表面胺基改性的过渡金属类水滑石催化剂,采用XRD、N2吸附、FTIR、TEM和元素分析对其进行了表征。以O2为氧化剂,在无溶剂的条件下,考察其对一系列醇选择性氧化反应的催化性能。结果表明,所制备的改性类水滑石催化剂仍保留类水滑石载体的层状结构,而载体的元素组成显著影响其改性催化剂的性能;在较优的反应条件下,仲醇、环烷醇和芳香醇均可被选择性氧化成相应的醛或酮。
类水滑石; 表面改性; 选择性氧化; 醇; 无溶剂
醇选择性氧化生成相应的醛或酮是有机合成中的重要反应,能为医药、香料等行业提供必需的原料或中间体。传统的氧化方法经常使用化学计量的无机氧化剂,三废问题严重,已逐渐被O2和H2O2这类清洁、廉价的氧化剂所取代[1-8]。空气或氧气因廉价、易得,且氧化副产物仅为水,无疑是理想的氧化剂。但O2要进行选择性氧化反应必须断裂O—O双键,该过程常需在高温高压、有机溶剂和/或贵金属为催化剂的条件下进行[5-6]。从节能减排和环境友好的角度出发,制备高效的、廉价的非均相过渡金属催化剂,在无溶剂和温和的反应条件下选择性催化氧化醇生成醛或酮,具有重要的理论和实践意义。
过渡金属类水滑石催化剂,因其层板元素的可调变性和层间阴离子的可交换性,被广泛地用作催化剂或催化剂载体,用于醇类的选择性氧化反应[9-14]。笔者[15]曾制备了表面胺基改性的三元CuNiAl类水滑石催化剂,在丙三醇(甘油)选择性氧化制备甘油酸的反应中表现出了较好的催化性能。但类水滑石载体的元素组成对催化剂性能的影响尚不明确。为此,笔者制备了一系列表面改性的过渡金属二元和三元类水滑石,详细讨论了载体组成对催化剂性能的影响,并进一步测试了该催化剂在其它醇类选择性氧化反应中的催化性能。
1 实验部分
1.1 试剂与仪器
N-(β-氨乙基)-γ-氨丙基三甲氧基硅烷,购自百灵威公司;其他所用试剂均购自上海化学试剂公司。所有试剂均为分析纯。
Rigaku Dmax-rA型X-光衍射仪;VarioEL型元素分析仪;ARL-3520型电感耦合等离子体原子发射光谱仪;ASP 2000型自动物理吸附仪。
1.2 样品制备
1.2.1 二元、三元类水滑石的合成[15]
先将0.09 mol的二价金属硝酸盐和0.03 mol的三价金属硝酸盐配制成120 mL溶液A。将0.06 mol 的(NH4)2CO3配制成120 mL溶液B。将A和B在室温下同时滴加到120 mL去离子水中,剧烈搅拌。在滴加的过程中保持溶液的pH值在10.0±0.5左右,约1.0~1.5 h滴加完毕,然后60℃下老化2 h。将所得胶体转移到晶化釜中,100℃下水热处理24 h,过滤,用去离子水洗至中性,100℃烘干,即得二元过渡金属类水滑石催化剂。
制备三元类水滑石催化剂时,所配制的溶液A中含有3种过渡金属硝酸盐各0.04 mol,其余原料用量和制备方法同二元过渡金属类水滑石。
1.2.2 类水滑石的表面改性[15]
将3.5 g类水滑石在60℃、0.01 Pa下预处理2 h,然后加至含有0.02 mol硅烷偶联剂(N-(β-氨乙基)-γ-氨丙基三甲氧基硅烷)的100 mL甲苯中。所得混合液N2保护下回流7 h。减压抽滤,所得固体样品用无水乙醇索氏抽提48 h,以脱除吸附在载体表面的偶联剂。进而在60℃、0.02 Pa 下真空干燥3 h,即得表面改性的类水滑石,记作M1M2M3-HT-C5H10N2H3,其中M1M2为二价过渡金属,M3为三价过渡金属。
1.3 催化氧化反应
1.3.1 丙三醇和1,2-丙二醇氧化反应
在100 mL三颈烧瓶中加入0.4 mol/L的丙三醇(或1,2-丙二醇)溶液25 mL,加入一定量的催化剂,4 mol/L的氢氧化钠10 mL,以氧气为氧源,在一定温度下反应。反应一定时间后取样,离心分离,0.45 μm滤膜过滤,采用Agilent 1200高效液相色谱仪分析产物组成。色谱仪配有美国Bio-Rad Aminex-HPX-87H离子排阻色谱柱 (300 mm×7.8 μm),流动相0.005 mol/L 硫酸水溶液,0.5 mL/min;示差和Uv-vwd检测器,波长210 nm,333 K,进样量10 μL。
1.3.2 其他醇氧化反应
在100 mL三颈烧瓶中加入一定量的醇和非均相催化剂,以氧气为氧源,反应进行一段时间后,冷却、过滤出催化剂。采用上海海欣色谱有限公司GC-920型气相色谱仪分析滤液组成,N2作为载气,4 mL/min,FID检测器,HP-5毛细管柱。
按式(1)、(2)计算反应转化率(x)、目的产物选择性(s)。
(1)
(2)
式(1)、(2)中,n0、n1、n2分别为原料中、反应掉的和转化成目的产物的反应物的物质的量。
2 结果与讨论
2.1 表面改性类水滑石催化剂的组成和结构
表1为所制备表面改性类水滑石样品的元素组成和比表面积。由表1可见,表面改性的类水滑石的水滑石层板上金属元素组成与其母体类似,说明表面改性过程中并没有金属元素损失。同时,表面改性的二元类水滑石或三元类水滑石间元素组成类似,那么类水滑石催化剂性能的差异应归结于其金属元素本性。
考虑到不同载体组成的类水滑石催化剂的晶型和结构相似,选取4种样品的XRD、N2吸附-脱附等温线和FT-IR谱分别示于图1。由图1(a)可知,所有样品均出现了d003、d006、d009和d110衍射峰,说明所制备的样品具有典型的类水滑石层状结构[16-18]。另外,与其母体相比,表面改性的类水滑石的d003、d006衍射峰向小角方向迁移,而d110衍射峰未见明显变化。通常认为,d003、d006衍射峰与类水滑石的层间距有关,而d110衍射峰受层板上金属元素分布情况影响[19-20]。表面改性类水滑石的d003、d006衍射峰的迁移,是由于表面有机基团的引入而导致了类水滑石层间距增加;而d110衍射峰未迁移说明表面改性过程中并没有金属元素损失,与元素分析结果一致。
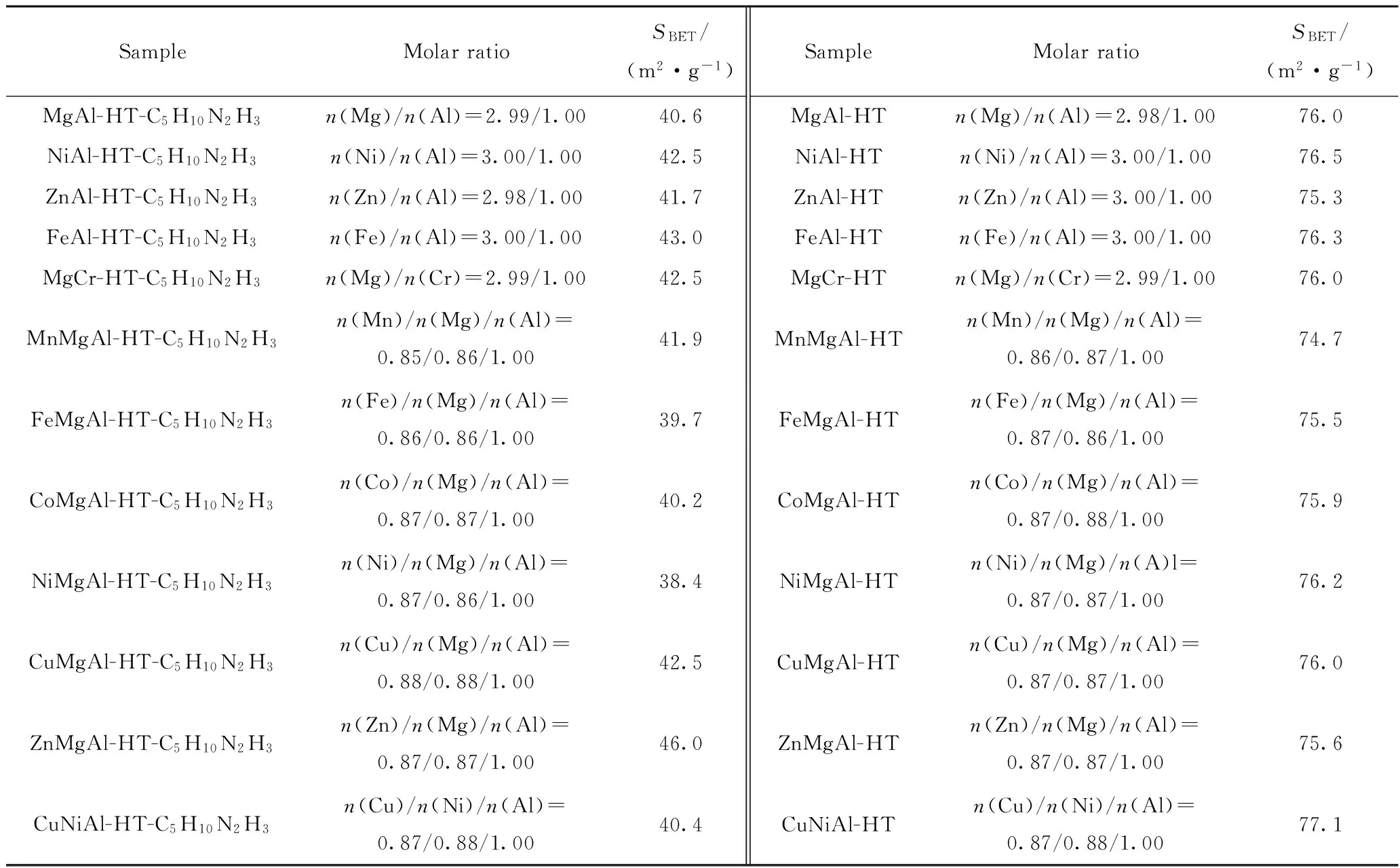
表1 表面改性类水滑石样品的组成和比表面积(SBET)Table 1 Composition and SBET of surface-modified hydrotalcite-like compounds


图1 表面改性类水滑石样品的XRD谱、N2吸附-脱附等温线和FT-IR谱Fig.1 XRD patterns and N2 adsorption-desorptionisothermals and FT-IR spectra of surface-modified hydrotalcite-like compounds(a) XRD; (b) N2 adsorption-desorption isothermals; (c) FT-IR(1) CuNiAl-HT; (2) CuNiAl-HT-C5H10N2H3;(3) CuMgAl-HT; (4) CuMgAl-HT-C5H10N2H3
由图1(b)可知,所有的类水滑石样品均具有IV型N2吸附-脱附等温线,并且有清晰的滞后环,说明所制备的类水滑石由于粒子凝聚而形成了介孔结构[21]。同时,与其母体相比,表面改性的类水滑石的比表面积明显降低(见表1),这可归结于表面有机基团的引入。
由图1(c)可知,两种表面改性的类水滑石在1040 cm-1处出现了Si—O—Si的特征峰,在3424和1015 cm-1处出现了N—H和C—N的伸缩振动峰。而这些特征峰在其母体类水滑石的FT-IR谱中并未出现,进一步证实已经成功制备了表面改性的类水滑石。图2给出了CuMgAl-HT-C5H10N2H3的TEM照片。由图2可以看出,表面改性的类水滑石样品仍具有典型的类水滑石层状结构,与XRD表征结果一致。而且,粒径分布在20~50 nm范围。
2.2 表面改性的类水滑石催化剂的催化性能
以丙三醇选择性氧化反应为探针,考察所制备的类水滑石催化剂的催化性能,结果列于表2。由表2可知,以表面胺基改性的类水滑石为催化剂时,催化活性能较高,主产物为部分氧化产物——甘油酸。这可能是由于表面胺基基团的引入增加了催化剂的表面Lewis碱性,促进了反应中间产物烷氧基C—H键活化生成甘油醛(速控步骤)[15],甘油醛再进一步氧化得主产物甘油酸。当二元类水滑石用作催化剂时,除MgAl-HT-C5H10N2H3和NiAl-HT-C5H10N2H3外,其它二元水滑石的丙三醇转化率均小于30%。MgAl-HT-C5H10N2H3为催化剂时的催化活性能最高,丙三醇转化率高达36.5%,而甘油酸选择性为52.1%。

图2 CuMgAl-HT-C5H10N2H3的TEM照片Fig.2 TEM image of CuMgAl-HT-C5H10N2H3

表2 不同表面改性的类水滑石对丙三醇选择性氧化反应的催化性能Table 2 Catalytic performance of different surface-modified hydrotalcite-like compounds in GLY selective oxidation
GLY—Glycerol; OXAL—Oxalate; TAR—Tartronate; GLYAC—Glyceric acid; GLYC—Glycolic acid; FORM— Formic acid
Reaction conditions: GLY 10 mmol; NaOH 40 mmol; Catalyst 0.2 g;O2flow 60 mL/min; 60℃;4 h
当在MgAl水滑石层板上进一步引入第三过渡金属后,所制备的三元水滑石对丙三醇选择性氧化反应的催化性能显著不同。CoMgAl-HT-C5H10N2H3和ZnMgAl-HT-C5H10N2H与MgAl-HT-C5H10N2H3的催化性能类似,说明Co和Zn作为第三过渡金属的催化活性有限。其余4种三元水滑石的催化性能都比相应二元水滑石显著提高,其中催化性能提高幅度最大的是CuMgAl-HT-C5H10N2H3和CuNiAl-HT-C5H10N2H3,而这两种催化剂催化性能差别不大。这说明Cu是丙三醇选择性氧化反应的活性物种[15],这可能是由于Cu物种易与中间产物甘油醛的醛基作用,从而促进了丙三醇氧化反应[21]。以甘油酸产率为基准,以CuMgAl-HT-C5H10N2H3为催化剂时,丙三醇转化率最高可达67.5%,而甘油酸选择性为79.5%。
2.3 反应条件对CuMgAl-HT-C5H10N2H3催化丙三醇选择性氧化反应的影响
反应条件对CuMgAl-HT-C5H10N2H3催化丙三醇选择性氧化反应性能影响的结果示于图3。由图3(a)可知,在60℃、催化剂用量0.2 g的条件下反应6 h,随着氧化剂用量的增加,丙三醇转化率持续上升,不过升幅逐渐趋缓;甘油酸选择性先升高后降低,这可能由于过量的氧化剂将甘油酸进一步深度氧化成了其它副产物。以甘油酸为目标产物时,O2用量80 mL/min为宜。
由图3(b)可知, 在O2用量80 mL/min、60℃条件下反应6 h,随着催化剂用量的增加,丙三醇转化率和甘油酸选择性均急速升高;催化剂用量增加到0.2 g后,继续增加催化剂用量,丙三醇转化率和甘油酸选择性均下降,这可能由于随着催化剂用量的增加导致该多相反应的扩散阻力增加所致。
由图3(c)可知,在O2用量80 mL/min、催化剂用量0.2 g、60℃条件下,反应6 h时,反应已基本达到平衡,这说明丙三醇选择性氧化反应进行得较快;继续延长反应时间,丙三醇转化率变化不大,但甘油酸选择性急速下降,说明过长的反应时间仅会增加甘油酸进一步氧化和裂解生成副产物的机会。
从图3(d)可见,在O280 mL/min、催化剂0.2 g、反应6 h的条件下,反应温度从20℃升高到60℃,丙三醇转化率急速上升,这可能由于该反应是在多相催化体系下进行,反应温度升高则有利于反应物与催化剂间的接触,从而使丙三醇转化率提高;继续升高温度,丙三醇转化率升高的趋势变缓,而甘油酸选择性大幅度下降,说明相对于丙三醇选择性氧化过程而言,过高的反应温度更有利于其它副反应的进行。通过以上实验,该CuMgAl-HT-C5H10N2H3催化丙三醇选择性氧化反应的最佳条件应为,O2用量80 mL/min、催化剂用量0.2 g、反应温度60℃、反应时间6 h。此时,丙三醇转化率可达72.0%,甘油酸选择性为75.2%。

图3 反应条件对CuMgAl-HT-C5H10N2H3催化丙三醇选择性氧化反应的影响Fig.3 Effects of reaction conditions on the catalytic selective oxidation of GLY over CuMgAl-HT-C5H10N2H3(a) The effect of oxidant dosage; (b) The effect of catalyst amount; (c) The effect of reaction time; (d) The effect of reaction temperature Other reaction conditions: GLY of 10 mmol; NaOH of 40 mol
2.4 CuMgAl-HT-C5H10N2H3催化剂的重复使用性能
在最佳的反应条件下,考察CuMgAl-HT-C5H10N2H3催化剂在丙三醇选择性氧化反应中的重复使用性能,结果列于表3。使用过的催化剂用去离子水和无水乙醇清洗,在60℃下真空干燥过夜,保持反应条件不变,用于反应中。由表3可知,CuMgAl-HT-C5H10N2H3在丙三醇选择性氧化反应重复使用7次后仍具有较高的催化活性。对重复使用7次后的催化剂进行元素分析发现,催化剂的元素组成并未见明显变化(n(Cu)/n(Mg)/n(Al) =0.88/0.87/1.00),说明在较温和的反应条件下,该催化剂具有良好的稳定性。

表3 CuMgAl-HT-C5H10N2H3催化丙三醇选择性氧化反应的重复使用性能Table 3 Reusability of CuMgAl-HT-C5H10N2H3 in the catalytic selective oxidation of GLY
Reaction condition: Glycerol 10 mmol; NaOH 40 mol;Catalyst 0.2 g; O2flow 80 mL/min;60℃; 6 h
2.5 CuMgAl-HT-C5H10N2H3对其它醇选择性氧化反应的催化性能
以CuMgAl-HT-C5H10N2H3为催化剂,用于一系列醇的选择性氧化反应中。结果表明,一元醇中,烷基仲醇、环烷醇和苯甲醇均能被高效地氧化成相应的醛和酮。而烷基伯醇的氧化反应,需要较长的反应时间,且主产物是相应的脂肪酸,与芳香基伯醇(苯甲醇)不同。二元醇和三元醇的氧化反应主要发生在端位羟基上,生成的主产物是相应的羟基羧酸。以O2为氧化剂时,醇首先被氧化成相应的醛和酮,其中酮是最终氧化产物,而醛则进一步被氧化成羧酸,因此烷基仲醇或环烷醇氧化生成的酮的产率较高;而相比于芳香醛,一元醛看起来更易被氧化成相应的羧酸。

表4 CuMgAl-HT-C5H10N2H3在催化醇氧化反应中的性能Table 4 Catalytic performance of CuMgAl-HT-C5H10N2H3catalyst in oxidation of alcohols1)
1) 40 mol NaOH was also needed
Reaction conditions: Alcohol 10 mmol; Catalyst 0.2 g; O2flow 80 mL/min; 60℃; 6 h
3 结 论
(1)成功地制备出了一系列表面改性的过渡金属类水滑石催化剂,在无溶剂的条件下,以O2为氧化剂,催化醇选择性氧化反应,表现出较高的催化活性。
(2)类水滑石载体的元素组成明显影响催化剂的催化性能,以Cu为类水滑石层板二价金属阳离子源所制得的含Cu类水滑石的催化性能最佳。
(3)在较优的反应条件下,仲醇、环烷醇和苯甲醇的氧化主产物是其相应的酮和醛,而一元伯醇、二元醇和三元醇的氧化主产物是相应的羧酸。
[1] PARMEGGIANI C, CARDONA F. Transition metal based catalysts in the aerobic oxidation of alcohols[J].Green Chem, 2012, 14(3): 547-564.
[2] 石先莹, 韩晓燕, 马文娟, 等. 过渡金属催化醇氧化反应的研究进展有机化学[J].有机化学, 2011, 31(3): 297-305. (SHI Xianying, HAN Xiaoyan, MA Wenjuan, et al. Recent progress in oxidation of alcohols catalyzed by transition metal[J].Chin J Org Chem, 2011, 31(3): 297-305.)
[3] MARKO I E, GILES P R, TSUKAZAKI M, et al. Copper-catalyzed oxidation of alcohols to aldehydes and ketones: An efficient, aerobic alternative[J].Science, 1996, 274(5295): 2044-2046.
[4] BRINK G, ARENDS I W C E, SHELDON R A. Green, catalytic oxidation of alcohols in water[J].Science, 2000, 287(5458): 1636-1639.
[5] RAJABI F, KARIMI B. Efficient aerobic oxidation of alcohols using a novel combinationn-hydroxy phthalimide (NHPI) and a recyclable heterogeneous cobalt complex[J].J Mol Catal A: Chem, 2005, 232(1-2): 95-99.
[6] ZHAO H, CHEN Q R, WEI L, et al. Chem in form abstract: A highly efficient heterogeneous aerobic alcohol oxidation catalyzed by immobilization of bipyridine copper(I) Complex in MCM-41[J].Tetrahedron, 2015, 71(46): 8725-8731.
[7] SHA J, ZHENG E J, ZHOU W J, et al. Selective oxidation of fatty alcohol ethoxylates with H2O2over Au catalysts for the synthesis of alkyl ether carboxylic acids in alkaline solution[J].J Catal, 2016, 337(1-2): 199-207.
[8] CANG R B, LU B, LI X P, et al. Iron-chloride ionic liquid immobilized on SBA-15 for solvent-free oxidation of benzyl alcohol to benzaldehyde with H2O2[J].Chem Eng Sci, 2015, 137(1): 268-275.
[9] ZHOU W Y, LIU J, PAN J G, et al. Effect of Mg2+on the catalytic activities of CoMgAl hydrotalcites in the selective oxidation of benzyl alcohol to benzaldehyde[J].Catal Commun, 2015, 69(5): 1-4.
[10] QIAO D, XU C L, XU J. Aerobic oxidation of benzyl alcohol over Co3O4/rehydrated hydrotalcite catalysts: The promotional effect of hydrotalcite support[J].Catal Commun, 2014, 45 (5): 44-48.
[11] DU Y Y, WANG Q, LIANG X, et, al. Hydrotalcite-like MgMnTi non-precious-metal catalyst for solvent-free selective oxidation of alcohols[J].J Catal, 2015, 331(1): 154-161.
[12] DIXIT M, MISHRA M, JOSHI P A, et al. Chem physico-chemical and catalytic properties of Mg-Al hydrotalcite and Mg-Al mixed oxide supported copper catalysts[J].J Ind Eng, 2013, 19(2): 458-468.
[13] CHOUDHARY V R, CHAUDHARI P A, NARKHEDE V S. Solvent-free liquid phase oxidation of benzyl alcohol to benzaldehyde by molecular oxygen using non-noble transition metal containing hydrotalcite-like solid catalysts[J].Catal Commun, 2003, 4(45): 171-175.
[14] 王亮, 孟祥举, 肖丰收. 水滑石负载Au纳米粒子的制备及其催化醇氧化反应[J].催化学报, 2010, 31(8): 943-947. (WANG Liang, MENG Xiangju, XIAO Fengshou. Au nanoparticles supported on a layered double hydroxide with excellent catalytic properties for the aerobic oxidation of alcohols[J].Chin J Catal, 2010, 31(8): 943-947.)
[15] WU G D, WANG X L, HUANG Y, et al. Selective oxidation of glycerol with O2catalyzed by low-cost CuNiAl hydrotalcites[J].J Mol Catal A: Chem, 2013, 379(15): 185-191.
[16] CHOUDARY B M, KANTAM M L, NEERAJA V, et al. Layered double hydroxide fluoride: A novel solid base catalyst for C—C bond formation[J].Green Chem, 2001, 3(5): 257-260.
[17] ZHOU H, ZHOU G L, JIANG X Z. A heck reaction catalyzed by Pd supported on LDH-F hydrotalcite[J].J Mol Catal, 2006, 248(1-2): 26-31.
[18] BELLOTTO M, REBOURS B, CLAUSE O, et al. A reexamination of hydrotalcite crystal chemistry[J].J Phys Chem, 1996, 100(20): 8527-8534.
[19] CAVANI F, TRIFIRO F, VACCARI A. Hydrotalcite-type anion clays: preparation, properties and applications[J].Catal Today, 1991, 11(2): 173-301.
[20] LABAJOS F M, RIVES V, ULIBARRI M A. Effect of hydrothermal and thermal treatments on the physicochemical properties of Mg-Al hydrotalcite-like materials[J].J Mater Sci, 1991, 27(6): 1546-1552.
[21] ZHOU C H, BELTRAMINI J N, LIN C X, et, al. Selective oxidation of biorenewable glycerol with molecular oxygen over Cu-containing layered double hydroxide-based catalysts[J].Catal Sci Technol, 2011, 1(2): 111-122.
Selective Oxidation of Alcohols Catalyzed by Surface Modified Hydrotalcite-Like Compounds
WANG Xiaoli1, SHANG Congxiao2, WU Gongde1, LIU Hao1
(1.DepartmentofEnvironmentandTechnology,NanjingInstituteofTechnology,JiangsuNanjing, 211167,China;2.SchoolofEnvironmentScience,UniversityofEastAngelia,Norwich,NR4 7TJ,UK)
A series of surface modified hydrotalcite-like compounds were prepared and characterized by XRD, N2adsorption-desorption, FT-IR, TEM and elemental analysis. The obtained compounds were used as catalyst for the solvent-free selective oxidation of alcohols with O2as oxidant. The results reviewed that the obtained surface modified catalysts still showed the good pattern characteristics of hydrotalcite. Moreover, the elemental composition of hydrotalcite-like support influenced significantly the catalytic performance of relative catalysts. Under the optimal reaction conditions, secondary alcohol, cyclanol and aromatic alcohol could be selectively oxidized to their corresponding aldehydes or ketones.
hydrotalcite-like compounds; surface modified; selective oxidation; alcohol; solvent-free
2016-06-06
国家自然科学基金(21003073,21203093)、江苏省自然科学基金(BK20141388,BK20161481)和江苏省高校“青蓝工程”和南京工程学院“学术拔尖人才工程”项目资助
王晓丽,女,副教授,博士,从事环境友好型催化材料的研发及应用;Tel:025-86118960;E-mail:wangxiaoli212@njit.edu.cn
吴功德,男,副教授,博士,从事环境友好型催化材料的研发及应用;Tel:025-86118960;E-mail:wugongde@njit.edu.cn
1001-8719(2017)02-0349-07
O643.32
A
10.3969/j.issn.1001-8719.2017.02.021
