禽源多杀性巴氏杆菌多位点序列分型研究
2017-03-16李伟杰田野岂晓鑫蒋颖魏财文蒋桃珍中国兽医药品监察所北京100081
李伟杰,田野,岂晓鑫,蒋颖,魏财文,蒋桃珍(中国兽医药品监察所,北京 100081)
禽源多杀性巴氏杆菌多位点序列分型研究
李伟杰,田野,岂晓鑫,蒋颖,魏财文,蒋桃珍*
(中国兽医药品监察所,北京 100081)
为了解国内禽源多杀性巴氏杆菌流行情况,对分离自18省份的84株多杀性巴氏杆菌采用荚膜多重PCR分型和多位点序列分型对其血清型和基因型进行鉴定。结果表明:禽源多杀性巴氏杆菌主要以血清A型为主,占96.4%(81/84);多位点序列分型可将禽源多杀性巴氏杆菌分为 5种ST型,其中ST129为主要流行型,占94.0%(79/84)。本研究为我国禽源多杀性巴氏杆菌的流行病学监测和基因多样性提供了数据支持。
多杀性巴氏杆菌;荚膜分型;多位点序列分型
禽霍乱是由多杀性巴氏杆菌(Pasteurellamultocida)引起的鸡、鸭和鹅等多种禽类的一种接触性、败血性传染病[1]。病禽、康复禽或健康带菌禽是主要的传染源,主要通过被污染的饲料、饮水经消化道感染,多发生于性成熟的禽类,自然感染潜伏期为2~9 d。在潮湿、多雨、气温较高的季节时有发生。本病是危害我国养禽业的重要细菌性传染病之一。
脉冲场凝胶电泳(PFGE)[2]、肠道细菌基因间重复序列(ERIC-PCR)指纹图谱技术[3]和多位点序列分型(MLST)[4]等方法推动了对多杀性巴氏杆菌分子流行病学和基因多样性的研究。现在MLST已经成为病原菌基因分型的金标准,在分子流行病学调查中得到广泛应用[5-7]。由于国内对禽源多杀性巴氏杆菌的基因多样性和分子流行病学状况研究的不多,因此本研究拟对分离和收集的禽源多杀性巴氏杆菌进行MLST分型,以便为我国多杀性巴氏杆菌病暴发的流行病学监测和基因多样性研究提供支持。
1 材料与方法
1.1 菌株 84株分离株分离自国内的不同地区和不同年代(表1),由中国兽医微生物菌种保藏管理中心提供。

表1 多杀性巴氏杆菌的血清分型和MLST分型
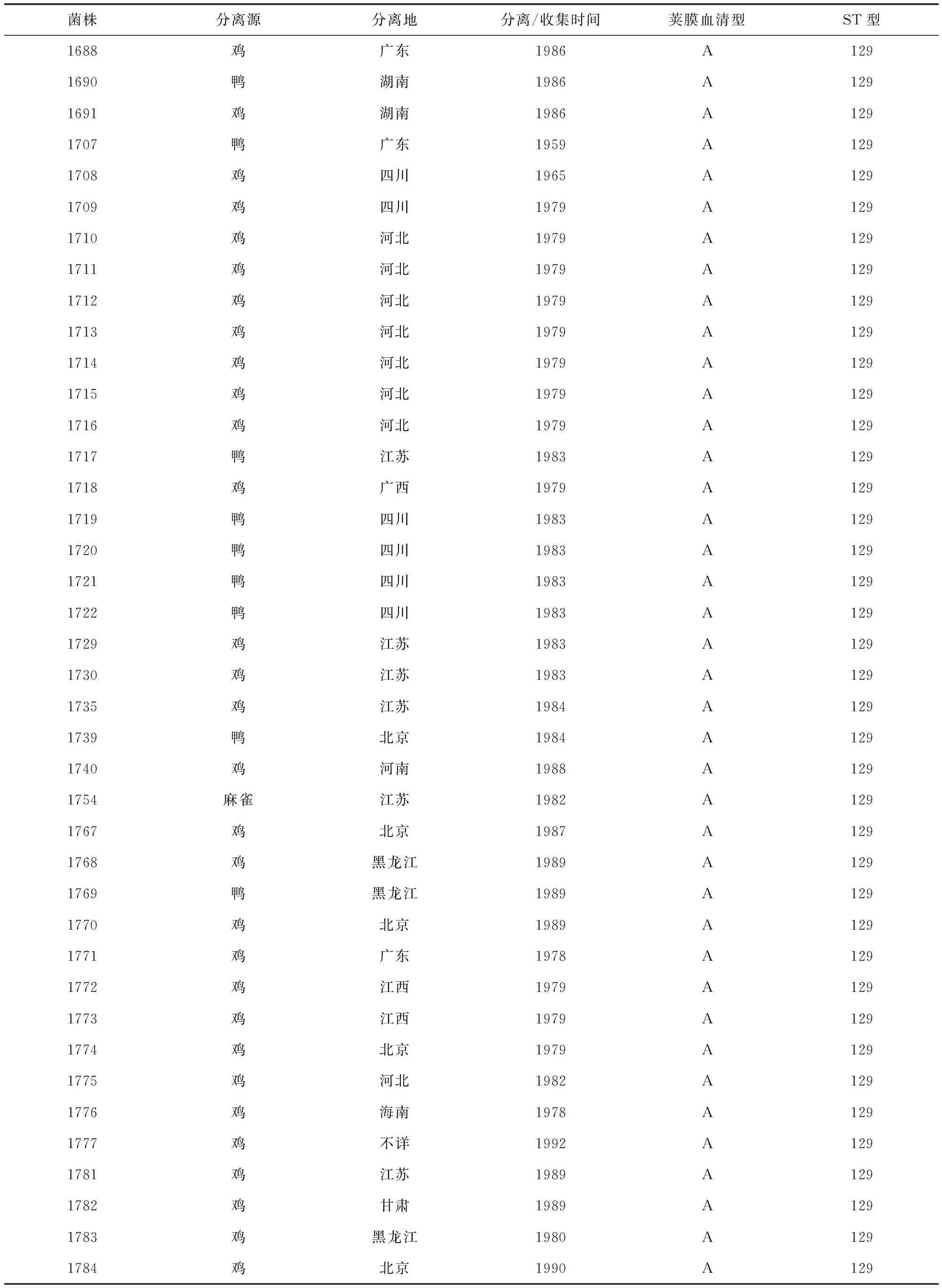
续表

续表
1.2 主要试剂 胰蛋白胨大豆琼脂(TSA)和胰蛋白胨大豆肉汤(TSB)购自OXOID公司,马血清购自GIBCO公司,Ex Taq酶、DL2000 DNA Maker购自宝生物工程(大连)有限公司,琼脂糖购自Biowest公司,Goldview购自北京赛百盛基因技术有限公司。
1.3 菌株DNA的提取 分离株在含5%马血清的TSA培养基上,37 ℃培养24 h采用热裂解法[8]提取基因组 DNA,挑取纯培养菌落于100 μL无菌蒸馏水中,沸水浴10 min,然后冰浴10 min,12000 r/min离心1 min,上清作为PCR扩增的模板DNA。
1.4 菌株kmtI基因的扩增及序列分析 按照文献方法[9]对分离株进行kmtI基因的PCR扩增,扩增产物测序后与 NCBI 核酸数据库进行 BLAST序列比对。
1.5 菌株血清型的鉴定 按照Townsend等[9]建立的多杀性巴氏杆菌荚膜多重PCR方法对分离株血清型进行鉴定,引物见表2,PCR扩增产物用1.5%的琼脂糖凝胶进行电泳检测。

表2 多杀性巴氏杆菌种鉴定、荚膜血清分型和MLST的引物
*在zwf-1对应的引物不能有效扩增的情况下使用
1.6 MLST 分型 根据Subaaharan等[4]建立的禽源多杀性巴氏杆菌 MLST 分型方法,对本研究中84株分离株的7个看家基因(腺苷酸环化酶基因adk、酯酶基因est、6-磷酸-甘露糖异构酶基因pmi、葡萄糖-6磷酸脱氢酶基因zwf、苹果酸脱氢酶基因mdh、谷氨酸脱氢酶基因gdh、磷酸葡萄糖异构酶基因pgi)进行扩增及测序,引物见表2。序列经MEGA7软件编辑后,提交到RIRDC MLST在线数据库进行比对,获得菌株的序列型,并利用 MEGA7软件对RIRDC MLST 数据库中的部分 ST 型进行序列比对,构建系统发育树,分析其分子进化关系。
2 结果与分析
2.1 分离株的kmtI鉴定 通过对 84株分离株进行kmtI基因的扩增和测序,提交 GenBank进行 BLAST 比对,结果显示与多杀性巴氏杆菌的相似性均达 99 %以上。表明本研究中收集和分离的84株分离株均为多杀性巴氏杆菌。
2.2 血清分型 利用荚膜多重PCR 方法将 84株多杀性巴氏杆菌分为 A和B共2种血清型,其中81株为A型,占96.4%;其余3株为B型,且均分离自霍乱鸡(表1)。
2.3 MLST分型 对84株多杀性巴氏杆菌分别进行adk、est、pmi、zwf、mdh、gdh和pgi7个看家基因的扩增和测序,结果显示可以将其分为 ST129、ST122、ST107、ST62和ST44 5种 ST 型,其中禽源多杀性巴氏杆菌主要以 ST129 型为主,占94%(79/84)具体见表1。利用 MEGA7对本研究确定的5个ST型和国内报道的其他ST型[10]进行序列分析,结果表明:国内分离株ST122和ST44亲缘关系最近,ST62和ST58亲缘关系最近;主要流行的ST-129型与ST122、ST44、ST62、ST58具有较近的亲缘关系,在同一大的分支上;ST8和ST107与其他的ST型亲缘关系较远(图1)。

图1 84株禽源多杀性巴氏杆菌的多位点序列系统进化树
3 讨论与小结
多杀性巴氏杆菌根据荚膜抗原可分为A、B、D、E和F 5种血清型,本研究通过荚膜多重PCR方法对84株禽源多杀性巴氏杆菌(主要分离收集自1953年至1990年)进行血清分型,结果有81株为荚膜A型。程安春等[11]对从1990-1995年分离自四川省不同地区的256株鸭源多杀性巴氏杆菌进行血清分型,其中254株为荚膜A型,2株未定型;程龙飞等[12]收集2007-2013年福建及邻近省份分离的95株禽源多杀性巴氏杆菌,经鉴定荚膜型全为A型;Wang等[5]对2011-2012年分离自江苏省不同地区的40株禽源多杀性巴氏杆菌流调结果显示全部为荚膜A型。以上研究都表明多年来国内引起禽霍乱的优势血清型为A型。
多杀性巴氏杆菌的MLST是由多位点酶电泳(MLEE)衍生出来,主要通过看家基因序列的多态性对细菌进行分类[4]。由MLST得到的分型结果可与数据库中已有的信息进行比对,从而使不同地点和不同时间分离的菌株可以进行横向和纵向比较。目前多杀性巴氏杆菌多位点序列分型的在线数据库有两个(http://pubmlst.org/pmultocida/):Multiple host MLST由英国格拉斯哥大学开发,针对不同宿主来源的多杀性巴氏杆菌;RIRDC MLST由澳大利亚动物研究所开发,针对禽源多杀性巴氏杆菌。截止2016年11月18日,RIRDC MLST数据库中已经鉴定有329种 ST 型。本研究通过对84株多杀性巴氏杆菌MLST的鉴定,获得5个ST型,主要以 ST129为主,占94%(79/84),与文献报道[5,10]的一致。还鉴定到 ST122、ST107、ST62和ST44,这在禽源多杀性巴氏杆菌中为国内首次报道。由于MLST能够区分亲缘关系较近的菌株,能够对爆发的流行菌株进行溯源,因此本研究中基因型相同的79株菌株可能来源于同一株多杀性巴氏杆菌。考虑到ST129型已在斯里兰卡[6]、印度[7]和丹麦等(http://pubmlst.org/pmultocida/)许多国家被发现,此基因型可能在全球都有分布。同时它可以从发生禽霍乱的鸡、鸭、鹅和麻雀体内分离到,说明它具有多动物宿主的特性。
综上所述,本研究为禽源多杀性巴氏杆菌的流行病学提供了一些本底数据,为今后多杀性巴氏杆菌的监测起到了支撑作用,同时对于研制有效的疫苗预防和控制禽霍乱有一定的帮助。
[1] Wilson B A, Ho M.Pasteurellamultocida: from zoonosis to cellular microbiology [J]. Clinical Microbiology Reviews, 2013, 26 (3): 631-655.[2] Blackall P J, Miflin J K. Identification and typing ofPasteurellamultocida: a review [J]. Avian Pathology, 2000, 29 (4): 271-287.
[3] Loubinoux J, Lozniewski A, Lion C,etal. Value of enterobacterial repetitive intergenic consensus PCR for study ofPasteurellamultocidastrains isolated from mouths of dogs [J]. J Clin Microbiol, 1999, 37 (8): 2488-2492.
[4] Subaaharan S, Blackall L L, Blackall P J. Development of a multi-locus sequence typing scheme for avian isolates ofPasteurellamultocida[J]. Vet Microbiol, 2010, 141(3/4): 354-361.
[5] Wang Y, Zhu J,Lu C,etal. Evidence of circulation of an epidemic strain ofPasteurellamultocidain Jiangsu, China by multi-locus sequence typing (MLST) [J]. Infection, Genetics and Evolution, 2013, 20: 34-38.
[6] Hotchkiss E J, Hodgson J C, Lainson F S,etal. Multilocus sequence typing of a global collection ofPasteurellamultocidaisolates from cattle and other host species demonstrates niche association [J]. BMC Microbiol, 2011, 11: 115-123.[7] Sarangi L N, Thomas P, Gupta S K,etal. Molecular epidemiology ofPasteurellamultocidacirculating in India by multilocus sequence typing [J]. Transbound Emerg Dis, 2016, 63(2): 286-292.
[8] 李伟杰,魏财文,田野,等. 猪源多杀性巴氏杆菌荚膜分型及外膜蛋白H基因序列分析[J]. 中国畜牧兽医,2015,42 (1): 32-37.
[9] Townsend K M. Boyce J D, Chung J Y,etal. Genetic organization ofPasteurellamultocidacap loci and development of a multiplex capsular PCR typing system [J]. J Clin Microbiol, 2001, 39(3): 924-929.
[10]王林柏,孙久鹤,郭东春,等. 国内部分地区多杀性巴氏杆菌荚膜血清型和基因型的研究[J]. 中国预防兽医学报,2016,38 (2): 116-119.
[11]程安春,汪铭书,陈孝跃,等. 256株鸭源多杀性巴氏杆菌血清学鉴定及病原特性研究[J]. 中国兽医科技,1997,27(7):13-15.
[12]程龙飞,许利娜,林建生,等. 福建及邻近省份禽源多杀性巴氏杆菌的分离鉴定[J]. 中国动物传染病学报,2014,22(4):40-44.
(编辑:李文平)
Multi-locus Sequence Typing ofPasteurellamultocidaIsolated from Avian
LI Wei-jie,TIAN Ye,QI Xiao-xin,JIANG Ying,WEI Cai-wen,JIANG Tao-zhen*
(ChinaInstituteofVeterinaryDrugControl,Bejing100081,China)
To investigate the epidemic status of thePasteurellamultocidaisolated from avian, eighty-fourP.multocidaisolates collected from 18 provinces were subject to identifications of the serotypes and genotypes by capsular multiplex PCR and multi-locus sequence typing. The results showed thatP.multocidaisolated from avian were mainly classified into serotype A, accounting for 94.6%. Five different sequence types including ST129, ST122, ST107, ST62, ST44 were identified by MLST, and the predominate genotype was ST129, accounting for 94.6%. The present study provides data support for the epidemiological surveillance and genetic diversity ofP.multocidaisolated from avian.
Pasteurellamultocida; capsular serotyping; multi-locus sequence typing
2016-11-21
A
1002-1280 (2017) 02-0001-06
S852.61
生物安全关键技术研发(2016YFC1201603);国家微生物资源平台(NIMR-5)
李伟杰,副研究员,从事兽医微生物和兽用生物制品研究。
蒋桃珍。E-mail:jiangaozhen@ivdc.org.cn
