中日两国中药PCT专利申请比较研究
2017-02-16张芙婧谌侃
张芙婧,谌侃
·调查与研究·
中日两国中药PCT专利申请比较研究
张芙婧*,谌侃*
中药作为中华民族的宝贵财富,具有历史悠久、资源广泛、成本低廉、毒副作用小等特点,并在科研、产品以及市场方面具有明显的产业优势。截至 2014 年,我国中药产业年规模已达 4100 亿元以上,但中药类产品出口仅为24.99 亿美元,尤其是出口成药比例不足出口中药的 30%。国际市场上中药销售额中,日本、韩国等“洋中药”所占份额已高达 80% ~ 90%[1]。由此可见,当前我国中药产业的国际市场地位以及国际竞争水平与其行业整体规模之间严重失衡,难以走出国门成为困扰国内企业发展的共同难题。造成这种局面的原因是多方面的,缺乏知识产权保护是重要的因素之一。如果能够有效利用“专利先行”战略则可以实现对市场的提前占有和对竞争对手的挤压。
由于专利具有地域性特点,即,专利权仅在进行专利申请并获得授权保护的国家或地区有效,因此当选择“专利先行”战略时,国内企业也迫切需要在存在市场布局的相应国家或地区进行专利申请。在此背景下,具有申请程序简化优势的 PCT 申请作为当前主流的向外专利申请途径也逐渐为国内申请人所知。PCT 是《专利合作条约》(Patent Cooperation Treaty)的英文缩写,根据 PCT 的规定,专利申请人可以通过 PCT 途径递交国际专利申请,向多个国家或地区申请专利。
日本是世界上接受、应用中药较早、较好的国家,其汉方药与我国中药同根同源。1976 年,日本厚生省确定了汉方药医疗保险制度,即批准可以使用中国《伤寒杂病论》的210 个古方生产汉方药,汉方药产业随之得到迅猛发展[2],经过数十年,其汉方药研发和市场占有水平在世界均处于领先地位。以中成药市场为例,其在全球市场中所占份额已高达 75%。同时,日本一直重视专利战略,近年更是提出“知识产权立国”,以推动国家经济和技术的进步[3]。日本企业大都建立了系统完善的专利战略,并通过 PCT 申请等手段在世界范围内积极推进专利申请和专利布局。他山之石,可以攻玉,本文将针对近年来中日两国中药的 PCT 专利申请整体态势进行比较分析,以使我们更好发现自身存在的潜在缺陷或不足,并为国内企业制定合理的向外专利申请策略提供理论依据。
1 数据来源和检索方法
选择国家知识产权局提供的外文数据库(VEN)作为数据来源,对技术来源国为日本或中国且申请日介于 2009 –2014 年的中药 PCT 专利申请进行统计(鉴于 2015 年申请的 PCT 专利申请大多尚未公开,故仅统计到 2014 年)。检索的主要条件设置为:(WO2009 or WO2010 or WO2011 or WO2012 or WO2013 or WO2014)/AP and (CN or JP)/PR and (A61K36 or A61K35)/IC。进一步筛选剔除实质内容与中药无关的专利申请以得到最终的专利文献池,针对实际分析项对相应数据逐一手工提取统计,最终得到符合条件的日本PCT 专利申请共 171 项,中国 PCT 专利申请 265 项。
2 中日两国中药 PCT 专利申请比较研究结果
2.1 申请量趋势
由日本和中国 2009 – 2014 年中药 PCT 专利申请数量(图 1)可见,日本近年来中药 PCT 专利申请数量呈现整体平稳态势,除 2009 年为 43 项外,2010 – 2013 年四年间每年都为 30 项左右,2014 年有所下降,仅为 16 项。而中国则呈现了快速增长趋势,虽然 2009、2010 年两年的申请数量少于日本,但从 2011 年开始逐年大幅增加,2014年虽降为 42 项,但仍高于日本。2014 年中、日两国申请数量均有所下降是因为部分 PCT 专利申请尚未国际公开,数据展现不完整所致。这六年内中国整体的申请数目一共是265 项,已经远超过日本的 171 项。
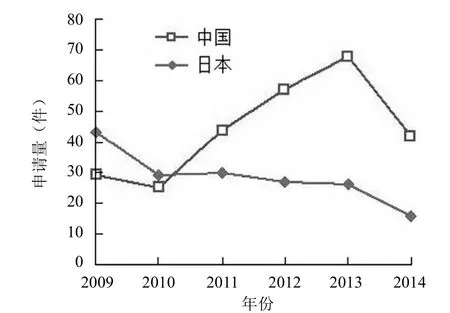
图 1 中日两国 2009 – 2014 年中药 PCT 专利申请量
由以上数据可见,国内申请人进行中药 PCT 专利申请的热情正在逐渐增加,而更多数目的申请同时也意味着更多的中药创新成果可能在国外获得授权保护,这对我们中药产业走出国门是至关重要的。但我们也应看到,当前国内 PCT专利申请量仍然处于相对较低的水平,以上数量并不能完全体现国内中药领域的整体创新速度,在未来的一段时间内,预计以上申请量仍将维持高位增长态势。
2.2 申请人分析
横向比较日本和中国申请人类型(图 2)发现,日本申请主体为企业,占比高达 85%;其次是科研院所,占比12%;个人申请仅占 3%。虽然中国申请主体也为企业,但个人申请占比高达 36%。相比于个人,企业具备较强的整体研发实力和资金投入,能够确保其专利成果具备较高实用价值并能快速推广应用,从而实现最终的市场价值。中国申请中相当比例的个人申请也在一定程度上影响了其创新高度及专利产出能力。此外,虽然中国和日本申请中来自科研院所的申请比例相同,但日本科研院所申请中涉及与企业联合申请的比例也明显高于中国,所述联合可同时利用科研院所的技术研发优势以及企业的资金设备优势,从而实现产研对接,这也是国内科研院所和企业在进行中药创新研发时可参考借鉴的合作模式。

图2 中日两国中药 PCT 申请申请人类型
进一步分析中日两国申请量前十的申请人(图 3)可发现,日本申请量前十的申请人均为企业,且株式会社资生堂、花王株式会社、狮王株式会社等日化企业的申请量相比小林株式会社、株式会社东洋新药、日清药业等传统制药企业更高,这种局面的形成一方面是由于中药除具备治疗应用外,还广泛用于化妆、保健、食品等领域,以上日化企业积极扩展中药的领域适用性并由此产生了良好的经济效益,专利申请热情也相对较高;另一方面也与日本对汉方药的管理政策紧密相关,日本的汉方制剂按照《药事法》分为医疗用汉方制剂和一般用汉方制剂,日本厚生劳动省要求作为处方药,医疗用汉方制剂必须具有标准的质量、疗效、高稳定性和易于管理。考虑到汉方制剂成分的复杂性,汉方制药企业认为集中投资用于推进汉方药市场普及要比研发新药更有意义,基于这种形势,制药企业的中药专利申请相对较少。

图3 中(A)日(B)两国中药 PCT 申请量排名前十的申请人分布
中国申请量前十的申请人中有 7 家企业、1 所高校以及 2 个个人。对于其中企业而言,共包括 6 家制药企业和1 家日化企业,其中仅有天津天士力制药有限公司属于2015 年中国医药上市公司价值排行榜 50 强企业,该榜单中的大量大型中医药企业,如云南白药、康美药业、太极集团、同仁堂等,或者完全未提交 PCT 申请,或者仅提交了少量 PCT 申请,表明国内大型中药企业对于国外专利布局缺乏与其市场地位和研发实力相匹配的申请热情。此外,来自日化企业等非传统中药企业的中国 PCT 申请相对较少,表明国内对于中药应用领域的扩展水平相对落后于日本,这也成为国内企业利用传统中药优势走出国门的一个潜在突破口。
2.3 进入国家(地区)分析
PCT 专利申请包括国际阶段和国家阶段,国际阶段包括 PCT 申请的受理、形式审查、国际检索和国际公布等必经程序,而进入国家阶段的程序不是自动发生的,必须由申请人来选择启动。要想获得某个国家的专利,专利申请人还必须履行进入该国家的手续,由该国的专利局对申请进行审查。换而言之,PCT 专利申请只有进入相应国家(地区)才能发挥其专利申请的实际价值。
横向比较中日两国中药领域 PCT 专利申请进入国家阶段的数据发现,平均每项日本 PCT 申请进入 1.80 个其他国家,且 58% 的申请至少进入一个其他国家;相较而言,平均每项中国 PCT 申请仅进入 0.79 个其他国家,且至少进入一个其他国家的申请比例仅为 24.9%。剔除个人申请,仅针对国内企业申请进一步统计发现,其在以上分析项中的表现也分别仅为 0.93 个其他国家和 29.0% 的进入比例,可见,即便仅考虑国内企业申请人,其进入其他国家或地区的数据水平也远低于日本。
由上可见,中国 PCT 申请在进入国家(地区)数目和比例方面均远低于日本 PCT 申请,大量申请的进度仅停留在国际阶段而未进入国家阶段,导致其最终无法在任何国家获得具有保护意义的专利权。国内中药企业在提交 PCT 专利申请时一方面应提前对专利布局进行充分准备,明确希望获得专利授权保护的国家或地区,避免出现申请夭折在国际阶段而造成经济和创新成果损失的情形;另一方面,在条件允许的情况下也应在指定时间内积极启动进入国家程序,在有价值的目标市场实现专利申请的全面覆盖。
进一步分析中日两国 PCT 申请进入国家(地区)的分布情况,得到图 4。由图 4 可见,中日两国 PCT 申请进入的国家(地区)整体较为一致,主要包括两类情形:一类是中药使用历史悠久、对中药接受认可度较高的东亚和东南亚地区,包括中国、日本、韩国、越南等;一类是经济发达、具备较强消费能力和较大市场容量的发达国家(地区),包括美国、欧洲、澳大利亚和加拿大等。对于日本申请而言,其进入的国家(地区)主要集中在中国、美国、欧洲、韩国,以上国家占其全部进入量的 85% 以上,其中进入中国的专利申请最多,占其全部 PCT 专利申请的 35%,表明日本申请人很重视在中国的专利布局。对于中国申请而言,其进入的国家(地区)则相对较为分散,主要为美国、欧洲、日本、加拿大、澳大利亚、韩国和中国香港,以上国家(地区)占其全部进入量的 60% 左右,其中进入美国的专利申请最多,占其全部 PCT 专利申请的 16%,表明美国是中国申请人的主要专利布局市场。由于同时进入多个不同国家需要较大的申请费用投入,国内申请人在选择进入具体国家(地区)时,也可遵循上述专利布局分布,瞄准主要中药传统市场以及主要发达经济体,由此实现与市场导向相关的针对性专利布局。

图4 中日两国中药 PCT 申请进入国家(地区)的分布情况
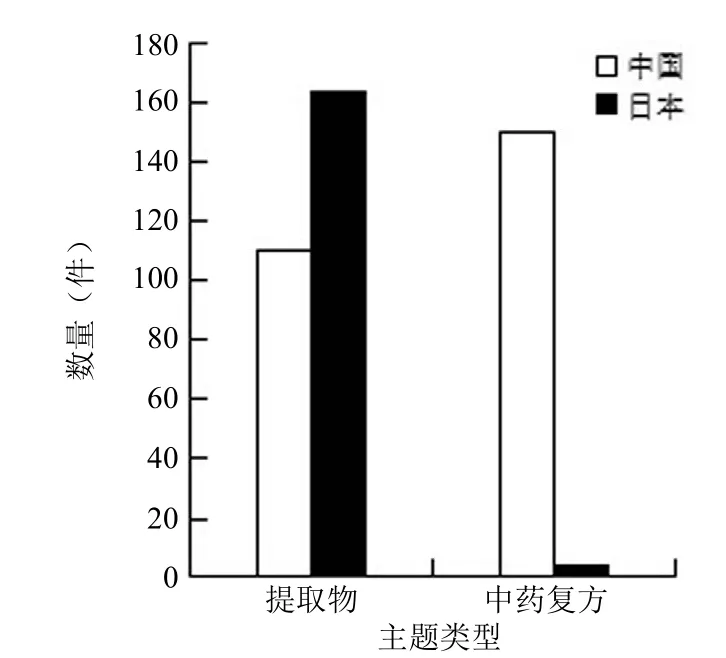
图5 中日两国中药 PCT 申请第一独立权利要求主题分布情况
2.4 权利要求主题
中药产品专利申请主题包括复方、有效部位(提取物)和有效单体(天然来源化合物),以上三者所代表的中药技术水平依次增强。由于一般情况下,有效单体涉及天然药物化学,其研究手段和作用方式更贴近西药(其 IPC 主分类号也为 A61K31 而非 A61K36),故本文统计和分析侧重比较复方和提取物主题。中日两国中药 PCT 申请第一独立权利要求主题分布情况见图 5。经统计,日本在 2009 – 2014年间中药 PCT 申请中复方和提取物主题的申请数目分别为 4 项和 164 项,提取物专利申请占比高达 95.9%。复方申请量低的原因在于日本对汉方药的发明专利保护限于药用植物及其提取物、生物制品、药用植物提取物的组方(只限于中国古代的 210 个汉方,如安中散、芍药甘草汤等),不保护以药用植物本身为原料的中药复方[4]。日本国内专利制度的此种规定也直接影响了日本向外申请专利的主题选择。
与以上数据相对应的,对中国中药 PCT 申请进行统计发现,国内申请的主要主题类型是复方,共 155 项,占比58.5%,其次是提取物,占 39.2%。剔除个人申请,仅针对国内企业申请进一步统计发现,其专利申请中提取物主题占比也仅为 49.7%。
复方制剂最大的缺陷在于有效成分及其结构、作用机制相对复杂,很难用现代科学理论解释各单味药之间的关系和作用,给其规范化、标准化生产带来了很大的困难[5]。欧美等多数发达国家对于复方中药制剂也并不予以认可,其国际化道路任重道远。建议国内申请人在中药研发中利用现代化学和医学手段对中药进行提取分离和疗效验证,同时增加有效成分或有效部位主题专利申请,减少保护范围较为局限且难以规范化、标准化生产实施的复方主题申请,提高我国中药的技术水平和中药专利的科技含量。
2.5 适应证类型
通过对中日两国中药 PCT 申请所针对适应证分布情况进行统计,结果如图 6。
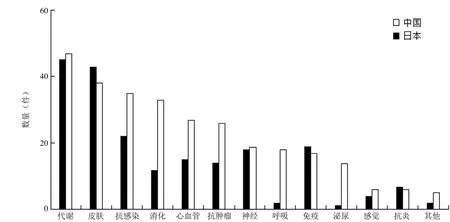
图6 中日两国中药 PCT 申请所针对适应证类型分布情况
通过图 6 发现,中日两国申请针对的适应证类型整体保持一致,而且涉及代谢、皮肤和抗感染这三种疾病类型的专利申请数目在中日两国均排名前三,表明其在针对适应证类型的研发热点上有很大程度的重叠。
涉及代谢、皮肤疾病的专利申请之所以较多,笔者认为主要有以下原因,一方面,以三高(高血压、高血糖、高血脂)等为代表的代谢疾病是当前社会中普遍存在的高流行性疾病,且其慢性病程往往需要持续的药物治疗,市场对于新型治疗药物的需求十分旺盛,且许多中药对于代谢疾病等具有较好的治疗效果;其次,针对代谢、皮肤疾病的防治除可应用于药物领域外,同时也可扩展到美容、保健品等领域,如很多改善皮肤状态的药物都可以应用于化妆品领域,调节血脂、血糖的代谢类药物也可制备成保健品的形式。就日本而言,由于汉方药尚未完全纳入日本的卫生保健系统,还处于西药的补充替代地位,加上《药事法》对于医疗用汉方制剂的严格限制,因此,大量企业转而申请应用广泛、市场巨大且门槛较低的保健品和美容产品,这也造成了针对代谢、皮肤疾病等的专利申请占据主流以及大量日化企业等成为重要申请人。
国内申请人在进行中药研发和 PCT 专利申请时也可参考以上适应性类型分布,一方面,明晰当前的适应证研究热点,并以市场需求为导向进行有针对性的研发;另一方面,针对适应证类型进行适当的中药应用领域扩展,在当前很多中药产品作为药物很难通过外国药政部门的审查而进入世界市场的背景下,基于适应证类型而适当扩展至化妆品、保健品、食品等交叉领域,并由此针对性强化专利布局,也是当前中药走出国门的一种重要途径。
3 结语
专利保护是加强我国中药产业核心竞争力的重要手段,随着与国际中药市场的接轨和中药现代化的发展,可以预期专利将成为我国中药发展的有力武器。本文通过比较分析中日两国中药 PCT 专利申请的整体态势,给出了有关国内专利申请人进行向外申请的一些个人建议,供大家研究参考。
[1] Liu LY. The traditional Chinese medicine protecting under patent. Electron Intellect Property, 2004(10):31-33. (in Chinese)
刘丽英. 专利制度下的中药保护. 电子知识产权, 2004(10):31-33.
[2] Jiang R, Shen AL. The patent protection policy of Japanese herbal medicine and its significance. Chin Med J Res Prac, 2012, 26(2):76-78. (in Chinese)
江茹, 沈爱玲. 日本汉方药的专利保护政策及其借鉴意义. 现代中药研究与实践, 2012, 26(2):76-78.
[3] Guo DH, Xiao SY, Liu TH, et al. Patent analysis of Japanese traditional Chinese medicine in China. Chin J Information Traditional Chin Med, 2008, 15(8):1-3. (in Chinese)
郭德海, 肖诗鹰, 刘铜华, 等. 日本在华中药领域专利分析. 中国中医药信息杂志, 2008, 15(8):1-3.
[4] Wu J, Li X. Analysis of patent policy for natural drugs abroad and its revelation of Chinese materia medica protection in China. Chin Traditional Herbal Drugs, 2010, 41(11):1909-1912. (in Chinese)
吴晶, 李欣. 国外天然药物专利政策分析及对我国中药保护的启示. 中草药, 2010, 41(11):1909-1912.
[5] Zhang YY, Luo AJ. Comparative study on patent information analysis of traditional Chinese medicine at home and abroad. Soft Sci Health, 2009, 23(1):100-103. (in Chinese)
张艳艳, 罗爱静. 基于国内外中药专利信息分析的对比研究. 卫生软科学, 2009, 23(1):100-103.
10.3969/cmba.j.issn.1673-713X.2017.01.018
100190 北京,国家知识产权局专利局专利审查协作北京中心医药部
张芙婧,Email:haohaizi666@126.com
2016-04-20
*同为第一作者
