疑诊肺栓塞患者患病风险评估的新模型
2017-02-11赵洋子苏广胜李卉吴曦子曾仁庆李蕙伊刘畅赵丽徐俊杰崇巍
赵洋子,苏广胜,李卉,吴曦子,曾仁庆,李蕙伊,刘畅,赵丽,徐俊杰,崇巍
(中国医科大学1.附属第一医院急诊科,沈阳 110001;2.附属盛京医院心内科,沈阳 110004;3.附属第四医院心内科,沈阳 110032;4.附属第一医院放射科,沈阳 110001;5.附属第一医院检验医学科,卫生部艾滋病免疫学重点实验室,沈阳 110001)
疑诊肺栓塞患者患病风险评估的新模型
赵洋子1,苏广胜2,李卉3,吴曦子1,曾仁庆1,李蕙伊1,刘畅1,赵丽4,徐俊杰5,崇巍1
(中国医科大学1.附属第一医院急诊科,沈阳 110001;2.附属盛京医院心内科,沈阳 110004;3.附属第四医院心内科,沈阳 110032;4.附属第一医院放射科,沈阳 110001;5.附属第一医院检验医学科,卫生部艾滋病免疫学重点实验室,沈阳 110001)
目的 建立新的肺栓塞(PE)患病风险评估模型,提高肺动脉CTA的阳性检出率。方法 将研究样本中PE患病组和非患病组组间有统计学差异的变量纳入logistic回归分析,构建疑诊PE的患病风险评估模型。根据模型求得的每位患者的患病概率,绘制受试者工作(ROC)曲线并确定截断值。另收集验证样本评价该模型的诊断效能。结果 对研究样本的单因素分析显示,共17个变量在患病和非患病2组间存在统计学差异。其中不明原因的呼吸困难、整条腿肿胀/凹陷性水肿、D⁃二聚体和年龄是患PE的独立危险因素。由ROC曲线确立模型的截断值为0.38。验证样本显示,本研究提出的PE患病风险评估模型可将我院肺动脉CTA阳性检出率从27%提高至54%。结论 新的PE患病风险评估模型可提高肺动脉CTA的检出率。
肺栓塞;患病风险评估模型;肺动脉CTA;D⁃二聚体
肺栓塞(pulmonary embolism,PE)是急诊和住院患者常见的急重症,存在猝死风险。由于PE的临床表现缺乏特异性,典型胸痛、咯血、呼吸困难三联征同时出现的患者十分少见,故其诊断率并不理想[1]。当患者出现难以解释的呼吸困难、胸痛、咯血、心悸、晕厥、背痛等心肺系统表现时,应警惕其罹患PE的可能,将其列为疑诊对象[2⁃3]。诊断PE的金标准是肺动脉造影。肺动脉CTA(computed tomo⁃graphic pulmonary angiography,CTPA)因其高敏感度(83%)和高特异度(96%)在临床上已经替代肺动脉造影[4⁃6]。尽管CTPA的普及使更多的疑诊PE患者得以明确诊断[7⁃8],但是其阳性检出率并未提高,反而存在资源浪费的现象[9],辐射暴露[10]和碘对比剂[11]对健康的影响则要求临床上慎重进行CTPA检查,并且提高CTPA的阳性检出率。因此亟需准确、简单和实用的PE患病风险评估模型,用以筛选需要行CTPA的患者。
1 材料与方法
1.1 研究样本
连续收集2014年2月至6月于中国医科大学附属第一医院行CTPA的疑诊PE患者191例。其中CTPA检查结果显示阳性者70例,阴性者121例。记录与PE有关的病史、症状、体格检查和实验室指标。
1.2 验证样本
按样本量计算公式计算验证样本所需样本量,另收集2016年1月至2月就诊于中国医科大学附属第一医院行CTPA的疑诊PE患者106例。其中CT⁃PA检查结果显示阳性者29例,阴性者77例,记录相关指标。
1.3 统计学分析
所有数据输入Excel 2013,采用SPSS 22.0软件进行统计学分析。正态分布的计量资料以x±s表示,组间比较采用t检验;非正态分布的计量资料以中位数(四分位数间距)表示,组间比较采用非参数秩和检验。模型构建采用logistic回归分析。绘制受试者工作(receiver operating characteristic curve,ROC)曲线,得出截断值。计算准确度、敏感度、特异度、漏诊率、误诊率、阳性预测值和阴性预测值以评价模型的诊断效能。
2 结果
2.1 PE患病风险评估模型的建立
2.1.1 PE患病危险因素的单因素分析:将研究样本中的191例疑诊PE患者按其CTPA检查结果分为阳性(70例)与阴性(121例)2组。比较2组间有关病史、症状、体格检查和实验室指标,P<0.2为差异有统计学意义。结果显示,在CTPA检查结果阳性和阴性2组患者中,不明原因呼吸困难、单侧下肢腓肠肌疼痛或肿胀、整条腿肿胀/凹陷性水肿、反常的心动过缓、高血压、冠心病、急性心肌梗死、肾病综合症、近期创伤或骨折、因各种原因的制动/长期卧床>3 d、妊娠/产褥期、植入人工假体(髋关节或膝关节置换)、年龄、休克指数、心率及血D⁃二聚体有统计学差异,见表1。
2.1.2 Logistic回归分析和模型构建:将上述17个2组间有统计学差异的因素纳入logistic回归分析,性别变量尽管与患病无关,但同时作为变量强制纳入回归分析,使用逐步法构建模型,P<0.05为差异有统计学意义。结果显示,不明原因的呼吸困难、整条腿肿胀/凹陷性水肿、D⁃二聚体和年龄为PE患病的独立危险因素。见表2。据此建立PE患病风险评估模型,患病概率P的计算方法如下:P=ExpA/(1+ExpA),A=0.793×不明原因的呼吸困难+1.677×整条腿肿胀/凹陷性水肿+0.134×D⁃二聚体-0.025×年龄-0.281。上述模型中不明原因的呼吸困难、整条腿肿胀/凹陷性水肿取0(无)或1(有),D⁃二聚体、年龄取其数值部分,0.281为常数项。
2.1.3 患病风险评估模型中患病概率P的截断值确定:计算研究样本中的患者的患病概率值P,对其绘制ROC曲线,见图1。曲线下面积为0.776(95%CI:0.708~0.845),截断值取0.38,敏感度为0.726,特异度为0.744。如果P>0.38,则认为该患者患PE高风险,本研究样本中共有83例,实际CTPA阳性率62%;反之,若P<0.38,则为低风险,共108例,阳性率18%。
2.2 PE患病风险评估模型的评价
验证样本为疑诊PE的106例,其中29例CTPA阳性,CTPA的阳性检出率为27%。如表3所示,将验证样本中的患者按患病概率P的截断值分为高风险和低风险2组,与CTPA结果进行比较,计算出不同截断值下PE患病风险评估模型的准确度、敏感度、特异度、阳性预测值及阴性预测值。当患病概率(P)的截断值取0.38时,模型的准确度和阳性预测值最高,诊断效能最优,可将我院CTPA的阳性检出率从上述的27%提高至54%。
3 讨论
MINIATI等[12]利用和本研究类似的方法,建立了预测疑诊PE患者患病概率的模型Pisa评分。该模型中的变量共有16个,模型的ROC曲线下面积为0.88,而本研究模型则为0.776,这可能与本研究的样本量较少有关。尽管MINIATI等[13]在其建立Pisa模型的一系列前期研究的基础上,摒弃了胸部影像学表现,但其中仍包含诸如心电图改变、血气分析结果、肺部啰音、心脏杂音等比较主观或容易受环境影响的指标,这些指标的缺点是难以标准化。与此类似,LE GAL等[14]剔除掉Geneva评分血气分析和胸部影像学表现这2个难以标准化的指标,提出了改良Geneva评分。本研究尤其关注到这一点,纳入的与PE有关的症状、体征和实验室检查结果都比较客观[15]。
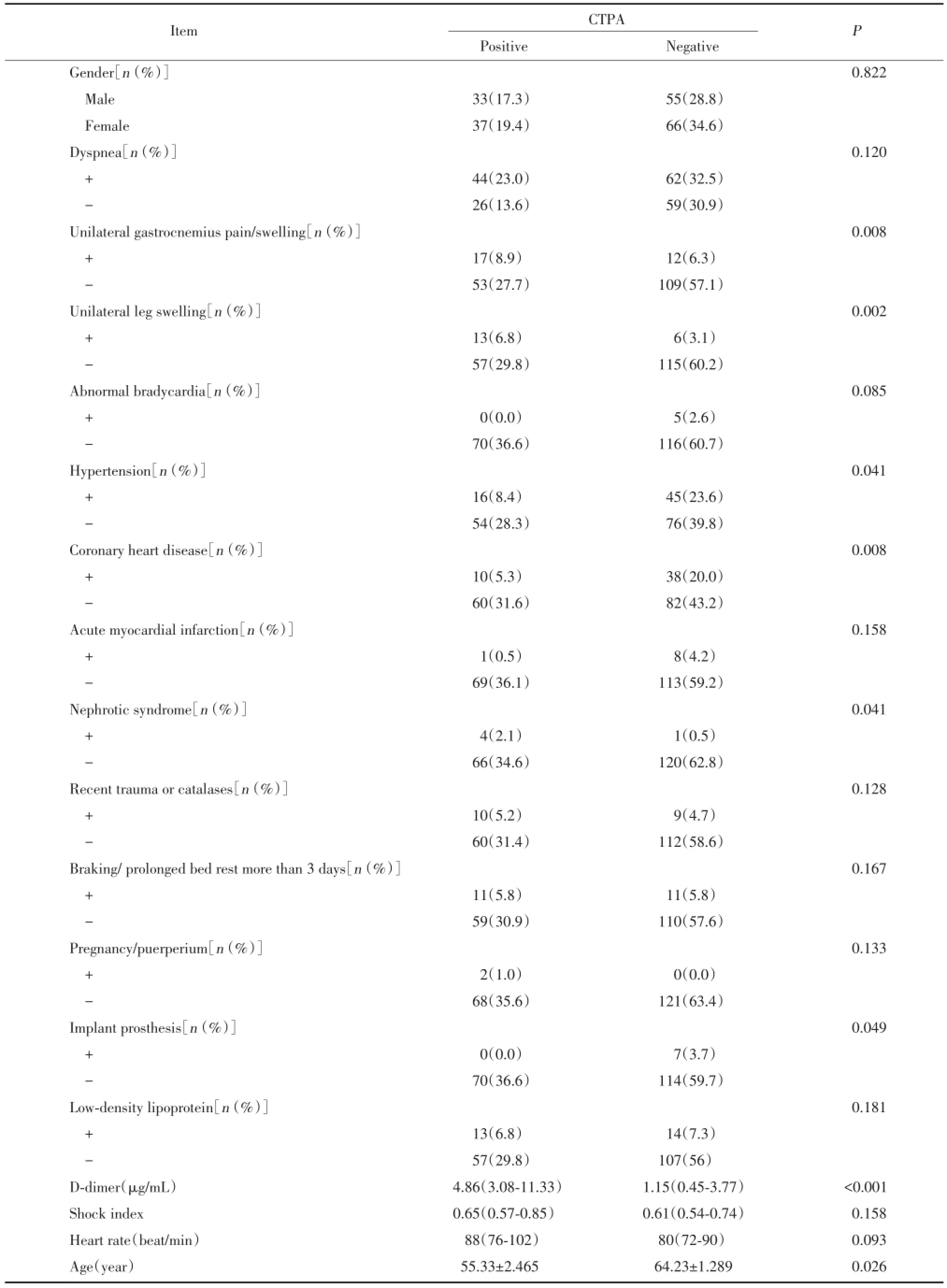
表1 疑诊PE患者的临床表现之单因素分析Tab.1 Basic characters of suspected patients with univariate analysis
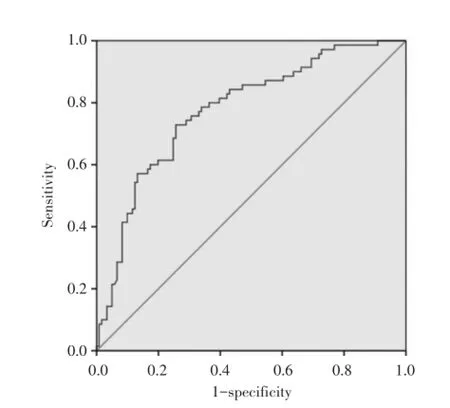
图1 风险评估模型的ROC曲线Fig.1 ROC of prediction model of the clinical probability
目前临床常用的PE患病风险评估模型,如Wells评分、Geneva评分,只引入了患者的症状和体征而没有实验室检查指标。因此,欧洲心脏病学会或美国医师协会推荐的急性PE诊断流程中,均需要在上述PE患病风险模型基础上,结合实验室检查D⁃二聚体,对PE的风险进行两步评估。而本研究提出的患病风险评估模型直接将不明原因呼吸困难(症状)、单侧腿肿(体征)和D⁃二聚体(实验室检查)一步纳入,使患病风险的评估过程得以简化,便于判断疑诊患者是否需要进一步行CTPA检查。具体来说,应用本研究提出的新模型计算患者的患病概率P,如果P>截断值0.38,则推荐患者行CTPA检查。临床医生可在电脑上方便地使用该模型进行计算,获得疑诊PE患者的年龄、D⁃二聚体、是否存在不明原因的呼吸困难和整条腿肿胀/凹陷性水肿等参数,就可做出是否推荐CTPA检查的临床决策。
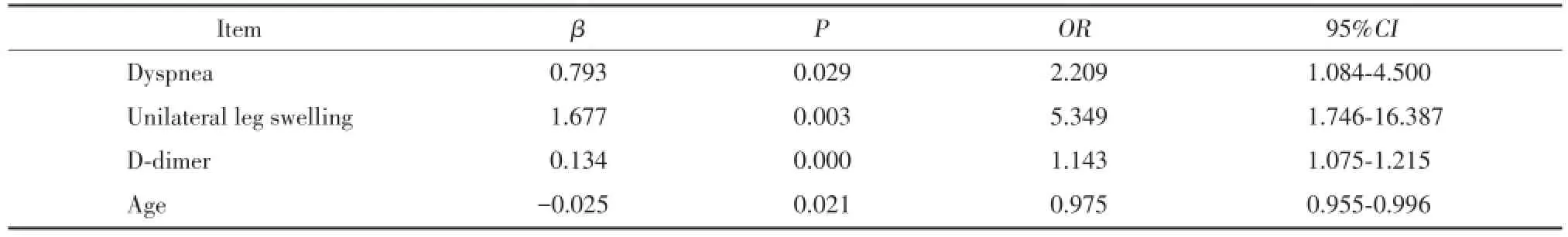
表2 评估PE患病风险的logistic回归模型Tab.2 Logistic regression model for risk prediction of suspected patients
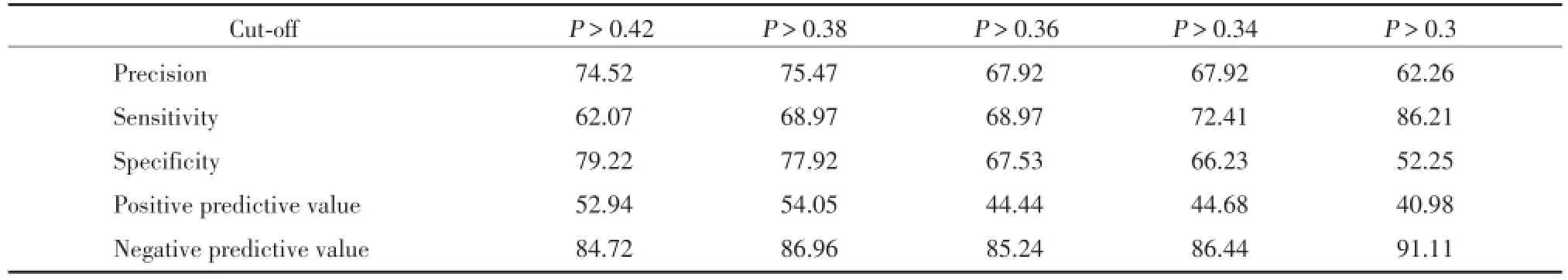
表3 不同截断值下PE患病风险评估模型的诊断效能对比(%)Tab.3 The diagnostic efficiency evaluations of different cut⁃off values(%)
本研究属于回顾性研究,在收集患者资料时不可避免地会出现信息不全的问题,从而丢失了部分病例,以至于模型构建时的研究样本样本量相对较少。本研究建立的PE患病风险评估模型简化了PE诊断流程,改善了患者对临床医生的依从性,提高了CTPA的检出率,尤其适于在急诊科应用。
[1]CHUNILALl SD,EIKELBOOM JW,GINSBERG JS,et al.Does this patient have pulmonary embolism?[J].JAMA,2003,290(21):2849-2958.DOI:10.1001/jama.290.21.2849.
[2]KONSTANTINIDES SV,TORBICKI A,AGNELL G,et al.2014 ESC Guidelines on the diagnosis and management of acute pulmo⁃nary embolism[J].Eur Heart J,2014.35(45):3145-2146.DOI:10.1093/eurheartj/ehu393.
[3]RAJA AS,GREENBERG JO,SCHUUR JD,et al.Evaluation of pa⁃tients with suspected acute pulmonary embolism:best practice ad⁃vice from the clinical guidelines committee of the american college of physicians[J].Ann Intern Med,2015.163(9):701-711.DOI:10.7326/M14⁃1772.
[4]ENG J,KRISHNAN JA,BASS EB,et al.Accuracy of CT in the diag⁃nosis of pulmonary embolism:a systematic literature review[J].Am J Roentgenol,2004,183(6):1819-1827.DOI:10.2214/ajr.183.6.01 831819.
[5]MAYO JY,THAKUR Y.Pulmonary CT angiography as first⁃line im⁃aging for PE:image quality and radiation dose considerations[J]. Am J Roentgenol,2013,200(3):522-528.DOI:10.2214/ajr.12.99 28.
[6]PINES JM,LESSLER AL,MARK COURTNEY D,et al.The mortal⁃ity benefit threshold for patients with suspected pulmonary embolism[J].Acad Emerg Med,2012,19(9):E1109-E1113.DOI:10.1111/ j.1553⁃2712.2012.01432.x.
[7]BOONE JM,BRUNBERG JA.Computed tomography use in a tertia⁃ry care university hospital[J].J Am Coll Radiol,2008,5(2):132-138.DOI:10.1016/j.jacr.2007.07.008.
[8]FANIKOS J,RAO A,GOLDHABER SZ,et al.Hospital costs of acute pulmonary embolism[J].Am J Med,2013,126(2):127-132. DOI:10.1016/j.amjmed.2012.07.025.
[9]HALL WB,TRUITT SG,CARSON SS,et al.The prevalence of clini⁃cally relevant incidental findings on chest computed tomographic an⁃giograms ordered to diagnose pulmonary embolism[J].Arch Intern Med,2009,169(21):1961-1965.DOI:10.1001/archinternmed. 2009.360.
[10]JR ESA,BUTLER PF,APPLEGATE KE,et al.American college of radiology white paper on radiation dose in medicine[J].J Am Coll Radiol,2007,4(5):272-284.DOI:10.1016/j.jacr.2007.03. 002.
[11]SIKKENS JJ,BEEKMAN DG,SMULDERS YM,et al.How much overtesting is needed to safely exclude a diagnosis?A different per⁃spective on triage testing using bayes’theorem[J].PLoS One,2016,11(3):e0150891.DOI:10.1371/journal.pone.0150891.
[12]MINIATI M,BOTTAI M,PASSERA M,et al.Simple and accurate prediction of the clinical probability of pulmonary embolism[J]. Am J Respir Crit Care Med,2008,178(3):290-294.DOI:10.1164/rccm.200802⁃207OC.
[13]MINIATI M,MONTI S,BOTTAI M,et al.A structured clinical model for predicting the probability of pulmonary embolism[J]. Am J Med,2003,114(3):173-179.
[14]LE GAL G,RIGHINI M,PERRIER A,et al.Prediction of pulmo⁃nary embolism in the emergency department:the revised Geneva score[J].Ann Intern Med,2006,144(3):165-171.
[15]SUZUKI T,LYON A,SAGGAR R,et al.Biomarkers of acute car⁃diovascular and pulmonary diseases[J].Eur Heart J Acute Cardio⁃vasc Care,2016,5(5):416-433.DOI:10.1177/204887261665230 9.
(编辑 于 溪)
A New Risk Assessment Model for Suspected Pulmonary Embolism
ZHAO Yangzi1,SU Guangsheng2,LI Hui3,WU Xizi1,ZENG Renqing1,LI Huiyi1,LIU Chang1,ZHAO Li4,XU Junjie5,CHONG Wei1
(1.Department of Emergency Medicine,The First Hospital,China Medical University,Shenyang 110001,China;2.Departmen of Cardiology,Shengjing Hospital,China Medical University,Shenyang 110004,China;3.Departmen of Cardiology,The Fourth Affiliated Hospital,China Medical University,Shenyang 110032,Chi⁃na;4.Radiology,The First Hospital,China Medical University,Shenyang 110001,China,5.Key Laboratory of AIDS Immunology of Ministry of Health,Department of Laboratory Medicine,The First Hospital,China Medical University,Shenyang 110001,China)
Objective To develop a predictive model for pulmonary embolism(PE)based on the related clinical symptoms,signs,and the labo⁃ratory index,so as to improve the positive rate of CTPA.Methods The model was developed from a database of 119 patients with suspected PE. The risk factors of suspected PE were analyzed by logistic regression analysis,which included significant differences in the prevalence of PE be⁃tween non⁃diseased and non⁃diseased groups.Receiver operating characteristic(ROC)curves was draw to determine the cut⁃off value of the clini⁃cal probability.It was validated in an independent sample of 106 patients with suspected PE.Results According to the univariate analysis,17 of 51 variables show a significant difference between PE and non⁃PE patients.The model comprised 4 variables:age,dyspnea,D⁃dimer and unilater⁃al leg swelling.The area under the ROC curve is 0.776,and the cut⁃off value is supposed to be 0.38.In the validation sample,27%patients had PE confirmed by CTPA.The prevalence of PE was 54%when the clinical probability was above 0.38.Conclusion The proposed predictive mod⁃el in this study can improve the positive rate of CTPA,simplify the diagnosis process of suspected PE patients.
pulmonary embolism;prediction model of the clinical probability;computed tomographic pulmonary angiography;D⁃dimer
R447
A
0258-4646(2017)03-0266-04
10.12007/j.issn.0258⁃4646.2017.03.019
赵洋子(1990-),女,硕士研究生.
崇巍,E-mail:chongweixiena@126.com
2016-09-07
网络出版时间:
