激素反添加法在GnRHa治疗EMS中的疗效及安全性
2017-01-20王越凤刘高焰
王越凤,刘高焰,陈 涛
(四川省彭州市人民医院,四川 彭州 611930)
激素反添加法在GnRHa治疗EMS中的疗效及安全性
王越凤,刘高焰,陈 涛
(四川省彭州市人民医院,四川 彭州 611930)
目的 探讨促性腺激素释放激素激动剂(GnRHa)联合激素反添加法在治疗子宫内膜异位症(EMS)中的有效性及安全性。方法将2012年1月至2013年7月经彭州市人民医院诊治并确诊为子宫内膜异位症的患者共计108例随机分入反添加组和单用组,每组各54例,比较两组患者治疗前后或月经来潮后Kupperman评分、绝经症状、激素水平、骨密度及VAS评分上的差异。结果治疗末,两组患者Kupperman评分均有不同程度上升,但反添加组上升程度低于单用组,差异具有统计学意义(t=7.332,P<0.01),且反添加组绝经症状以潮热改善为主;在激素水平上,反添加组雌二醇(E2)水平(22.62±10.42)pg/mL略高于单用组(14.35±7.42)pg/mL,促卵泡激素(FSH)水平(2.41±0.93)mIU/mL略低于单用组(5.23±1.89)mIU/mL;此外,反添加组治疗前后骨质无明显流失,而单用组在左髋部、腰椎L1~4骨质流失较为明显(t左髋部=10.445、t腰椎L1~4=5.531,均P<0.05);另外,对于痛经、盆腔痛、性交痛等疼痛指标,反添加组改善效果优于单用组。结论GnRHa联合激素反添加法在治疗子宫内膜异位症时,不仅可使部分激素水平处于有效治疗窗内,减少绝经症状的发生,同时还有助于延缓骨质流失,减少疼痛症状,从而提高患者服药依从性及治疗效果,值得临床推广应用。
子宫内膜异位症;促性腺激素释放激素激动剂;反加法;骨密度
子宫内膜异位症(endometriosis,EMS)是指具有生长功能的子宫内膜于子宫内膜腔外位置进而引发疼痛、月经异常、不孕等临床症状,其多见于育龄女性,发病率约占该人群2%~5%[1],是妇科常见病之一。目前,鉴于尚未完全明确该病的发病机制,故根据其临床表现及治疗特征多将其归为雌激素依赖性疾病进行治疗。因此,药物治疗仍是对该病的有效治疗措施,其中因促性腺激素释放激素激动剂(gonadotropin-releasing hormone agonist,GnRHa)的治疗效果显著而在临床上大量应用。但近年来临床资料证实,长时间给予GnRHa可引发低激素血症、骨丢失等副作用[2],因此,如何在不影响治疗效果的情况下,减少因药物过量引发的毒副作用成为目前研究的重点之一。目前基于GnRHa的反添加法,通过GnRHa联合其他药物使用,在不影响药效的前提下,可有效地减少GnRHa用量,从而降低毒副作用发生概率[3];但对于GnRHa的反添加法具体治疗措施仍缺乏公共标准,对治疗的有效性及安全性尚缺乏大量的临床数据,因此,本研究通过比较单用GnRHa与采用反添加法GnRHa的治疗效果,为更好地临床应用提供理论及实际依据。
1 资料与方法
1.1 一般资料
选取2012年1月至2013年7月间在彭州市人民医院妇产科就诊并经手术治疗确诊为子宫内膜异位症(巧克力囊肿)患者108例,患者年龄22~48岁,平均年龄(32.4±4.2)岁。依据美国生育协会修订的内膜异位症分期(Revise American Fertility Society,RAFS)病例均为Ⅲ~Ⅳ期。纳入标准:①暂无生育要求;②治疗前3个月未进行任何激素治疗;③无严重的肝肾心等疾病;④无免疫系统疾病;⑤患者均保留子宫,采取一侧或双侧异位囊肿剥离术;⑥患者自愿加入研究并签署知情同意书。采用随机分组法,将108例分入GnRHa单用组和GnRHa反添加组,每组54例,其中GnRHa单用组患者年龄23~47岁,平均年龄(32.1±4.3)岁,RAFS:Ⅲ级26例,Ⅳ级28例,RAFS评分29.8±8.4;GnRHa反添加组患者年龄22~48岁,平均年龄(32.0±4.4)岁,RAFS:Ⅲ级27例,Ⅳ级27例;RAFD评分29.4±8.5。两组患者的年龄、RAFS评分比较差异均无统计学意义(t年龄=1.233;tRAFS=1.315,均P>0.05),可纳入统计分析。
1.2 方法
两组患者均采取保留子宫治疗,并与术后3~5天或月经周期1~2天皮下注射醋酸曲谱瑞林3.75mg(进口注册号:H20110290),间隔28日注射1次,共注射3次;反添加组每日睡前服用戊酸雌二醇片1mg/d(国药准字:J20080036)和醋酸甲羟孕酮片4mg/d(国药准字:H33020715)。分别于患者术前、用药后3个月末以及月经来潮后对其进行相应随访及检查。
1.3 评估标准
1.3.1 更年期综合征严重程度评分
更年期综合征严重程度评分(Kupperman)用于测定患者在治疗末期低雌激素状态下的绝经症状情况,包括潮热、乏力、失眠、骨痛、性生活及情绪波动,6项加合即为总分,分值越高代表患者症状越明显。
1.3.2 激素测定
采用放射免疫法分别于治疗前和治疗后12周对患者促卵泡激素(follicle stimulating hormone,FSH)、促黄体生成素(luteinizing hormone,LH)、血清雌二醇(serum estradiol,E2)进行检测。
1.3.3 骨密度检测
采用Hologic公司的双能X线骨密度仪(型号:Discovery Wi)分别于治疗前及治疗后检测患者左髋部、左股骨颈、腰椎L1~4的骨密度。
1.3.4 视觉疼痛量表评定
于治疗前、治疗后、月经复潮后,采用视觉疼痛量表(VAS)评估痛经、盆腔疼痛及性交痛的程度,具体方法如下:选取一根标有刻度的标尺,依次由0标记到10,其中0为无痛,10为剧痛,由患者根据自己疼痛情况选着合适疼痛数值。
1.4 统计学方法
2 结果
2.1 两组更年期综合征严重程度评分情况
单用组与反添加组患者治疗前Kupperman评分比较差异无统计学意义(P>0.05);治疗后,单用组与反添加组Kupperman评分比较差异有统计学意义(P<0.01);且反添加组治疗前后Kupperman评分比较差异无统计学意义(P>0.05),见表1。
两组患者绝经症状得分显示,只有治疗后潮热症状比较差异有统计学意义(P<0.05),见表2。
两组患者在治疗末期各项绝经症状发生率中,单用组各项发生率均高于反添加组,但仅潮热症状发生率在两组间存在差异(P<0.01),见表3。
表1 两组患者治疗前后Kupperman得分情况
表2 两组患者绝经症状得分情况分析
(转下表)

(续上表)

表3 两组患者绝经症状发生情况分析[n(%)]
2.2 两组患者激素检测情况
治疗后,两组患者的FSH、LH、E2检测结果均较治疗前有明显下降,且组内比较差异均存在统计学意义(均P<0.01),两组患者的FSH和E2指标中存在组间差异(均P<0.05),见表4。
表4 两组患者激素检测结果分析
2.3 两组骨密度测量情况
两组患者治疗前后的左髋部、左股骨颈、腰椎L1~4处骨密度比较,反添加组治疗前后骨密度无明显降低(t左髋部=0.443、t左股骨颈=0.534、t腰椎L1~4=0.663,均P>0.05);单用组患者左髋部、腰椎L1~4较治疗前骨丢失严重,且单用组治疗前后比较差异均有统计学意义(t左髋部=10.445,P<0.01;t腰椎L1~4=5.531,P<0.05),而左股骨颈治疗前后差异无统计学意义(t左股骨颈=1.219,P>0.05),见表5。
2.4 视觉疼痛量表评分情况
治疗后两组各项疼痛检测值均有所改善,且组内治疗前后比较差异均有统计学意义(均P<0.05)。治疗末,反添加组改善效果即优于单用组(均P<0.01)。此外,单用组患者在月经来潮后,其治疗效果与治疗前比较差异存在明显统计学意义(P<0.01),见表6。
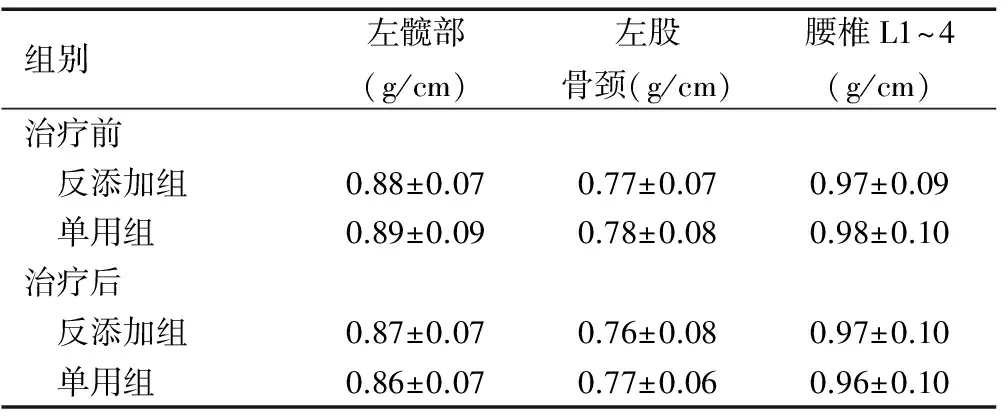
表5 两组患者治疗前后骨密度丢失情况分析
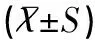
表6 两组患者各项VAS疼痛评分比较结果
注:治疗末,两组患者均存在闭经,故未统计痛经情况;反添加组4人,单用组4人均为未婚女性,未参与性交痛及疼痛总分统计;组内比较*P<0.05,**P<0.01,组间比较ΔP<0.05。
3 讨论
3.1 促性腺激素释放激素激动剂的研究现状
1982年,Meldrum等首次报道了GnRHa可用于子宫内膜异位症的治疗,因该药物相对于天然GnRH具有更高的亲和力及较长的半衰期在临床上获得大量应用。研究证实,GnRHa的使用可营造低雌激素环境致异位内膜萎缩,并有助于异位内膜细胞凋亡,减少异位细胞血管内皮生长因子表达及炎症介质的释放,从而抑制异位细胞生长,改善患者腹腔内微环境,进而缓解患者痛经、盆腔疼痛、性交痛等临床症状[4],提高了患者的生活质量,但药物的副作用在一定程度上限制了其应用。有研究发现,连续使用GnRHa 3~5周后,部分患者外周血中E2下降,其临床表现主要为潮热、性欲减退、头疼、失眠等症状;同时骨质丢失也是该药常见副作用之一[5],这些因素正是导致患者用药依从性差的主要原因。因此,为有效避免长时间大剂量的使用该药物,有学者提出在GnRHa的使用过程中联合激素的反添加法[6],其为基于不同组织对于激素存在不同的敏感性,通过调整给药浓度,选择既不刺激内膜细胞生长,还能有效抑制骨流失,达到合理的给药剂量及给药周期[7],从而有效减少了药物副作用的发生。
3.2 促性腺激素释放激素激动剂反添加法的优势
本研究显示,GnRHa反添加法在治疗效果上并不差于单独使用GnRHa,但在并发症的发生率上,前者明显少于后者,提示前者具有较高的疗效及安全性。两组患者Kupperman评分均有不同程度上升,但反添加组上升程度低于单用组。本资料中对于最为关注的低激素血症及骨密度流失情况显示,两组激素水平均有一定程度下降,但在E2水平上,反添加组下降幅度低于单用组,而在FSH水平上前者下降幅度高于后者。目前临床长期大量使用GnRHa后可出现诸如低雌激素血症,并表现出潮热、性欲减退,头疼等症状,而人为给予补充剂量雌激素可在一定程度上缓解低激素水平所引起的各种症状,但并不能完全克服因雌激素分泌不足所引起生理表现。此外,本资料还显示治疗前后的左髋部、左股骨颈、腰椎L1~4处骨密度检测结果,反添加组相对于单用组更能有效避免患者骨密度流失(均P<0.05),这与雌激素可直接作用于成骨细胞受体,并抑制破骨细胞具有直接的相关性,从而增加骨量合成并减少骨量丢失。另外还发现,采用反添加法的患者在痛经、盆腔疼痛、性交痛方面的改善效果优于单独用药患者,且疼痛总分明显低于后者(均P<0.05)。由于GnRHa在治疗过程中的副作用主要是由患者体内雌激素水平显著下调所致,因此采用激素反添加法在一定程度上可起到维持体内激素水平,缓解GnRHa药物的副作用。但是,鉴于EMS本身是一种雌激素依赖性疾病,若过量使用雌激素仍可能加剧病灶的发展,从而出现疗效降低的情况。因此,若能在治疗的同时,对患者雌激素水平进行持续监测,并根据监测结果,适当调整给药剂量及周期,则将有助于减少GnRHa药物的副作用,但这仍需要大量的临床数据支持。
综上所述,采用GnRHa联合激素反添加法可在不减低治疗效果的前提下,有效减轻患者潮热等更年期症状,并有助于提高患者生活质量,减少骨质流失,提高用药依从性,具有较高的安全性及治疗效果,值得临床推广应用。
[1]Vieille P, Masia F, Donici I,etal.A case of digestive occlusion on an endometriosis lesion after treatment by GnRH agonist[J].J Gynecol Obstet Biol Reprod (Paris),2012,41(7):668-671.
[2]张绍芬.促性腺激素释放激素激动剂治疗与骨量丢失[J].中国实用妇科与产科杂志,2014,30(5):326-329.
[3]牛子儒,岳晓静,孔群钰,等.反加疗法在促性腺激素释放激素激动剂治疗内异症中减缓骨量流失的荟萃分析[J].中华妇产科杂志,2013,48(5):338-343.
[4]Imamura T, Khan K N, Fujishita A,etal.Effect of GnRH agonist therapy on the expression of human heat shock protein 70 in eutopic and ectopic endometria of women with endometriosis[J].Eur J Obstet Gynecol Reprod Biol,2014,180:16-23.
[5]Nirgianakis K, Bersinger N A, McKinnon B,etal.Regression of the inflammatory microenvironment of the peritoneal cavity in women with endometriosis by GnRHa treatment[J].Eur J Obstet Gynecol Reprod Biol,2013,170(2):550-554.
[6]何永珍,坑艳,许旭.促性腺激素释放激素激动剂联合反向添加疗法治疗子宫内膜异位症的临床疗效研究[J].中国全科医学,2011,14(17):1914-1916.
[7]吴德斌,洪莉,洪莎莎,等.反向添加疗法治疗子宫内膜异位症疗效的Meta分析[J].实用妇产科杂志,2013,29(1):25-29.
[专业责任编辑:杨文方]
Efficacy and safety of hormone anti-add method in GnRHa for treatment of endometriosis
WANG Yue-feng, LIU Gao-yan, CHEN Tao
(People’sHospitalofPengzhouCity,SichuanPengzhou611930,China)
Objective To discuss the efficacy and safety of gonadotropin-releasing hormone agonist (GnRHa) combining hormone anti-add method in the treatment of endometriosis (EMS). Methods From January 2012 to July 2013 totally 108 cases of EMS confirmed in People’s Hospital of Pengzhou City were randomly divided into anti-add method group and single therapy group with 54 cases in each. Comparison was made between two groups in Kupperman score before and after treatment or after menstrual onset, menopausal symptoms, hormone levels, bone density, and scores on VAS. Results At the end of treatment, Kupperman increased to various degrees in both groups. The extent of increase in the anti-add method group was less than single therapy group with significant difference (t=7.332,P<0.01), and the dominant improvement was hot flushes in the former group. Considering hormone levels, E2level in anti-add method group (22.62±10.42) pg/mL was slightly higher than that of single therapy group (14.35±7.42) pg/mL, and FSH level (2.41±0.93) mIU/mL was slightly lower than that of single therapy group (5.23±1.89) mIU/mL. In addition, the anti-add method group had no significant bone loss, while bone loss was significant in left hip and L1-4 lumbar spine in single therapy group (tvalue was 10.445 and 5.531, respectively, bothP<0.05). For improvement of pain indexes such as dysmenorrhea, pelvic pain and sexual pain, anti-add method group obtained better results.Conclusion In the treatment of EMS, GnRHa combining hormone anti-add method can not only keep some hormone levels within therapeutic window and reduce the incidence of menopausal symptoms, but also help to slow down bone loss and reduce pain. Thereby it can improve patients’ medication compliance and treatment efficacy, and it is worthy of clinical application.
endometriosis (EMS); gonadotropin-releasing hormone agonist (GnRHa); anti-add method; bone mineral density (BMD)
2015-05-08
王越凤(1981-),女,主治医师,主要从事妇科临床工作。
刘高焰,副主任医师。
10.3969/j.issn.1673-5293.2016.06.026
R711.71
A
1673-5293(2016)06-0748-04
