妇痛宁颗粒质量标准研究
2017-01-16石云,金华
石 云,金 华
(1.天津中新药业集团股份有限公司红桥分公司,天津 300090; 2.天津中医药大学,天津 300193)
妇痛宁颗粒质量标准研究
石 云1,金 华2*
(1.天津中新药业集团股份有限公司红桥分公司,天津 300090; 2.天津中医药大学,天津 300193)
目的:建立妇痛宁颗粒质量标准。方法:采用薄层色谱法对方中赤芍、丹参、肉桂进行定性鉴别;采用高效液相色谱法对丹酚酸B进行含量测定。色谱柱为Agilent Eclipse Plus-C18(100 mm×4.6 mm,3.5 μm),流动相为甲醇-甲酸-水-乙腈(28∶1∶61∶10),流速为1.0 ml/min;柱温为25 ℃。 结果:薄层色谱中的特征斑点明显,重现性好,无干扰;丹酚酸B在0.258 4~155.04 μg范围内线性关系良好(r=0.999 9),平均回收率为99.43%, RSD为1.25%。 结论:本法专属性强、准确、快速,可用于妇痛宁颗粒的质量控制。
妇痛宁颗粒,丹酚酸B,高效液相色谱法,薄层色谱法
妇痛宁颗粒由丹参、肉桂、赤芍、皂角刺、川楝子、三棱等中药精制而成,具有活血化瘀、温经止痛之效,临床用于子宫内膜异位症、痛经、子宫肌瘤、附件炎等症,疗效突出。方中丹参为君药,具有活血祛瘀、通经止痛、清心除烦、凉血消痈之功[1]。为更好地控制产品质量,笔者采用薄层色谱法对方中赤芍、丹参、肉桂进行了鉴别,采用高压液相色谱法对丹酚酸B进行了含量测定。
1 仪器与试药
1.1 仪器 JYO2G型凝胶成像仪(北尔君意东方电泳设备有限公司);硅胶G薄层板;硅胶GF254薄层板(均青岛海洋化工厂出品);Agilent Technologies 1260 Infinity 高效液相色谱仪;XP205型十万分之一天平(METTLER TOLEDO公司);JD400-3型万分之一天平(沈阳龙腾电子有限公司)。
1.2 试药 芍药苷对照品(批号110736-201337,中国食品药品检定研究院);丹酚酸B对照品(批号120923-201113,中国食品药品检定研究院);桂皮醛对照品(批号121363-201102,中国食品药品检定研究院);妇痛宁颗粒(批号1411014、1402004、1309011,某医院制剂室);乙醇、三氯甲烷、乙酸乙酯、甲苯、乙醚、无水乙醇、正己烷、冰醋酸、香草醛硫酸、盐酸均为分析纯;甲醇、甲酸、乙腈均为色谱纯(天津康科德科技有限公司)。超纯水自制。
2 薄层色谱鉴别方法与结果
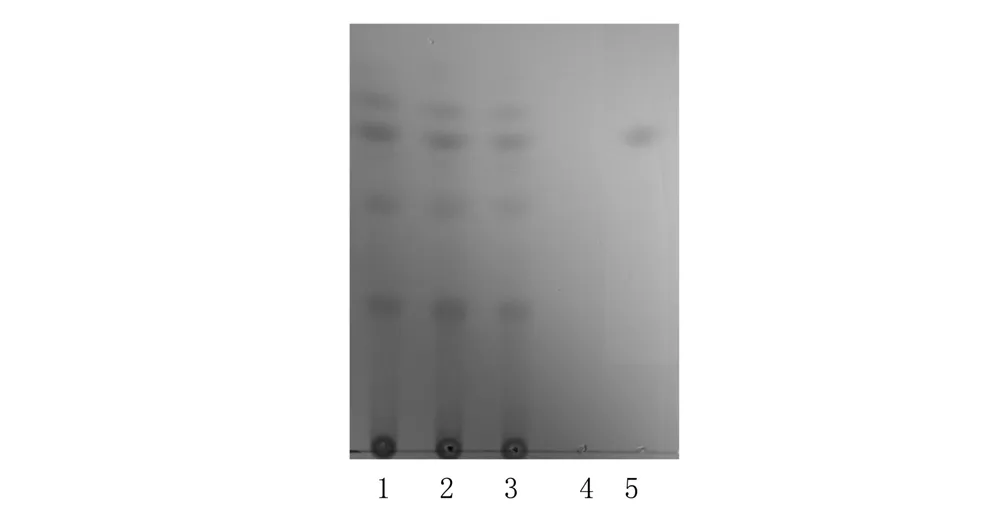
2.1 赤芍鉴别 取本品20 g,加乙醇70 ml,超声10 min,滤过,滤液蒸干,残渣加乙醇5 ml使溶解,作为供试品溶液。另取芍药苷对照品,加乙醇制成1 ml含2 mg的溶液,作为对照品溶液。根据处方比例,称取除赤芍外的其余药材,按颗粒剂的制备工艺制成阴性样品,同供试品溶液的制备方法制成无赤芍的阴性对照溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述两种溶液各4 μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱对应的位置上显相同颜色的斑点。结果见图1。

1.阴性对照 2.芍药苷对照品 3~5.供试品
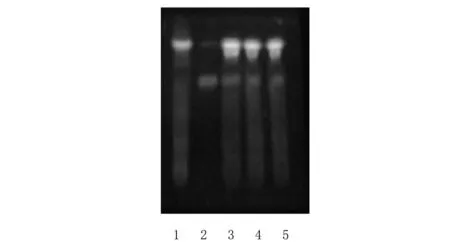
2.2 丹参鉴别 取本品20 g,加乙醇50 ml,超声处理50 min,离心,取上清液作为供试品溶液。另取丹酚酸B对照品溶液。根据处方比例,称取除丹参外的其余药材,按颗粒剂的制备工艺制成阴性样品,同供试品溶液的制备方法制成无丹参的阴性对照溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取上述两种溶液各6 μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲苯-甲酸-甲醇(1.5∶2∶1∶10.1)为展开剂,展开,取出,晾干,置紫外光灯(365 nm)下检视。供试品色谱中,在与对照品色谱对应的位置上显相同颜色的荧光斑点。结果见图2。
1~3.供试品 4.阴性对照 5.丹酚酸对照品
2.3 肉桂鉴别 取本品20 g,加乙醇30 ml,冷浸30 min,时时振摇,滤过,滤液作为供试品溶液。另取桂皮醛对照品,加乙醇制成1 ml含1 μg的对照品溶液。根据处方比例,称取除肉桂外的其余药材,按颗粒剂的制备工艺制成阴性样品,同供试品溶液的制备方法制成无肉桂的阴性对照溶液。照薄层色谱法(《中国药典》2015年版四部通则0502)试验,吸取供试品溶液10 μl,对照品溶液4 μl分别点于同一硅胶GF254薄层板上,以正己烷-乙醚-冰醋酸(5∶5∶0.1)为展开剂,展开,取出,晾干,置紫外光灯(254 nm)下检视。供试品色谱中,在与对照品色谱对应的位置上显相同颜色的斑点。结果见图3。
1.阴性对照 2.桂皮醛对照品 3~5.供试品
3 丹酚酸B含量测定
3.1 色谱条件 C18(100 mm×4.6 mm,3.5 μm)色谱柱;流速1.0 ml/min;柱温:25 ℃;进样量:10 μl。流动相:甲醇-甲酸-水-乙腈(28∶1∶61∶10);检测波长:286 nm。
3.2 溶液制备
3.2.1 对照品溶液制备 精密称取丹酚酸B对照品适量,用75%甲醇溶解,制成浓度为0.129 2 mg/ml的丹酚酸B对照品溶液。
3.2.2 供试品溶液制备 取妇痛宁颗粒(批号1411014)约2 g,经精密称定后置于50 ml量瓶中,加入75%甲醇适量,超声30 min,取出放冷,加75%甲醇定容至刻度,摇匀,以微孔滤膜过滤,得供试品溶液。
3.2.3 阴性对照溶液制备 按处方配比例与制备供试品相同方法制得阴性对照品(缺丹参)。再按供试品溶液制备方法,制得阴性对照溶液。
3.3 系统适用性试验 精取对照品溶液、供试品溶液和阴性对照溶液各10 μl,进样,记录色谱图,见图4。阴性对照在丹酚酸B对照品对应处无干扰。理论塔板数按丹参酚酸B计算为8 201,符合规定。丹酚酸B的分离度为R1=3.71,R2=2.47,均大于1.5。所以选择性良好。
3.4 线性关系考查 将对照品溶液分别稀释成浓度为0.025 84、0.051 68、0.077 52、0.103 36、0.129 2和0.155 04 mg/ml,分别进样10 μl,得峰面积。以浓度(μg/ml)为横坐标,峰面积为纵坐标进行线性回归,回归方程为:Y=969.56X+7.163 7(r=0.999 9),结果表明进样量在25.84~155.04 μg/ml浓度范围内线性关系良好。
3.5 精密度试验 精密吸取对照品溶液10 μl,连续进样5次,测定峰面积,结果RSD为0.7%,说明仪器精密度良好。
3.6 重复性试验 称取同一批样品(批号1411014)制备5份供试品溶液,进样,测定峰面积,RSD为0.9%,表明重复性良好。
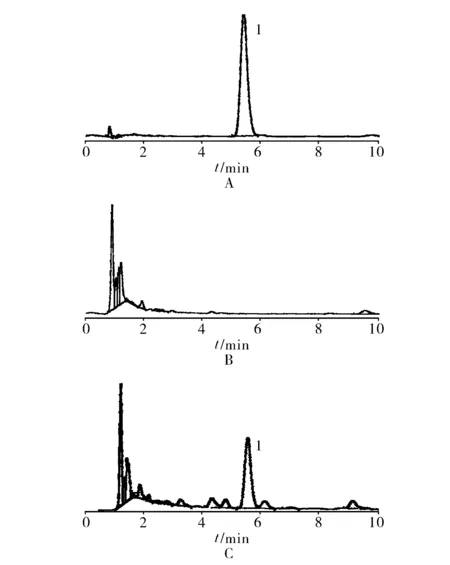
1.丹酚酸B
3.7 稳定性试验 精取同一供试品溶液,分别于0、4、8、12、16、20和24 h进样,测定峰面积,RSD为0.47%,表明供试品溶液在24 h内稳定。
3.8 加样回收试验 精密称取已知丹酚酸B含量的妇痛宁颗粒(批号1411014,含丹酚酸B 0.33%)6份,放置50 ml量瓶中,分别加入已知浓度的对照品2.5 ml,加入75%甲醇,超声30 min。进样,测定峰面积,计算加样回收率、RSD。结果平均回收率为99.43%,RSD为1.25%,见表1。

表1 回收率试验结果表
3.9 样品含量测定 精密称取样品,按上述条件制成供试品溶液,测定峰面积,结果见表2。
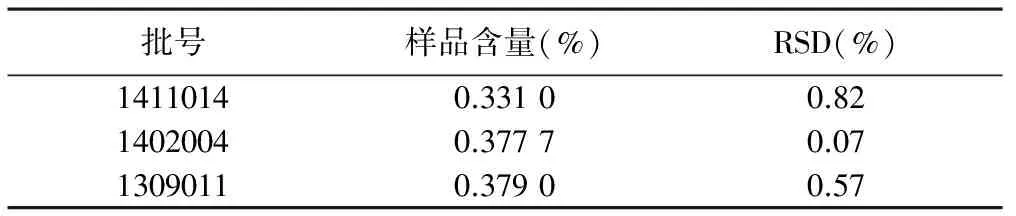
表2 样品含量测定结果表(n=3)
4 讨论
4.1 定性鉴别 丹参、赤芍、肉桂为本方中主药,故对此3种药进行定性鉴别,在鉴别方法制定时,从供试品溶液制备、展开剂组成及比例的选择、点样量、控制拖尾等方面,参考了《中国药典》方法及相关文献报道[2-6],进行了摸索优化,确定了最佳条件,方法简单、可靠。但薄层色谱图也显示实验还需更精进,赤芍图供试品点样量稍大,丹参图的阴性对照品点样量偏少,肉桂图有拖尾;供试品的批次还可增加。方中其他药的薄层鉴别尚需完善。
4.2 含量测定条件的确定
4.2.1 处理方法的选择 本试验在处理方法选择时,对加热回流和超声处理两种方法进行比较,由于丹参酸类成分对热不稳定,高温会破坏其有效成分[7],结果显示超声法的提取效果要优于加热回流法。试验中还对超声溶剂甲醇的用量(25、50 ml)以及超声时间(10、20、30 min)及甲醇浓度(100%、75%)的提取效果进行考查:75%甲醇50 ml,超声提取30 min,效果最好。
4.2.2 流动相的选择 丹酚酸B检测方法参照《中国药典》,流动相为甲醇-甲酸-水-乙腈(30∶1∶59∶10)。在此基础上,按高效液相色谱法标准操作规范[8]调整比例进样,根据峰形、分离度、保留时间及理论塔板数参数,最终定为甲醇-甲酸-水-乙腈(28∶1∶61∶10)。
1 中国药典[S].一部.2015:77
2 许勇,诸艳蓉,王柯,等.复方丹参胶囊的质量标准研究[J].中国医药工业杂志,2012,43(12):1020-1023
3 王志萍,韦慧鲜,申文慧,等.脑血栓片中芍药苷的定性定量测定[J].时珍国医国药,2008,19(5):1161-1162
4 刘元昆,张立贤,刘英.芪参清幽胶囊的薄层鉴别研究[J]. 中国执业药师,2014,11(11):23-25
5 武晓林,李敏,刘哲.牡丹皮和白芍的生药学鉴别[J]. 安徽农业科学,2014,42(31):10914-10915
6 汪祺,孙磊,郑笑为,等.冠脉宁片(胶囊)现行标准中丹参薄层鉴别比较研究[J]. 时珍国医国药,2014,25(11):2667-2669
7 周长新,罗厚蔚,丹羽正武.丹参水溶性化学成分的研究[J].中国药科大学学报,1999,30(6):411-416
8 中国药品生物制品检定所.中国药品检验标准操作规范[M].北京:中国医药科技出版社,2010:81-86
Establishment of quality standard for futongning granules
Shi Yun1,Jin Hua2
(1.Tianjin Zhong Xin Pharmaceutical Group Corporation Limited Hongqiao branch,Tianjin 300090;2.Tianjin University of Traditional Chinese Medicine,Tianjin 300193)
Objective:To establish a quality standard for futongning granules.Methods:Paeonia lactiflora,Salvia miltiorrhiza,Cinnamomum cassia were identificated by TLC and salvianolic acid B was determinated by HPLC.Parameters: Agilent Eclipse Plus - C18(4.6 mm× 100 mm,3.5 μm) was used stationary phase at a temperature of 25 ℃ and methanol-formic acid-water-acetonitrile (28∶1∶61∶10) as mobile phase at a flow rate of 1.0 ml/min; detection wavelength was set at 286 nm. Results:The components were completely identified and no interference spot was found on the plate by TLC. The concentration of salvianolic acid B showed a good linearity with peak areas over 25.84~155.04 μg/ml, The average recovery was 99.43% with RSD of 1.25%. Conclusion:The TLC and HPLC methods established here are simple,reliable and stable, being suitable for the quality control of futongning granules.
futongning granules,salvianolic acid B,HPLC,TLC
2016-06-27
*通讯作者:金华,E-mail:zyxyjin@163.com。
R917
A
1006-5687(2016)04-0007-03
