清心牛黄片中芍药苷含量测定方法的探索
2017-01-16聂晓洁尹云泽王守旺
聂晓洁,尹云泽,赵 欣,王守旺
(1.天津中医药大学,天津 300193; 2.天津中新药业集团股份有限公司乐仁堂制药厂,天津 300112)
清心牛黄片中芍药苷含量测定方法的探索
聂晓洁1,尹云泽2,赵 欣2,王守旺2
(1.天津中医药大学,天津 300193; 2.天津中新药业集团股份有限公司乐仁堂制药厂,天津 300112)
目的:建立HPLC法测定清心牛黄片中芍药苷的含量。方法:Symmetry C18色谱柱(150 mm×4.6 mm,5 μm);以乙腈-0.1%磷酸水(12∶88)为流动相;检测波长为230 nm;柱温30 ℃;流速1 ml/min。结果:芍药苷在3.312 5~53 μg/ml浓度范围内线性关系良好(R2=0.999 9),回收率为96.18%,RSD为0.42%。结论:建立的含量测定标准可以更有效地控制药品质量。
清心牛黄片,芍药苷,含量测定,高效液相色谱法
清心牛黄片由白芍、肉桂、阿胶、桔梗、山药、蒲黄、大豆黄卷、大枣、麦冬、甘草、白蔹、柴胡、党参、当归、川芎、苦杏仁、防风、白术、干姜、黄芩、茯苓、六神曲、牛黄、雄黄、水牛角浓缩粉、琥珀和冰片等27味药组成,具有清心化痰、镇惊祛风之功效,主治神志昏乱、言语不清、痰涎壅盛、头晕目眩、中风不语、半身不遂。该药现行质量标准收载于《卫生部药品标准中药成方制剂》第十九册。为提高清心牛黄片的质量控制水平,现将其质量标准进行提高,建立了白芍中芍药苷的含量测定方法。
1 仪器与试药
1.1 仪器 E 2695高效液相色谱仪(美国Waters公司);2489紫外检测器(美国Waters公司);Empower 3.0工作站。
1.2 试药 芍药苷对照品(批号110736-201136,中国食品药品检定研究院提供,供含量检测用);乙腈为色谱纯(德国Merk公司),水为去离子水(娃哈哈纯净水),其他试剂均为分析纯;清心牛黄片样品(批号D216011、D216013、D216018、D216022、D216024、D216029,由天津中新药业集团股份有限公司乐仁堂制药厂提供)。
2 方法与结果
2.1 色谱条件 Symmetry C18色谱柱(150 mm×4.6 mm,5 μm);以乙腈-0.1%磷酸水(12∶88)为流动相;检测波长为230 nm;柱温30 ℃;流速1 ml/min。理论塔板数按芍药苷峰计算应不低于2 000。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密称取芍药苷对照品10.88 mg,置于100 ml量瓶中,加甲醇溶解并稀释至刻度,摇匀;从中精密移取5 ml溶液,置于50 ml量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.2.2 供试品溶液的制备 取本品,除去包衣,研细,取约0.5 g,精密称定,置于具塞锥形瓶中,精密加入稀乙醇50 ml,称定重量,加热回流60 min,放冷,再称定重量,用稀乙醇补重,滤过,取续滤液,即得。
2.2.3 空白对照品溶液的制备 按处方配比,取除白芍以外的其他药味,按工艺制得片剂[1],再按“2.2.2”项下方法制得空白对照品溶液。精密吸取对照品、供试品和空白对照溶液,按“2.1”项下色谱条件进样分析,色谱图见图1。
2.3 线性关系考查 精密称取芍药苷对照品10.6 mg,置于100 ml量瓶中,加甲醇溶解并稀释至刻度,摇匀,配制成浓度为0.106 mg/ml的对照品溶液。依次稀释为0.053、0.026 5、0.013 25、0.006 625和0.003 312 5 mg/ml的系列溶液。依次进样10 μl,测定峰面积。以浓度为横坐标,峰面积为纵坐标,绘制标准曲线,得芍药苷的回归方程为Y=13 827 727.13X-2 493.80(R2=0.999 9),表明芍药苷在3.312 5~53 μg/ml范围内线性关系良好。
2.4 精密度试验 取同一批号样品(批号D216011),按照“2.2.2”项下供试品溶液制备操作,按“2.1”项下色谱条件分析,连续进样6次,测定样品中芍药苷峰面积。测得芍药苷峰面积平均值为180 216,RSD为0.22%,表明仪器精密度良好。
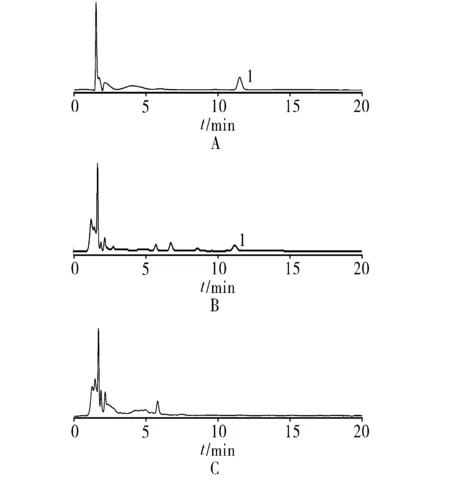
1.芍药苷
2.5 重现性试验 取同一批号(批号D216011)样品,共6份,按照“2.2.2”项下供试品溶液制备操作,按“2.1”项下色谱条件分析,测定每份样品中芍药苷含量。测得芍药苷含量平均值为1.281 1 mg/g,RSD为0.57%,表明重现性良好。
2.6 稳定性试验 取同一批号(批号D216011)样品,按照“2.2”项下供试品溶液制备操作,按“2.1”项下色谱条件分析,分别在0、3、6、9、12和15 h进样,测定样品中芍药苷峰面积。测得RSD为0.88%,说明15 h内供试品溶液稳定。
2.7 回收率试验 取同一批号(批号D216011)样品,约0.25 g,共6份,精密称定,分别精密加入芍药苷对照品(0.065 04 mg/ml,稀乙醇溶解)5 ml和稀乙醇45 ml,按“2.2.2”项下供试品溶液制备操作,制得供回收率用的供试品溶液,按“2.1”项下色谱条件分析,计算回收率。结果芍药苷的平均回收率为96.18%,RSD为0.42%,符合规定,结果见表1。
2.8 样品测定 取该品种6个批号的样品,按照“2.2.2”项下供试品溶液制备操作,按“2.1”项下色谱条件分析,测定6批样品中芍药苷的含量。每批测定3次,RSD均小于1.0%,结果见表2。
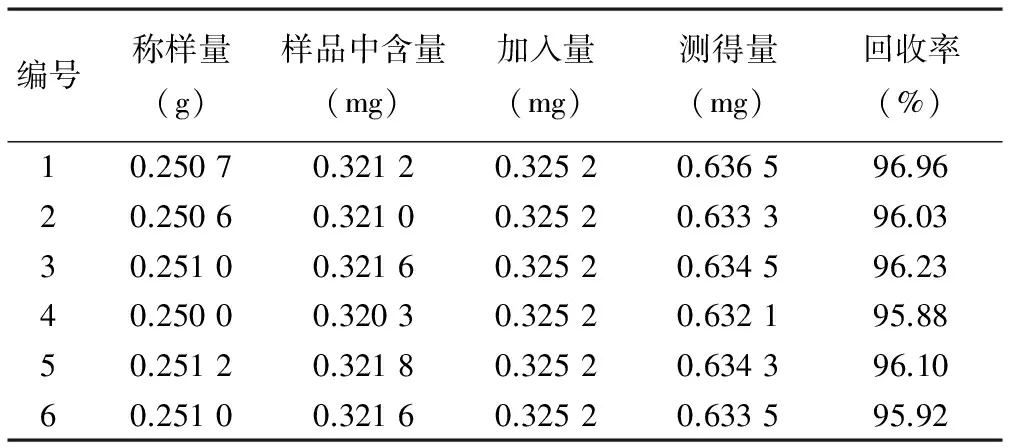
表1 芍药苷回收率试验结果(n=6)
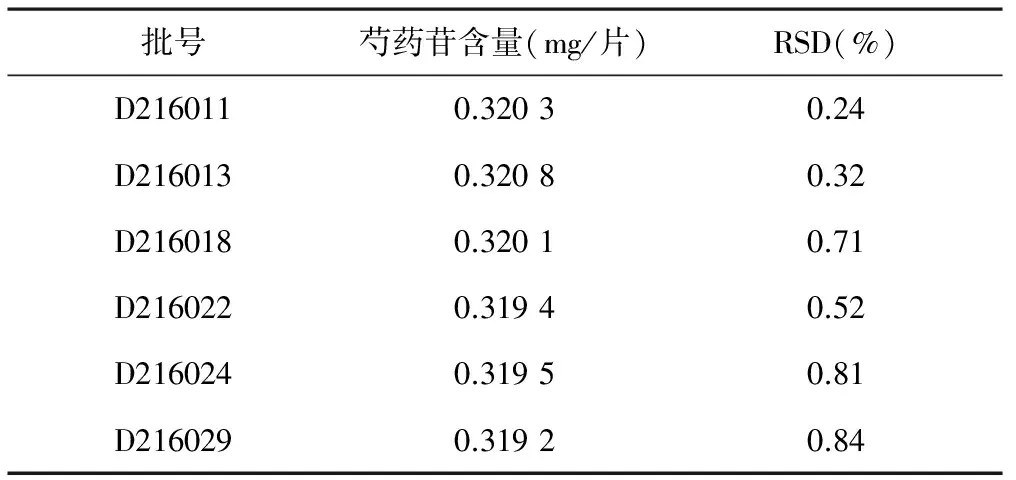
表2 样品含量测定结果(n=3)
3 讨论
3.1 提取方法的确定
3.1.1 提取溶剂的选择 参考《中国药典》2010年版第一部白芍含量测定项[2]的提取溶剂,确定提取溶剂为稀乙醇。
3.1.2 提取方式的选择 取同一批(批号D216011)样品,除去包衣,研细,取约0.5 g,精密称定,置于具塞锥形瓶中,精密加入稀乙醇50 ml,称定重量,以加热回流或者超声方式提取30 min,放冷,再称定重量,用稀乙醇补重,滤过,取续滤液。分别测定样品中芍药苷含量,结果表明,样品经加热回流提取后,供试品溶液中的芍药苷含量高于超声提取,故选用加热回流的提取方式。
3.1.3 溶剂量的选择 取同一批(批号D216011)样品,除去包衣,研细,取约0.5 g,精密称定,置于具塞锥形瓶中,分别精密加入稀乙醇25、50和75 ml,称定重量,加热回流30 min,放冷,再称定重量,用稀乙醇补重,滤过,取续滤液。分别测定样品中芍药苷含量,结果发现,当提取溶剂量为50 ml的时候,供试品溶液中的芍药苷含量最高,故选择提取溶剂量为50 ml。
3.1.4 提取时间的选择 取同一批(批号D216011)样品,除去包衣,研细,取约0.5 g,精密称定,置于具塞锥形瓶中,精密加入稀乙醇50 ml,称定重量,分别加热回流30、60和90 min,放冷,再称定重量,用稀乙醇补重,滤过,取续滤液。分别测定样品中芍药苷含量,结果表明,当提取时间为60 min时,供试品溶液中芍药苷的含量最高,故提取时间确定为60 min。
3.2 含量测定方法的建立 在本品处方中,白芍为君药,且白芍在《中国药典》2010年版一部[1]中的含量测定指标为芍药苷,因此选择芍药苷为该药品的定量指标。通过对不同提供方式、溶剂量和提取时间进行考查,确定了提取方法。采用不同品牌的色谱柱进行测定,含量基本一致,说明所建立方法的耐用性良好。
3.3 样品的测定结果讨论 样品测定结果显示,不同批次间的含量结果较为稳定,表明该企业所用药材的质量稳定。芍药苷的测定可以作为清心牛黄片中对白芍的测定方法与对清心牛黄片的质量控制的依据之一。通过上述研究,可以对清心牛黄片的深入性药理及临床研究提供帮助与探索依据。此次研究未对清心牛黄片开展其他药味的探索,只将作为君药的白芍进行含量测定方法的摸索,其他药味将作为后续的研究方向进行跟踪研究。
1 中国药典[S].一部.2010:96-97
2016-05-19
R927.2
A
1006-5687(2016)04-0015-03
