贝伐珠单抗治疗难治性瘤周脑水肿的近期疗效观察
2017-01-06苏进钱莹史克志刘洋易芳许新华
苏进钱莹史克志刘洋易芳许新华
·临床研究与应用·
贝伐珠单抗治疗难治性瘤周脑水肿的近期疗效观察
苏进①②钱莹①史克志①刘洋①易芳①许新华①②
目的:观察贝伐珠单抗(bevacizumab,BEV)治疗难治性瘤周脑水肿的近期疗效。方法:分析2014年4月至2016年4月三峡大学肿瘤防治中心收治的16例行BEV治疗的难治性瘤周脑水肿患者的临床资料,其中肺癌脑转移13例、乳腺癌脑转移2例、复发性胶质母细胞1例,所有患者对糖皮质激素、渗透性脱水剂等常规治疗不敏感。BEV每次使用剂量为5 mg/kg,每3~4周重复,至少接受1次以上BEV治疗;MRI测量治疗前、首次治疗后1个月、首次治疗后2个月瘤周水肿及瘤体体积并计算水肿指数;记录患者治疗前后临床症状,功能状态评分(KPS)及不良反应;采用t检验及最小显著性差异法比较组间差异。结果:16例患者治疗后临床症状均得到改善,KPS评分显著提高(P<0.001);全组患者瘤周水肿体积及肿瘤体积较治疗前明显缩小(P<0.05),水肿指数较治疗前显著降低,且未出现严重不良反应。结论:BEV可有效控制脑恶性肿瘤瘤周脑水肿,为难治性严重脑水肿患者改善生存质量争取治疗机会。
贝伐珠单抗 脑恶性肿瘤 瘤周脑水肿 水肿指数
脑恶性肿瘤是脑实质发生的原发性恶性脑瘤和转移性脑瘤的总称,在其发生发展过程中常伴有不同程度的瘤周水肿(peritumorous brain edema,PTBE)。肿瘤的增大和瘤周脑水肿的形成可导致颅内压进行性增高,降低患者生存质量,甚至危及生命。目前以地塞米松和甘露醇为代表的糖皮质激素和渗透性脱水剂治疗是PTBE的常规方法,其不良反应较严重,且部分患者表现为治疗不敏感甚至抗拒,即难治性瘤周水肿。既往研究证实,PTBE属于血管源性水肿范畴[1],血管内皮生长因子(vascular endothelial growth factor,VEGF)表达增多是瘤周水肿产生的主要因素[2]。近年来,VEGF抗体药物贝伐珠单抗(bevacizumab,BEV)在放射性脑坏死伴发的严重脑水肿治疗中疗效显著[3-7],而在与放射性脑坏死周围水肿具有相似病理机制的脑肿瘤瘤周水肿中报道较少[8-9]。本研究分析16例接受BEV治疗的难治性瘤周脑水肿患者临床资料,报道如下。
1 材料与方法
1.1 病例资料
分析2014年4月至2016年4月在三峡大学肿瘤防治中心经糖皮质激素及渗透性脱水剂治疗后不敏感,接受BEV治疗的脑恶性肿瘤伴严重瘤周水肿的临床资料16例,其中男性13例、女性3例,中位年龄59.5(33~65)岁。所有患者原发肿瘤、病理类型、临床分期、治疗经过、伴随疾病等数据完整;复发性胶质母细胞瘤1例,脑转移瘤15例中来源于肺癌13例、乳腺癌2例。主要临床症状为头晕、头痛、恶心、呕吐、视物模糊、语言困难、肢体感觉和(或)运动障碍等。BEV治疗前均已静脉滴注糖皮质激素和(或)甘露醇常规剂量治疗5 d以上,临床高颅压症状和(或)瘤周水肿指数缓解欠佳。全组治疗前瘤周水肿为104.22~634.08 cc(中位体积310.45 cc),瘤周体积为3.07~76.63 cc(中位体积19.60 cc)。13例患者在BEV治疗前已行全脑放疗或病灶局部大分割放射治疗,3例患者经BEV治疗后15~45 d接受脑肿瘤放疗。接受1个周期BEV治疗者6例;2个周期治疗7例;3个周期治疗2例;接受4个周期治疗者1例。
1.2 方法
1.2.1 治疗与评估方法患者每次BEV治疗剂量为5 mg/kg,0.9%的氯化钠注射液稀释后静脉滴注,每3~4周重复;首次滴注时间需>90 min;滴注结束后若无明显不良反应,后续治疗滴注时间调整为60 min;全部患者接受至少1次以上BEV治疗;治疗期间对症支持治疗常规进行;所有患者在首次治疗前1周和治疗后1个月和2个月行脑增强MRI检测,在T2WI FLAIR和T1WI序列下分别测量瘤周水肿和瘤体区域的变化情况;记录BEV治疗前后患者的临床症状、功能状态评分(KPS)及不良反应。按照NCI-CTCAE(4.0版)评价治疗的安全性。本研究方案经医院伦理委员会审核通过。所有受试者均经本人或其法定代理人签署知情同意书。
1.3 瘤周脑水肿评价标准
根据不同的时间复查头颅增强MRI,分别测量瘤周水肿和瘤体在横断位、冠状位和矢状位最大径(分别定义为a、b和c,单位为cm);参照Bitzer等[10]报道的计算据公式V=abc×π/6,分别计算包括水肿和瘤体在内的病变大小(V水肿+V瘤体,单位为cc)以及瘤体本身大小,二者之比为水肿指数(edema index,EI),即EI=(V水肿+V瘤体)/V瘤体;当EI=1时,无水肿;当1<EI≤1.5时,轻度水肿;当1.5<EI≤3时,中度水肿;当EI>3时,重度水肿。
1.3 统计学分析
采用SPSS 17.0软件进行统计学分析。各组数据特征采用t检验、最小显著性差异法(least-significant difference,LSD)比较组间差异。以P<0.05为差异具有统计学意义。
2 结果
2.1 临床疗效
16例患者经BEV治疗后,颅内压增高的症状和体征均得到不同程度的改善,治疗后KPS评分明显高于治疗前(62.5±12.38 vs.79.38±8.54,P<0.001);全组瘤周水肿体积经BEV治疗后1个月和2个月分别减少57.28%±20.64%和84.07%±8.78%,瘤体体积则分别缩小33.11%±15.03%和52.27%±20.55%,经LSD法检测治疗前与治疗后1个月和2个月瘤周水肿和瘤体体积的组间差异,差异均具有统计学意义(均P<0.001);全组治疗前EI的水平为28.21±31.51,首治后1个月和2个月EI均值水平下降至17.89±20.71和14.43±22.71,经LSD法检测治疗前与治疗后1个月和2个月EI均值水平的组间差异,差异均具有统计学意义(均P<0.005,表1)。各例患者瘤周水肿、瘤体及EI变化情况见图1。
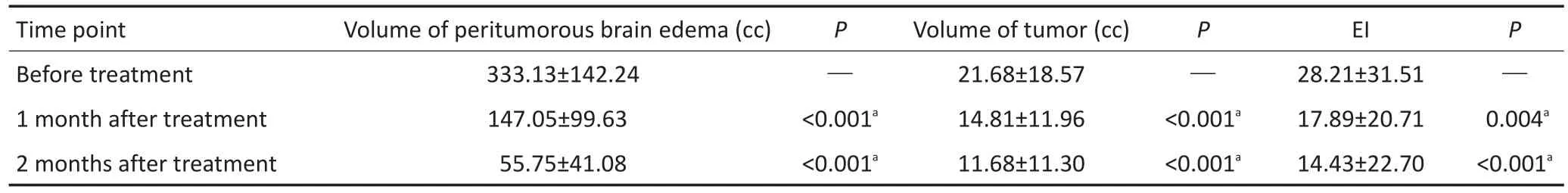
表1 治疗前后全组平均水肿指数比较(x±s)Table 1Mean EI before and after BEV treatment(x±s)

图1 贝伐珠单抗的治疗效果Figure 1Treatment effect of bevacizumab
2.2 典型病例
男性,诊断为右肺低分化腺癌脑转移,2015年2月曾行左侧额叶转移瘤X刀治疗(52 Gy/4 Gy/13 f)。2015年10月19日BEV治疗前MRI T2WI FLAIR相显示存在严重瘤周水肿(图2A),于2015年10月20日接受BEV 300 mg治疗,治疗后患者临床症状明显缓解,1个月后复查MRI(图2B)提示脑水肿显著减轻。总疗程仅使用1个周期BEV。
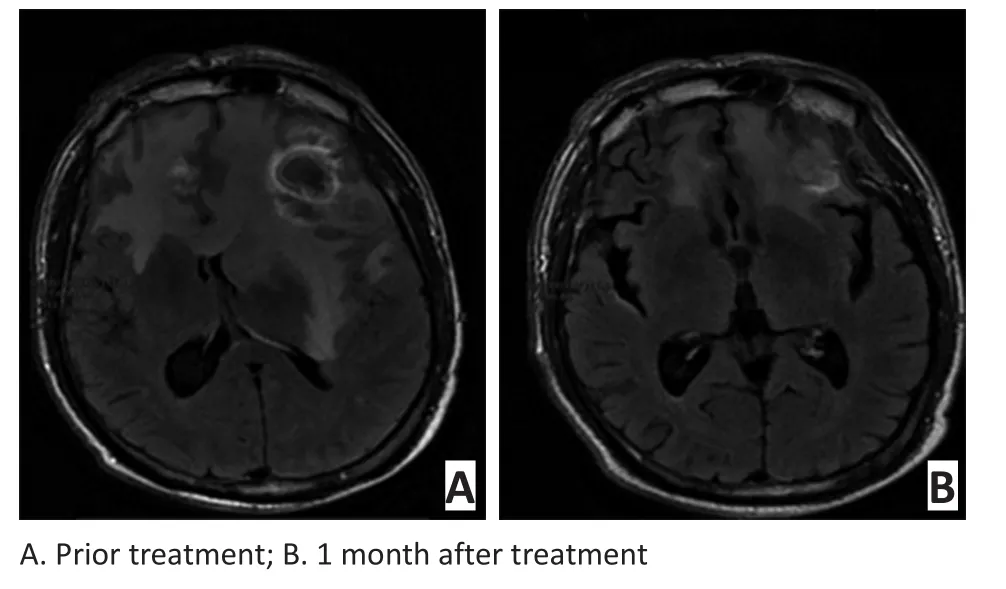
图2 接受BEV治疗前后的MRIFigure 2MRI image before and after BEV treatment
2.3 不良反应
16例患者中1例出现轻度过敏,经对症治疗后完全缓解。1例患者血压升高,最高至150/96 mmHg,短期使用口服血管紧张素转化酶抑制剂后降至正常水平。全组未出现2级及其以上不良反应。其他与BEV相关的皮疹、乏力、蛋白尿、血栓形成出血、胃肠道穿孔和充血性心脏衰竭均未见发生。
3 讨论
PTBE是脑恶性肿瘤常见的并发症,特别以恶性胶质瘤和脑转移瘤最易发生。其发生发展机制复杂,可能与VEGF及其受体、金属基质蛋白酶-9、水通道蛋白-4、白细胞介素-6、乏氧诱导因子-1α等因素有关,其中VEGF的表达与PTBE的形成关系最为密切[11-13]。
BEV是一种重组的人源化单克隆IgG1抗体,能特异性阻断VEGF及其内皮细胞表面受体(Flt-1和KDR)结合,抑制内皮细胞增殖和活化,降低血管通透性,促进肿瘤内部血管系统“正常化”,从而达到抗血管生成和抗肿瘤的作用。BEV在脑恶性肿瘤中的应用,始于其对恶性胶质瘤的治疗。Berghoff等[14]报道BEV治疗15例放射性脑坏死患者的临床资料,结果显示病灶体积及水肿体积在MRI上均有不同程度的缩小,开启了BEV治疗放射性脑坏死的新篇章。Furuse等[15]报道1例前期激素及放射治疗无效的乳腺癌脑转移伴严重瘤周水肿的患者,给予BEV治疗后症状显著缓解,生活基本恢复自理。李子晨等[16]报道21例BEV单药治疗放射性脑损伤的疗效,结果显示MRI T2相水肿体积平均减少53.9%±22.13%。Zhuang等[4]报道14例立体定向放射治疗后诊断为放射性脑坏死的患者,经BEV治疗后,83.3%(10/12)患者临床症状明显好转,64.29%(9/14)患者水肿指数改善,92.86%(13/14)的患者脑坏死灶体积缩小,且无2级以上不良反应发生。此外,有研究报道BEV对于首次治疗有效后复发的患者,再次使用BEV仍可达到良好的效果[17]。
脑转移瘤瘤周水肿与放射性脑坏死伴发的脑水肿具有相似的病理机制,同属于血管源性水肿。鉴于BEV在放射性脑坏死中的良好疗效,本研究推测BEV对于脑转移瘤周水肿可能具有相似的疗效,但目前关于BEV治疗瘤周脑水肿的研究报道尚少,且均为小样本案例报道。Zustovich等[9]报道使用BEV治疗18例瘤周脑水肿患者,客观控制率达100%,其中客观有效率达60%。赵儒钢等[8]运用BEV治疗难治性瘤周水肿,结果显示78.6%患者治疗后头晕、头痛症状明显减轻,全组治疗后瘤周水肿体积较疗前明显减少(P<0.05),EI较治疗前亦有降低的趋势,但差异无统计学意义。本研究结果显示,全组16例患者经BEV治疗后,颅内压增高的症状和体征均得到不同程度的改善,治疗后KPS评分明显高于治疗前(62.5±12.38 vs.79.38±8.54,P<0.001);全组瘤周水肿体积经BEV治疗后1、2个月后,分别减少57.28%± 20.64%和84.07%±8.78%,瘤体体积则分别缩小33.11%±15.03%和52.27%±20.55%,EI水平显著下降,差异均具有统计学意义(均P<0.005)。患者瘤周水肿的减轻和一般状况的改善,为下一步的治疗提供了机会。
既往文献报道BEV应用过程中各种出血的发生率高达30%,其中包括牙龈出血、血尿、颅内出血、结膜出血及注射部位出血等[18],而对于脑转移瘤患者,Khasraw等[19]报道在胶质瘤和脑转移患者中应用BEV发生出血概率为3.7%,而未应用BEV的患者中同样有3.6%的出血发生率,因此认为BEV并不增加脑恶性肿瘤脑出血的风险。张玉梅等[20]应用BEV联合培美曲塞治疗非小细胞肺癌在疲乏、骨髓抑制、转氨酶/胆红素升高、皮疹/黏膜炎、胃肠道反应、末梢神经炎、咯血/出血、胃肠道穿孔、动脉血栓栓塞和高血压等不良反应上与对照组比较均无显著性差异。本研究中,16例患者中仅1例轻度过敏、1例血压升高,经对症处理后缓解,全组未出现脑出血及2级以上不良反应,显示出BEV良好的安全性。
综上所述,本研究结果显示贝伐珠单抗可有效控制脑恶性肿瘤瘤周水肿,改善患者生存质量,为治疗伴有严重瘤周水肿的脑肿瘤患者提供新的思路,但因病例尚少,期待大规模多中心的临床试验探索。
[1]Zhao WP,Chen QX.Relationship of meningioma peritumoral edema,angiogenesis and expressions of vascular endothelial growth factor[J].Chin J Exp Surg,2015,32(3):611-613.[赵卫平,陈谦学.脑膜瘤组织瘤周水肿、新生血管与血管内皮生长因子表达的关系[J].中华实验外科杂志,2015,32(3):611-613.]
[2]Gerstner ER,Duda DG,Di Tomaso E,et al.VEGF inhibitors in the treatment of cerebral edema in patients with brain cancer[J].Nat Rev Clin Oncol,2009,6(4):229-236.
[3]Levin VA,Bidaut L,Hou P,et al.Randomized double-blind placebocontrolled trial of bevacizumab therapy for radiation necrosis of the central nervous system[J].Int J Radiat Oncol Biol Phys,2011,79 (5):1487-1495.
[4]Zhuang H,Yuan X,Zheng Y,et al.A study on the evaluation method and recent clinical efficacy of bevacizumab on the treatment of radiation cerebral necrosis[J].Sci Rep,2016[Epub ahead of print].
[5]Lubelski D,Abdullah KG,Weil RJ,et al.Bevacizumab for radiation necrosis following treatment of high grade glioma:a systematic review of the literature[J].J Neurooncol,2013,115(3):317-322.
[6]Wang Y,Wang E,Pan L,et al.A new strategy of CyberKnife treatment system based radiosurgery followed by early use of adjuvant bevacizumab treatment for brain metastasis with extensive cerebral edema[J].J Neurooncol,2014,119(2):369-376.
[7]Matuschek C,Bölke E,Nawatny J,et al.Bevacizumab as a treatment option for radiation-induced cerebral necrosis[J].Strahlenther Onkol,2011,187(2):135-139.
[8]Zhao RG,Meng XY,Shen G,et al.Efficacy analysis of bevacizumab in brain metastases patients with serious cerebral edema[J].Chin Clin Oncol,2016,21(3):233-237.[赵儒钢,孟祥颖,申戈,等.贝伐珠单抗治疗脑转移瘤难治性瘤周水肿的疗效分析[J].临床肿瘤学杂志,2016,21(3):233-237.]
[9]Zustovich F,Ferro A,Lombardi G,et al.Bevacizumab as front-line treatment of brain metastases from solid tumors:a case series[J]. Anticancer Res,2013,33(9):4061-4065.
[10]Bitzer M,Opitz H,Popp J,et al.Angiogenesis and brain oedema in intracranial meningiomas:influence of vascular endothelial growth factor[J].Acta Neurochir(Wien),1998,140(4):333-340.
[11]Gao J,Liu YH,Yan L,et al.Research progress on peritumoral edemarelated molecular biology factors of the metastasis tumor of brain [J].Chin J Clin Oncol,2014(8):534-537.[高佳,刘彦慧,阎玲,等.脑转移瘤瘤周水肿相关分子生物学因素研究进展[J].中国肿瘤临床,2014,(8):534-537.]
[12]Jiang S,Xia R,Jiang Y,et al.Vascular endothelial growth factors enhance the permeability of the mouse blood-brain barrier[J].PLoS One,2014,9(2):e86407.
[13]Wei HM,Qin SK,Yin XJ,et al.Inhibition and mechanism on combination of recombinant human endostatin and cisplatin in mouse model bearing S180 tumor ascite[J].Chin J Cancer Prev Tre,2015, 22(06):442-446.[魏红梅,秦叔逵,殷晓进,等.重组人血管内皮抑制素联合顺铂对小鼠腹水瘤抑制作用及其机制探讨[J].中华肿瘤防治杂志,2015,22(06):442-446.]
[14]Berghoff AS,Sax C,Klein M,et al.Alleviation of brain edema and restoration of functional independence by bevacizumab in brainmetastatic breast cancer:a case report[J].Breast Care(Basel), 2014,9(2):134-136.
[15]Furuse M,Kawabata S,Kuroiwa T,et al.Repeated treatments with bevacizumab for recurrent radiation necrosis in patients with malignant brain tumors:a report of 2 cases[J].J Neurooncol,2011,102 (3):471-475.
[16]Li ZC,Rong XM,Li Y,et al.Efficacy of bevacizumab monotherapy on radiation-induced brian necrosis[J].Chin J Radiol Med Prot,2014, 34(3):188-191.[李子晨,容小明,李艺,等.贝伐珠单抗治疗放射性脑损伤的疗效研究[J].中华放射医学与防护杂志,2014,34(3):188-191.]
[17]Rong XM,Tang YM.Clinical observation of bevacizumab monotherapy on radiation-induced brian necrosis[J].Chin J Radiol Med Prot, 2013,33(5):563-565.[容小明,唐亚梅.贝伐珠单抗治疗放射性脑损伤的临床观察[J].中华放射医学与防护杂志,2013,33(5):563-565.]
[18]Kreisl TN,Zhang W,Odia Y,et al.A phaseⅡtrial of single-agent bevacizumab in patients with recurrent anaplastic glioma[J].Neuro Oncol,2011,13(10):1143-1150.
[19]Khasraw M,Holodny A,Goldlust SA,et al.Intracranial hemorrhage in patients with cancer treated with bevacizumab:the Memorial Sloan-Kettering experience[J].Ann Oncol,2012,23(2):458-463.
[20]Zhang YM,Li CS,Chen YH.Bevacizumab and pemetrexed combination therapy clinical observation of patients with non-small cell lung cancer[J].Chin J Cancer Pre Tre,2014,21(01):51-54.[张玉梅,李春姗,陈逸恒.贝伐单抗联合培美曲塞治疗非小细胞肺癌临床观察[J].中华肿瘤防治杂志,2014,21(01):51-54.]
(2016-07-21收稿)
(2016-09-22修回)
(编辑:孙喜佳校对:郑莉)
Clinical efficacy of bevacizumab for the treatment of serious peritumorous brain edema
Jin SU1,2,Ying QIAN2,Kezhi SHI2,Yang LIU1,Fang YI1,Xinhua XU1,2
1First College of Clinical Medical Science,China Three Gorges University;Department of Oncology,Yichang Central People's Hospital, Yichang 443003,China;2Cancer Center,China Three Gorges University,Yichang 443003,China
Objective:To investigate the efficacy of bevacizumab on the treatment of serious peritumorous brain edema.Methods:A total of 16 patients with malignant brain tumors and serious peritumorous brain edema,(13 cases of lung cancer,2 cases of breast cancer,and 1 case of recurrent glioblastoma)were analyzed.Treatment with glucocorticoids,osmotic dehydration,and other conventional approaches were not effective for these patients.Bevacizumab was administered at a dose of 5 mg/kg at least once every three or four weeks.The Karnofsky performance score(KPS)and the changes in cerebral edema symptoms,such as cerebral edema volume,tumor volume,edema index(EI),and changes in magnetic resonance imaging(MRI)were compared before and after treatment.The ttest and least-significant difference method were used to compare treatment groups.Results:All bevacizumab-treated patients had reduced symptoms.The KPS after treatment was significantly higher than that before treatment(P<0.001).The cerebral edema volumes,tumor volumes,and EI of 16 patients were significantly decreased(P<0.05).Bevacizumab caused mild clinical side effects.Conclusion:Preliminary results showed that treatment of serious peritumorous brain edema with bevacizumab was safe and effective.
bevacizumab,malignant brain tumor,peritumorous brain edema,edema index

10.3969/j.issn.1000-8179.2016.23.859
①三峡大学第一临床医学院,宜昌市中心人民医院肿瘤科(湖北省宜昌市443003);②三峡大学肿瘤防治中心
许新华xuxinhua@medmail.com.cn
苏进专业方向为恶性肿瘤放化疗。
E-mail:sujin15253@126.com
