伪狂犬病毒的microRNAs靶基因预测及功能鉴定
2016-12-01李国新郑旭晨童光志
刘 飞,童 武,郑 浩,李国新,梁 超,郑旭晨,田 青,童光志
(中国农业科学院上海兽医研究所,上海200241)
·研究论文·
伪狂犬病毒的microRNAs靶基因预测及功能鉴定
刘 飞,童 武,郑 浩,李国新,梁 超,郑旭晨,田 青,童光志
(中国农业科学院上海兽医研究所,上海200241)
为研究猪伪狂犬病毒(Pseudorabies virus,PRV)编码的微小RNA(microRNA,miRNA)的功能,本研究通过生物信息学预测结合双荧光素酶报告系统验证方法,对病毒miRNA(virus miRNA,vmiRNA)进行靶基因鉴定。结果表明,PRV编码的prv-miR-LLT1、prv-miR-LLT7和prv-miR-LLT9对病毒转录极早期基因IE180有抑制作用,prv-miR-LLT7对参与调控病毒复制的UL48基因有抑制作用。初步研究表明这些vmiRNA可能在病毒感染过程中具有基因调控作用,本研究结果为进一步研究PRV vmiRNA在病毒复制、免疫逃避及潜伏感染过程中的功能奠定了基础。
伪狂犬病毒;微小RNA;靶基因
伪狂犬病毒(Pseudorabies virus,PRV)为疱疹病毒科(Herpesviridae)成员,感染动物后具有发病迅速、嗜神经性和潜伏感染特性。微小RNA(microRNA,miRNA)是长约22~24 nt的小分子非编码RNA。miRNA通常与靶基因mRNA的3'UTR发生不同程度的互补,可以对mRNA进行降解(完全互补)和翻译抑制(不完全互补)。疱疹病毒vmiRNA(virus miRNA,vmiRNA)通常参与病毒潜伏感染、裂解感染或潜伏再激活等生理过程[1,2],从而发挥与免疫逃避、抑制宿主细胞凋亡和维持潜伏感染等重要作用[3]。
目前为止,研究发现PRV共编码11条vmiRNA,均位于PRV基因组潜伏转录相关因子(LLT)区,被命名为prv-miR-LLT1~prv-miR-LLT11[4-6]。已有研究表明,缺失prv-miR-LLT1~prv-miR-LLT9这9 条vmiRNA后,不影响PRV在其天然宿主猪体内的三叉神经节中建立潜伏感染,但会使一些宿主基因上调,导致与细胞免疫相关的功能受损,可能预示着PRV vmiRNA可能参与免疫抑制等过程[7],但这些vmiRNA的功能尚不清楚。本研究通过生物信息学预测结合实验验证方法,初步鉴定了PRV vmiRNA的靶基因,为进一步研究PRV或其他疱疹病毒vmiRNA的功能奠定基础。
1 材料和方法
1.1 细胞与毒株 HeLa细胞株、PRV变异毒株JS-2012均由本实验室保存。
1.2 载体与主要试剂 pmirGLO Dual-Luciferase miRNA Target Expression Vector购自Promega公司;PCR试剂购自大连宝生物有限公司(TaKaRa);限制性内切酶购自NEB公司;ClonExpress®II One Step Cloning Kit购自诺唯赞公司;基因组DNA提取试剂盒、胶回收试剂盒购自OMEGA公司;质粒提取试剂盒及TOP-10感受态细胞购自天根生物科技有限公司;Dual-Luciferase Reporter Assay System购自Promega公司;Lipofectamin 3000转染试剂、OPTIMEM培养基购自Invitrogen公司;miRNA mimics由上海吉玛制药技术有限公司合成;胎牛血清(FBS)和 DMEM 培养基购自Gibco公司。
1.3 vmiRNA靶基因预测 本文使用miRanda软件(http://www.microrna.org/microrna/home.do)预测PRV vmiRNA靶向病毒基因的3'UTR。限定的条件为miRNA序列5'端开始1~9 nt的碱基处不允许错配(允许G-U配对),同时G-U配对的总量≤3。
1.4 双荧光素酶重组载体构建 根据miRanda软件预测结果,获取到miRNA靶基因信息后,综合预测结果及各个靶基因的功能,进行靶基因的筛选。然后根据GenBank中登录的PRV JS-2012(NO.KP257591)基因组序列,利用CE Design V1.03软件,设计5'端带有载体同源臂的特异性引物,引物均由上海桑尼生物工程有限公司合成,见表1。

表1 vmiRNA靶基因3'UTR的PCR扩增引物Table1 Primers used in PCR amplifi cation for 3'UTR of vmiRNA target gene
以JS-2012的DNA为模板,利用特异性引物扩增各靶基因的3'UTR片段,50 μL反应体系。反应条件如下:94℃预变性5 min;94℃变性30 s,68℃退火15 s,72℃延伸0.5~2.5 min,30个循环;72℃延伸10 min。PCR产物经回收纯化后,利用重组酶将目的片段定向重组至经Nhe I线性化的pmirGLO双荧光素酶载体中。转化后挑菌送至上海桑尼有限公司测序。
1.5 vmiRNA与双荧光素酶载体共转染 将HeLa细胞铺于24孔板,待细胞汇合度为80%左右时。按照人工说明书,利用Lipo 3000转染试剂,将合成的PRV miRNA mimics/乱序的NC mimics对照与重组载体/pmirGLO空载体对照分别进行共转染(每孔转染量:mimics 80 pmol,质粒DNA 100 ng)。共转染后24 h检测荧光素酶相对表达情况。每个样品做3个复孔,并进行3次生物学重复。
1.6 荧光素酶表达水平检测 按照人工操作说明书配制新鲜的1×PLB、萤火虫发光液LARⅡ及萤火虫终止液Stop&Glo®。用1×PBS清洗细胞2次,弃净PBS。每孔加入200 μL 1×PLB裂解液,室温轻摇培养板15 min。将裂解后的细胞移至新EP管中,10 000×g离心 30 s,吸取20 μL上清至检测的96孔板中。将自动进样器1和2分别放置适量的LARII 和Stop&Glo®试剂。测量时,设置参数每孔加入100 μL LARII,检测萤火虫萤光素酶。加入100 μL Stop&Glo®试剂,检测海肾萤光素酶的活性,使用2 s延迟和10 s读数。其他孔如此循环操作。
2 结果
2.1 vmiRNA对病毒基因的调控预测 利用miRanda软件对PRV已知的11条vmiRNA与56个PRV的基因3'UTR进行了靶基因预测。结果表明,vmiRNA与病毒靶基因形成了一个复杂的基因调控网络。一条miRNA能靶向多个基因,如prv-miR-LLT1能靶向EP0、IE180、UL14、UL25、UL48、UL44、UL39、UL33和LLT等多个基因。一个基因同时也能受到多个靶基因的调控,如IE180基因可以受prvmiR-LLT1、prv-miR-LLT7、prv-miR-LLT9、prvmiR-LLT10和prv-miR-LLT11的调控。因此,我们选择与病毒复制、转录激活及毒力相关的UL1、UL14、UL48、UL52、US3、EP0和IE180基因,作为进一步验证的靶基因。选取的验证的靶基因见表2。
2.2 vmiRNA的病毒靶基因验证 将测序正确的重组质粒分别命名为pmiR-EP0U、pmiR-US3U、pmiRUL1U、pmiR-UL14U、pmiR-U52U、pmiR-IE180U 和pmiR-UL48U。将合成的vmiRNA分别与相应重组载体共转染至HeLa细胞中,检测vmiRNA作用于靶基因的3'UTR后,对萤火虫荧光素酶表达水平的影响,结果见图1。

表2 选取验证的vmiRNA及其靶基因Table2 The vmiRNAs and target genes used in this study
双荧光素酶检测结果,发现prv-miR-LLT1、prv-miR-LLT7和prv-miR-LLT9对PRV转录极早期基因IE180有抑制作用,其中prv-miR-LLT-1的抑制作用较显著(P<0.05)。prv-miR-LLT7对参与病毒复制调控的UL48基因有显著抑制作用(P<0.05),说明这些vmiRNA可能具有调控病毒复制或维持潜伏感染等功能。本研究中其他vmiRNA则对相应靶基因无抑制作用,而prv-miR-LLT3对UL14及UL48,prv-miR-LLT10对UL48及UL52的作用,因为prvmiR-LLT3和prv-miR-LLT10本身会对pmirGLO空载体具有明显的下调作用,所以这两个miRNA可能抑制了载体上的启动子活性,从而导致荧光素酶表达水平下降。
3 讨论
1993年miRNA被发现以来[8],研究人员对这种结构相对简单的小分子的形成机制、功能和作用方式充满了好奇。随着研究的深入,miRNA的一些调控机制正在逐渐明晰,miRNA可以通过其短小的“种子区”识别并结合mRNA的3'UTR,通过抑制转录或者翻译过程达到调控的目的[9]。现有的关于vmiRNA的功能研究主要集中于双链DNA病毒,且大多数的研究成果集中于疱疹病毒。已有研究表明vmiRNA在疱疹病毒中对建立和维持潜伏感染及再激活、免疫逃避和细胞生存等过程中发挥重要作用。如α-疱疹病毒科的HSV-1和HSV-2,γ-疱疹病毒科的EBV、KSHV和β-疱疹病毒科的CMV编码的vmiRNA能够靶向病毒编码的基因,许多是靶向病毒立即早期基因从而调控病毒的复制,或与病毒在宿主中建立及维持潜伏感染和再激活作用有关[10]。有些vmiRNA则在病毒的生命过程通过调控细胞基因发挥免疫逃避的作用,以创造更有利于病毒生存,在病毒生活周期中扮演重要的角色。
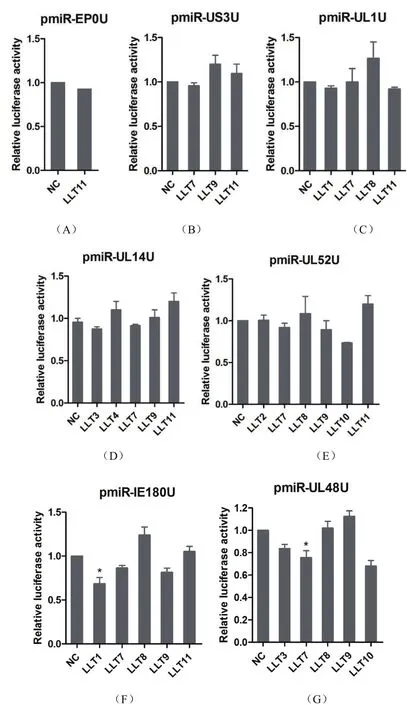
图1 荧光素酶报告系统验证vmiRNA对病毒靶基因3'UTR的作用Fig.1 Function analysis of vmiRNA-gene on 3'UTR by the luciferase reporter system
目前,miRNA靶基因的预测为miRNA功能鉴定提供一个验证的数据支持。我们通过miRanda靶基因预测软件分析,发现vmiRNA与病毒的mRNA之间能够形成复杂的基因调控网络。我们选择与PRV复制和转录激活相关的IE180、EP0、UL52、UL48、UL14、UL1和US3基因进行验证。结果表明,prvmiR-LLT1、prv-miR-LLT7和prv-miR-LLT9对IE180有抑制作用,prv-miR-LLT7对UL48有抑制作用。说明这几个vmiRNA在病毒感染后可能会抑制PRV的复制,从而有利于PRV维持潜伏感染或免疫逃避等过程,该结果与文献报道的prv-miR-LLTs可能调控极早期基因IE180结果相一致[4]。而其他vmiRNA未见对预测的靶基因有显著抑制作用。总而言之,相对于蛋白的强大调控作用,miRNA分子很小不会被宿主免疫系统识别和清除,可以在病毒生命周期中起到多层次的微调控作用,从而创造一个有利于病毒生存的环境。目前,对PRV vmiRNA功能研究尚处于探索阶段,相关文献报道较少。本研究结果为进一步探讨PRV vmiRNA在病毒复制、免疫逃避及潜伏感染过程中的功能奠定了基础。
[1] Boss I W, Plaisance K B, Renne R.Role of virus-encoded microRNAs in herpesvirus biology[J].Trends Microbiol, 2009, 17(12): 544-553.
[2] Cullen B R.Viral and cellular messenger RNA targets of viral microRNAs[J].Nature, 2009, 457(7228): 421-425.
[3] Kozomara A, Griffiths-Jones S.miRBase: annotating high confidence microRNAs using deep sequencing data[J].Nucleic Acids Res, 2014, 42 (Database issue): D68-D73.
[4] Wu Y Q, Chen D J, He H B, et al.Pseudorabies virus infected porcine epithelial cell line generates a diverse set of host microRNAs and a special cluster of viral microRNAs[J].PLoS one, 2012, 7(1): e30988.
[5] Anselmo A, Flori L, Jaffrezic F, et al.Co-expression of host and viral microRNAs in porcine dendritic cells infected by the pseudorabies virus[J].PLoS one, 2011, 6(3): e17374.
[6] Timoneda O, Nunez-Hernandez F, Balcells I, et al.The role of viral and host microRNAs in the Aujeszky'sdisease virus during the infection process[J].PLoS one, 2014, 9(1): e86965.
[7] Mahjoub N, Dhorne-Pollet S, Fuchs W, et al.A 2.5-kilobase deletion containing a cluster of nine microRNAs in the latency-associated-transcript locus of the pseudorabies virus affects the host response of porcine trigeminal ganglia during established latency[J].J Virol, 2015, 89(1): 428-442.
[8] Lee R C, Feinbaum R L, Ambrost V.The C.elegans heterochronic gene lin-4 encodes small RNAs with antisense complementarity to lin-14[J].Cell, 1993, 75(5): 843-854.
[9] Lim L P, Glasner M E, Yekta S, et al.Vertebrate micro RNA genes[J].Science, 2003, 299(5612): 501.
[10] Grey F, Hook L, Nelson J.The functions of herpesvirusencoded microRNAs[J].Med Microbiol Immunol, 2008, 197(2): 261-267.
TARGET PREDICTION AND FUNCTIONAL IDENTIFICATION OF PSEUDORABIES VIRUS-ENCODED MICRORNAS
LIU Fei, TONG Wu, ZHENG Hao, LI Guo-xin, LIANG Chao, ZHENG Xu-chen, TIAN Qing, TONG Guang-zhi
(Shanghai Veterinary Research Institute, CAAS, Shanghai 200241, China)
In order to understand the function of microRNA (miRNA) encoded by Pseudorabies virus (PRV), the objective of the present study was to defi ne potential vmiRNA-gene interaction based on bioinformatic analysis in combination with the dual luciferase reporter assay system.The results showed prv-miR-LLT1, prv-miR-LLT7 and prv-miR-LLT9 targeted the transcription activator IE180 gene and prv-miR-LLT7 targeted the UL48 gene involved in viral DNA replication.These vmiRNAs might have regulatory functions in the course of PRV infection.The results were of signifi cance for further research on functions of vmiRNAs regarding virus replication, immune evasion and latent infection.
Pseudorabies virus; microRNA; target gene
S852.659.1
A
1674-6422(2016)02-0008-05
2016-01-16
上海市自然科学基金项目(14ZR1448900);上海市科技兴农重点攻关项目(沪农科攻字(2015)第1-7号);中央级公益性科研院所基本科研业务费专项资金项目(2014JB02)
刘飞,女,博士研究生,预防兽医学专业
童光志,E-mail:gztong@shvri.ac.cn
