利用剩余试剂进行Sysmex XE5000全自动血液分析仪的性能验证
2016-11-04张迎久孙艳艳
刘 丽,李 梅,薛 暄,王 辉,张迎久,孙艳艳
(首都医科大学石景山教学医院/北京市石景山医院检验科 100043)
·临床研究·
利用剩余试剂进行Sysmex XE5000全自动血液分析仪的性能验证
刘丽,李梅,薛暄,王辉,张迎久,孙艳艳△
(首都医科大学石景山教学医院/北京市石景山医院检验科100043)
目的探讨合并剩余试剂进行Sysmex XE5000全自动血液分析仪的性能验证。方法将Sysmex XE5000仪器的原装剩余稀释液、4DL、FFS试剂分别进行合并,利用合并的残液以国际血液学标准化委员会、美国临床和实验室标准协会制定的评价方案为标准进行评价试验。结果利用剩余试剂进行的仪器性能验证,全血细胞计数精密度、准确度、正确度、线性范围良好,携带污染率低,2种进样模式相关性好,实验室内结果可比性好。结论Sysmex XE5000全自动血液分析仪可对剩余试剂合并再利用,且能保证检测质量,降低检测成本。
ISO 15189;全自动血液分析仪;剩余试剂;性能验证;精密度;携带污染率
医学实验室ISO15189《医学实验室质量和能力的专用要求》指出,申请认可的实验室应对设备、检测系统或方法的主要分析性能进行验证,达到临床检测的标准[1]。该院检验科使用的Sysmex XE 5000血液分析仪,以半导体激光器的流式细胞计数为基础[2-3]。现探讨利用在效期内合并仪器的剩余试剂,参考国际血液学标准化委员会、美国临床和实验室标准协会(CLSI)的相关性能评价文件,以该院健康体检者、门诊患者及住院患者的EDTA-K2抗凝血为研究对象,对Sysmex XE5000血液分析仪进行性能评价实验[4]。
1 资料与方法
1.1一般资料EDTA-K2抗凝静脉血标本来自该院健康体检者、门急诊患者、血液科住院患者,标本采集严格按照《全国临床检验操作规程(第3版)》执行[5]。
1.2仪器与试剂日本Sysmex公司生产的XE 5000全自动血液分析仪。所用校准品和质控品均为该仪器的配套产品,试剂全部为原装试剂,其中稀释液、4DL、FFS为效期内合并的剩余原装试剂,合并剩余试剂为同一项目、同一批号试剂,将瓶中剩余试剂每7~8瓶合并为1瓶。轻轻充分混匀,将气泡小心吸出。所有合并试剂保证正确环境下保存、有效期内使用。
1.3检测方法[6]按照《WS/T406-2012 临床血液学检验常规项目分析质量要求》《医学实验室质量和能力认可准则》《全国临床检验操作规程》,利用有效期内、正确环境下保存的合并试剂,对Sysmex XE5000进行本底计数验证、携带污染率验证、批内精密度和日间精密度验证、线性范围验证、正确度验证、不同吸样模式的结果可比性、仪器间可比性验证及精密度验证。
1.3.1本底计数验证使用稀释液作为标本,在血球仪上连续检测3 次,3 次检测结果的最大值要求在允许范围内。
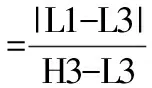
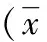
1.3.4日间精密度验证至少使用正常和异常2个水平的全血质控品,在检测当天至少进行1次室内质控剔除失控数据后,按批号或月份计算在控数据的变异系数。
1.3.5线性范围验证根据CLSI EP6-P文件选取1份高值全血标本(H),按100%、80%、60%、40%、20%、0%的比例进行稀释,每个稀释度重复测定3次,计算均值。均值与理论值作比较(偏离应小于10%),计算Y=aX+b,验证线性范围。若斜率a在1.00±0.05范围内,相关系数r≥0.975或r2≥0.95。白细胞(WBC)、红细胞(RBC)、血红蛋白(Hb)、血小板(PLT)项目满足要求的线性范围在厂家说明书规定的范围内,则线性验证合格。
1.3.6正确度验证正确度验证以偏倚为评价指标,使用20 份检测结果在参考区间内的新鲜全血,每份标本检测1次,计算20 次检测结果的均值,以校准实验室的定值为标准,计算偏倚。正确度验证的允许偏倚判定标准CV分别:WBC≤5.00%,RBC≤2.00%,Hb≤2.50%,红细胞压积(HCT)≤2.50%,PLT≤6.00%,平均红细胞体积(MCV)≤3.00%,平均血红蛋白含量(MCH)≤3.00%,平均血红蛋白浓度(MCHC)≤3.00%。
1.3.7不同吸样模式的结果可比性验证仪器校准后,取5份全血标本,分别使用手动进样和自动进样2种不同模式进行检测,每份标本各检测2次,计算2种模式下检测结果均值间的偏差,结果应符合《临床血液学检验常规项目的分析质量要求》,偏差要求分别:WBC≤5.00%,RBC≤2.00%,Hb≤2.00%,HCT≤3.00%,MCV≤3.00%,PLT≤7.00%。
1.3.8仪器间可比性验证取20份临床标本,有一定浓度要求,以该科内部规范操作检测系统(贝克曼LH780 分析仪)为参考仪器,Sysmex XE5000为比对仪器,分别进行检测,以内部规范操作检测系统(贝克曼LH780 分析仪)的测定结果为标准,计算相对偏差,WBC、RBC、Hb、PLT、HCT、MCV、MCH、MCHC 结果偏倚符合WS/T406-2012《临床血液学检验常规项目分析质量要求》中要求的比例(≥80%)。
1.3.9准确度验证使用5份北京市室间质评物分别进行单次检测,计算5份标本检测结果与靶值(室间质评反馈结果)的相对偏差,每个检测项目的相对偏差符合《临床血液学检验常规项目的分析质量要求》(行业标准)比例(≥80%)。各参数变异系数分别为:WBC 5.00%,RBC 6.00%,Hb 6.00%,HCT 9.00%,PLT 20.00%,MCV 7.00%,MCH 7.00%,MCHC 8.00% 。
2 结 果
2.1本底计数Sysmex XE5000血液分析仪检测WBC、RBC、Hb、PLT本底值均为“0”,符合判定标准,验证合格。
2.2携带污染率WBC、RBC、Hb、PLT 的携带污染率分别为0.05%、0.15%、0、0.09%, 均小于标准1%,符合判定标准,验证合格。
2.3批内精密度正常水平全血标本检测后,WBC、RBC、Hb、HCT、PLT、MCV、MCH、MCHC 的CV值分别为1.95%、0.42%、0.25%、0.90%、1.02%、0.55%、0.46%、1.08%,均小于判定标准(3.75%、1.50%、1.00%、1.50%、4.00%、1.00%、2.00%、2.00%),验证合格。
2.4日间精密度本试验检测的中、低2个水平的质控品,其中中值水平的CV值为:WBC 1.08%,RBC 0.57%,Hb 0.52%,HCT 1.10%,PLT 1.70%,MCV 0.94%,MCH 0.84%,MCHC 1.30%;低值水平的CV值为:WBC 1.86%,RBC 0.77%,Hb 0.99%,HCT 1.37%,PLT 3.85%,MCV 0.93%,MCH 1.16%,MCHC 1.17%均小于判定标准。验证合格。
2.5线性范围WBC、RBC、Hb、PLT 4项的线性范围验证,a值(1.00±0.05)及r(≥0.975)均在判定标准要求范围内,验证合格。见表1。
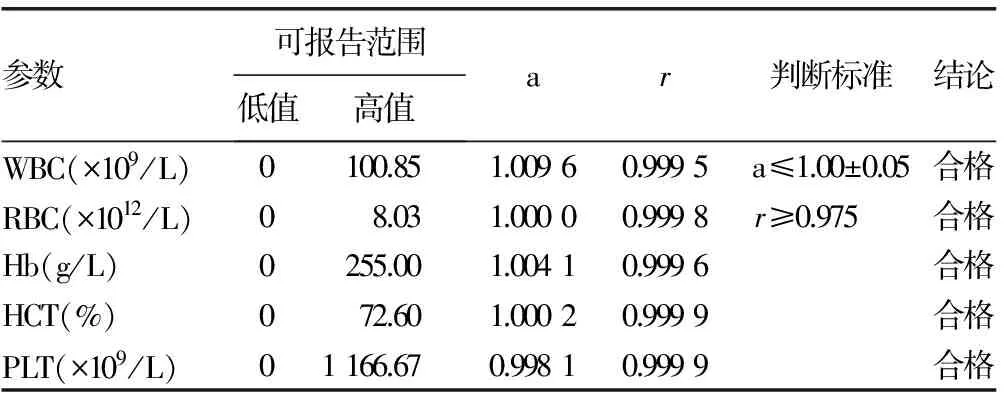
表1 Sysmex XE5000线性范围评价结果
2.6正确度以实验室内部规范操作检测系统的测定均值为标准,进行本仪器检测的WBC、RBC、Hb、HCT、PLT、MCV、MCH、MCHC均值计算偏移。结果WBC、RBC、Hb、HCT、PLT、MCV、MCH、MCHC的偏移分别为4.73%、1.99%、1.72%、0.45%、1.99%、2.72%、1.05%、2.02%;均小于WS/T406-2012 判定标准,正确度验证合格。
2.7不同吸样模式可比性手动进样模式与自动进样模式WBC、RBC、Hb、HCT、MCV、PLT的偏差分别为3.94%、0.84%、0.15%、1.03%、0.16%、4.72%,均小于WS/T406-2012判定标准,不同吸样模式可比性验证合格。
2.8仪器间可比性Sysmex XE5000分析仪与贝克曼 LH780分析仪的可比性结果,20 份标本的WBC、RBC、Hb、PLT、HCT、MCV、MCH、MCHC 结果偏倚符合率分别为90%、100%、100%、90%、100%、100%、100%、100%,均大于80%,符合WS/T406-2012 判定标准,验证合格。
2.9准确度使用5份北京市质评物进行单次检测,计算每份标本检测结果与靶值(室间质评反馈结果)的相对偏差,WBC、RBC、Hb、PLT、HCT、MCV、MCH、MCHC结果偏差分别为:1号质控物0.5%、2.6%、0、3.3%、0、0.5%、2.9%、3.4%;2号质控物0.4%、2.1%、1.5%、4.9%、0.9%、2.6%、1.0%、3.8%;3号质控物1.0%、3.2%、1.1%、4.1%、1.2%、0.5%、2.4%、3.2%;4号质控物1.1%、1.7%、0.7%、4.9%、2.6%、3.1%、0.7%、4.1%;5号质控物:2.2%、0.8%、1.5%、4.6%、1.4%、3.4%、0.6%、2.9%。均小于WS/T406-2012 判定标准,验证合格。
3 讨 论
Sysmex XE5000血细胞分析仪是目前临床广泛应用的仪器之一,其检测结果的准确性直接影响临床对疾病的诊断和治疗[8]。但该仪器使用的进口试剂价格昂贵,本研究探讨剩余试剂进行仪器方法学验证,为检测结果提供溯源性。ISO15189明确要求:分析系统应具有完整性和有效性,实验室应使用与分析系统相适应的试剂、校准品、质控品和消耗品等,并应提供测定结果的溯源性[9]。近年来原卫生部及各级临床检验中心也一再明确要求保证分析系统有效性。实际工作中由于成本因素,进行剩余试剂的合并使用,但并未进行仪器方法学验证,缺乏依据,影响系统的完整性、有效性。本研究利用EP15A CLSI标准化文件,对该仪器有效期内、正确保存的合并剩余试剂进行仪器的性能验证,结果表明,仪器的本底计数、携带污染率、批内精密度、日间精密度、线性范围、正确度、不同吸样模式可比性、仪器间可比性、准确度均达到WS/T406-2012 判定标准。
本研究结果显示,Sysmex XE5000全自动血液分析仪可对稀释液、4DL、FFS的剩余试剂合并再利用,且能保证检测质量,有效降低检测成本;同时,根据使用Sysmex XE5000的总结,并且查阅大量文献,Sysmex XE5000全自动血液细胞分析仪性能良好,具有携带污染率低、精密度高、线性范围宽及结果准确等优点,能够满足大、中型医院的临床检测需求[10-11]。
[1]中国合格评定国家认可委员会.ISO 15189医学实验室质量和能力认可准则[S].北京:中国合格评定国家认可委员会,2008:1236.
[2]Hedley BD,Keeney M,Chin-Yee I,et al.Initial performance evaluation ofthe UniCel(R)DxH 800 Coulter(R) cellularanalysis system[J].Int J Lab Hematol,2011,33(1):45-56.
[3]陆进,金燕,吴元健.Sysmex XE5000血液分析仪检测非血体液细胞的性能评价[J].临床检验杂志,2012,30(4):318-319.
[4]何俊,陈莉,赵美英.Sysmex XT5000i 全自动血液细胞分析仪应用评价[J].国际检验医学,2009,30(9):917-920.
[5]叶应妩,王毓三,申子瑜.全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:496.
[6]刘志昂,陆婷婷,苏靖凯.BC-5380全自动血细胞分析仪的性能评价[J].实验与检验医学,2013,31(4):407-408,395.
[7]胡晓波,宋颖,王青,等.ICSH血液分析仪评价指南介绍(2004年版上)[J].检验医学,2014,29(12):1201-1206.
[8]彭黎明,丛玉隆.我国血细胞自动分析中存在的问题及对策[J].中华检验医学杂志,2005,28(9):885-887.
[9]金逸,王雪琴,陆慧,等.罗氏COBAS化学发光仪残留试剂检测CA72-4、CYFRA211的初步评估[J].中国血液流变学杂志,2012,22(4):698-699.
[10]丛玉隆,乐家新.Sysmex XE2100 自动血细胞分析和白细胞分类的复检规则探讨[J].中华检验医学,2008,31(7):752-757.
[11]夏万宝,张冬青,侯彦强,等.XE2100型血液分析仪应用性能评价[J].国际检验医学杂志,2015,31(21):3194-3197.
,E-mail:sjslab@163.com。
10.3969/j.issn.1673-4130.2016.19.061
A
1673-4130(2016)19-2790-02
2016-02-11
2016-06-24)
