恩替卡韦对乙型肝炎患者干扰素诱导单核因子作用*
2016-11-04张利霞
张利霞
(遵义医学院第五附属(珠海)医院感染科,广东珠海 519100)
·论著·
恩替卡韦对乙型肝炎患者干扰素诱导单核因子作用*
张利霞
(遵义医学院第五附属(珠海)医院感染科,广东珠海 519100)
目的探讨恩替卡韦抗病毒治疗过程中不同时期慢性乙型肝炎(HBV)患者外周血中干扰素诱导单核因子(Mig)的水平变化。方法40例应用恩替卡韦治疗的慢性乙型肝炎患者,采用ELISA 法定量检测治疗前后的血清Mig水平,并同时检测乙型肝炎表面抗原(HBsAg)、乙型肝炎e抗原(HBeAg)、HBV DNA水平。结果使用恩替卡韦抗病毒治疗后,血清Mig及HBsAg、HBeAg、HBV DNA明显下降,且治疗后24周比治疗后12周下降明显,差异均有统计学意义(P<0.05)。结论恩替卡韦能下调Mig,降低血清HBsAg、HBeAg、HBV DNA 水平,有利于控制疾病进展。
慢性乙型肝炎;干扰素诱导单核因子;恩替卡韦
乙型肝炎病毒(HBV)感染是严重危害人类健康的全球性公共卫生问题,每年约100万人病死于与HBV感染相关的疾病[1-3]。既往研究表明细胞免疫异常可能是HBV发病的重要原因[4]。虽然慢性病毒性肝炎的致病机制还未完全清楚,但已明确证实免疫病理损伤起重要作用,其中趋化因子的作用也日益受到重视。现监测服用恩替卡韦治疗慢性乙型肝炎患者不同时期外周血中干扰素诱导单核因子(Mig)水平,探讨Mig在肝脏免疫损伤中的重要作用,并通过恩替卡韦治疗前后Mig水平的动态变化,了解抗病毒药物对患者免疫状态的影响,为临床治疗方案的选择、评价疗效和判断预后提供新的思路,报道如下。
1 资料与方法
1.1一般资料该科2014年1月至2015年12月收治的慢性乙型肝炎患者40例,男33例,女7例,年龄20~50岁,平均年龄(30.5±2.5)岁。均符合《慢性乙型肝炎防治指南(2010年版)》的诊断标准,纳入标准:血清乙型肝炎表面抗原(HBsAg)阳性(+)、乙型肝炎e抗原(HBeAg)阳性(+)、抗-e抗原(抗-HBe)阳性(+)、HBV DNA(+),HBV DNA≥1.0×105copy/mL),丙氨酸氨基转移酶(ALT)升高,且下限高于正常值2倍,病程均超过6个月。排除其他病毒感染和引起肝功能损害的原因。3个月内未曾用过抗病毒和免疫抑制剂治疗。
1.2方法(1)所有患者自愿接受恩替卡韦抗病毒治疗,并签署知情同意书。患者在一般保肝、降酶、退黄治疗基础上给予恩替卡韦(博路定)0.5 mg,口服1次/日,观察24周。(2)分别于用药前、用药12、24周晨起空腹采集外周静脉血3管,每管5 mL,分离血清置-20 ℃冰箱保存备用,分别用于Mig、HBsAg、HBeAg水平及HBV DNA载量检测。(3)采用双抗体夹心酶联免疫(ELISA)法检测Mig,试剂采用上海江莱生物科技有限公司提供的Mig试剂盒,严格按照说明书进行操作。使用免疫荧光定量,应用该院检验科提供的罗氏E-170及配套试剂检测HBsAg和HBeAg水平,运用荧光定量聚合酶链反应(PCR),采用该院检验科提供的伯乐PCR分析仪及配套试剂进行HBV DNA载量检测。
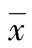
2 结 果
2.1患者治疗前后各指标检测结果比较40例患者治疗12、24周后血清Mig与HBsAg、HBeAg、HBV DNA水平明显下降,与治疗前比较,差异有统计学意义(P<0.05)。治疗24周与治疗12周比较,差异有统计学意义(P<0.05)。见表1。
2.2采用Spearman相关性分析不同时期Mig与HBsAg、HBeAg、HBV DNA水平变化的相关性显示,患者治疗前Mig水平与HBsAg、HBeAg、HBV DNA水平呈负相关(r=-0.462,P<0.05),治疗12、24周Mig水平与HBsAg、HBeAg、HBV DNA水平呈正相关(r=0.153,P<0.05)。
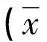
表1 患者治疗前后各指标检测结果比较±s)
注:与治疗前比较,△P<0.05; 与治疗12周比较,*P<0.05。
3 讨 论
HBV感染引起肝脏炎性中T 淋巴细胞介导细胞免疫参与其发生发展,而淋巴细胞迁移至肝细胞的过程受多种因子的影响,其中发现趋化因子与淋巴细胞受体的相互结合是重要因素之一。趋化因子是一类能使细胞发生趋化作用的细胞因子总称,在对外界抗原刺激产生免疫应答过程中可吸引活化的T淋巴细胞、单核细胞及自然杀伤细胞等,通过 G蛋白偶联受体途径进入炎性损伤区域并发挥作用[5]。干扰素诱导蛋白-10(IP-10)和Mig是国内外新发现的CXC类的趋化因子,主要是由干扰素等诱导产生[6]。研究表明在慢性HBV感染应答中,CXC趋化因子IP-10和Mig的高表达可强烈吸引T细胞至肝脏,一方面协助机体清除感染肝细胞,另一方面通过分泌损害肝脏炎性递质导致肝病进展[7]。Kakimi等[8]利用HBV转基因鼠模型,被动转导对HBV特异的CTL,发现肝脏中IP-10和Mig迅速增高,如果阻断这些趋化因子就会减少宿主源性单核细胞在肝脏的浸润,从而降低肝组织损伤的严重性。有证据表明肝炎病毒感染可诱导感染肝细胞及血管内皮细胞高表达趋化因子IP-10,表达CXCR3的T细胞可受IP-10的吸引,迁移至感染的组织,导致大量肝细胞损伤[9-10]。由于炎性部位肝细胞大量坏死,损伤可能进一步导致被动脱落进入血液循环的IP-10明显增加,而血清IP-10水平与肝脏炎性损害程度有关,也就是说肝脏炎性损害程度越重,血清IP-10水平越高。临床上对IP-10的研究报道甚多,而对Mig的研究相对较少。本研究通过对40例运用恩替卡韦抗病毒治疗的患者不同时期Mig表达水平进行分析比较,证实治疗后Mig水平均低于治疗前,差异有统计学意义(P<0.05)。
目前慢性乙型肝炎的治疗以抗病毒抑制病毒复制为主,无法彻底清除乙型肝炎病毒,而抗病毒治疗最理想的目标是能够达到HBsAg血清学转换,其次是达到HBeAg血清学转换和维持低水平的病毒载量。国内外研究表明血清HBsAg与HBeAg、HBV DNA载量之间有一定相关性,监测血清HBsAg水平能够较准确地反映HBV DNA在体内的复制情况[11]。有学者研究表明,HBsAg和HBV DNA水平之间有良好的相关性,定量检测血清HBsAg可反映宿主体内HBV DNA水平,对评价抗病毒治疗的疗效和判断预后具有重要意义[12]。目前恩替卡韦(博路定)是临床常用的环戊基鸟嘌呤核苷类抗病毒药物,其三膦酸盐与HBV多聚酶的天然底物dGTP竞争,可抑制HBV复制过程中的DNA多聚酶启动、反转录及HBV DNA正链合成过程,阻断病毒复制[13]。本研究结果表明,患者治疗12、24周后HBsAg、HBeAg、HBV DNA水平均低于治疗前,差异有统计学意义(P<0.05);治疗24周HBsAg、HBeAg、HBV DNA水平均低于治疗12周,差异有统计学意义(P<0.05),提示恩替卡韦能有效降低乙型肝炎病毒载量,但慢性乙型肝炎不仅是病毒性疾病,也是免疫性疾病,目标是通过抗病毒治疗实现持久免疫控制,恩替卡韦是否具有免疫调控作用尚不清楚,有待进一步研究证实。
综上所述,趋化因子Mig参与了慢性乙型肝炎的炎性反应,同时也发挥重要的免疫调节作用。Mig可作为疗效监测指标之一,且与HBsAg、HBeAg、HBV DNA有密切联系。应用恩替卡韦抗病毒治疗的过程中检测外周血趋化因子 Mig水平变化,有助于观察机体的免疫状态,为临床合理用药提供依据,同时对Mig机制的深入研究,将有利于进一步了解慢性乙型肝炎患者炎性发生、发展的机制。
[1]Lai CL,Ratziu V,Yuen MF,et al.Viral hepatitis B[J].Lancet,2003,362:2089-2094.
[2]Tan C,Xuan B,Hong J,et al.RNA interference against hepatitis B virus with endoribonuclease-prepared siRNA despite of the target sequence wariations[J].Virus Res,2007,126:172-178.
[3]Snyder LL,Esser JM,Pachuk CJ,et al.Vector design for liver-specific expression of multiple interfering RNAs that target hepatitis B virus transcripts[J].Antiviral Res,2008,80:36-44.
[4]罗亚文,林世德,罗军敏,等.重型乙型肝炎患者血清干扰素诱导蛋白-10、干扰素的检测及临床意义[J].中华传染病杂志,2008,26(4):244-247.
[5]Wang J,Zhao JH,Wang PP,et al.Expression of CXC chemokine IP-10 in patients with chronic hepatitis B[J].Hepatobiliary Pancreat Dis Int,2008,7(1):45-50.
[6]Liu MT,Chen BP,Oertel P,et al.The T cell chemoattrant IFN-inducible protein 10 is essential in host defense against viral-induced neurologic disease[J].J Immunol,2000,165:2327-2330.[7]赵金红,钱丽丽.趋化因子及其受体在肝脏疾病中的作用[J].齐齐哈尔医学院学报,2006,27(4):42.
[8]Kakimi K,Lane TE,Wieland S,et al.Blocking chemokine responsive to gamma-2/interferon IFN-gamma inducible protein and monokine induced by IFN-gamma activity in vivo reduces the pathogenetic but not the antiviral potential of hepatitis B virus-specific cytotoxic T lymphocytes[J].J Exp Med,2001,194(12):1755.
[9]Vadan R,Gheorghe L,Becheanu G,et al.Predictive factors for the severity of liver fibrosis in patients with chronic hepatitis C and moderate alcohol consumption[J].Rom J Gastroenterol,2003,12(3):183-187.
[10]Boisvert JJ,Sarobe P,Boya PH,et al.A recombinant adenovirus encoding hepatitis C virus core and E1 proteins protects mice against cytokine-induced liver damage[J].Hepatology,2003,37(2):461-470.
[11]江宇泳,李红梅,王融冰.慢性乙型肝炎病毒感染与T淋巴细胞亚群的变化[J].中国医刊,2008,43(3):204.
[12]卢峰,廖雪雁,石爽,等.乙型肝炎病毒表面抗原定量检测的临床意义[J].肝脏,2009,14(2):65.
[13]Inada M,Yokosuka O.Current antiviral therapies for chronic hepatitis B[J].Hepatol Res,2008,38(6):535-542.
The function of entecavir to Mig in patients with chronic hepatitis*
ZHANGLixia
(DepartmentofHospitalInfection,theFifthAffiliatedHospitalofZunyiMedicalCollege,Zhuhai,Guangdong519100,China)
ObjectiveTo investigate the function of entecavir to γ-interferon induced monokine(Mig) for chronic hepatitis B patients.MethodsThe 40 cases of chronic hepatitis B patients were treated with entecavir tablet.The Mig level were detected by ELISA in 40 patients in the time before and after treatment of 12 weeks and 24 weeks;HBsAg,HBeAg level were analyzed by using electrochemiluminescence and HBV-DNA was tested by using real-time quantitative PCR(FQ-PCR).ResultsMig and HBsAg,HBeAg,HBV DNA levels were significantly lower than before treatment in the 40 patients(P<0.05).Compared with those in the time of 12 weeks after treatment,those indexes after treatment 24 weeks were significantly decreased(P<0.05).ConclusionEntecavir treatment can reduce the level of Mig,HBsAg and HBeAg,HBV DNA,and help to control disease progression in chronic hepatitis B.
chronic hepatitis B;γ-interferon induced monokine;entecavir
广东省珠海市卫生和计划生育委员会医学科研课题(2014087)。
张利霞,女,主治医师,主要从事临床病毒性肝炎的诊治研究。
10.3969/j.issn.1673-4130.2016.19.001
A
1673-4130(2016)19-2661-03
2016-04-20
2016-06-15)
