复方沙棘片的制备和质量标准研究
2016-11-01王小宁杨黎彬张存劳
王小宁,杨黎彬,张存劳
(西安医学院,陕西西安710021)
复方沙棘片的制备和质量标准研究
王小宁,杨黎彬,张存劳
(西安医学院,陕西西安710021)
优化复方沙棘片的制备工艺和处方,研究制定复方沙棘片的质量标准。以颗粒性状、片剂的外观、硬度和崩解时限为指标,确定最优制备工艺和处方;采用薄层色谱鉴别法对复方沙棘片中总黄酮和原花青素进行定性鉴别;采用紫外-可见分光光度法对有效成分总黄酮和原花青素进行定量测定。结果表明,复方沙棘片的最优处方和制备工艺为:以淀粉和糊精(2∶1)的混合物为稀释剂,60%乙醇为黏合剂,0.5%硬脂酸镁为润滑剂,用16目筛湿法制粒,50℃下干燥60 min,整粒后压片。薄层色谱鉴别法专属性强,黄酮、原花青素的斑点清晰,紫外-可见分光光度法测定沙棘总黄酮和葡萄籽原花青素的线性范围分别为:0.01 mg/mL~0.05 mg/mL(r=0.999 0),0.01 mg/mL~0.05 mg/mL(r=0.999 5),平均加样回收率分别为 100.36%(RSD=0.97%,n=5)、98.53%(RSD=2.66%,n=5)。所制的复方沙棘片外观好、硬度适中、崩解速度快,所建立的定性、定量分析方法简便易行,准确度高,能够有效控制片剂的质量。
沙棘;葡萄籽;原花青素;片剂;质量标准
沙棘(Hippophae rhamnoides)为胡颓子科酸刺属的灌木或小乔木,别名醋柳、黑刺、酸刺,我国主要分布在西北、华北、东北及西南等十多个省区。沙棘为药食同源植物,它含有多种生理活性物质,如 VC、VE、VA、胡萝卜素、叶酸、氨基酸、蛋白质、不饱和脂肪酸等,能提高人体免疫能力、抗肿瘤、有效防止冠心病和动脉粥样硬化以及抗氧化抗衰老等,因此具有很好的营养保健和药用价值[1-2]。原花青素(proanthocyanidins,PC)是天然植物中广泛存在的一大类多酚类化合物的总称,是目前为止所发现的最强的抗氧化剂和自由基清除剂[3]。已有研究证实葡萄籽提取物中原花青素的含量丰富,因此目前对葡萄籽中原花色素的开发利用备受重视[4-5]。沙棘和原花青素因其较高的生物活性价值被认可,但在开发保健药品方面涉及的比较少。本实验立足于沙棘提取物和葡萄籽提取物的保健功效,将其作为片剂主要成分,研究复方沙棘片剂的处方和制备工艺,并建立片剂的质量标准,为沙棘和原花青素的开发利用提供参考。
1 材料与仪器
1.1 仪器
101-3-5型电热恒温鼓风干燥箱:上海跃进医疗器械厂;北洋YD-20型智能片剂硬度仪、ZB-1D型智能崩解仪:天津天大天发科技有限公司;KQ3200E型超声波清洗器:昆山市超声仪器有限公司;BS210S电子分析天平:北京赛多利斯天平有限公司;UV762紫外-可见分光光度计:上海佑科有限公司;方筛(12、16、100目)。
1.2 试剂
沙棘果粉、葡萄籽提取物:青海康普德生物科技股份有限公司;糊精(药用级)、淀粉(药用级)、硬脂酸镁(药用级)、滑石粉(药用级)、微粉硅胶(药用级):智诚生物科技有限公司;芦丁标准品(批号:MUST-13040302)、原花青素标准品(批号:MUST-13031802):成都曼斯特生物科技有限公司。
2 方法与结果
2.1 处方筛选
2.1.1 稀释剂的选择
选择淀粉与糊精不同配比的混合物作为稀释剂,用60%的乙醇作为黏合剂制备软材,16目筛制粒,在60℃的恒温干燥箱中烘干,16目整粒,冷却后称重,加入总量0.5%的硬脂酸镁,混匀送入压片机压片,考察制粒过程中的颗粒成型比及产品的光洁度、硬度、崩解度,结果见表1。

表1 不同稀释剂对制粒及压片的效果Table 1 The effect of different diluents on granulation and tablet
由表1可知,当淀粉和糊精以2∶1的比例混合时,颗粒成型性较好,片面光洁,硬度和崩解时限均符合要求。故选用这一配比固定稀释剂来考察其他辅料对该压片工艺的影响。
2.1.2 黏合剂的选择
以淀粉和糊精(2∶1)的混合物作为稀释剂,分别用水、30%乙醇、60%乙醇,30%PEG乙醇溶液作为黏合剂,16目筛制粒,烘干后,16目筛整粒,称重后加入0.5%的硬脂酸镁混匀后压片,考察制得颗粒及压片效果,结果见表2。

表2 不同黏合剂对制粒及压片的效果Table 2 The effect of different adhesives on granulation and tablet
由表2可知,淀粉和糊精的混合物本身黏性不大,需要加入黏度较高的黏合剂;60%的乙醇溶液作为黏合剂,黏合效果最好,容易制粒,颗粒具有很好的可压性,优于其它3种黏合剂。
2.1.3 润滑剂的选择
以淀粉和糊精(2∶1)的混合物作为稀释剂,60%的乙醇溶液作为黏合剂,16目筛制粒,16目筛整粒。称重后分为3份,分别加入总量0.5%的硬脂酸镁、滑石粉、微粉硅胶,混合均匀后分别压片,考察压片的效果。结果见表3。
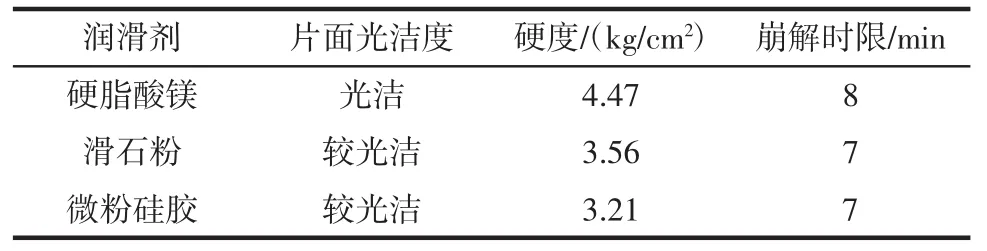
表3 不同润滑剂对制粒及压片的效果Table 3 The effect of different lubricants on granulation and tablet
试验结果表明滑石粉和微粉硅胶润滑效果一般;硬脂酸镁润滑效果较好,片剂表面光滑。通过试验对比,可以选择0.5%硬脂酸镁作为该沙棘复方片剂的润滑剂。
2.2 制备工艺优化
2.2.1 制粒粒径的选择
按选定处方制备软材后分为2份,分别用14、16目筛制粒,50℃烘干60 min,分别用14、16目筛整粒。同时考察片剂的硬度、表面光洁度、崩解时限。实验结果见表4。
由表4可知,各粒径均较易制粒,16目筛制粒后,颗粒均匀性好,片剂表面光滑度较好,从整体效果考虑,16目筛制粒效果最佳。

表4 不同粒径对制粒和压片的效果Table 4 The effect of different size on granulation and tablet
2.2.2 烘干时间的选择
按选定处方制粒,将制备的颗粒平均分为3份于恒温干燥箱中50℃下干燥,分别在60、80、100 min时从干燥箱中取出,加入润滑剂混匀后进行压片,检查片剂的表面光洁度、硬度、崩解时限,结果见表5。

表5 不同烘干时间对制粒和压片的效果Table 5 The effect of different drying time on granulation and tablet
由表5可知,当干燥时间为100 min时,颗粒较硬,时间为60、80 min时,颗粒松散度较好且片剂光滑度较好,综合片剂的硬度和崩解时限,将烘干时间选定在60 min。
2.2.3 烘干温度的选择
按选定的处方制粒,将制备的颗粒平均分为3份于恒温干燥箱中,分别在40、50、60℃下干燥60 min后,从干燥箱中取出,加入润滑剂混匀后进行压片,检查片剂的表面光洁度、硬度、崩解时限,结果见表6。

表6 烘干温度对制粒和压片的效果Table 6 The effect of drying temperature on granulation and tablet
由表6可知,当温度在60℃时,片剂表面光洁度和硬度均较好。
综上所述,通过单因素考察法确定最佳工艺为:制粒粒径为16目、干燥时间为60 min、烘箱温度为50℃。最佳处方为:稀释剂为淀粉和糊精(2∶1)的混合物、黏合剂为60%乙醇、润滑剂为0.5%硬脂酸镁。
2.3 TLC鉴别
2.3.1 供试液、对照品溶液和阴性对照液的制备
取复方沙棘片剂6片,捣碎,取粗粉约2.0 g,精密称定,将粉末置50 mL具塞锥形瓶中,加60%乙醇50 mL,超声5 min,放冷,称重,用60%乙醇补足减失重量,用干燥滤纸过滤,精密量取续滤液1 mL,作供试液。分别精密称取芦丁对照品5.0 mg,用60%乙醇制成浓度为0.1 mg/mL的芦丁对照品溶液和原花青素对照品溶液。阴性对照液:模拟复方沙棘片的制备方法,不加沙棘和葡萄籽提取物制备片剂,用60%乙醇提取后作阴性对照液。
2.3.2 黄酮的TLC鉴别
照薄层色谱法(中国药典2010年版一部附录ⅥB)分别吸取对照品和样品溶液3 μL,点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以v(甲苯)∶v(乙酸乙酯)∶v(甲酸)= 5∶2∶1 为展开剂,展开,取出,晾干,置紫外灯(254 nm)下视检,样品色谱中,在与对照品色谱相应的位置上,显示出相同颜色的斑点。结果见图1。

图1 黄酮的薄层鉴别Fig.1 TLC chromatogram of Proanthocyanidins
2.3.3 原花青素的TLC鉴别
照薄层色谱法(中国药典2010年版一部附录ⅥB)分别吸取对照品和样品溶液3 μL,点于同一以羧甲基纤维素钠为黏合剂的硅胶G薄层板上,以v(甲苯)∶v(丙酮)∶v(乙酸)= 3∶4∶1为展开剂,展开,展距 8 cm,取出,晾干,置紫外灯(254 nm)下视检,样品色谱中,在与对照品色谱相应的位置上,显示出相同颜色的斑点,结果见图2。
2.4 含量测定
2.4.1 最大吸收波长的确定
按2.4.2项下的方法分别对芦丁标准品溶液显色,在400 nm~700 nm波长处扫描,结果显示芦丁标准品在510 m波长处有最大吸收,原花青素标准品在570 nm处有最大吸收。

图2 原花青素的薄层鉴别Fig.2 TLC chromatogram of Proanthocyanidins
2.4.2 标准曲线的建立
分别精密量取“2.3.1”项下的芦丁对照品溶液0.0、1.0、2.0、3.0、4.0、5.0 mL 至 10 mL 容量瓶中,各加 60%乙醇溶液使成5 mL,精密加入5%NaNO2溶液0.3 mL,摇匀,静置6 min,加入10%Al(NO3)30.3 mL,摇匀,静置6 min;加入4%NaOH溶液4mL,摇匀,用60%乙醇定容至刻度,摇匀,静置15 min显色,于510 nm波长处测定其吸光度[6]。以吸光度A为纵坐标,对照品浓度C(mg/mL)为横坐标绘制标准曲线,得线性回归方程 A=6.610 0C+0.017 7,r=0.999 0,芦丁的线性范围为0.01 mg/mL~0.05 mg/mL。
分别精密量取“2.3.1”项下的原花青素对照品溶液0.0、1.0、2.0、3.0、4.0、5.0 mL 于 10 mL 容量瓶中,加入1%香草醛溶液2.25 mL,8%盐酸溶液1.75 mL,用甲醇定容至10 mL,摇匀,显色20 min,于529 nm处测量吸光度值[7]。以吸光度A为纵坐标,对照品浓度C(mg/mL)为横坐标绘制标准曲线,得线性回归方程A=14.880C+0.009 2,r=0.999 5,原花青素的线性范围为0.01 mg/mL~0.05 mg/mL。
2.4.3 精密度试验
精密量取芦丁对照品溶液,按照“2.4.2”项下的方法显色,在510 nm处连续测定6次吸光度,其RSD为0.2%,精密量取1.0 mL原花青素对照品溶液,按照“2.4.2”项下的方法显色,在529 nm处连续测定6次吸光度,RSD为0.1%。结果表明:该法仪器的精密度良好。
2.4.4 重复性试验
取供试品溶液5份,按照“2.4.2”项下方法分别对总黄酮和原花青素成分显色,测定吸光度,计算总黄酮成分的RSD为0.20%,原花青素成分的RSD为0.45%。结果表明:该方法重复性良好。
2.4.5 稳定性试验
分别精密量取供试品溶液,按照“2.4.2”项下方法显色后,分别于 0、1、4、8、12、24 h 测定其吸光度,计算总黄酮成分的RSD为2.38%(n=5),原花青素成分的RSD为1.31%(n=5)。结果表明:供试品溶液中的总黄酮和原花青素成分在24 h内稳定。
2.4.6 加样回收率试验
分别精密量取已知含量的处方溶液各5份,每份1.0 mL,分别加入芦丁对照品和原花青素对照品溶液0.1、0.2、0.3、0.4、0.5 mL,按照“2.4.2”项下方法显色,于510 nm波长下测定吸光度,计算其加样回收率,结果表明:该法测定结果的准确度较高。结果见表7。
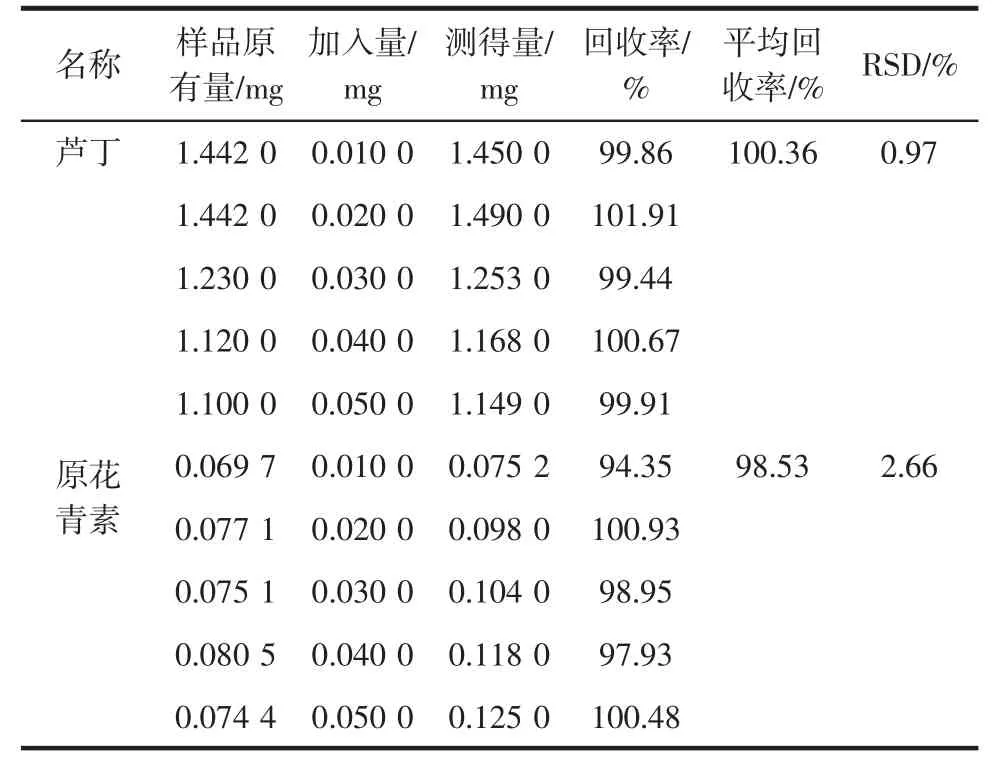
表7 加样回收率试验结果(n=5)Table 7 Results of the sample recovery tests(n=5)
2.4.7 样品测定
取三批复方沙棘片,按2.3.1项下方法制备供试液,按总黄酮和原花青素含量测定方法测定吸收度,计算总黄酮和原花青素的含量,结果见表8。
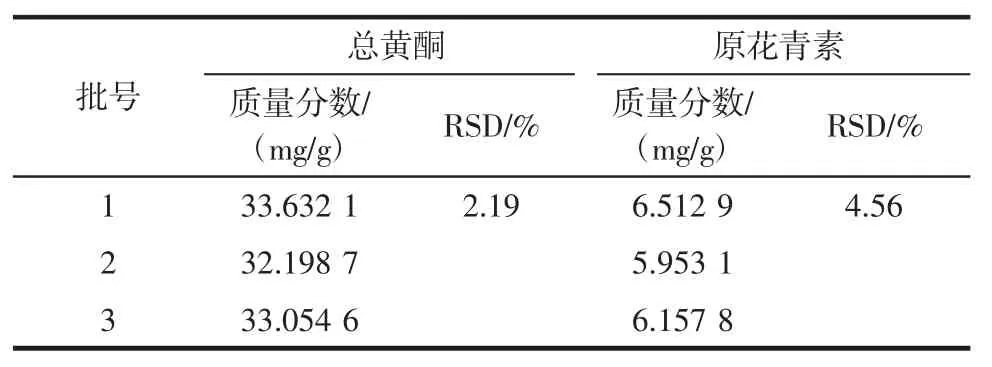
表8 样品含量测定结果Table 8 Results of content determination in 3 batches of samples
3 讨论
1)通过单因素考察法确定复方沙棘片的最佳制备工艺为:制粒粒径为16目、干燥时间为60 min、烘干温度为50℃。最优处方为:稀释剂为淀粉和糊精(2∶1)混合物、黏合剂为60%乙醇、润滑剂为0.5%硬脂酸镁。
2)本研究采用薄层色谱(TLC)法对复方沙棘片中的沙棘黄酮和原花青素进行了定性鉴别,所采用的方法具有较强的专属性,斑点清晰,分离效果好。
3)目前研究中沙棘的检测方法常用的有:高效液相色谱法和紫外-可见分光光度法,但高效液相色谱法常用来测定单一成分,紫外法多用来测定总含量[8]。复方沙棘片中的总黄酮和原花青素的含量测定选用紫外-可见分光光度法,测定方法简便、可行,其中原花青素的含量测定根据文献报道采用改良后的方法,显色时间较快,显色稳定性较好[9]。该含量测定方法既满足了沙棘总黄酮和原花青素的含量测定要求又节约了试验成本,达到了试验预期的效果。
4)本研究所制备的复方沙棘片的保健效果及功效还有待考究,后期本课题组将对片剂功能性成分的释放及对人体的保健效果进行深入探索。沙棘和原花青素的药理作用使其在食品、药品以及化妆品领域均有广阔的前景,值得进一步研究。
[1] 刘勇,廉永善,王颖莉,等.沙棘的研究开发评述及其重要意义[J].中国中药杂志,2014,39(9):1547-1552
[2] 张郁松,罗仓学.沙棘资源开发与沙棘黄酮提取[J].食品研究与开发,2005,26(3):46-47
[3] 张冰若,劳业兴,苏薇薇.原花青素的研究现状及开发前景[J].中药材,2003,26(12):90-95
[4] 辛立波,李晓波,於洪建,等.葡萄籽低聚原花青素化学成分及抗氧化研究[J].食品研究与开发,2012,33(8):40-43
[5] 赵超英.葡萄籽提取物原花青素的营养保健功能[J].中国食品卫生杂志,2000,12(6):38-40
[6] 郑京.沙棘叶中总黄酮的提取与测定[J].江苏化工,2008,36(1):36-38
[7] 樊金玲,陶冠军,朱文学.香草醛/硫酸比色法测定两种原花色素含量的比较[J].食品科学,2007,28(9):467-472
[8] 陆敏,张绍岩,张文娜.高效液相色谱法测定沙棘汁中7种有机酸[J].食品科学,2012,33(14):235-237
[9] 李春阳,许时婴,王璋.低浓度香草醛-盐酸法测定葡萄籽、梗中原花青素含量的研究[J].食品工业科技,2004,25(6):128-133
Study on Preparation and Quality Standard of Compound Sea Buckthorn Tablets
WANG Xiao-ning,YANG Li-bin,ZHANG Cun-lao
(Xi'an Medical University,Xi'an 710021,Shaanxi,China)
To optimize the preparation and prescription of tablets and study the quality standards of sea buckthorn tablets.Used mesh size,drying time and drying temperature as factors to determine the best preparation process,and used the different kinds of fillers,adhesives,lubricants as factors to optimize the prescription.The total flavonoids and proanthocyanidins were identified by TLC and determined by UV-visible spectrophotometry.Use a mixture of starch and dextrin (2 ∶1)as the filler,60%ethanol as binder and 0.5%magnesium stearate as lubricant.Granulate by 16 mesh sieve with 50℃as drying temperature and 60 min as drying time.The identification method was exclusive.The TLC sports were fairly clear.The determination of flavonoids and proanthocyanidins kept the good linear relation in the concentration ranges of 0.01 mg/mL~0.05 mg/mL(r=0.999 0),0.01 mg/mL~0.05 mg/mL (r=0.999 5).The average recoveries of flavonoids and proanthocyanidins were 100.36%and 98.53%respectively.The compound sea buckthorn tablets have good appearance,hardness and disintegrate fast.The qualitative and quantitative analysis method is simple and accurate.It can effectively control the quality of the tablet.
hippophae rhamnoides;grape seeds;proanthocyanidins;tablet;quality standard
10.3969/j.issn.1005-6521.2016.14.020
陕西省科技厅项目:沙棘抗氧化功能食品研发(2012k17-04-01)
王小宁(1987—),女(汉),讲师,硕士,主要从事新药研发。
2015-05-13
