顶空气相色谱法同时测定原料药中多种残留溶剂的应用研究
2016-10-15杨丽蓉赵红磊张筱
杨丽蓉 赵红磊 张筱
(潍坊市食品药品检验检测中心,山东 潍坊261205)
顶空气相色谱法同时测定原料药中多种残留溶剂的应用研究
杨丽蓉赵红磊张筱
(潍坊市食品药品检验检测中心,山东 潍坊261205)
目的:建立顶空气相色谱法同时测定原料药中有机溶剂残留量的方法。方法:采用顶空气相色谱法,DB-1701毛细管柱(30 m×0.25 mm×0.25 μm),检测器为氢火焰离子化检测器,氮气为载气,测定原料药中的残留溶剂,用外标法计算。结果:在此色谱条件下,各有机溶剂能得到有效分离,在所考察的浓度范围内线性关系良好,r=0.997 1~0.999 6,精密度介于1.05%~2.57%(n=5)之间,加标平均回收率为96.9%~100.8%。结论:该方法能较好地应用于原料药中多种溶剂残留量的同时测定,能有效地缩短检验时间,提高检验效率。
残留溶剂;顶空气相色谱法;原料药
药品中的残留溶剂系指在原料药或辅料的生产中,以及在制剂制备过程中使用的,但在工艺过程中未能完全除去的有机溶剂[1]。药物残留溶剂分析是化学合成药质量控制的重要环节[2-5]。残留溶剂的测定方法常采用气相色谱法[6-10],顶空气相色谱法不仅能减少对色谱系统的污染,且能富集待测物,提高检测灵敏度[11]。本文尝试用顶空气相色谱法同时测定奥美拉唑和马来酸氯苯那敏原料药中的多种残留溶剂,取得了较好效果。
1 仪器与试药
1.1 仪器
岛津GC-2010型气相色谱仪;DANI HSS8650型顶空进样器。
1.2 试药的种类及选择
N,N-二甲基甲酰胺(DMF),甲醇,乙腈,丙酮和四氢呋喃为色谱纯,甲苯和二氯甲烷为分析纯;样品为奥美拉唑原料药和马来酸氯苯那敏原料药。乙腈、丙酮和二氯甲烷为弱极性试剂,四氢呋喃为中极性试剂,甲醇和乙腈为强极性试剂,以这6种试剂代表常见原料药中的残留溶剂。
2 方法与结果
2.1 色谱条件及色谱柱的选择
鉴于选择的溶剂包含强极性和弱极性,所以选择中极性色谱柱。色谱柱采用 DB-1701毛细管柱(30 m×0.25 mm×0.25 μm),程序升温,起始温度为50℃,维持7 min,以每分钟15℃的速度升温至110℃,再以每分钟20℃的速度升温至190℃;检测器为氢火焰离子化检测器(FID),进样口温度为180℃,检测器温度为250℃,载气为氮气,流速为1.0 mL/min,氢气流速为40.0 mL/min,空气流速为500.0 mL/min,尾吹流速为60.0 mL/min。顶空进样,顶空瓶孵育温度为95℃,孵育时间30 min,定量环温度110℃,传输线温度130℃,分流比10∶1。
2.2 溶液的制备
2.2.1 对照品溶液的制备分别精密称取甲醇301.22 mg,乙腈40.56 mg,丙酮 503.17 mg,四氢呋喃145.32 mg,二氯甲烷60.36 mg,甲苯90.28 mg,分别置10 mL容量瓶中,用N,N-二甲基甲酰胺稀释至刻度,作为对照品贮备液。精密量取各对照品贮备液5.00 mL置同一50 mL量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,作为混合对照品贮备液。
2.2.2 供试品溶液的制备精密称取奥美拉唑原料药和马来酸氯苯那敏原料药各约0.5 g,分别置20 mL顶空瓶中,精密加入N,N-二甲基甲酰胺5.00 mL,密封,作为供试品溶液。
2.3 方法学考察
2.3.1 专属性试验为确保顶空瓶中达到气液平衡,试验考察了95℃时不同孵育时间(15,30,45 min)对结果的影响,结果发现,孵育30 min时各对照品峰面积与孵育45 min时峰面积大小一致,而且大于孵育15 min时的对照品峰面积,这表明在95℃条件下孵育30 min即能达到气液平衡,因此试验采用95℃孵育30 min的顶空条件。
分别取空白溶剂、混合对照品溶液、供试品溶液按“2.1”色谱条件测定,各残留溶剂的分离度均符合要求。供试品溶液色谱图中无干扰峰,专属性良好。气相色谱图见图1~4。

图1 混合对照品溶液气相色谱图

图2 空白溶剂气相色谱图

图3 奥美拉唑原料药气相色谱图
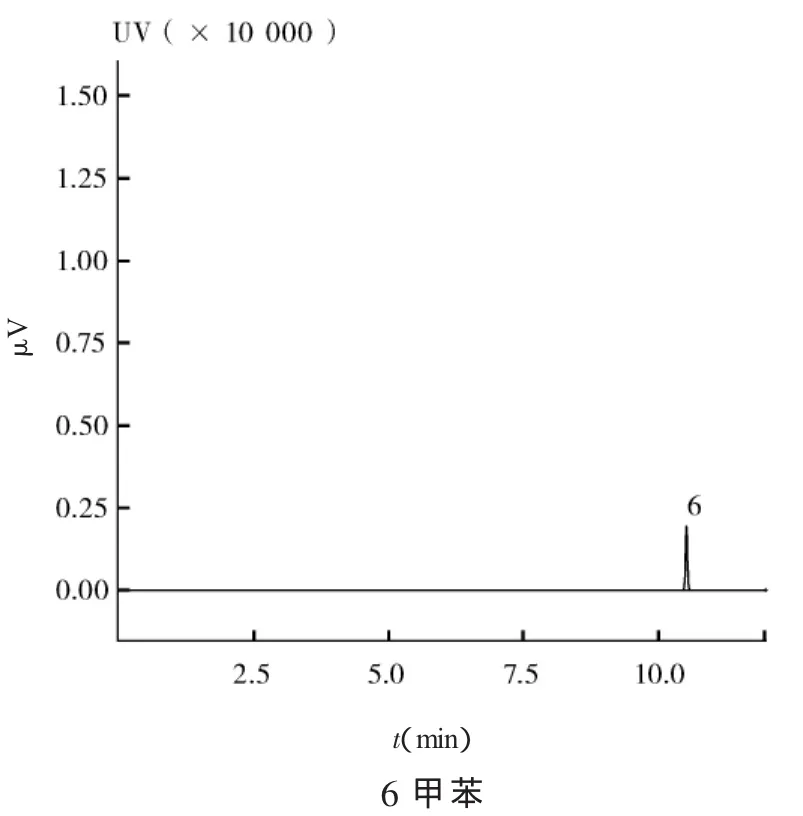
图4 马来酸氯苯那敏原料药气相色谱图
2.3.2 线性关系试验精密量取混合对照品贮备液 0.50,1.00,2.00,3.00,6.00,10.00 mL,分别置50 mL容量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,做为标准曲线的对照品溶液。分别精密量取5.00 mL置20 mL顶空瓶中,密封。按“2.1”项下的色谱条件测定。以质量浓度X (μg/mL)对峰面积Y线性回归,回归方程见表1。2.3.3精密度考察取同一对照品溶液5.00 mL,置于不同20 mL顶空瓶中,按“2.1”方法测定,以相对标准偏差(RSD)进行精密度考察。结果如下:甲醇 1.95%,乙腈 2.57%,丙酮 1.86%,四氢呋喃1.05%,二氯甲烷 2.02%,甲苯2.17%(n=5),表明精密度良好。
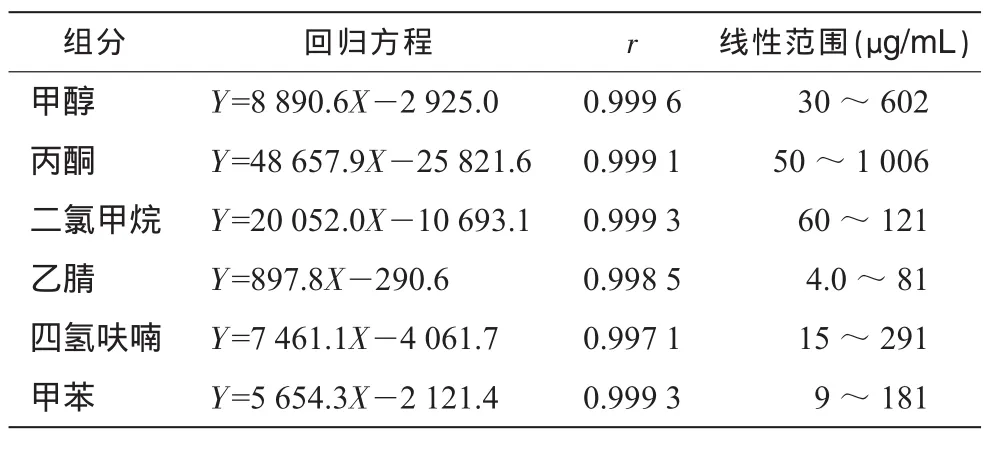
表1 回归方程与线性范围
2.3.4 回收率分别精密量取各对照品贮备液0.40,0.50,0.60 mL分别置 100 mL量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,分别作为80%,100%,120%浓度水平的溶液。分别称取奥美拉唑、马来酸苯那敏原料药各9份于不同顶空瓶(20 mL)中,每份约0.5 g,分别精密加入5.00 mL上述3个浓度水平的溶液,每个水平平行3份。照“2.1”的色谱条件测定,计算回收率。结果如下:甲醇,丙酮,二氯甲烷,乙腈,四氢呋喃,甲苯的平均回收率分别为100.4%,100.5%,99.2%,96.9%,99.3%,100.8%,RSD分别为 2.1%,2.0%,1.9%,2.5%,2.9%,3.0%(n=9),表明方法回收率良好。
2.3.5 检测限取对照品贮备液适量,逐步稀释,根据“2.1”的色谱条件进行测定,按信噪比 S/N 为 3∶1考察,结果甲醇,丙酮,二氯甲烷,乙腈,四氢呋喃,甲苯的最低检测限分别为:0.10,0.05,0.20,0.04,0.14,0.96 μg/mL,能满足检验要求。
2.3.6 稳定性考察取混合对照品储备液3.00 mL 置50 mL容量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀。分别精密量取5.00 mL置20 mL顶空瓶中,密封。按“2.1”项下的色谱条件测定峰面积,与放置12,24,36,48 h分别测定的峰面积的RSD(n=5)均小于5%,说明日内与日间稳定性均良好。
2.3.7 样品测定用“2.1”所述色谱条件对奥美拉唑原料药样品和马来酸氯苯那敏原料药样品进行残留溶剂测定,结果见表2。

表2 样品中残留溶剂的测定结果(n=3) (g/g)
3 讨论
本文以极性不同6种残留溶剂为代表,以两种不同的原料药为样本,建立检测方法,同时测定不同原料药中的各种残留溶剂。通过试验确定了样品95℃孵育30 min即能达到气液平衡,能最大限度地检测出样品中的残留溶剂。试验还考察了方法的线性关系、精密度、回收率和检测限,结果如下:甲醇在30~ 300 μg/mL、丙酮在50~500 μg/mL、二氯甲烷在60~ 601 μg/mL、乙睛在4.0~40.3 μg/mL、四氢呋喃在7.2~72.4 μg/mL、甲苯在9.6~ 96.1 μg/mL范围内线性关系良好,精密度介于1.05% ~ 2.57%(n=5)之间,加标平均回收率为96.9% ~ 100.8%,甲醇、丙酮、二氯甲烷、乙腈、四氢呋喃、甲苯的最低检测限分别为:0.10,0.05,0.20,0.04,0.14,0.96 μg/mL。试验还以奥美拉唑与马来酸氯苯那敏为代表样品进行了残留溶剂的测定,结果良好。试验结果表明,该方法能较好地应用于原料药中多种溶剂残留量的同时测定,能有效地缩短检验时间,提高检验效率。
[1] 国家药典委员会.中华人民共和国药典(2015年版)四部[S].北京:中国医药科技出版社,2015:105.
[2] 雷利利,蒋晔,何小稳.室温离子液体对多种有机溶剂残留的同时顶空分析[J].分析化学,2010,38(4):577-580.
[3] 高伟,许有国,徐广振,等.顶空气相色谱法测定延胡索酸泰妙菌素中有机溶剂残留量[J].广东化工,2012,39(4):163-163,195.
[4] 郑景峰,林晨,陈燕华.顶空气相色谱法同时测定药品包装用复合膜中7种有机溶剂残留量[J].海峡药学,2009,21(12):62-64.
[5] 成海平.化学药物残留溶剂质量标准制定的原则与要求[J].中国新药杂志,2008,17(20):1814-1816.
[6] 高秀蕊,徐英,孙士民,等.顶空进样气相色谱法测定奥美拉唑原料药中的残留溶剂[J].齐鲁药事,2008,27(12):716-717.
[7] 陈小青,朱侃,陈华明,等.盐酸沙格雷酯有机溶剂残留量的GC法测定[J].南京师大学报(自然科学版),2011,34(2):60-63.
[8]章燕,周征.顶空气相色谱法测定氟哌啶醇中有机溶剂残留量[J].中国药业,2012,21(20):36-37.
[9] 马君刚,丁春瑞,营丽君.顶空气相色谱法测定植物油中的溶剂残留量[J].食品工程,2013(4):50-52.
[10] 周丽丽,陆兔林.顶空气相色谱法在中药研究中的应用[J].宜春学院学报,2010,32(12):4-5.
Headspace Gas Chromatography for Simultaneous Determination of Several Residual Solvents in API
Yang Lirong,Zhao Honglei,Zhang Xiao(Weifang Center for Food and Drug Control,Shandong Weifang 261061,China)
Objective:To establish a headspace gas chromatography method for simultaneous determination of several residual solvents in API.Methods:Headspace gas chromatography was performed using nitrogen as carrier gas and FID detectors.Residual solvents were separated by DB-1701 capillary column(30 m×0.25 mm×0.25 μm)and calculated by external standard method.Results:Residual solvents were effectively separated by the method.Good linear relationship was observed within the investigated concentration range(r=0.997 1~ 0.999 6).The precision ranged from 1.05%to 2.57%(n=5),while the mean spike recovery rate was 96.9%~ 100.8%.Conclusion:The developed method may be used for simultaneous determination of various residual solvents in API,by which the test may be shortened effectively and the test efficiency may increase.
Residual Solvents;Headspace Gas Chromatography;API
10.3969/j.issn.1672-5433.2016.09.003
2016-05-10)
杨丽蓉,女,药师。研究方向:化学药品检验。通讯作者E-mail:165617610@qq.com
