H PLC测定清平颗粒中人参皂苷Rg1的含量
2016-10-15石晶萍洪丽萍
石晶萍 洪丽萍
(扬子江药业集团有限公司质量管理部质量检测中心,江苏 泰州225321)
H PLC测定清平颗粒中人参皂苷Rg1的含量
石晶萍洪丽萍
(扬子江药业集团有限公司质量管理部质量检测中心,江苏 泰州225321)
目的:建立高效液相色谱法测定清平颗粒中人参皂苷Rg1含量。方法:色谱柱为Agilent ZORBX Eclipse plus C18(4.6 mm×100 mm,3.5 μm),流动相:乙腈(A)-水(B),检测波长:203 nm,流速:1.0 mL/min,柱温:25℃,进样量:10 μL。结果:人参皂苷Rg1在0.013 2~0.423 0 mg/mL范围内呈良好线性关系,r=1.000 0;回收率:98.0%,RSD:0.3%。结论:该测定方法操作简便,准确可行,可用于清平颗粒中人参皂苷Rg1的定量分析。
高效液相色谱法;清平颗粒;人参皂苷Rg1;含量测定
清平颗粒(成分:羚羊角、赭石、石决明、钩藤、菊花、地黄、女贞子、地龙、川牛膝、天南星(毒)、三七、黄芩、桃仁、玄参、石膏、槐花、薄荷脑)功能:滋阴潜阳,化瘀通络。用于阴虚阳亢或肝阳上亢型高血压,有效改善头痛、眩晕、心悸等症状。人参皂苷Rg1是其主成分三七的主要有效成分之一[1],具有明显的抗炎、镇痛作用,具有促进海马神经元突起生长,提高神经可塑性,增强学习能力与记忆力,抗衰老,抗疲劳,提高免疫力,辅助抗肿瘤,修复性功能等作用,在高端保健、辅助抗肿瘤、防治老年痴呆等神经退行性疾病方面具有广阔的应用前景[2]。其抗氧化作用、抑制NO合成及抑制辣椒素受体激活可能是其发挥作用的机制[3]。
由于清平颗粒的原质量标准(国家食品药品监督管理总局国家药品标准 WS-5247(B-0247)-2014Z)含量测定主要测定清平颗粒的人参皂苷Rg1含量,所以本研究仅针对清平颗粒中主活性成分之一人参皂苷Rg1定量检测开展相关方法学研究。由于原质量标准的含量测定方法是采用薄层扫描法,考虑到薄层扫描法的准确性和重现性较差,现在药典已较少采用,为保证清平颗粒含量测定数据的准确性,本研究参考《中国药典》(2015年版)[4]的高效液相色谱法(HPLC)的相关要求,对清平颗粒中人参皂苷Rg1含量测定的方法进行了研究和方法学验证,结果表明该测定方法准确可行,可用于人参皂苷Rg1的定量分析。现报道如下。
1 试药和试液
清平颗 粒(批号:15010241,15010341,15010541,规格:12 g/袋);人参皂苷 Rg1(批号:110703-201529,含量95.0%,中国食品药品检定研究院提供);甲醇(批号:20130609)、正丁醇(批号:20131025)、氨水(批号:20131108),均由国药集团化学试剂有限公司提供;乙腈(色谱纯,批号:I729430409,Merck)。
2 仪器
美国安捷伦公司的Agilent 1200高效液相色谱仪和 Agilent 1260高效液相色谱仪,瑞士梅特勒公司Mettler Toledo XP205电子天平,昆山市超声仪器有限公司的KQ-250B超声仪,上海索普仪器公司的DZF-6050型真空干燥箱。
3 方法与结果
3.1 色谱条件
色谱柱:AgilentZORBXEclipseplusC18(4.6 mm×100 mm,3.5 μm);流动相:乙腈(A)-水(B);检测波长:203 nm;流速:1.0 mL/min;柱温:25℃;进样量:10 μL,流动相的比例见表1。

表1 流动相比例
3.2 溶液配制方法
3.2.1 对照品溶液的制备取人参皂苷Rg1对照品适量,精密称定,加甲醇制成每1 mL含0.1 mg的溶液,即得,对照品溶液色谱图见图1。

图1 人参皂苷Rg1对照品溶液HPLC图
3.2.2 供试品溶液的制备取本品(批号:15010241)内容物约 2.0 g,研细,精密加入甲醇50 mL,超声(250 W,40 kHz)30 min,滤过,弃去初滤液,精密量取续滤液25 mL,蒸干,残渣加水20 mL溶解,用水饱和的正丁醇振摇提取3次,每次20 mL,合并正丁醇层,再用氨试液充分洗涤2次,每次40 mL,弃去氨液,正丁醇层再用正丁醇饱和的水洗涤2次,每次30 mL,合并正丁醇液蒸干,残渣加甲醇溶解,转移至10 mL量瓶中,加甲醇至刻度,摇匀,即得,供试品色谱图见图2。

图2 供试品溶液HPLC图
3.3 系统适用性、精密度、专属性考察
样品溶液准备:按“3.2”项下方法配制人参皂苷Rg1对照品溶液、供试品溶液,进样顺序:空白溶剂(甲醇),人参皂苷 Rg1对照品溶液,供试品溶液,理论板数按人参皂苷Rg1峰计算应不低于6 000。对照品与供试品理论塔板数按人参皂苷Rg1峰计算均不低于6 000,分离度大于1.5,系统适用性符合要求,结果见表2。

表2 系统适用性考察
3.4 线性关系考察试验
精密称取人参皂苷Rg1对照品11.13 mg,加甲醇制成浓度为0.423 mg/mL的对照品母液,逐级稀释成浓度分别为 0.211 0,0.106 0,0.052 9,0.026 4,0.013 2 mg/mL的对照品溶液。分别精密吸取上述对照品系列溶液各10 μL,由低浓度至高浓度进样。按“3.1”项下色谱条件进行测定。
以对照品浓度(mg/mL)为横坐标,对照品峰面积为纵坐标进行线性回归,绘制标准曲线,结果见表3,表明人参皂苷Rg1在0.013 2~0.423 0 mg/mL范围内线性关系良好。
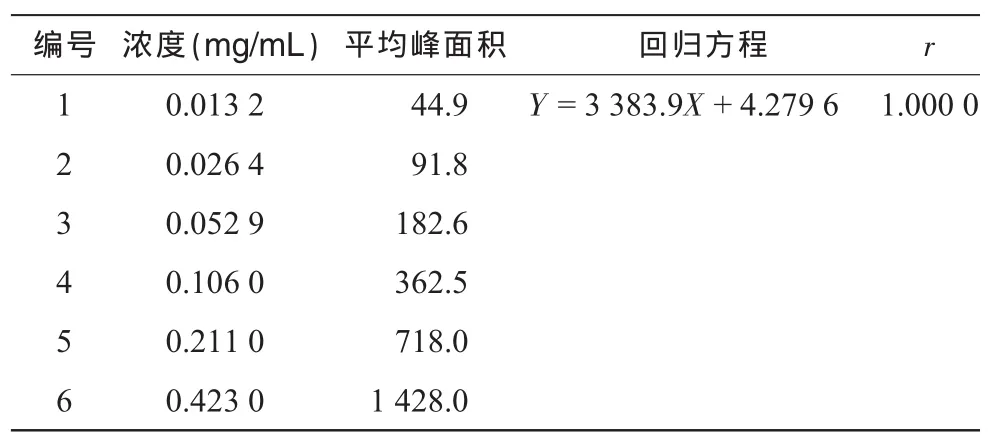
表3 线性结果
3.5 重复性试验
精密称取批号为:15010341的清平颗粒6份,称样量分别为:1.998 1,2.001 4,2.001 1,2.006 4,1.997 2,2.009 8 g,按照“3.2.2”项下制备方法制备供试品溶液,进行测定。计算药品中人参皂苷Rg1含量和RSD值,具体数值见表4。结果表明,供试品中人参皂苷 Rg1平均含量为 0.64 mg/g,RSD=1.4%,该方法重复性良好。

表4 重复性试验
3.6 准确度试验
对照品溶液:精密称取人参皂苷 Rg1对照品13.00 mg,加甲醇制成浓度为0.012 mg/mL的加样回收对照品溶液。
供试品溶液:采用加样回收法,精密称取9份已知含量同一批号的样品(批号:15010341),称样量分别为:1.009 0,1.004 5,1.002 2,1.007 7,1.009 8,0.991 6,1.003 3,1.004 9,0.999 8 g;前3份样品分别精密加入上述加样回收对照品溶液25 mL,中间3份样品分别精密加入上述加样回收对照品溶液50 mL,后3份样品分别精密加入上述加样回收对照品溶液75 mL,按照“3.2.2”项下供试品溶液的制备方法制备。分别吸取上述溶液各10 μL,注入液相色谱仪进行测定,按以下公式计算回收率,结果见表5。

表5 回收率试验结果
回收率 (%)=(实测人参皂苷Rg1质量-样品中人参皂苷Rg1质量)/加入人参皂苷Rg1对照品质量 ×100%。
结果表明,供试品中人参皂苷 Rg1平均回收率为98.0%,RSD=0.3%,该方法回收率良好。
3.7 中间精密度试验
另一位实验人员使用另一台仪器,使用不同色谱柱Agilent ZORBX Eclipse plus C18(4.6 mm× 100 mm,3.5 μm),SN(序列号):USUXR07971,精密称取批号为 15010341的清平颗粒 6份,称样量分别为:2.003 1,2.003 6,2.005 1,2.006 5,2.001 5,2.004 9 g,按照“2.1.2”项下的制备方法制备供试品溶液,进行测定。计算药品中人参皂苷Rg1含量、RSD;结果见表6,RSD为1.6%,表明该方法中间精密度良好,随机变动因素对实验结果影响较小。

表6 中间精密度试验结果
4 讨论
在其他条件不变的情况下,分别改变溶液放置时间、流速、柱温、检测波长及流动相比例,考察实验条件的微小变动对结果的影响。
4.1 稳定性试验
精密称取人参皂苷Rg111.91 mg,称取批号为15010341的清平颗粒1.999 4 g,按照“2.1”项下溶液配制方法配制对照品溶液和供试品溶液,分别于配制后0,2,4,8,12,16,24 h进行测定。
计算出对照品峰面积RSD为1.1%,供试品峰面积RSD为1.4%,表明对照品溶液和供试品溶液在24小时内稳定,见表7。

表7 稳定性试验结果
4.2 色谱条件改变
取批号为15010541的清平颗粒,在其他条件不变的情况下,分别改变柱温、检测波长、流速及流动相比例,考察微小变动对试验结果的影响。试验结果见表8。
结果表明,测定条件有小的变动对测定结果基本无影响。

表8 色谱条件微小变动影响结果
5 结论
通过对清平颗粒中人参皂苷Rg1含量测定的方法进行方法学验证,并通过改变溶液放置时间、流速、柱温、检测波长及流动相比例后的试验结果表明对测定结果无影响,可以确定HPLC专属性强,准确可行,可以用于清平颗粒中主活性成分人参皂苷Rg1的定量分析。
[1] 安明,赵国君,韦新成.人参皂苷Rg1保护心血管和中枢神经系统的药理活性研究进展[J].中国临床药理学杂志,2012,28(1):40-41.
[2] 张均田.人参冠百草[M].2版.化学工业出版社,2012:95-98.
[3] 谢暕.人参皂苷Rg1抗炎、镇痛作用及其作用机制[J].中国医院药学杂志,2013,33(19):30-35.
[4] 国家药典委员会.中华人民共和国药典(2015年版)四部[S].北京:中国医药科技出版社,2015:59-60.
[5] 李文娜,肖苑,黄燮南.人参皂苷Rg1非心血管和神经系统药理活性研究进展[J].中国药理学通报,2012,28(6):22.
[6] 王巧云,吴峰阶.人参皂苷Rg1对局灶性脑缺血再灌注大鼠脑组织NOS活性及蛋白表达的影响[J].中国病理生理杂志,2011,27(12):39.
[7] 黄海英.人参皂苷Rg1药理作用研究进展[J].实用中医药杂志,2012,28(7):45.
[8] 何道同,王兵,陈珺明.参皂苷药理作用研究进展[J].辽宁中医药大学学报,2012,14(7):22.
[9] 邱楠楠,卢丹,张庆贺,等.紫红参的HPLC指纹图谱研究[J].辽宁中医杂志,2013,40(8):10.
[10] 金银萍,焉石,闫梅霞,等.三七总皂苷中人参皂苷Rg1的分离制备[J].人参研究,2011(1):33.
[11] 洪丽萍,黄加秀,蔡亚兰,等.HPLC测定清洁验证残留物非诺贝特的含量[J].中国执业药师,2015,12(8):28-31.
Determination of Ginsenoside Rg1Content in Qingping Keli by HPLC
Shi Jingping,Hong Liping(Yangtz River Pharmacitical Group Co.,Ltd,Jiangsu Taizhou 225321,China)
Objective:To establish a HPLC method for determination of ginsenoside Rg1content in qingping keli. Methods:Separation was carried out on an Agilent ZORBX Eclipse plus C18(4.6 mm×100 mm,3.5 μm)column using acetonitrile(A)-water(B)as mobile at a detection wavelength of 203 nm and a flow rate of 1.0 mL/min.The column temperature was 25℃ while the sample load was 10 μL.Results:The linear range of ginsenoside Rg1concentration was 0.013 2~ 0.423 0 mg/mL(r=1.000 0).The average recovery of sample was 98.0%,with a RSD of 0.3%. Conclusion:This method is simple,accurate and feasible,which may be used for the quantitative determination of ginsenoside Rg1in qingping keli.
HPLC;Qingping Keli;Ginsenoside Rg1;Content Determination
10.3969/j.issn.1672-5433.2016.09.006
2016-05-03)
洪丽萍,女,执业药师。研究方向:药物分析和标准研究。通讯作者E-mail:hongliping@yangzijiang.com
