地质聚合物及其在重金属废水处理中的应用
2016-10-12崔学民李巧云徐梦雪刘子涵葛圆圆广西大学化学化工学院南宁530004
唐 青,崔学民,贺 艳,李巧云,徐梦雪,刘子涵,葛圆圆广西大学 化学化工学院,南宁530004
地质聚合物及其在重金属废水处理中的应用
唐青,崔学民,贺艳,李巧云,徐梦雪,刘子涵,葛圆圆
广西大学 化学化工学院,南宁530004
研究人员很早就发现了地质聚合反应终产物中存在类沸石结构。由于不同地质聚合物中硅铝比以及碱组分含量并不固定,因此很难确定地质聚合物中类沸石相的结构。从众多文献中可以看出,地质聚合物与低硅沸石具有组成和结构的相似性。本文阐述了地质聚合物与沸石之间的物质和结构遗传特性,为地质聚合物材料用于吸附和固化重金属离子的研究提供理论依据。目前,利用地质聚合物类分子筛结构来吸附、固定重金属离子以处理重金属废水成为一个研究热点。作为一种绿色、廉价的重金属吸附剂,地质聚合物对铅、铜、镍、铬、镉等重金属都有较好的吸附效果,重金属溶液的初始浓度、pH值、吸附温度、吸附剂用量均对吸附效果有着重要影响。通过对吸附过程中动力学和热力学进行研究发现,地质聚合物对重金属离子的吸附过程更符合二级动力学,且为Langmuir单分子层化学吸附。目前针对地质聚合物吸附重金属离子的吸附条件已有较详细的研究,在适宜条件下能达到较好的吸附效果,吸附量明显高于4A分子筛,这也表明了地质聚合物在去除废水中重金属离子的高效性。
地质聚合物;类沸石结构;重金属离子废水;吸附;离子交换;水处理
地质聚合物是建立在传统胶凝材料基础上的一种新型无机Si-Al质胶凝材料,近年来研究十分活跃。对此类材料的命名,国际上一般称为“Mineral Polymer”、“Geopolymeric Materials”、“Inorganic Polymeric Materials”、“Aluminosilicate Polymer”等,国内则通常称为“土壤聚合物”、“矿物聚合物”、“人造矿物聚合物”、“免烧陶瓷”、“地质聚合物”等。实际上,地质聚合物是一种具有三维网络结构的无机聚合物。“地质聚合物 (Geopolymer)”这个术语源于1978年,是法国教授Davidovits[1-4]在一篇美国专利中提出的,专门用来代指聚铝硅酸盐矿物,原意是该材料的形成类似于地质成岩过程。目前,“地质聚合物”这一名称已经得到国内学术界的普遍认同。
在最初Davidovits提出铝硅酸盐地质聚合物这一概念的时候[1-4],地质聚合物体系的合成温度就是在150°C以上,与合成沸石时所需的水热温度相近。但是,关于低温地质聚合反应过程与水热合成沸石的反应过程是不是同一类反应这一问题还缺乏有力的实验证据。地质聚合物凝胶相常被描述成无定型相,近年来许多研究者把地质聚合物描述成半晶质或多晶材料,特别是在较高温度下合成的地质聚合物产物更容易产生一些类沸石结晶相。然而由于这些凝胶相的组成和结构非常复杂,而且终产物中还存在未反应的原材料,很难进行定性和定量分析,因此对地质聚合物凝胶相的物理化学性质很少进行详细分析。
无定型的铝硅酸盐地质聚合物的终产物结构是凝胶相的一种,这种凝胶相与水热形成沸石的铝硅酸盐前驱体凝胶相非常类似,只是由于分析检测手段的限制,这种无定型相的具体分子结构没有得到进一步确定。胶凝材料研究人员对胶凝系统中产生的类沸石相也非常感兴趣,因为沸石为多孔材料,可以用于交换、吸附阳离子或者进行催化反应等[5]。
Deventer等人[6-9]曾推断地质聚合物中有纳米尺度的类沸石有序结构,但没有提出实验依据。崔学民等[10-14]通过纯化铝硅酸盐地质聚合反应体系,调整配比组成和养护工艺,利用合成铝硅酸盐粉体和偏高岭土地质聚合物体系,通过水热反应得到了晶化程度高、晶体转化率高的NaA型沸石、八面沸石以及方沸石等多晶体;并制备了微孔沸石分子筛膜用于海水淡化、乙醇/水分离等领域。
因此,研究地质聚合物的类沸石结构对地质聚合物形成机理,并针对其类沸石结构展开应用研究,特别是利用其多孔结构和离子交换能力处理重金属离子废水,具有十分重要的意义。
1 地质聚合物研究概况
1.1地质聚合物的概念
地质聚合物也称无机聚合物或无机高分子,其广义概念为:含无定形氧化铝和二氧化硅的铝硅酸盐矿物与碱、水玻璃或磷酸、磷酸盐混合,在强碱或强酸条件下经缩聚反应生成的由铝氧四面体、硅氧四面体或磷氧四面体构成的无定形三维网络凝胶体。由于碱基地质聚合物研究早且广泛,通常说的地质聚合物泛指碱基地质聚合物[15,16]。随着人类环境保护和可持续发展意识的增强,地质聚合物的研究及其应用引起了人们的极大兴趣。目前,地质聚合物在陶瓷、铸造、水泥、混凝土、防火材料、耐火制品、装饰石材、建筑材料、粘结剂、辐射和有毒废弃物固化等众多场合得到应用。
地质聚合物的原料来源广泛,如天然硅酸盐,包括粘土、高岭土等,还有工业产生的废弃物,包括粉煤灰、矿渣、炉渣、尾矿、熔岩等。从材料组成角度来看,目前已经得到一定发展和应用的地质聚合物体系按照阳离子分类,主要分为MeO (Me主要指Ca或Mg 等碱土元素)-Al2O3-SiO2-H2O、Me2O (Me指K、Na等碱金属元素)-Al2O3-SiO2-H2O或者Me2O (Me指K、Na等碱金属元素-CaO (或MgO)-Al2O3-SiO2-H2O三个体系[1-4,15,16]。
1.2国外地质聚合物研究历史
人类在古代就已经开始应用地质聚合物。据考古学家分析,最古老的地质聚合物制作是具有25000年历史的陶瓷制品 —— “沃尔道夫的维纳斯 (Venus of Willendorf)”(图1)。该陶瓷是利用粘土经地聚合反应生成的[2],在敞开的火焰中烧制,温度最高达300°C ~ 400°C。古罗马水泥也是一类地质聚合物,采用焙烧的石灰石与火山灰混合制备[1,2]。Davidovits等[1,2]甚至还提出了古埃及金字塔也是地质聚合物人造石头堆砌而成的学说。
20世纪30年代,Purdon[17]在研究波特兰水泥硬化机理时提出了“碱激活”理论:少量的NaOH可使水泥中的硅、铝化合物溶解后形成硅酸钠和偏铝酸钠,其生成物再与Ca(OH)2反应形成硅酸钙、铝酸钙矿物和NaOH,从而使水泥硬化,NaOH在整个反应中起到“催化剂”的作用。此后,前苏联科学家发现[2]:用于地聚合反应的激发剂,除了氢氧化钠以外,还包括碱金属的氢氧化物、氟化物、碳酸盐、磷酸盐、硫酸盐、硅酸盐和铝硅酸盐等。20世纪60年代,Glukhovsky提出了更为复杂的“碱液反应”固化机理[18],其过程为:(1) 硅铝酸盐的溶解;(2) 硅酸盐凝胶的形成;(3) 复杂晶态产物的形成。到了20世纪70年代,Davidovits[2]对地质聚合物的内部结构进行了细致的研究。他以硅铝比 (Si/Al) 为依据,将地质聚合物的结构大致分为三类[2]:PS (Si/Al = 1)、PSS (Si/Al = 2) 和PSDS (Si/Al = 3)。
自20世纪80年代开始,对地质聚合物的研究变得更为活跃,并且在碱矿渣水泥研究方面取得了重大突破。Malone等人[19]发现,碱或碱土金属离子迅速进入溶液后,在炉渣颗粒表面形成胶状硅酸钠层;铝氧化物溶解于硅酸钠中形成半晶态状的托贝莫来石;随着水份的脱析排出,而形成多种沸石及类沸石相。

图1 沃尔道夫的维纳斯Figure 1 Venus of Willendorf
20世纪90年代之后,尤其是以1999年在美国和2002年在澳大利亚分别召开的地质聚合物国际会议[20]为标志,一些国际性研究所和地质聚合物生产公司相继成立,关于地质聚合物合成和应用方面的研究进入了一个突飞猛进的时代。
1.3国内地质聚合物研究概况
我国对地质聚合物的研究起步较晚,目前在基础研究和应用研究两个方面都取得了一些进展。其中,基础研究主要围绕地质聚合物的合成、工艺条件、理论分析等方面展开,而应用研究方面则主要集中在建筑材料领域。
杨南如[21,22]综合分析了碱胶凝材料的历史现状以及不同碱胶凝材料体系的性能,并从物理和化学方面介绍了其形成理论、水化生成物的特性和机理。杨南如[23]与曾燕伟[24]通过对Purdon提出的碱催化机理、Palomo提出的沸石前驱体机理和Davidovits提出的沸石机理进行了全面细致的分析,认为碱胶凝材料的原料都是Si-O-Si或Si-O-A1键的聚合体。
张云升等[25]在分析煅烧高岭土分子结构的基础上建立了其结构代表模型,然后利用计算化学中的半经验AM1 算法研究该模型在高碱环境下溶解的全过程。
陶文宏等[16]研究了胶凝材料的性能随水玻璃模数、煅烧温度、碱含量变化的规律,并采用X-射线、扫描电镜等表征方法对胶凝材料的地聚合化产物的种类、形貌进行了分析,探讨了地质聚合物胶凝材料的聚合机理。
马鸿文等[26]将含钾岩石经破碎、选矿后得到含钾长石的精矿粉,将其与烧碱或纯碱混合,将混合物在500°C ~ 850°C条件下焙烧成熟料后,与烧碱、水搅拌混合成胶体状,通过静置、老化、晶化、过滤等过程控制得到含钾母液,含钾母液再进行酸化中和、经提取分离得到K2CO3钾肥。
谢吉星等[27]以高岭土和垃圾焚烧飞灰两种原料,氢氧化钾为碱激发剂制备出不同原料配比的地质聚合物材料。力学性能检测结果表明,当地质聚合物材料中焚烧飞灰的含量在70% 时,地质聚合物材料28 d抗压强度达到最大值19.36 MPa。重金属浸出实验证明,地质聚合物材料对垃圾焚烧飞灰中的重金属有明显的固化效果。
曹德光等[28]在煅烧高岭土基地质聚合物的研究方面也取得了一定的成果。他们利用核磁共振技术对煅烧高岭土和水玻璃的结构进行了研究,探讨了煅烧高岭土结构、水玻璃的类型和模数、碱含量及养护条件等对地质聚合物形成的影响规律。
金漫彤等[29]探讨了用煅烧高岭土、碱激活剂合成地质聚合物的过程中,原料组成配比、加入水的量对地质聚合物性能的影响。
贾德昌等[30-33]对地质聚合物的强韧化进行了大量的研究。在地质聚合物中掺入纤维 (短碳纤维,碳化硅纤维) 或者陶瓷颗粒等,发现拨出、桥连、界面脱粘、诱导裂纹偏转和裂纹分支等机制对地质聚合物起到了明显的强韧化作用,力学性能成倍提高。
崔学民等[34-36]利用溶胶-凝胶法合成铝硅酸盐前驱体材料并制备了碱基地质聚合物和磷酸基地质聚合物。研究发现,合成Al2O3-nSiO2粉体在300ºC煅烧即具有碱激发活性,远低于天然高岭土材料产生碱激发活性所需的煅烧温度。这一研究结果为地质聚合物理论研究提供了一种新的角度。
1.4地质聚合物材料的结构
通常所说的地质聚合物是指碱基地质聚合物,它是由铝硅酸盐工业废弃物或活性铝硅酸盐矿物在强碱溶液中经过解聚、缩聚和凝胶网络化过程形成的一种聚合度较高的三维网络凝胶材料[1-4]。这种解聚-缩聚反应不断的发生,促使地质聚合物材料强度不断增强,耐高温和耐酸碱腐蚀性等各种优异性能也逐渐体现出来。
与水泥材料相比,地质聚合物的聚合度要高得多。水泥材料中存在大量的无定型物质和水化晶体,因而难以承受高温。而地质聚合物的结构是三维网络状结构,在高温下其结构的完整性仍然能保持,因此能耐更高的温度[2]。
与陶瓷材料相比,陶瓷材料是多晶体系,构成陶瓷材料的重要结构相是晶粒间的晶界,陶瓷材料最薄弱的环节正是这种多包含无定型物质的晶界,而陶瓷材料的整体性能也是由晶界的性质决定的。地质聚合物材料的结构是三维网络状结构,各项性能和特性都来自于 [-Si-O-Al-O]n骨架,另外还具有玻璃态、“类晶态”两种结构,不存在完全的晶体和晶界。这一结构决定了地质聚合物材料的性能更优于陶瓷材料[1-4]。
碱基地质聚合物的分子表达式为[1-4]:

其中,M代表碱金属元素,X为碱金属离子数目,Z为聚合物结构单元中硅氧四面体的数目 (一般取1,2或3),n为地质聚合物的聚合度,w为化学结构水的数目。
Davidovits[2]总结了三种地质聚合物的形式,分别为单硅铝聚合物 (PS),双硅铝聚合物(PSS) 和三硅铝聚合物 (PSDS),如图2所示。
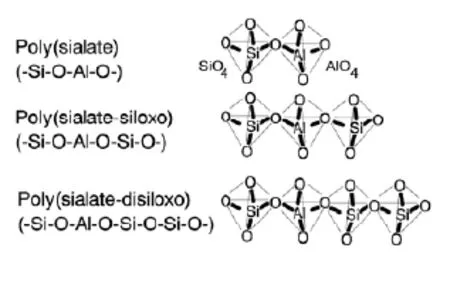
图2 地质聚合物的结构单元[2]Figure 2 Chemical structure units of geopolymers[2]
Dadovits[2]在制备沸石材料时发现目标产物中除了沸石晶体外,还有少量的无定形凝胶体材料。Dadovits通过改变反应条件获得了以无定形相为主的三维网络凝胶体材料 (图3),并把这种材料命名为地质聚合物 (Geopolymers),同时提出了地质聚合物的反应机理。Deventer和Provis进一步系统研究了地质聚合物的反应机理,发现在地质聚合物中存在有少量的纳米晶,提出地质聚合物是一种类沸石材料[8]。根据Ostwald定律,任何一种晶体的形成都会经过一个中间状态,最后转化为最稳定的晶体结构[38]。因此,很多研究人员在地质聚合物研究中经常发现类沸石结构。实际上,Deventer课题组[6-9]在研究地质聚合物的时候,也曾推断地质聚合物中有纳米尺寸的有序结构,但没有提出实验依据。崔学民课题组[10,12-14]根据实验数据和前人的研究成果,发现地质聚合物实际上是形成沸石分子筛前的铝硅酸盐凝胶体胶结而成的非晶固相材料,由于硅铝钠之间的配比以及反应条件没有达到晶化要求,因此地质聚合物仍保持了凝胶体的非晶结构;当给予其适当的晶化条件后,地质聚合物就将继续晶化从而形成沸石分子筛。目前,崔学民课题组利用地质聚合物凝胶水热法已经成功合成了NaA、NaX以及八面沸石 (FAU) 和方沸石等低硅沸石。这些研究结果都直接验证了地质聚合物凝胶中包含的类沸石结构与沸石之间具有物质和结构的遗传关系。
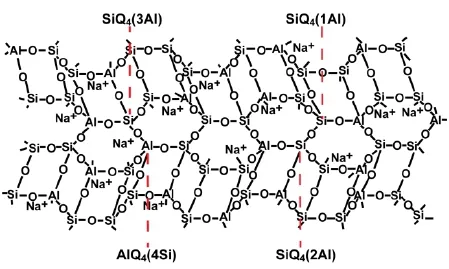
图3 地质聚合物的三维结构模型[37]Figure 3 Three-dimensional structure model of geopolymer[37]
1.5地质聚合物材料的反应机理
根据Davidovits理论[1-4],地质聚合物的形成过程可分为四个阶段: (l) 硅铝酸盐矿物粉体在碱性溶液中溶解;(2) 硅四面体和铝四面体由固体颗粒表面向液相扩散;(3) 反应物中加入的铝硅酸盐使碱硅酸盐溶液与硅四面体和铝四面体之间聚合形成凝胶相;(4) 凝胶相和剩余反应物之间溶解扩散以及凝胶相颗粒重排,排除剩余水分,固化形成地质聚合物。上述四个阶段可以简要概括为:铝硅酸盐固体组分的溶解络合、分散迁移、浓缩聚合和脱水硬化。地质聚合反应过程为各种铝硅酸盐与强碱性硅酸盐溶液之间的化学反应与化学平衡过程。虽然这种聚合机理有其一定局限性 (如不能够解释地质聚合物的真实三维结构,也说明不了地质聚合物中剩余未反应物质的存在形式),但是其合理性已通过浸出实验、核磁共振和扫描电镜综合分析证实。
地质聚合反应过程如图4所示:硅铝酸盐矿物的溶解导致了凝胶的形成,同时硅四面体与铝四面体聚合形成非晶或半结晶的三维空间结构。聚合过程中,铝由初始的四配位、五配位和六配位全部转变成四配位的 [AlO4] 并且和 [SiO4] 结合形成网状结构;当凝胶固化时,部分水分蒸发掉,其余部分则形成结构水或吸附在材料内部的纳米孔内。
目前,关于碱溶液与铝硅酸盐聚合反应活性的影响因素还不十分清楚,特别是从分子结构尺度很难表征其反应活性,只能通过宏观力学性能表征聚合反应的活性大小。研究铝硅酸盐无机聚合物结构的最有效手段是固体核磁共振技术 (Magic-Angle Sample-Spinning Nuclear Magnetic Resonance, MAS-NMR)[38,39]。该方法是把均匀的固体粉末置于转子中,使转子围绕与外磁场呈大约54.7°的角度高速旋转,消除某些核间的相互作用,使谱窄化,得到高分辨率谱。在研究中,化学位移是一个很重要的物理量,它能反映核的配位数、聚合度、次邻近和次次邻近核的影响以及键长键角等结构变化。结合X射线衍射分析、高分辨透射电镜,基本可以表征出该材料的分子结构。虽然铝硅酸盐聚合物材料体系的聚合反应机理仍然存在争论,但这并不妨碍该材料体系在诸多领域的应用。

图4 形成地质聚合物的反应过程[2]Figure 4 Reaction process of forming geopolymer[2]
翁履谦等[40]在对铝硅酸盐离子团中离子的部分电荷计算的基础上,研究了铝组分在地质聚合物合成中的作用机制,认为铝组分对地质聚合物聚合反应有显著的促进作用。根据上述聚合机理,许多种天然硅铝酸盐矿物如 偏高岭石、高炉炉渣、粉煤灰等都可以合成较高强度的地质聚合物。
图5为文献[6-9]中有关煅烧高岭土、粉煤灰及其地质聚合物的27Al MAS NMR 谱。从图5 (a) 和 (c) 可知,偏高岭土中存在四配位、五配位和六配位三种结构,与碱反应后,所有铝的配位都转变为四配位。图5 (b) 和 (d) 中粉煤灰中铝配位的变化规律类似,也是由四配位、六配位转化为四配位[6-9]。
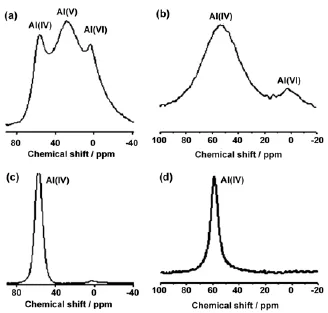
图5 煅烧高岭土、粉煤灰及其地质聚合物的27Al MAS NMR 谱;(a) 煅烧高岭土铝谱;(b) 粉煤灰铝谱;(c) 煅烧高岭土地质聚合物铝谱;(d) 粉煤灰地质聚合物铝谱[6-9]Figure 527Al MAS-NMR spectra of (a) typical metakaolin, (b) typical fly ash, (c) metakaolin-based geopolymer, and (d) fly ash-based geopolymer[6-9]
由于天然矿物及固体废弃物中杂质的存在影响了对材料反应原理的研究,人们试图采用具有化学活性的纯硅铝源材料来代替天然矿物。人工合成类高岭土材料是一种较好的选择。崔学民等[34-36]利用溶胶凝胶法合成类高岭土材料Al2O3-2SiO2粉体,该粉体具有较高的反应活性,能够和碱液或磷酸发生激烈的聚合反应。值得一提的是,合成的Al2O3-2SiO2粉体经过300ºC煅烧就产生了五配位铝 [如图6 (c) 所示],远远低于煅烧高岭土的600ºC,而且合成粉体中铝元素在碱中的溶解度也大于煅烧高岭土。与煅烧高岭土制备的地质聚合物相比,研究发现由合成Al2O3-2SiO2粉体与碱反应后制备的地质聚合物也具有类似的非晶结构,但合成地质聚合物抗压强度却低于煅烧高岭土基地质聚合物。研究结果表明,地质聚合物前驱体材料中五配位铝的存在及铝的溶解性并不能完全反映地质聚合反应的活性[34, 36]。
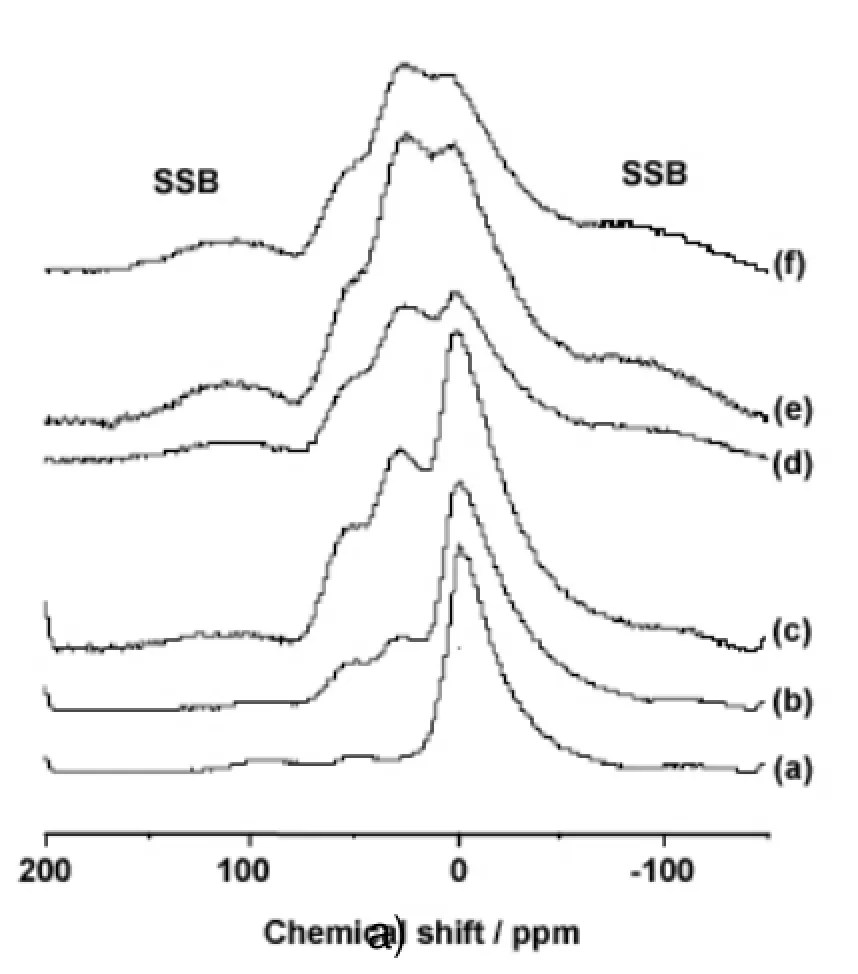
图6 合成粉体不同温度煅烧后的27Al MAS NMR谱[34,36]:(a) 105ºC干燥后的凝胶;(b) 200ºC煅烧;(c) 300ºC煅烧;(d) 600ºC煅烧;(e) 800ºC煅烧;(b) 900ºC煅烧。SSB表示旋转边峰。Figure 627Al MAS NMR spectra of the dried gel and calcined powders at different calcined temperatures: (a) dried gel at 105ºC; (b) calcined at 200ºC; (c) calcined at 300ºC; (d) calcined at 600ºC; (e) calcined at 800ºC; (f) calcined at 900ºC. (SSB stands for spinning sidebands)[34,36]
1.6地质聚合物材料研究现状及特点
国内外对地质聚合物的研究主要集中在以下几个方面:(1) 地质聚合物复合材料;(2) 地质聚合物结构材料和修补材料;(3) 地质聚合物固封有毒废料或放射性废料;(4) 地质聚合物的耐久性;(5) 地质聚合物的环保效益;(6) 地质聚合物的高温性能究。
Davidovits[1-4]对固封核废料的新型地质聚合物材料进行了研究。Lyon等[41]成功将地质聚合物应用于无机耐火材料。Valeria[42]对无机Si-Al地质聚合物材料的合成及组成特点进行了研究。van Deventer研究组[6-9]对地质聚合物的原料性能影响因素、工业固体废弃物利用、合成机理与结构、固化有害金属元素等多方面内容进行了研究。Palomo 等[43]以粉煤灰为原料合成地质聚合物材料,试验结果表明,粉煤灰基地质聚合物材料的性能在很多方面优于水泥,而地质聚合物材料的合成成本与水泥相当。Bakharevt[44]采用粉煤灰、氢氧化钠和硅酸钠溶液制备成地质聚合物材料,在制备过程中主要研究了高温养护对微观结构、相组成、强度增长的影响,其关键点是室温养护与高温养护相结合对强度增长和相组成的影响。实验证明,在采用高温养护前,先进行长时间的室温养护对材料强度的增长是有利的,在此条件下只需高温养护24 h所得地质聚合物的强度与仅采用高温养护30 d所得的强度相当。Dimitrios在制备粉煤灰基地质聚合物的实验过程[45]中发现,地质聚合物材料的强度随着水含量的减少和硅酸钠浓度的增加而增大,在氢氧化钠浓度为6.6 M时,其材料强度达到40 MPa。Feng等[46]利用粉煤灰、水玻璃作为原料,双氧水作为发泡剂,制备了多孔粉煤灰基地质聚合物,具有良好的保温效果:获得的样品孔隙率达到79.9%,导热系数仅为 0.0744 W/mK,抗压强度为 0.82 MPa,作为工业隔热材料有很好的应用前景。
国内外地质聚合物方面的应用研究体现出如下几个特点[47]:
(1) 多以固体废弃物和天然矿物 (如粉煤灰、矿渣、钢渣、火山灰、烧粘土等) 为原料制备地质聚合物;
(2) 主要围绕建筑材料产品进行开发;
(3) 对地聚反应机理研究较少,一般都沿用Davidovits理论;
(4) 没有大规模工业化的产品。BASF公司2011年推出的PCI GeofugR以及澳大利亚Zeobond生态混凝土产品算是产业化比较成功的例子;
(5) 部分研究针对重金属离子和核废料固化,且有所应用。

表1 国内外重金属治理的主要技术[50]Table 1 Major technologies for the treatment of heavy metal pollution[50]
2 地质聚合物用于重金属离子废水的研究
重金属废水主要来源于电镀、电池、印刷电路等产业,可通过水或土壤-食用生物-人体食物链富集后进入人体,危害人体健康,引起疾病。其中,镉在人体中积累可引起急、慢性中毒,使人关节处长满疙瘩,破坏骨胳,致使骨痛、瘫痪等;铜元素是人体必需的微量元素,但是摄入铜离子浓度过高会出现恶心、呕吐、肾功能衰竭、中枢神经系统抑制等症状;铅主要对中枢神经系统、血红细胞和肾脏造成危害。由此可见,重金属的危害是非常巨大的[48,49]。目前国内外治理重金属污染水体的主要方法有化学沉淀法、电解法、离子交换法、膜分离法、吸附法、生物修复法等[50](表1)。
近年来,地质聚合物由于具有三维网状类分子筛结构、在水溶液中具有的良好稳定性和机械性能以及廉价环保不易产生二次污染等优点,作为一类重要的重金属吸附剂吸引了科研工作者的注意力。学者们针对地质聚合物对重金属吸附的最佳条件以及吸附机理等进行了深入的研究。

表2 不同吸附剂对重金属离子吸附量的比较Table 2 Comparison of ion adsorption amounts between different adsorbents
2.1地质聚合物吸附剂种类
地质聚合物原料来源广泛,制备流程简单,能耗小,基本不排放CO2,同时具有较好的力学性能和耐高温性能,在多孔材料、建筑保温、防火、杂化材料、固封有毒物质等方面具有良好的应用前景[51,52]。目前,已有研究者采用不同原料制备得到粉煤灰基地质聚合物、偏高岭土基地质聚合物用于重金属吸附。针对不同使用环境,出现了粉末、颗粒、多孔球、无机膜等多种形式的吸附剂。表2列出了文献报道的一些研究结果,一些典型的研究工作简述如下。
(1) 粉末吸附:Cheng等[55]以偏高岭土为原料、水玻璃为碱激发剂制得地聚合物浆料,经注模成型后将其破碎研磨成粉末状,用于水溶液中重金属的吸附,对Cu2+、Pb2+的吸附量分别达到54.54 mg/g和100.00 mg/g。Nikolicc 等[61]将粉煤灰经过机械活化后,通过碱激发作用在室温条件下制备地质聚合物,研究其性能和对Pb2+的固定化作用。发现机械活化的粉煤灰制备的地质聚合物对Pb2+的固定效果比原始粉煤灰制备的地质聚合物更好,地质聚合物孔隙率低、强度高,Pb2+的浸出浓度也降低。
(2) 球形吸附剂:Ge[57]以偏高岭土、水玻璃为主要原料,通过添加十二烷基硫酸钠 (K12) 和双氧水 (H2O2) 作为发泡剂,采用悬浮固化法制备球形多孔球形吸附剂。球形吸附剂的比表面积达到53.95 m2/g,明显高于同配方条件下的粉末吸附剂 (9.65 m2/g)。该球形吸附剂对Cu2+和Pb2+均有较好的吸附效果,吸附量分别达到52.63 mg/g和131.98 mg/g。
(3) 膜法处理:Xu[62]以偏高岭土和水玻璃为原料制备得到自支撑地质聚合物无机膜,材料的抗压强度可达20 MPa,孔径大小为20 nm ~ 100 nm,对纳米Al2O3的截留率可达到100%,可用于膜法水处理。Ge[56]以偏高岭土和水玻璃为原料制备出自支撑地质聚合物无机膜用于处理重金属Ni2+,对Ni2+初始浓度为450 mg/l的溶液,吸附量可达到44.36 mg/g。
采用偏高岭土或者是粉煤灰作为原料对吸附剂的吸附性能并没有太大影响。在适当条件下,两类吸附剂对金属离子均能表现出较好的吸附性能。这是因为两种原料本身的成分很接近,主要为SiO2和Al2O3,生成地质聚合物的反应过程也比较接近,最后生成的地质聚合物均为三维网络结构。
从表2可以看出,不同形态的吸附剂对重金属的吸附能力有所不同,按吸附能力从强到弱顺序为粉末或颗粒、多孔球、无机膜。在重金属溶液中,粉末或颗粒吸附剂与溶液接触的表面积最大,能够为吸附反应提供更多的活性位点,吸附量较其他形态的吸附剂大,吸附效果更好,但不利于进行连续处理和回收。无机膜可用于连续水处理,在吸附重金属离子的同时还可以截留去除絮状沉淀物和有机污染物[56];但相对于粉末和颗粒状吸附剂,膜式吸附剂与重金属溶液的接触不够充分,实际利用的吸附位点有限,导致单位质量吸附剂的重金属吸附量较低,吸附剂利用率相对较低。多孔球吸附剂可装于柱中用于连续处理,便于回收;而且由于多孔球经过发泡剂的作用,内部有大量孔道,为吸附反应提供了更多的吸附位点,吸附量也较大,与粉末吸附剂较接近[57-60]。
2.2地质聚合物吸附剂的制备
一般可用粉煤灰、偏高岭土等硅铝化合物与碱溶液 (NaOH溶液或水玻璃溶液) 按照一定配比混合均匀形成浆料,再经一定条件 (低于100°C) 养护成型后即可制备得到地质聚合物。将地质聚合物块体材料破碎、研磨后即得到粉末和颗粒吸附剂。粉末及颗粒吸附剂一般作为静态吸附使用,将吸附剂浸泡于重金属溶液中,吸附饱和后再进行过滤回收。为了增大吸附接触面积,一般需将粉末研磨得较细。但粉末吸附剂如果过细,则有可能在溶液中发生团聚,实际利用的吸附位点也有限[57,58]。
制备多孔球吸附剂需要在浆料中加入发泡剂 (如十二烷基硫酸钠和双氧水) 以增加孔隙率,再通过悬浮固化法制备得到。多孔球的粒径较容易通过悬浮固化的工艺进行控制。多孔球可用于静态吸附,也可用于柱状连续处理工艺,处理效率高,且便于回收[59]。
自支撑无机膜是将浆料倒入固定形状的模具中进行养护成型而得到。无机膜可利用不同形状的模具制成片状、管状、板状等形状。在无机膜水通量较小的情况下,可通过加压或抽真空来达到较高的处理效率。自支撑无机膜制作工艺简单,处理面积大,容易在工业上得到大规模应用[55,62]。

图7 初始浓度对Cu2+去除率的影响 (温度:25°C;pH:6;剂量:2 g/l;接触时间:120 min)[54]Figure 7 Effect of the initial concentration on Cu2+removal efficiency (Temperature: 25°C, pH: 6, dose:2 g/l, contact time: 120min)[54]
2.3吸附性能
重金属溶液的初始浓度:如图7所示,地质聚合物吸附剂在重金属离子初始浓度低至10 mg/l时仍具有较好的吸附性能。随着初始浓度升高,去除率降低,单位吸附剂吸附量增加。在初始浓度较低的情况下,吸附剂可以提供充分的吸附位点来吸附溶液中的重金属离子。随着初始浓度升高,吸附剂的单位吸附量增加,但一定剂量的吸附剂能提供的吸附位点有限,致使大量金属离子残留在溶液当中,去除率下降。此时增加吸附剂的剂量,可以达到提高去除率的效果。
pH值:在吸附过程中,H3O+能与重金属离子形成竞争吸附,还会影响重金属离子的存在状态,所以pH值对溶液中重金属离子的吸附有着重要影响。如图8所示,当pH值在1 ~ 5范围内,随着pH值的增加,地质聚合物吸附剂对重金属的吸附量明显增加。在pH值较低的条件下,溶液中的H3O+浓度较高,此时吸附剂的大量吸附位点被H3O+占据,导致可用于重金属吸附的活性位点较少,重金属离子吸附量较少。随着pH值的增加,溶液中的H3O+浓度降低,与重金属离子的竞争关系减弱,重金属离子处于主导地位,大量重金属离子被吸附在地质聚合物表面,从而使重金属离子的吸附量增加[53]。另一方面,随着溶液的pH值增加至6,溶液中的重金属离子容易与OH-结合成Pb(OH)3-,致使地质聚合物吸附剂重金属离子吸附量降低[55]。

图8 pH值对Pb去除率的影响 (初始浓度:100 ppm;温度:25°C;剂量:0.07 g;接触时间:120 min)[53]Figure 8 Effect of pH value on Pb uptake (100ppm concentration, temperature 25°C, dose 0.07g, and contact time 120 min)[53]
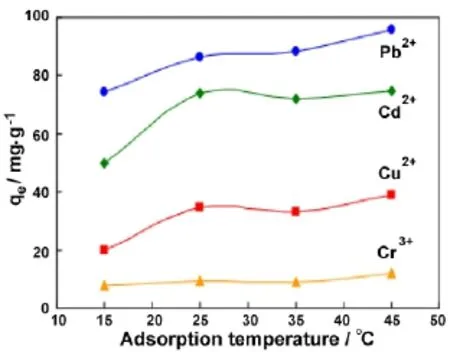
图9 温度对重金属吸附反应的影响 (pH = 4;重金属离子溶液100 ml;地质聚合物 0.1 g)[55]Figure 9 Effect of adsorption temperature on heavy metal adsorption (pH = 4, heavy metal solution 100 ml; geopolymer: 0.1g)[55]
吸附温度:温度对重金属离子的吸附也有着重要影响。研究表明:随着温度升高,重金属离子吸附量增加 (图9)。升高温度有利于溶液中离子的扩散运动,从而提高吸附反应的速度;另一方面,由于地质聚合物对重金属离子的吸附为吸热反应,升高反应温度能够使反应平衡向正反应方向移动,增加了反应的程度,从而提高了离子吸附量[63]。
吸附剂用量:在重金属离子浓度一定的情况下,增加吸附剂用量可以提高溶液中重金属离子的去除率R,这是因为吸附剂用量增加,提供的重金属吸附位点增加,可吸附更多的重金属离子,从而提高了去除率[64]。但是,如图10所示,在去除率R升高的同时,单位吸附剂的吸附量降低,说明吸附剂的利用率下降。所以在吸附试验中,往往结合去除率和吸附剂单位吸附量来决定吸附剂的最佳用量。不同吸附剂的最佳用量从0.7 g/l ~ 3 g/l不等。
接触时间:不同吸附剂吸附不同重金属离子所需要的吸附平衡时间不同。在关于粉煤灰基地质聚合物吸附剂对Cu2+的吸附研究[54]中发现,接触15 min后Cu2+的去除率显著提高,达到81.26%,此后去除率只有轻微的提高;所以最后采用的接触时间为120 min,足以使反应充分。在关于粉煤灰基地质聚合物吸附剂对Pb2+的吸附研究中[53],在最初30 min,Pb2+去除率达到80.24% (图11);继续接触至1 h,去除率只有轻微变化,故实验最终采用的接触时间为120 min。在葛圆圆[58]的研究中,偏高岭土基地质聚合物多孔球对Cu2+的吸附在36 h才达到平衡。
在达到吸附平衡前,吸附剂的吸附量和离子的去除率增加比较迅速,这主要是因为吸附前期有大量未被占用的吸附位点,重金属离子更容易被吸附;随着时间的延长,越来越多的吸附位点被重金属离子占用,提供给剩余重金属离子的吸附位点减少,导致吸附剂的吸附量和离子去除率增加缓慢,并逐渐趋于饱和,达到吸附平衡。粉末吸附剂达到吸附平衡所需要的时间相比较多孔球吸附剂更短。可能是因为粉末吸附剂表面的活性吸附位点基本都暴露在溶液当中,金属离子的扩散阻力较小,吸附反应开始后溶液中的离子更容易接触到吸附位点并且占据位点。而多孔球由于其多孔结构,其中的活性吸附位点还有大部分存在于多孔球内部的孔道结构中。重金属离子从溶液中扩散到内部的孔道结构中需要克服扩散阻力,经过一定的路程和扩散时间。所以相比较粉末吸附剂,多孔球吸附剂达到吸附平衡的时间较长。

图10 地质聚合物用量对Cu2+去除的影响[57](pH值:5;初始浓度:50 mg/l;平衡接触时间:48h)Figure 10 Effect of geopolymer dosage on Cu2+removal (pH = 5; initial concentration 50 mg/l; equilibrium contact time 48h)[57]

图11 接触时间对Pb2+去除率的影响 (初始浓度:100 ppm;温度:25°C;剂量:0.07 g;pH值:5)[53]Figure 11 Effect of contact time on Pb2+uptake (100 ppm concentration, temperature 25°C and dosage = 0.07g, pH = 5)[53]
2.4动力学及热力学研究
动力学研究:通常采用准一级动力学和准二级动力学模型对反应过程进行模拟计算以研究吸附过程中的反应机理。文献[53-55,57]对地质聚合物吸附重金属离子过程中的动力学进行了研究,结果证明,无论是粉煤灰基还是偏高岭土基,地质聚合物吸附剂对重金属离子的吸附过程均更符合准二级动力学模型。准二级动力学模型是指吸附过程受化学吸附机理控制,涉及到吸附剂与吸附质之间的电子共用或电子转移[65]。由此也可以得出,地质聚合物对重金属离子有化学吸附的作用。对比各离子的吸附速率常数可以看出,在相同条件下,偏高岭土基地质聚合物吸附剂对各离子的吸附速率不同 (Pb2+> Cd2+> Cu2+> Cr3+),这与金属离子的大小、水化自由能以及金属离子活性有关[55]。
等温吸附过程:Mohammad[54]采用Langmuir和Freundlich模型对吸附过程进行模拟,通过比较相关系数可以得出,Langmuir模型的相关系数明显高于Freundlich模型,而且用Langmuir模型计算得出的理论吸附值与实验室更接近。说明粉煤灰基地质聚合物对Cu2+的吸附过程更符合Langmuir吸附的特点,即吸附为单分子层吸附,可见地质聚合物吸附剂的吸附位点分布均匀。在对其他重金属离子 (Pb2+、Cd2+、Cr3+) 进行的吸附研究[55]也得到了相同的结果。
热力学研究:Mohammad[54]还进一步通过计算不同吸附温度下的焓值、熵值、吉布斯自由能对吸附过程进行了热力学研究,结果如表 3所示。焓值、熵值均为正值,吉布斯自由能随着温度的升高逐渐减小,这说明该吸附反应为吸热反应,适合在高温下进行[66]。吉布斯自由能为负值,说明在此条件下吸附剂对Cu2+的吸附反应是自发进行的[67]。吉布斯自由能在15 kJ/mol ~ 30 kJ/mol之间,说明该吸附反应主要为化学反应。

表3 地质聚合物吸附铜离子的热力学参数[54]Table 3 Thermodynamic parameters of copper adsorption on geopolymer[54]
2.5吸附剂再生
吸附剂吸附重金属后在一定条件下解析即可重复利用。解析可在水、酸性溶液 (盐酸、硝酸)、中性溶液 (EDTA-2Na) 中进行,使重金属离子从吸附剂的表面脱附。使用水洗的方式解析率相对较低,为1% ~ 13% 不等[55];升高解析温度可以提高解析率。用酸性溶液如盐酸、硝酸浸泡吸附剂,解析率较高,可达到100%;这主要是因为酸溶液中大量的H+与重金属离子的交换作用。H+具有较高的水化自由能,能替换被吸附的重金属离子。但如果酸性太强,H+能替换地质聚合物骨架中的Al3+,破坏地质聚合物的基本结构;在这种情况下,解析后的地质聚合物吸附剂也没有了吸附的功能。地质聚合物在pH < 4的环境下Al3+开始溶出,结构被破坏,稳定性变弱[56]。所以用酸溶液来解析重金属离子时,应严格控制酸溶液的浓度,在保证吸附剂结构不被破坏的前提下提高解析率。使用EDTA-2Na溶液来进行解析,解析率可达到95%[60]。EDTA-2Na溶液虽然为中性,但其中的EDTA官能团可以与Cu2+螯合,将Cu2+从吸附剂上解析。而且EDTA-2Na溶液为中性,不会破坏吸附剂的结构。
3 结束语
本文结合国内外众多相关文献,对地质聚合物的组成、结构以及国内外研究进展进行了综述,并着重评价了地质聚合物吸附剂在重金属离子吸附中应用情况,对吸附机理进行了归纳总结。
地质聚合物对重金属离子的吸附主要为化学吸附,吸附过程为自发进行的吸热反应,符合准二级动力学模型。升高温度有利于吸附反应的进行,提高吸附量。H+与重金属离子存在竞争吸附,所以适当提高pH有利于提高吸附量。结合文献来看,目前对吸附反应条件如温度、pH值、重金属离子浓度、吸附剂剂量对吸附效果的影响均有详细的研究,但大多只是考察了地质聚合物吸附剂对单独一种离子的吸附性能,未进行多重离子竞争吸附的研究。另外对于吸附剂的循坏再生研究较少,作为一种用于处理环境问题的材料,其自身在环保方面的循环利用问题也要解决。
[1] DAVIDOVITS J. Recent progresses in concretes for nuclear waste and uranium waste containment [J]. Acta Physiologiae Plantarum, 1994, 19 (3): 285-293.
[2] DAVIDOVITS J. Geopolymer Chemistry & Application [M]. Saint-Quentin, France: Institute geopolymer, 2008.
[3] DAVIDOVITS J. Goepolymers: inorganic polymeric new materials [J]. Journal of Thermal Analysis, 1991, 37: 1633-1656
[4] DAVIDOVITS J. Geopolymers: man-made rock deosynthesis and the resulting development of very early high strength cement [J]. Journal of Materials Education, 1994, 16 (2-3): 91-139.
[5] BRECK DW. Zeolite Molecular Sieves: Structure, Chemistry and Use [M]. New York: John Wiley & Sons, 1974.
[6] VAN JAARSVELD JGS, VAN DEVENTER JSJ. The effect of metal contaminants on the formation and properties of waste-based geopolymers [J]. Cement and Concrete Research, 1999, 29 (8): 1189-1200.
[7] VAN DEVENTER JSJ, PROVIS JL, DUXSON P, et al. Reaction mechanisms in the geopolymeric conversion of inorganic waste to useful products [J]. Journal of Hazardous Materials, 2007, 139 (3): 506-513.
[8] PROVIS JL, LUKEY GC, DEVENTER JSJV. Do geopolymers actually contain nanocrystalline zeolites? A reexamination of existing results [J]. Chemistry of Materials, 2005, 17 (12): 3075-3085.
[9] VAN DEVENTER JSJ, PROVIS JL, DUXSON P, et al. Technological, environmental and commercial drivers for the use of geopolymers in a sustainable materials industry [J]. Minerals Engineering, 2007, 20: 1261-1277.
[10] 贺艳. 地质聚合物原位转化NaA分子筛制备机理研究与应用[D]. 南宁: 广西大学博士学位论文, 2013.
[11] CUI XM, HE Y, LIU LP, et al. NaA zeolite synthesis from geopolymer precursor [J]. MRS Communications, 2011, 1(1): 49-51.
[12] HE Y, CUI XM, MAO J, et al. The hydrothermal transformation of solid geopolymers into zeolites [J]. Microporous & Mesoporous Materials, 2012, 161: 187-192.
[13] HE Y, CUI XM, LIU XD, et al. Preparation of self-supporting NaA zeolite membranes using geopolymers [J]. Journal of Membrane Science, 2013, 447 (22): 66-72.
[14] 冒进, 王艺频, 刘菁, 等. 地质聚合物原位合成八面沸石膜及其渗透汽化性能[J]. 硅酸盐学报, 2013, (9): 1244-1250.
[15] 贾屹海. Na-粉煤灰地质聚合物制备与性能研究[D]. 北京: 中国矿业大学 (北京) 博士学位论文, 2009.
[16] 陶文宏, 付兴华, 孙凤金, 等. 地聚物胶凝材料性能与聚合机理的研究[J]. 硅酸盐通报, 2008, (4): 730-735.
[17] PURDON AO. The action of alkalis on blast furnace slag [J]. Journal of Society of Chemical Industry, 1940, 59: 191-202.
[18] DUXSON P, FERNANDEZ JA, PROVIS JL, et al. Geopolymer technology: the current state of the art [J]. Journal of Materials Science, 2007, 42 (9): 2917-2933.
[19] MALONE PG, RANDALL CA, KIRKPATRICK T. Potential applications of alkali-activated aluminosilicate binders in military operations [R]. WES/MP/GL-85-15. Vicksburg, Mississipi: U.S. Army Corps of Engineers, 1985.
[20] PROFANNIE VAN DEVENTER, et al. Geopolymer [C] // Proceedings Third International Conference on Geopolymer, The University of Melboume, Melboume, Australia,2002: 9–13.
[21] 杨南如. 碱胶凝材料形成的物理化学基础 (II) [J]. 硅酸盐学报, 1996, 24 (4): 459-465.
[22] 杨南如. 碱胶凝材料形成的物理化学基础 (I) [J]. 硅酸盐学报, 1996; 24 (2): 209-215.
[23] 杨南如. 化学激发胶凝材料的原料和激发机理[C] // 北京:水泥与混凝土利废技术与可持续发展论坛, 2006.
[24] 曾燕伟, 方永浩, 徐玲玲. 化学激发胶凝材料研究进展[M]. 南京: 东南大学出版社, 2005.
[25] 张云升, 孙伟, 李宗津, 等. 用半经验AM1算法研究地聚合反应中的溶解过程[J]. 建筑材料学报,2005; 8 (5): 485-494.
[26] 马鸿文, 白志民, 王万金, 等. 一种用含钾岩石制取钾肥的方法; 中国, CN1184091 [P]. 1998-06-10
[27] 谢吉星, 印杰, 陈俊静, 等. 地聚合材料固化处理垃圾焚烧飞灰[J]. 环境工程学报, 2010; 4: 935-939.
[28] 曹德光, 苏达根, 宋国胜. 低模数硅酸钠溶液的结构及其键合反应特性[J]. 硅酸盐学报, 2004; 32 (8): 1036-1039.
[29] 金漫彤, 沈学优. 土壤聚合物的制备及其固化重金属离子的研究[J]. 化工环保, 2005; 25 (2): 84-87.
[30] LIN T, JIA D, WANG M, et al. Effects of fibre content on mechanical properties and fracture behaviour of short carbon fibre reinforced geopolymer matrix composites [J]. Bulletin of Materials Science, 2009; 32 (1):77-81.
[31] LIN T, LIANG D, JIA D, et al. Effects of fiber length on mechanical properties and fracture behavior of short carbon fiber reinforced geopolymer matrix composites [J]. Materials Science & Engineering A, 2008; 497: 181-185.
[32] 何培刚, 贾德昌, 王美荣, 等. C(uf)/铝硅酸盐聚合物复合材料的制备和力学性能[J]. 稀有金属材料与工程, 2011, (S1): 247-251.
[33] 郑斌义. 单向连续SiCf增强铝硅酸盐聚合物基复合材料的力学性能[D]. 哈尔滨: 哈尔滨工业大学硕士学位论文, 2013.
[34] CUI XM, LIU LP, ZHENG GJ, et al. Characterization of chemosynthetic Al2O3-2SiO2geopolymers [J]. Journal of Non-Crystalline Solids, 2010, 356: 72-76.
[35] LIU LP, CUI XM, QIU SH, et al. Preparation of phosphoric acid-based porous geopolymers [J]. Applied Clay Science, 2010, 50: 600-603.
[36] ZHENG GJ, CUI XM, ZHANG WP, et al. Preparation of geopolymer precursors by sol–gel method and their characterization [J]. Journal of Materials Science, 2009, 44 (15): 3991-3996.
[37] 杨南如, 岳文海. 无机非金属材料图谱手册[M]. 武汉: 武汉工业大学出版社, 2000.
[38] 徐如人. 分子筛与多孔材料化学[M]. 北京: 科学出版社, 2004.
[39] HE Y, CUI XM, LIU XD, et al. Preparation of self-supporting NaA zeolite membranes using geopolymers [J]. Journal of Membrane Science, 2013, 447: 66-72.
[40] 翁履谦, KWESI SC, 宋申华, 等. 地质聚合物合成中铝酸盐组分的作用机制[J]. 硅酸盐学报, 2005; 33 (3): 276-280.
[41] LYON RE, BALAGURU PN, ANDREW F, et al. Fire-resistant aluminosilicate composites [J]. Fire & Materials, 1997, 21 (21): 67-73.
[42] BARBOSA VFF, MACKENZIE KJD, THAUMATURGO C. Synthesis and characterisation of materials based on inorganic polymers of alumina and silica: sodium polysialate polymers [J]. International Journal of Inorganic Materials, 2000, 4 (2): 309-317.
[43] CRIADO M, JIMENEZ AF, PALOMO A. Effect of sodium sulfate on the alkali activation of fly ash [J]. Physical Review C, 2010, 32 (8): 589-594.
[44] BAKHAREV T, Geopolymeric materials prepared using Class F fly ash and elevated temperature curing [J]. Cement & Concrete Research, 2005, 35 (6): 1224-1232.
[45] PANIAS D, GUANNPPOULOU IP, PERRAKI T. Effect of synthesis parameters on the mechanical properties of fly ash-based geopolymers [J]. Colloids & Surfaces A, 2007, 301 (1–3): 246-254.
[46] FENG J, ZHANG R, GONG L, et al. Development of porous fly ash-based geopolymer with low thermal conductivity [J]. Materials & Design, 2015, 65 (3): 529-533.
[47] INADA M, EGUCHI Y, ENOMOTO N, et al. Synthesis of zeolite from coal fly ashes with different silica-alimina composition [J]. Fuel, 2005, 84 (2-3): 299-304.
[48] MATHEIKAL JT, YU Q. Biosorption of lead(II) and copper(II) from aqueous solutions by pre-treated biomass of Australian marine algae [J]. Bioresource Technology, 1999, 69 (3): 223-229.
[49] WANG X, PEI Y, LU M , et al. Highly efficient adsorption of heavy metals from wastewaters by graphene oxide-ordered mesoporous silica materials [J]. Journal of Materials Science, 2015, 50 (5): 2113-2121.
[50] HASHIM MA, MUKHOPADHYSAY S, SAHU JN, et al. Remediation technologies for heavy metal contaminated groundwater [J]. Journal of Environmental Management, 2011, 92 (10): 2355-2388.
[51] DAVIDOVITS J. 地质聚合物应用30多年来的成败市场发展趋势及潜在的突破[C] // 海口: 水泥技术交流大会暨全国水泥技术交流大会, 2005.
[52] 宋晓玲. 地聚物/聚氯乙烯复合材料的制备及性能研究[D]. 南宁: 广西大学博士学位论文, 2013.
[53] AL-ZBOOM K, AL HMS, HANI FB. Fly ash-based geopolymer for Pb removal from aqueous solution [J]. Journal of Hazardous Materials, 2011, 188 (1-3): 414-421.
[54] AL-HARAHSHEH MS, ZBOON KA, AL-MALHADMEH L, et al. Fly ash based geopolymer for heavy metal removal: A case study on copper removal [J]. Journal of Environmental Chemical Engineering, 2015, 3: 1669-1677.
[55] CHENG TW, LEE ML, KO MS, et al. The heavy metal adsorption characteristics on metakaolin-based geopolymer [J]. Applied Clay Science, 2012, 56 (1): 90-96.
[56] GE YY, YUAN Y, WANG KT, et al. Preparation of geopolymer-based inorganic membrane for removing Ni2+from wastewater [J]. Journal of Hazardous Materials, 2015, 299: 711-718.
[57] GE YY, CUI XM, KONG Y, et al. Porous Geopolymeric Spheres for Removal of Cu(II) from Aqueous Solution: Synthesis and Evaluation [J]. Journal of Hazardous Materials, 2014, 283: 244–251.
[58] 葛圆圆. 偏高岭土地质聚合物基重金属离子吸附剂的制备及其性能研究[D]. 南宁: 广西大学博士学位论文, 2015.
[59] TANG Q, GE YY, WANG K et al., Preparation of porous P-type zeolite spheres with suspension solidification method [J]. Materials Letters, 2015, 161: 558-560.
[60] TANG Q, GE YY, WANG K et al., Preparation and characterization of porous metakaolin-based inorganic polymer spheres as an adsorbent [J]. Materials and Design, 2015, 88: 1244-1249.
[61] NIKOLIC V, KOMLJENOVIC M, MARJANOVIC N, et al. Lead immobilization by geopolymers based on mechanically activated fly ash [J]. Ceramics International, 2014, 40 (6): 8479-8488.
[62] XU MX, HE Y, WANG CQ, et al. Preparation and characterization of a self-supporting inorganic membrane based on metakaolin-based geopolymers [J]. Applied Clay Science, 2015, 115: 254-259.
[63] WANG S, LI L, ZHU ZH. Solid-state conversion of fly ash to effective adsorbents for Cu removal from wastewater [J]. Journal of Hazardous Materials, 2007, 139 (2): 254-259.
[64] KUMAR PS, SENTHAMARAI C, DURGADEVI A, et al. Adsorption kinetics, mechanism, isotherm, and thermodynamic analysis of copper ions onto the surface modified agricultural waste [J]: Environmental Progress & Sustainable Energy, 2014, 33 (1): 28-37.
[65] 赵振国. 吸附作用应用原理[M]. 北京: 化学工业出版社, 2005.
[66] DONAT R, AKDOGAN A, ERDEM E, et al. Thermodynamics of Pb2+and Ni2+adsorption onto natural bentonite from aqueous solutions [J]. Journal of Colloid & Interface Science, 2005, 286 (1): 43–52.
[67] BULGARIU L, RAOI M, BULGARIU D. et al. Equilibrium study of Pb(II) and Hg(II) sorption from aqueous solutions by moss peat [J]. Environmental Engineering & Management Journal, 2008, 7 (5): 511-516.
Geopolymer: Research Progress and Its Applications in Removing Heavy Metal from Water
TANG Qing, CUI Xue-Min, HE Yan, LI Qiao-Yun, XU Meng-Xue, LIU Zi-Han, GE Yuan-Yuan
Guangxi Key Lab of Petrochemical Resource Processing and Process Intensification Technology, School of Chemistry and Chemical Engineering, Guangxi University, Nanning 530004, China
In the study of geopolymer, the researchers found very early that the end products of geopolymerization have zeolite-like structures. Because the Si/Al molar ratios and alkali component contents are not fixed in different geopolymers, it is difficult to determine the zeolite-like structure in geopolymer. As can be seen from the numerous studies, both the geopolymer and zeolite have similarities in composition and structure. This article identified the structural heredity characteristic between the geopolymer and zeolites, in order to provide a theoretical foundation for exploring geopolymer and broaden the application field of geopolymer. Nowadays, extensive studies have been conducted concerning the potential applications of geopolymers in adsorbing and immobilizing heavy metal in wastewater treatment based on its zeolite-like structure. As a green and low-cost heavy metal adsorbent, geopolymers have excellent performance on Pb2+, Cu2+, Ni2+, Cr3+, Cd2+adsorption. Theinitial ion concentration, pH of heavy metal solution, adsorption temperature, and adsorbent dosage have significant impact on the adsorption amount of adsorbent. The kinetic and isotherm researches show that the adsorption process of geopolymer is fit to the second order kinetic model and is proved to be Langmuir adsorption, which is monolayer adsorption. There has been detail researches focused on adsorption conditions of geopolymer adsorbent, and excellent adsorption performance could be obtained under optimal condition. The adsorption amount of geopolymer adsorbent is obviously higher than 4A molecular sieve. It fully demonstrated the feasibility of using geopolymer as heavy metal adsorbent.
Geopolymer; Zeolite-like structure; Heavy metal wastewater; Adsorption; Ion exchange; Water treatment.
TB321
1005-1198 (2016) 04-0253-17
A
10.16253/j.cnki.37-1226/tq.2016.05.003
唐青,女,1990年出生,湖南永州人,博士研究生,就读于广西大学。2013年9月进入广西大学攻读硕士学位,并于2015年12月开始硕博连读,师从崔学民研究员。主要从事地质聚合物球转化分子筛、地质聚合物球对金属离子和气体的吸附以及地质聚合物压裂支撑剂的相关研究,目前已经发表SCI论文6篇,其中第一作者3篇。

崔学民,男,1971年生,山东利津县人,现任广西大学化学化工学院研究员、博士生导师,广西高校卓越学者及卓越创新团队带头人,广西高校优秀人才、广西青年科技奖获得者,现任中国硅酸盐学会特陶分会理事、广西碳酸钙行业协会常务副会长,《功能材料》编委等。主要从事地质聚合物材料合成机理、凝胶结构表征研究及其在新型水泥基材料、吸附分离材料、无机膜材料和化学建材等领域的应用。近十年来主持国家自然科学基金项目5 项,获得省部级一、二等科研奖励4项;发表SCI论文90多篇,17项发明专利得到授权。
2016-04-14
2016-06-20
国家自然科学基金 (51561135012; 21566006; 51262002)
唐 青 (1990 -),女,湖南永州人,博士研究生。Email:783976402@qq.com。
崔学民 (1971 -),男,山东利津人,教授。Email:cui-xm@tsinghua.edu.cn。
