山梨醇和甘露醇制备高碳烃液体燃料的研究
2016-09-26吕东灿赵仲麟袁志华马斌强刘运权
吕东灿,袁 帅,赵仲麟,袁 超,袁志华,马斌强,刘运权
(1.河南农业大学理学院,河南 郑州 450002; 2.四川农业大学机电学院,四川 雅安 625014;3.河南农业大学机电工程学院,河南 郑州 450002; 4.厦门大学能源学院,福建 厦门 361102)
山梨醇和甘露醇制备高碳烃液体燃料的研究
吕东灿1,袁 帅2,赵仲麟1,袁 超1,袁志华3,马斌强1,刘运权4
(1.河南农业大学理学院,河南 郑州 450002; 2.四川农业大学机电学院,四川 雅安 625014;3.河南农业大学机电工程学院,河南 郑州 450002; 4.厦门大学能源学院,福建 厦门 361102)
在温和条件下研究了氢碘酸还原生物质基多元醇制备液体燃料的过程,使用气相色谱质谱仪(GC-MS)和红外光谱仪(FT-IR)分析了产物组成。结果表明,山梨醇和甘露醇为原料制备的液体产物中主要成分是C12H16、C12H18、C12H20、C12H22和C18H26等烃类物质。通过与碱的醇溶液反应将副产物碘代烷转化为烃,经旋转蒸发和减压蒸馏获得纯净的高碳烃产品。山梨醇、甘露醇以及二者混合物制备出的高碳烃的产率分别是81.1%、73.2%和77.3%。本研究获得的高碳烃产品是一种有前景的液体燃料,其含水量为0.1%,密度为0.83~0.84 g·mL-1,含氧量为2.0%~2.2%,热值均高于42 MJ·kg-1。
生物质;山梨醇;甘露醇;氢碘酸;高碳烃
能源短缺和环境污染逐渐成为威胁全球人类生存与发展的问题,清洁、可再生能源的开发受到了广泛的关注。生物质具有储量大、可再生、清洁等优点,已成为一种具有广阔发展前景的可再生能源[1,2]。目前,生物质转化为液体燃料的途径主要是发酵制备乙醇[3]和热解或液化制备生物油[4]。然而,现有的转化方法都存在一定的局限性。发酵制燃料乙醇的碳转化率低,发酵溶液中乙醇浓度低,需要后续分离步骤;生物油成分复杂、含腐蚀性的酸类、热值低、稳定性差[5],限制了其在工业中的应用[6]。因此,迫切需要开发一种更为高效的液体燃料制备工艺,使人们能够选择性的制备热值较高的目标产物。生物质基多元醇是转化制备能源产品的重要平台化合物[7,8]。多元醇的转化中,最具代表性的是水相重整法[9-12]。在双功能催化剂作用下,山梨醇经水相重整过程可转化为C6和C9的烷烃物质,其转化过程的反应机理也被提出。要制备更多碳原子数的烃,可以通过在反应过程中引入丙酮来增长碳链。该方法开拓了一种多元醇制备高碳烃的新工艺,但是目前还存在如反应条件比较苛刻(高温高压)、反应过程复杂和需要昂贵的催化剂等问题。氢碘酸还原多元醇制备烃类是另一种较有前景的多元醇转化方法[13]。氢碘酸与多元醇反应产生烃类和碘单质,与此同时,在反应体系中加入的共存还原剂将碘单质重新还原为碘化氢继续反应。整个过程条件温和、耗能低、不需要催化剂,因此氢碘酸还原多元醇制备烃类是一种新颖经济的多元醇转化工艺。作者研究了以山梨醇为原料时,反应条件对产物产率和选择性的影响,并提出了可能的反应机理[14]。在实际生物质裂解过程中,产物往往是山梨醇和甘露醇的混合物[15,16]。因此,需要考察甘露醇为原料时被氢碘酸还原的产物情况和甘露醇的存在对山梨醇的转化的影响。本研究旨在考察山梨醇和甘露醇被氢碘酸还原的产物组成情况及产物的性质。使用GC-MS和FT-IR分析了油相产物的组成及结构特征。此外,使用水分测定仪、元素分析仪和热值测定仪等分析了高碳烃产品的理化性质,以期为氢碘酸还原多元醇制备高碳烃这一工艺的深入研究提供理论基础。
1 材料与方法
1.1材料
山梨醇(C6H14O6)和甘露醇(C6H14O6)购自上海阿拉丁试剂有限公司,纯度均为98%。其它试剂如氢氧化钾(KOH)、乙醇(C2H5OH)、二氯甲烷(CH2Cl2)、磷酸(H3PO4)和45%氢碘酸(HI)购自国药集团化学试剂有限公司,均为分析纯。
1.2方法
分别以山梨醇、甘露醇、山梨醇和甘露醇等量混合物为原料进行实验。各组实验中,多元醇、氢碘酸、亚磷酸和去离子水的质量分别为21.9、100.4、58.3、15.4 g。分别将各物质加入250 mL三口烧瓶中,反应体系加热并维持沸腾状态(温度约为120 ℃)回流反应12 h。反应结束后,待体系冷却至室温,收集油相。以山梨醇、甘露醇和二者混合物为原料反应获得的油相产物分别命名为SO1、MA1和MI1。
初始油相产物中含有碘己烷副产物,为得到纯度较高的烃类产品,采用碘己烷与KOH醇溶液反应的方法将其转化为烯烃。转化过程包括3步:在醇溶液中碘己烷与KOH反应;使用二氯甲烷萃取得到油相混合物;通过旋转蒸发分离二氯甲烷和烃类物质。转化条件参见文献[16]。获得的烃类产品分别命名为SO2、MA2和MI2。烃类物质通过减压蒸馏方法分别获得C6烯烃和高碳烃产品(SO3、MA3和MI3)。
1.3产物分析
产物的组成使用日本岛津公司(SHIMADZU)的气相色谱质谱仪(GC-MS)进行分析。色谱柱为Rtx-5MS色谱柱(30 m×0.25 mm×0.25 μm)。柱箱升温程序为30 ℃保持4 min, 以5 ℃·min-1的速率升温至220 ℃,然后以10 ℃·min-1的速率升温至270 ℃。离子源温度为200 ℃,接口温度为270 ℃。通过与NIST质谱库中标准物质对比,确定油相产品的物质组成。使用面积归一化法确定各物质的相对含量。
油相产物的红外分析仪器为iS 50光谱仪(美国Nicolet仪器公司)。油相产品含水量测定仪器为卡尔-费休水分测定仪(ASTM E203方法)(瑞士Mettler Toledo仪器公司)。元素组成测定装置为Vario EL III元素分析仪(德国Elementar公司)。高碳烃的低位热值测定仪为自动量热仪(上海电子器械技术公司)。以上定量测定均重复3次,结果取平均值。
2 结果与分析
2.1山梨醇产物组成
山梨醇为原料制备得到的初始油相SO1、碘己烷被转化后的油相SO2以及高碳烃产品SO3的组成见图1。高碳烃(SO3)的产率为81.1%。在SO1中,主要物质是2-碘己烷和C12、C18的烃类,这与作者前期研究一致[16]。C12和C18烃类主要是C12H16、C12H18、C12H20、C12H22和C18H26组成的混合物。它们是烯烃、芳香烃、烷烃及其同系物和同分异构体等。从山梨醇和C12、C18高碳烃产品的分子式可知,高碳烃物质是山梨醇反应过程中衍生出的C6物质发生二聚和三聚形成的[17]。
在SO1中,副产物为2-碘己烷,其在油相产品中的含量为21%。2-碘己烷与碱反应能够失去一分子碘化氢形成2-己烯和少量3-烯烃。由图1可知,SO2中不存在碘代烷物质,表明副产物已完全转化。己烯的沸点在68 ℃左右,能够很容易的通过蒸馏的方法将其分离出来。最终获得的高碳烃产品SO3只含有C12和C18烃类。

图1 山梨醇制备的油相产品的组成Fig.1 Components of the products converted from sorbitol
2.2甘露醇产物组成
甘露醇的反应过程及产物组成与山梨醇相似。如图2所示,MA1的主要物质是2-碘己烷和C12、C18的烃类物质(C6物质形成的二聚体和三聚体)。山梨醇和甘露醇具有相似的分子结构(互为同分异构体),但甘露醇为原料得到的初始油相MA1却含有更多的碘代烷。MA2中不存在碘代烷,C6物质为己烯C6H12。经过旋转蒸发和减压蒸馏,高碳烃产品MA3中只含有C12和C18烃。与山梨醇相比,以甘露醇为原料得到的高碳烃产品的产率较低,为73.2%。这是因为山梨醇和甘露醇的分子手性不同,导致与氢碘酸的反应过程不同。具体反应机理尚未见文献报道。因此,在与氢碘酸反应制备高碳烃过程中,山梨醇比甘露醇有更大的优势。
2.3山梨醇和甘露醇混合物产物组成
山梨醇和甘露醇的混合物为原料制备的产物的组成见图3。初始油相MI1中,主要成分是2-碘己烷和高碳烃物质。其中,2-碘己烷在MI1中的百分含量为24.7%。以山梨醇和甘露醇混合物为原料和以山梨醇或甘露醇为原料得到的产品成分相同,但含量不同。C6 物质形成的二聚体和三聚体如C12H18、C12H20、C12H22、C18H26、C18H28、C18H30和C18H34的分子量范围为138~244 g·mol-1。高碳烃产品MI3的产率为77.3%,介于山梨醇和甘露醇为原料的高碳烃产率之间。这表明,甘露醇并不会对山梨醇与氢碘酸的反应造成影响,反之亦然。
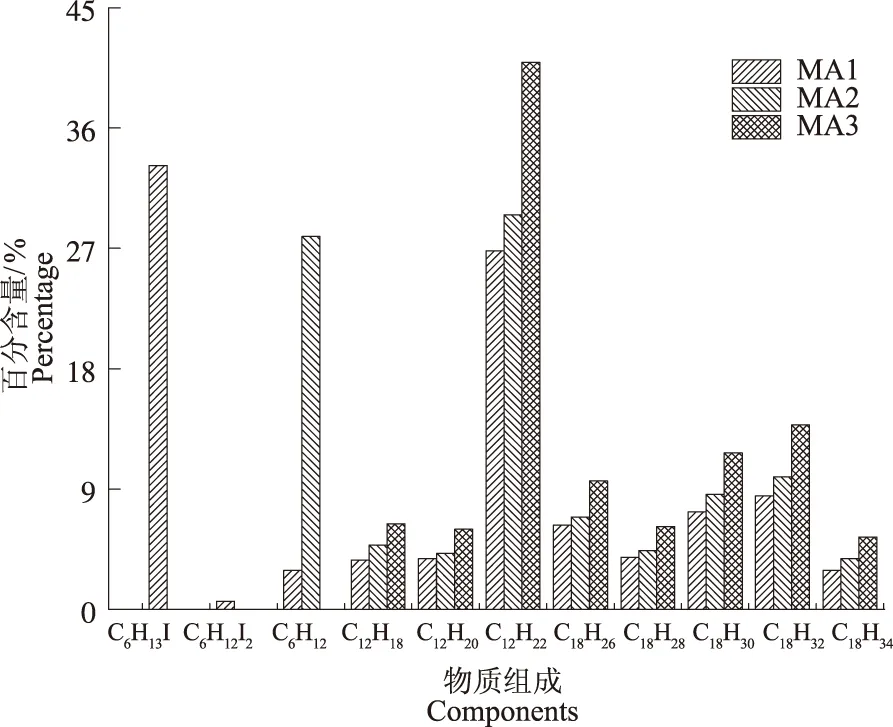
图2 甘露醇制备的油相产品的组成Fig.2 Components of the products converted from mannitol
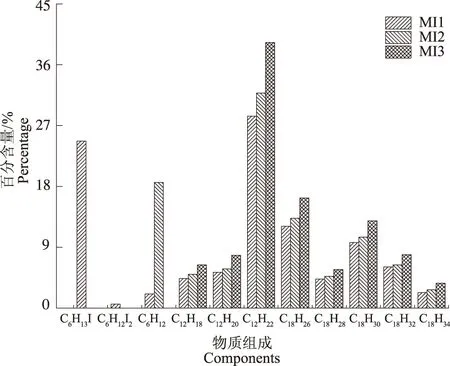
图3 山梨醇和甘露醇混合物制备的油相产品的组成Fig.3 Components of the products converted from the mixture of sorbitol and mannitol
2.4高碳烃产品的FT-IR分析


图4 高碳烃产品的红外光谱 Fig.4 Infrared spectra of the heavier hydrocarbons
2.5高碳烃产品的理化性质分析
表1为本研究中的高碳烃产品与典型的重油[18]的理化性质的比较。高碳烃产品的含水率均低于0.2%,这与重油相似。密度是燃料的一个重要性质,它对燃料雾化有重要的影响。本研究中高碳烃的密度与柴油密度相近,适合作为燃料使用。高碳烃中主要元素为C和H,且C/H较高。与重油相比,高碳烃产品的含氧量稍高,为1.8%~2.1%。氧元素可能是高碳烃产品中少量的含氧有机物引起的。但高碳烃产品中不存在N元素,因此在使用时不会产生氮氧化物等环境污染物。
热值是衡量燃料质量的一个重要指标。本研究中以山梨醇、甘露醇和二者混合物制备的高碳烃产品的热值分别为43.4、42.6、43.1 MJ·kg-1。与甘露醇相比,山梨醇为原料得到的高碳烃产品的产率和热值都更高。这可能是因为山梨醇和甘露醇与氢碘酸的反应过程稍有不同,高碳烃产品中各物质的相对含量也稍有不同。可见,山梨醇是制备高碳烃产品的一种更为合适的六元醇原料。另外,高碳烃产品的热值高于生物油(19 MJ·kg-1)和生物质柴油(33 MJ·kg-1)[19],甚至高于重油的热值。

表1 高碳烃产品和重油的理化性质比较Table 1 Typical properties of the heavier hydrocarbon fuels from polyols and the comparison with heavy fuel oil
因此,氢碘酸还原制备高碳烃的工艺是一种可行的、具有广阔前景的生物质转化制备液体燃料的工艺。
3 结论
在温和条件下,多元醇被氢碘酸还原可转化为高碳烃燃料。以山梨醇、甘露醇和二者等量混合物为原料进行实验,高碳烃产品均是C12H16、C12H18、C12H20、C12H22和C18H26等C6物质的二聚体和三聚体组成。高碳烃的产率分别是81.1%、73.2%和77.3%。与甘露醇相比,山梨醇在被氢碘酸还原制备高碳烃燃料产品方面具有更大的优势。理化性质分析结果表明,高碳烃产品含水量低(0.1%),密度(0.8 g·mL-1)和碳氢比(C/H≈7)与汽油、柴油相近,且不含氮、硫等环境污染物,热值高达42 MJ·kg-1。因此,本研究的高碳烃产品是一种清洁、环保、可再生的液体燃料,具有良好的应用前景。
[1] LI H, HONG H, JIN H G, et al. Analysis of a feasible polygeneration system for power and methanol production taking natural gas and biomass as materials [J]. Applied Energy, 2010, 87(9): 2846-2853.
[2] LYND L R, WYMAN C E, GERNGROSS T U. Biocommodity engineering [J]. Biotechnology Progress, 1999, 15(5): 777-793.
[3] BRETHAUER S, WYMAN C E. Review: continuous hydrolysis and fermentation for cellulosic ethanol production [J]. Bioresource Technology, 2010, 101(13): 4862-4874.
[4] VISPUTE T P, ZHANG H, SANNA A, et al. Renewable chemical commodity feedstocks from integrated catalytic processing of pyrolysis oils [J]. Science, 2010, 330: 1222-1227.
[5] BRIDGWATER A V. Review of fast pyrolysis of biomass and product upgrading [J]. Biomass Bioenergy, 2012, 38 (2): 68-94.
[6] BULUSHEV D A, ROSS J R H. Catalysis for conversion of biomass to fuels via pyrolysis and gasification: a review [J]. Catalysis Today, 2011, 171(1): 1-13.
[7] CHEN J, WANG S, HUANG J, et al. Conversion of cellulose and cellobiose into sorbitol catalyzed by ruthenium supported on a polyoxometalate/metal-organic framework hybrid [J]. Chem Sus, 2013, 6(8): 1545-1555.
[8] LUO C, WANG S, LIU H. Cellulose conversion into polyols catalyzed by reversibly formed acids and supported ruthenium clusters in hot water [J]. Angewandte Chemie, 2007, 46(40): 7636-7639.
[9] HUBER G W, CORTRIGHT R D, DUMESIC J A. Renewable alkanes by aqueous-phase reforming of biomass-derived oxygenates [J]. Angewandte Chemie, 2004, 43(12): 1549-1551.
[10] HUBER G W, CHHEDA J N, BARRETT C B, et al. Production of liquid alkanes by aqueous-phase processing of biomass-derived carbohydrates [J]. Science, 2005, 308: 1446-1450.
[11] CHHEDA J N, HUBER G W, DUMESIC J A. Liquid-phase catalytic processing of biomass-derived oxygenated hydrocarbons to fuels and chemicals [J]. Angewandte Chemie, 2007, 46(38): 7164-7183.
[12] KUNKES E L, SIMONETTI D A, WEST R M, et al. Catalytic conversion of biomass to monofunctional hydrocarbons and targeted liquid-fuel classes [J]. Science, 2008, 322: 417-421.
[13] ROBINSON J M, BURGESS C E, MANDAL H D, et al. Unique fractionation of biomass to polyols provides inexpensive feedstock for liquid fuels process [J]. Preprints of Papers, American Chemical Society, Division of Fuel Chemistry, 1996, 41: 1090-1093.
[14] LV D C, LIU Y Q, ZHANG B B, et al. Production of liquid hydrocarbons from sorbitol by reduction with hydroiodic acid [J]. Energy & Fuels, 2014, 28(6): 3802-3807.
[15] KOMANOYA T, KOBAYASHI H, HARA K, et al. Kinetic study of catalytic conversion of cellulose to sugar alcohols under low-pressure hydrogen [J]. Chemcatchem, 2014, 6(1): 230-236.
[16] BRANCO A, SANTOS J D G, PIMENTEL M M A M, et al. D-mannitol from agave sisalana biomass waste [J]. Industrial Crops and Products, 2010, 32(3):507-510.
[17] ROBINSON J M, BANUELOS E, BARBER W C, et al. Chemical conversion of biomass polysaccharides to liquid hydrocarbon fuels and chemicals [J]. Preprints of Papers, American Chemical Society, Division of Fuel Chemistry, 1999, 44(2): 224-227.
[18] CZERNIK S, BRIDGWATER A V. Overview of applications of biomass fast pyrolysis oil [J]. Energy & Fuels, 2004, 18(2): 590-598.
[19] DEMIRBAS A, DEMIRBA M F. Importance of algae oil as a source of biodiesel [J]. Energy Conversion and Management, 2011, 52(1): 163-170.
(责任编辑:蒋国良)
Studyonproductionofliquidhydrocarbonfuelsfromsorbitolandmannitol
LYU Dongcan1, YUAN Shuai2, ZHAO Zhonglin1, YUAN Chao1, YUAN Zhihua3, MA Binqiang1, LIU Yunquan4
(1.College of Sciences, Henan Agricultural University, Zhengzhou 450002, China; 2.College of Mechanical & Electrical Engineering, Sichuan Agricultural University, Ya’an 625014, China; 3.College of Mechanical & Electrical Engineering, Henan Agricultural University, Zhengzhou 450002, China; 4.College of Energy, Xiamen University, Xiamen 361102, China)
This paper describes the process of sorbitol and mannitol conversion to liquid heavier hydrocarbons via reduction with hydroiodic acid under mild reaction conditions. The compositions of the obtained products were analyzed using gas chromatography mass spectrometer (GC-MS) and Fourier transform infrared spectrometer (FT-IR). It is found that the products obtained from C6 polyols were mainly C12H16,C12H18,C12H20,C12H22and C18H26. The yields of heavier hydrocarbons from sorbitol, mannitol, and the mixture of sorbitol and mannitol were 81.1%, 73.2%, and 77.3%, respectively. To obtain pure hydrocarbon fuels, the obtained crude oil was treated with potassium hydroxide in an alcohol solution followed by rotary evaporation and vacuum distillation. The final liquid hydrocarbons obtained have a water content of 0.1%, densities of 0.83~0.84 g·mL-1, oxygen content of 2.0%~2.2%, and heating values >42 MJ·kg-1at room temperature, which is potentially a good transportation fuel for diesel replacement.
biomass; sorbitol; mannitol; hydroiodic acid; heavy hydrocarbons
S216; TK6
:A
2015-12-10
国家自然科学基金项目(21276214)。
吕东灿(1988-),女,河南商丘人,讲师,博士,从事生物质利用技术方面的研究。
刘运权(1963-),男,江西赣州人,教授,博士生导师。
1000-2340(2016)02-0209-05
