α-Fe2O3的制备及α-Fe2O3@SiO2复合纳米材料的吸附性能
2016-08-16李西营齐亚辉李明杰王昆鹏毛立群
李西营,齐亚辉,李明杰,王昆鹏,高 丽,刘 勇,毛立群
(河南大学 化学化工学院,河南 开封 475004)
α-Fe2O3的制备及α-Fe2O3@SiO2复合纳米材料的吸附性能
李西营*,齐亚辉,李明杰,王昆鹏,高丽,刘勇,毛立群
(河南大学 化学化工学院,河南 开封 475004)
采用不同分子结构的有机含氮化合物作为包裹剂成功制备了具有弱磁性的α-Fe2O3纳米颗粒,其形貌可以实现由饼状到不规则长方体及长方体的转变. 构成该α-Fe2O3纳米颗粒的前驱体α-FeOOH呈现梭形结构,通过一锅法可以在梭形α-FeOOH外面包裹一层介孔二氧化硅,煅烧后制备的α-Fe2O3@SiO2复合纳米材料对水相中的亚甲基蓝有良好的吸附效果,室温下最高去除率达97.3%. 针对制备的材料进行了XRD、SEM及磁学性能表征.
α-Fe2O3纳米粒子;α-Fe2O3@SiO2复合纳米材料;吸附
铁氧化物纳米材料因其原料价格低廉、环境友好、性质稳定、并且具有良好的磁学性能,被广泛应用于污水处理、电子器械、传感器、医疗设备中,铁氧化物纳米材料的制备也日渐为众人所重视[1-6].
根据铁氧化物中铁的价态不同可将其分为:氧化铁、氧化亚铁和四氧化三铁,其中氧化铁(Fe2O3)又名铁红,是红棕色粉末状物质,广泛应用于油漆涂料中,有三种不同类型:(α-,β-,γ-)Fe2O3.α-Fe2O3俗称赤铁矿,在室温条件下的物理化学性质较为稳定,合成方便,原料廉价,环境友好,因而大量应用在磁性记录、铁氧体的制备上面. 而纳米α-Fe2O3因为尺寸小、比表面积大,导致了它的物理化学性质相较于块状氧化铁更为优异;同时纳米α-Fe2O3在耐光、屏蔽紫外线、软磁性、抗酸碱腐蚀方面表现出其优异性能,这些性质可以保证其在长时间反应过程中保持较高的活性,并且,当反应进行完全后又易于从反应体系中分离出来,以便进行后续的处理. 因此纳米氧化铁材料被广泛应用于光催化、环境保护、锂电池、医学诊疗等方面[7-11]. 最近,通过控制纳米α-Fe2O3形貌以强化其特定性质成为研究的热点,目前形貌控制主要通过包裹剂种类、表面活性剂的结构及极性、反应温度等因素予以控制,其中高比表面积、高结晶度、小尺寸是研究者努力的方向[1-3,6-15].
改变实验条件可获得多种不同形貌的α-Fe2O3纳米材料,其中较为常见的有:纳米颗粒、纳米线、纳米棒、纳米管、纺锤形、纳米片、雪花状等[1-9]. 随着研究的不断加深,研究者认识到可以通过对α-Fe2O3纳米材料进行改性以实现它的功能化,其中表面包裹已经成为一种重要的手段. 本文中我们使用了不同的包裹剂来合成α-Fe2O3纳米材料. 实验进一步揭示了α-Fe2O3纳米颗粒前驱体α-FeOOH的梭形结构,并通过一锅法反应成功在α-FeOOH表面覆盖一层介孔二氧化硅,煅烧后进而得到α-Fe2O3@SiO2复合纳米材料,该复合材料对水相中的亚甲基蓝有良好的吸附性能,最高去除率可以达到97.3%,表明经SiO2包裹后的α-Fe2O3晶体有优异的吸附特性. 并采用粉末X射线衍射、扫描电镜、磁学系统针对样品进行了相关表征.
1 实验部分
1.1实验药品及试剂
正硅酸乙酯(TEOS)(AR)购自天津科密欧试剂公司;无水乙醇 (EtOH)(AR)购自安徽安特生物科技有限公司;试剂:FeCl3·6H2O (国药集团化学有限公司);四乙氧基硅烷(TEOS)(Alfa Aesar);亚甲基蓝(国药);十六烷基三甲基溴化铵(CTAB)(天津市科密欧化学试剂有限公司);包裹剂包括6种含氮有机化合物,分别为双(2-羟乙基)亚氨-三羟甲基丙烷(EEDNDP)(Acros)、哌嗪(PP)(Acros)、5-氮杂胞嘧啶核苷(AS)(Chem Great Wall)、L-谷氨酸(GTC)(Acros)、1,3,5均三嗪(STZ)(Alfa Aesar)、L-组氨酸(HTD)(Acros),包裹剂详细信息列于表1中. 溶剂水为超纯水.
1.2制备方法
1.2.1α-Fe2O3纳米颗粒的制备
称取2 g FeCl3·6H2O, 0.4 g 包裹剂,0.4 g CTAB并装入玻璃瓶中,加入50 g超纯水后放入集热式恒温加热磁力搅拌器中于60 ℃下搅拌2 h后,将充分反应的混合液用一次性吸管全部移入水热釜中,密封水热釜后放入160 ℃烘箱内并在静止状态下加热24 h.
水热结束后,将沉淀移入离心试管内,离心可得Fe2O3固体,在超声波清洗机里充分分散后用乙醇洗涤2遍,洗去表面吸附的有机物,然后放入80 ℃电热恒温鼓风干燥箱里加热6 h,干燥完成后将固体沉淀在研钵中研成粉末状,移入离心试管中待用.

表1 制备α-Fe2O3所采用包裹剂信息
1.2.2α-Fe2O3@SiO2纳米颗粒制备
称取4 g FeCl3·6H2O, 0.4 g 包裹剂L-组氨酸,0.4 g CTAB移入玻璃瓶中,加入50 g超纯水后放入集热式恒温加热磁力搅拌器中于60 ℃下搅拌1.5 h后出现固体沉淀,接着加入2 g TEOS,持续搅拌12 h,然后将液体用一次性吸管移入离心试管内,离心可得固体沉淀,在超声波清洗机里充分分散后用乙醇洗涤2遍,洗去表面粘附的有机物,然后放入80 ℃电热恒温鼓风干燥箱里干燥6 h,将干燥后固体倒入坩埚中并放在550 ℃马弗炉中焙烧6 h,最后既可得到表面包裹由介孔SiO2的α-Fe2O3纳米材料.
1.3结构表征
扫描电子显微镜,JSM 5600LV型,日本电子,工作电压为15 kV. X射线粉末衍射仪(XRD, Cu Kα,λ=1.541 8 nm),Bruker D8 Advance,工作电压及电流分别为40 kV, 40 mA. 磁学测量系统,MPMS3,美国Quantum Design. 紫外可见分光光度计,U4100,日立公司. 用于扫描电镜测试的样品在单晶硅片上制备,取微量制备的含有α-Fe2O3纳米颗粒的原液滴于裁剪成1 cm的单晶硅片上,随后将涂有液体的硅片粘贴在涂膜机上并启动涂膜机保持转速为2 000 rpm,持续约30 s,干燥后的硅片喷金后用于扫描电镜测试.
2 结果与讨论
2.1利用不同包裹剂制备α-Fe2O3纳米颗粒
水热过程中不同结构的包裹剂在Fe2O3不同晶面上的吸附能不同,这就导致Fe2O3晶体在生长过程中受包裹较少的面生长速度较快,最终导致不同结构的Fe2O3纳米颗粒,但由于分子间相互作用的复杂性,现在仍然缺乏针对目标产物Fe2O3纳米颗粒形貌合理的预测手段. 本实验中采用了6种不同结构的有机含氮化合物作为包裹剂,其结构式如表1所示. 由于这些含氮有机化合物有接受质子的能力,其水溶液显示弱碱性. 推测其反应机理如下[8,10-13]:
首先在包裹剂提供的弱碱性环境下Fe3+与OH-作用生成Fe(OH)3,Fe(OH)3进一步缩聚成为FeOOH,高温水热处理后得到稳定相α-Fe2O3纳米颗粒. 如图1所示,XRD图谱与标准图谱(JCPDS No. 5-669)比对的结果证实合成物质为α-Fe2O3的纯净物. 进一步的磁学表征证实α-Fe2O3呈现弱磁性,其剩余磁化强度为0.22 emu/g,磁感矫顽力为3 000 Oe.
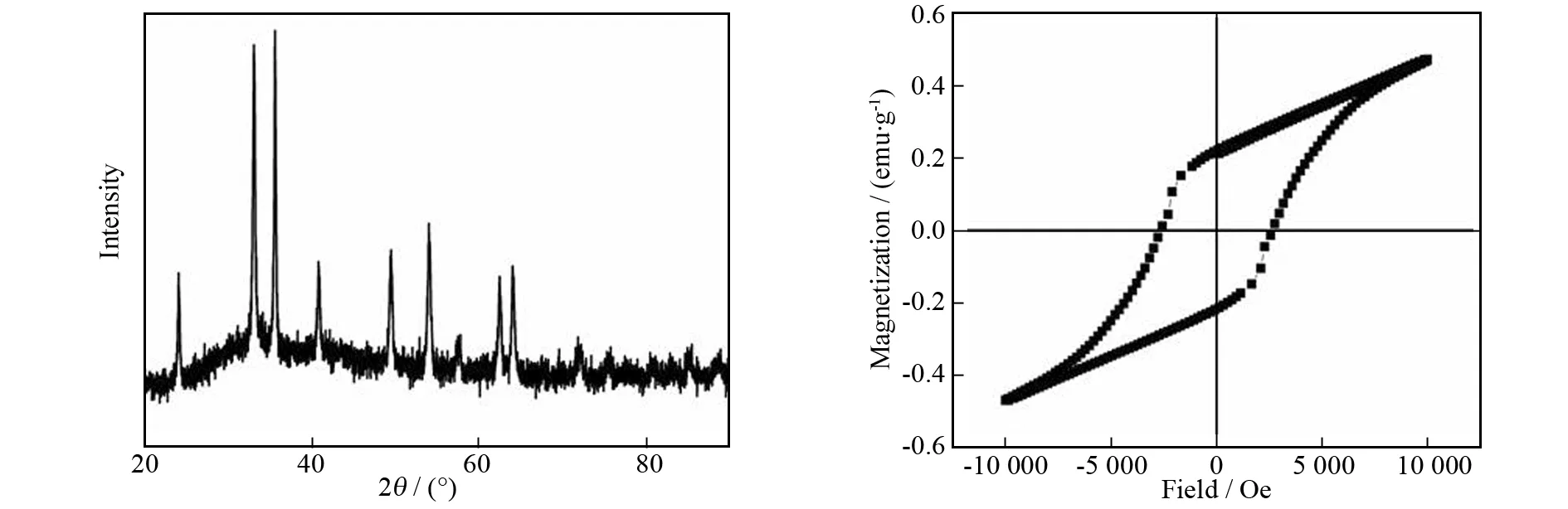
图1 制备的α-Fe2O3纳米颗粒XRD图谱及磁滞回线Fig.1 XRD pattern and magnetic hysteresis loop of as-prepared α-Fe2O3 nanoparticles
图2给出了不同包裹剂条件下的α-Fe2O3纳米颗粒的SEM图片. 从图2可以看出,α-Fe2O3颗粒粒径大约为1 μm. 通过改变包裹剂种类,可以实现针对α-Fe2O3颗粒形貌的调控,这里所制备的α-Fe2O3颗粒主要呈现饼型、不规则长方体及长方体形状,造成这种现象的原因可能与不同结构的包裹剂在α-Fe2O3颗粒表面吸附状态有关. 具有不同分子结构的包裹剂与氧化铁表面的选择性吸附能力不同,该选择性吸附不同程度上降低了晶体各晶面的晶面能,吸附在晶体表面的有机分子有可能促使晶体表面发生重构,这种变化来源于有机分子官能团电子结构与晶体表面原子间的相互作用[7-8]. 另外,包裹剂在不同晶面覆盖度差异会影响物质的分子或者晶核在材料界面处交换速率,进而对晶体生长及最终的形貌产生影响[8]. 实验中当包裹剂为组氨酸时α-Fe2O3颗粒边缘不规则,伴随着颗粒中间出现空洞的现象. 我们推测组氨酸为包裹剂时的α-Fe2O3颗粒的多样性可能与N原子所处的复杂环境有关. 根据组氨酸的结构可以看出,在组氨酸分子中,伯、仲、叔胺的N原子均存在,跟其它结构的包裹剂分子相比,组氨酸的N原子所处环境更加复杂. 当然,包裹剂分子结构与α-Fe2O3颗粒形貌间的本质联系需要更多实验及表征予以佐证,包括选取更多含有不同结构N原子的包裹剂控制α-Fe2O3颗粒形貌,以及傅立叶变换红外光谱、拉曼光谱、固态核磁表征考察目标产物的构成及包裹剂与α-Fe2O3颗粒分子间的相互作用.
考虑到α-Fe2O3颗粒是由α-FeOOH颗粒通过羟基缩合而成,我们进一步对80 ℃下形成的FeOOH进行了表征. 如图3所示,虽然α-Fe2O3颗粒的形貌不尽相同,但其前驱体α-FeOOH颗粒却是基本相同的,都呈现梭形结构,长度大约为300 nm,宽度为10~30 nm. 这说明包裹剂在低温环境仅仅提供弱碱性环境,包裹剂本身并不与α-FeOOH颗粒发生作用,但随着水热温度升高,尤其是超过120 ℃时,包裹剂会在α-Fe2O3颗粒不同的晶面上发生不同的吸附作用,进而影响最终的α-Fe2O3颗粒的形貌.

(a) 双(2-羟乙基)氨基(三羟甲基)甲烷; (b) 哌嗪; (c) 五氮杂胞嘧啶核苷; (d) L-谷氨酸; (e) 1,3,5均三嗪; (f) L-组氨酸.图2 采用不同包裹剂制备α-Fe2O3纳米颗粒的SEM图片Fig.2 SEM images of as-prepared α-Fe2O3 nanoparticles using various capping agents respectively corresponding to (a) EEDNDP, (b) PP, (c) AS, (d) GTC, (e) STZ and (f) HTD

图3 不同包裹剂下梭形α-FeOOH颗粒的SEM图片. (a) 谷氨酸;(b) L-组氨酸Fig.3 SEM images of spindle α-FeOOH nanoparticles synthesized by the capping agents of (a) GTC and (b) HTD
2.2α-Fe2O3@SiO2复合纳米材料的制备及其吸附性能
介孔二氧化硅包裹材料后会提供大的比表面积并且后继热处理过程不易发生颗粒间的团聚现象,包裹后的材料往往能够呈现更好的吸附、催化性能. 本实验中我们选取包裹剂为组氨酸时,当反应进行1.5 h后加入TEOS,继续反应12 h后离心出包裹有介孔二氧化硅的α-FeOOH纳米颗粒,550 ℃高温煅烧后即可制备出α-Fe2O3@SiO2复合纳米材料. 图4显示α-Fe2O3@SiO2复合材料很好的保持了梭形结构.
鉴于α-Fe2O3@SiO2纳米复合材料具有优异的吸附性能,我们进一步考察了该材料对水中亚甲基蓝的吸附性能. 实验首先称取0.025 gα-Fe2O3@SiO2复合纳米材料粉末加入到20 mL的浓度为530 μmol/L的亚甲基蓝溶液中,室温条件下搅拌. 取样时间分别为5、10、15、 25、35、45、60、75、105、135、195、255、315 min. 进一步对离心分离出的上层清液用紫外可见分光光度计进行表征,实验结果与标准曲线比对后可以得到α-Fe2O3@SiO2纳米复合材料随时间变化对亚甲基蓝的去除率. 图5中进一步给出了α-Fe2O3@SiO2纳米复合材料随时间变化去除亚甲基蓝的数据. 可以看出,当吸附时间为315 min时,亚甲基蓝去除率可以达到97.3%,因此α-Fe2O3@SiO2纳米复合材料对水中亚甲基蓝表现出优良吸附性能. 另外,由于α-Fe2O3具有弱磁性,当吸附完成后可以通过施加外加磁场的方法将吸附质从溶液中分离出来,如图5中(b)图显示.

图4 梭形α-FeOOH颗粒包裹介孔二氧化硅前后SEM照片. (a) 未包裹; (b) 包裹后Fig.4 SEM images of spindle α-FeOOH nanoparticles (a) before (b) after deposition of mesoporous silica layer

图5 (a) α-Fe2O3@SiO2复合材料去除亚甲基蓝数据. (b) 吸附前后溶液颜色变化. (c) α-Fe2O3@SiO2复合材料去除亚甲基蓝过程中不同时刻溶液颜色变化比较Fig.5 (a) Temporal removal ratio of methylene blue from water solution using α-Fe2O3@SiO2 as adsorbent. (b) Color of the aqueous solution of methylene blue before and after the addition of α-Fe2O3@SiO2. (c) Temporal pictures of aqueous solutions of methylene blue after centrifugation to separate the adsorbents of α-Fe2O3@SiO2
3 结论
采用不同的包裹剂成功制备具有弱磁性的α-Fe2O3颗粒,颗粒形貌可以通过改变包裹剂的分子结构予以调控,推测原因可能与在水热条件下包裹剂与α-Fe2O3颗粒不同晶面的吸附强度有关,可以实现针对α-Fe2O3颗粒形貌从饼型到长方体进而到空心结构的调控. 另外通过一锅法制备了包裹有介孔二氧化硅层的α-Fe2O3颗粒,由于该颗粒具有较大的表面积,在水相中可以有效去除亚甲基蓝,该方法制备简单,在水处理中有很好的应用前景.
[1] WANG B, WU H B, YU L, et al. Template-free formation of uniform urchin-likeα-FeOOH hollow spheres with superior capability for water treatment [J]. Adv Mater, 2012, 24: 1111-1116.
[2] AYACHI A A, MECHAKRA H, SILVAN M M, et al. Monodisperseα-Fe2O3nanoplatelets: synthesis and characterization [J]. Ceram Int, 2015, 41: 2228-2233.
[3] WU H X, ZHANG S J, ZHANG J M, et al. A Hollow-core, magnetic, and mesoporous double-shell nanostructure: in situ decomposition/reduction synthesis, bioimaging, and drug-delivery properties [J]. Adv Funct Mater, 2011, 21: 1850-1862.
[4] SHETE M D, FERNANDES J B. A simple one step solid state synthesis of nanocrystalline ferromagnetic a-Fe2O3with high surface area and catalytic activity [J]. Mater Chem Phys, 2015, 165: 113-118.
[5] PADASHBARMCHI Z, HAMIDIAN A H, ZHANG H W, et al. A systematic study on the synthesis ofα-Fe2O3multi-shelled hollow spheres [J]. RSC Adv, 2015, 5: 10304-10309.
[6] CHEN L Q, YANG X F, CHEN J, et al. Continuous shape and spectroscopy-tuning of hematite nanocrystals [J]. Inorg Chem, 2010, 49: 8411-8420.
[7] PENG Q S, ZHAO H Y, QIAN L, et al. Design of a neutral photo-electro-Fenton system with 3D-ordered macroporous Fe2O3/carbon aerogel cathode: high activity and low energy consumption [J]. Appl Catal B: Environ, 2015, 174/175: 157-166.
[8] 李松. 氧化铁基纳米材料的结构设计、表征与光催化性能研究 [D]. 沈阳: 东北大学, 2010: 29-38.
[9] HUANG X P, HOU X J, SONG F H, et al. Facet-dependent Cr(VI) adsorption of hematite nanocrystals [J]. Environ Sci Technol, 2016, 50: 1964-1972.
[10] SAYED F N, POLSHETTIWAR V. Facile and sustainable synthesis of shaped iron oxide nanoparticles: effect of iron precursor salts on the shapes of iron oxides [J]. Sci Rep, 2016, 5: 09733 1-14.
[11] FAN H, HUANG X, SHANG L, et al. Controllable synthesis of ultrathin transition-metal hydroxide nanosheets and their extended composite nanostructures for enhanced catalytic activity in the heck reaction [J]. Angew Chem Int Ed, 2016, 55: 2167-2170.
[12] TIYA-DJOWEA A, SAMUEL L, NOUPEYI G L, et al. Non-thermal plasma synthesis of sea-urchin likeα-FeOOH for the catalytic oxidation of orange II in aqueous solution [J]. Appl Catal B: Environ, 2015, 176/177: 99-106.
[13] PENKI T R, SHIVAKUMARA S, Minakshi M, et al. Porous flower-likeα-Fe2O3nanostructure: a high performance anode material for lithium-ion batteries [J]. Electrochim Acta, 2015, 167: 330-339.
[14] 刘翠,李保山. 纳米棒状α-Fe2O3的制备及其光催化性能[J]. 工业催化, 2007, 15: 51-54.
[15] 路燕琴, 朱丽, 何昭菊, 等. 沸石负载氧化铁吸附剂吸附除磷研究[J]. 环境工程, 2015, 4: 1-6.
[责任编辑:刘红玲]
Preparation ofα-Fe2O3and adsorption performance ofα-Fe2O3@SiO2nanocomposites
LI Xiying*, QI Yahui, LI Mingjie, WANG Kunpeng, GAO Li, LIU Yong, MAO Liqun
(CollegeofChemistryandChemicalEngineering,HenanUniversity,Kaifeng475001,Henan,China)
Weak magneticα-Fe2O3nanoparticles were prepared using organic molecules containing N atoms as capping agents. Morphologies of the formedα-Fe2O3nanoparticles undergo a continuous transformation from pie to irregular cube and then to cube shape. Furthermore, the phase ofα-FeOOH assuming the precursor ofα-Fe2O3nanoparticles possessed spindle structure and was coated by mesoporous silica layer by subsequent addition of TEOS via one-pot reaction. After calcination, the resultedα-Fe2O3@SiO2nanocomposite was prepared and afforded the adsorbent in removing methylene blue in aqueous phase. Under ambient condition, the removal efficiency was high up to 97.3%. These as-prepared products were characterized by XRD, SEM and magnetic tests.
α-Fe2O3nanoparticles;α-Fe2O3@ SiO2nanocomposite; adsorption
1008-1011(2016)04-0470-06
2016-01-17.
国家自然基金青年基金(21104016).
李西营(1977-),男,副教授,研究方向为功能纳米材料制备及应用.*通讯联系人,E-mail: xiyingli@henu.edu.cn.
TB333
A
