氮化硼纳米片及其凝胶材料的研究进展
2016-08-16付钦瑞王海龙方子林胡全钦段程皓鲁福身
付钦瑞,孟 园,王海龙,方子林,胡全钦,段程皓,鲁福身
(汕头大学 理学院 化学系,广东 汕头 515063)
氮化硼纳米片及其凝胶材料的研究进展
付钦瑞,孟园,王海龙,方子林,胡全钦,段程皓,鲁福身*
(汕头大学 理学院 化学系,广东 汕头 515063)
氮化硼纳米片具有高机械强度、良好的化学惰性和热稳定性等优点. 除了这些性质, 基于纳米氮化硼的凝胶材料还有高比表面积、大孔隙率等特点. 因此它在催化、储氢、除污和气体吸附等领域具有潜在的应用前景. 这篇综述主要介绍了氮化硼纳米片及其凝胶材料的制备, 举例说明了氮化硼凝胶的关键应用并加以展望.
氮化硼纳米片;凝胶;催化;储氢;除污
六方氮化硼(hexagonal boron nitride, 缩写为h-BN)是石墨的等电子体, 并且结构与之类似. 因此, 单层或少数层的六方氮化硼纳米片(boron nitride nanosheets, 缩写为BNNSs)具有很多类似于石墨烯(单层石墨, graphene)的优良性质. 例如良好的热传导性、优异的化学和热稳定性以及高的机械强度等. 但是由于B-N 键与C=C 键之间的差异(比如键的极性、电子离域等), BNNSs 又具有一些不同于石墨烯的独特性质. 例如, BNNSs 是绝缘体;具有很强的抗氧化性, 在空气中的热稳定温度可达1 000 ℃, 并且与酸、碱和熔融金属不易发生化学反应;在深紫外区有明显的吸收. 上述性质使BNNSs 在一些重要的关键应用领域(如催化载体、介电层、陶瓷和高分子复合材料等)都显示了独特的和潜在的应用价值[1-4].
基于氮化硼纳米片而构筑的凝胶材料也受到不同领域科学家的高度关注.相对于前者, 纳米氮化硼凝胶具有多孔结构和更大的比表面积. 因此在诸如气体储存、污染物的吸附和药物运输等领域有进一步的优势. 目前纳米氮化硼凝胶材料主要有水凝胶和气凝胶(包括三维多孔的泡沫或海绵材料). 氮化硼纳米材料本身没有明显的毒性[5], 因此氮化硼复合水凝胶有很好的生物相容性, 有望应用于药物运输或生物支架. 氮化硼气凝胶的多孔性使之适用于物质的吸附, 特别是有机污染物的吸附与净化. 因为氮化硼具有很强的抗氧化性和不可燃性, 因此吸附了有机污染物的氮化硼气凝胶可以通过灼烧的方式进行回收或循环使用. 这是石墨烯气凝胶不易实现的独特之处.
经过不懈的努力, 氮化硼纳米片及其凝胶材料取得了很多重要研究成果. 本文将对这些材料的制备和关键应用进行简要评述, 并加以展望.
1 氮化硼纳米片的制备
由于氮化硼纳米片与石墨烯结构类似, 因此人们往往借鉴石墨烯的制备方法来合成氮化硼纳米片. 例如通过化学气相沉积法(Chemical Vapor Deposition, 缩写为CVD)在金属基片上生长氮化硼纳米片或石墨烯;通过机械处理或溶剂分子的插层剥离块体氮化硼或石墨而得到单层和少数层的BNNSs 或石墨烯. 但是由于氮化硼层与层之间具有很强的啮合(lip-lip)作用, 因此制备氮化硼纳米片往往需要更苛刻的反应条件, 产率也相对更低[6-7].
1.1化学气相沉积法(CVD)
CVD 法制备氮化硼需要追溯到二十世纪六十年代. 1964 年, BASCHE 在专利中报道了以氨气和氯化硼为前驱体, 在1 450-2 300 ℃ 通过热分解制备氮化硼膜[8].1968 年, RAND 和ROBERTS 以氨气和硼烷为前驱体, 以硅或金属为基底制备出无定型氮化硼[9]. 但这些氮化硼厚度较大, 并不是少数层或单层的. 因此它们在性能和应用方面受到限制. 直到1990 年, PAFFETT 等人才以环硼氮烷为前驱体, 在Pt和Ru 基底上首次合成了单层六方氮化硼片[10]. BNNSs 的CVD 生长主要涉及3个方面:硼源与氮源、基底和生长条件. 通常CVD 法制备BNNSs 的前驱体可采用硼源和氮源的混合物(如BCl3-NH3, BF3-NH3, B2H6-NH3等), 也可使用单一的前驱体(如氨硼烷NH3BH3, 环硼氮烷B3N3H6). 后者相较于前者, 虽然稳定性稍差, 但其毒性小且B与N的化学计量比与氮化硼一样是1∶1, 因此被视为更理想的前驱体. BNNSs 可在许多过渡金属表面上生长, 如Ni、Cu、Pd、Pt、Cr、Fe、Mo、Ru 和Rh. 不同的基底, BNNSs 的生长过程不完全相同, 如以Pt 为基底时得到的BNNSs 的形状是弧形边缘的三角形;而以Cu 为基底时, BNNSs 首先在铜表面形成三角形的岛状结构, 然后合并生成完整的纳米片层;而在Ni 或Rh 基底上则没有固定的生长趋势[7,11]. 因此, 采用CVD 法制备BNNSs 时, 生成BNNSs 的形状与选择的基底材料种类密切相关. CVD 生长条件包括气压、温度和载气等. 从气压的角度可将CVD 分为常压化学气相沉积法(APCVD)和低压化学气相沉积法(LPCVD).载气可采用单一组分(如N2、H2、Ar 等)和混合组分(如Ar/H2等). 如SONG 等人以氨硼烷为前驱体, 在Cu 基底上、Ar/H2气流中和1 000 ℃ 下采用APCVD 制备出连续的、透明状的少数层BNNSs, 区域面积达到数平方厘米[12]. Cu 基底的晶格常数(0.255 nm)与h-BN 的面内晶格常数(0.25 nm)相近, 有利于形成大区域的BNNSs.另外, 铜箔的质量对于控制BNNSs 在基底上连续生长和层数至关重要. 而SHI 等人以环硼氮烷为前驱体, 在多晶Ni 基底上, N2气流中和400 ℃ 下同样制备出区域面积约为平方厘米的少数层BNNSs. 在此条件下提高生长温度并没有得到连续的氮化硼膜, 而是得到了表面粗糙或颗粒状的h-BN. 可能的原因是过高的生长温度会使前驱体与Ni 基底表面间的润湿性变差从而影响氮化硼膜的生长[13]. 这两项研究说明反应条件(如生长温度和基底等)综合影响BNNSs 的质量. KIM 等人以氨硼烷为前驱体, 无载气条件下通过LPCVD 法在Cu 基底上制备出高结晶度、纯净的单层BNNSs[14]. 不使用载气可避免前驱体热分解形成的质量较大的杂质扩散到Cu 基底上, 从而影响BNNSs 的纯度.
1.2机械剥离法
用于剥离h-BN 的机械力主要有拉力和剪应力. 二者剥离的原理是相似的, 即破坏h-BN 相邻层间弱的范德华力而不破坏层内强的共价键. 胶带粘力是一种简单的机械拉力, 2005 年NOVOSELOV 等人利用这种机械力剥离块体h-BN 而得到晶体完整的原子层厚度的BNNSs[15]. 但是这种方法效率低, 难以实现BNNSs 的批量制备. 目前, 研究人员已用球磨法取代低效的胶带剥离法. 如LI 等人利用湿法球磨制备出结晶度良好的少数层BNNSs[16]. 在球磨法制备BNNSs 过程中, 球与球磨剂的选择至关重要. 为了避免球磨过程中产生过大的剪应力而影响BNNSs 的质量(过多的缺陷), 通常采用大量的小球而少用大球;球磨剂通常选择高粘性且表面张力与h-BN 相似的溶剂. 如LI 等人选择苯甲酸苄酯为球磨剂, 其效果要好于水或乙醇[16-17]. 进一步地, 选用氨基化合物作为球磨剂能实现BNNSs 的剥离与修饰同步进行. 如LEI 等人选择尿素为球磨剂得到含有氨基团的BNNSs, 其分散液浓度高达30 mg/mL[18](图1). 虽然人们持续改进球磨条件来制备BNNSs, 但是所得BNNSs 的横向尺寸比胶带法小, 而且往往含有更多的缺陷. 另外, 采用涡流装置提供的剪应力在给定的角度和转速下也能有效的制备BNNSs. 如CHEN 等人将h-BN 分散到N-甲基吡咯烷酮中, 转移到倾斜角度为45 度的玻璃管中, 在8 000 rpm转速下产生的剪应力实现对h-BN 的剥离[19].

(a) 剥离示意图; (b) 浓度分别为0.5, 2.0, 6.0, 30 mg/mL 的少数层氮化硼胶体溶液及其丁达尔现象和稳定性.图1 剥离与分散过程示意图[18]Fig.1 Schematic illustration of the exfoliation and dispersion process[18]
1.3液相插层剥离法
溶剂的种类决定着插层剥离h-BN 的效果. 适合的溶剂应具有一定极性且能够分散h-BN, 使层状材料的剥离能最小化[20]. 研究显示表面张力与h-BN相接近的溶剂, 如N,N-二甲基甲酰胺(DMF)、N-甲基吡咯烷酮(NMP)、异丙醇(IPA)、乙二醇、甲基磺酸(MSA)和碱溶液等, 在超声条件下能克服氮化硼层与层间的范德华力从而实现剥离. 例如, ZHI 等人选择DMF 为溶剂超声剥离h-BN 得到一种横向尺寸稍微变小的BNNSs. 尺寸变小可能是在超声剥离过程中h-BN 层内缺陷部位的键断裂造成的[21]. 二氯亚砜(SOCl2)也是一种极性溶剂, 其表面张力为36.1 mN/m, 与原始h-BN 的表面张力很接近. 因此我们课题组选择SOCl2为溶剂, 超声剥离h-BN 得到BNNSs(图2). 其产率高达20%, 超过类似的文献报道[22].
单纯利用溶剂的插层来制备BNNSs, 通常产率低或分散性较差. 向溶剂中加入修饰试剂可在剥离h-BN 的同时实现BNNSs 的修饰或改性, 进而提高产率和改善其分散性. h-BN 中的B 和N 原子通过sp2杂化成键, 并有π电子的离域. 共轭有机分子可通过π-π相互作用对BNNSs 进行非共价键修饰. 2008 年, HAN 等人在含有共轭聚合物的1,2-二氯乙烷中超声剥离h-BN 得到BNNSs[23]. 我们课题组采用水溶性的聚苯乙烯磺酸钠(PSS)和3,4,9,10-苝四羧酸钠(SPTB)对BNNSs 进行了剥离与修饰, 所得BNNSs 分散液放置一个月后而不出现沉淀. 其TEM 图在电子光束下呈半透明状, 说明纳米片的厚度为纳米级;其选区电子衍射显示在剥离和修饰后, 依然保持了h-BN 的晶型(图3)[24]. 我们课题组还将柠檬酸与h-BN 的混合物在氩气保护下于170 ℃ 反应, 所得固体在水中超声分散制备出水溶性良好的ca-BNNSs, 并用于水凝胶的制备[25].

(a) 剥离示意图; (b, c) BNNSs的AFM图(插图为对应BNNSs的高度曲线);(d, e) BNNSs的TEM图和(f, g, h)边缘折叠的BNNSs的高分辨TEM图;其中图(h)是图(e)中选定区域的放大图.图2 SOCl2剥离的BNNSs[22]Fig.2 BNNSs exfoliated in SOCl2[22]

(a)PSS与SPTB修饰/剥离BNNSs的示意图;(b)PSS-BNNS的TEM图和选区电子衍射图.图3 BNNS的非共价键修饰[24]Fig.3 Non-covalent functionalization of BNNSs[24]
2 氮化硼凝胶的制备
随着BNNSs 合成方法的逐渐发展与完善, 出现了基于BNNSs 的凝胶材料.这种凝胶材料是通过物理或者化学方法将BNNSs 相互联接而成的三维多孔材料.相比于BNNSs, 凝胶不仅具有大的比表面积, 而且避免了加工过程中固态的BNNSs 重新堆垛而引起厚度增加的现象, 维持了BNNSs 的独特性质. 目前研究较多的是BNNSs 气凝胶, 主要利用含B和N 的小分子通过CVD 法合成. 而BNNSs水凝胶主要利用水溶性的BNNSs 通过物理或化学法交联而成.
2.1气凝胶
2.1.1模板法
制备气凝胶的模板主要为碳[26-32]和金属材料[33-37]等. 采用这两种模板生长氮化硼气凝胶的机理有所不同, 对于前者, 主要是在高温条件下实现B 和N 原子对C 原子的原位取代. 也就是说氮化硼的生长与碳材料模板的去除同步进行, 并且氮化硼凝胶大致维持所用模板的形貌与结构.如ROUSSEAS 等人以氧化硼和氮气为反应试剂成功将石墨烯气凝胶转换为低密度、高纯度(>95%)的氮化硼气凝胶(图4)[29]. 类似地, 如SONG 等人以氨硼烷为反应物, 以石墨烯和碳纳米管复合气凝胶为模板, 利用LPCVD法制备出含有氮化硼纳米片和纳米管的气凝胶[30]. 它的表面积可达1 051 m2/g、质量密度低至0.6 mg/cm3. 利用多孔碳材料模板除了可以制备高纯的氮化硼凝胶, 还可以通过控制反应条件(温度或反应时间等)实现碳原子的不完全取代, 进而得到含有C、B、N 三种元素的凝胶材料[32]. 对于多孔金属模板, 它既是氮化硼生长的基底又是催化剂. 因此反应结束后模板将被氮化硼材料包裹而存在于凝胶当中. 因此需要采用化学方法去除模板再得到氮化硼凝胶.YIN 等人以氨硼烷为原料、采用LPCVD 法在泡沫镍表面生长氮化硼薄膜, 得到了超低介电常数和超弹性的轻质氮化硼泡沫[33]. 氮化硼凝胶同样继承了泡沫镍的各向同性的和三维骨架结构. 另外, 人们利用多孔硅为模板间接地制备氮化硼凝胶材料. 如ALAUZUN 等人以合成的硅泡沫为模板先制备出碳泡沫, 然后由B 和N 取代C 得到高孔隙率和多级孔结构的氮化硼泡沫[38].
2.1.2无模板合成法
理论推测表明氮化硼纳米多孔结构的比表面积可以达到4 800 m2/g[39-40], 暗示着合成大比表面积的多孔氮化硼材料是可行的. 目前, 人们采用无模板法已经成功合成出较大比表面积的氮化硼凝胶材料[41-43]. 如WENG 等人利用硼酸和双氰胺经过无模板法制备了比表面积为1 900 m2/g 具有储氢功能的多孔氮化硼海绵[42].XUE 等人采用经济、无毒的硼酸、双氰胺甲醛树脂和氨经过无模板合成法制备出比表面积为1 406 m2/g 具有净化污水作用的氮化硼泡沫(图5)[43].利用模板法(特别是泡沫金属模板)合成的氮化硼气凝胶, 其比表面积受所用模板的限制, 与理论差距很大. 无模板合成法制备出的氮化硼凝胶, 其比表面积相对较大, 通常大于1 400 m2/g.

图4 (a)石墨烯气凝胶模板(左)和转化的氮化硼气凝胶(右)的照片;(b)氮化硼气凝胶中交联部位的高分辨TEM 图[29]Fig.4 (a) Photograph of a precursor graphene aerogel (left) and a converted BNaerogel (right); (b) High-resolution TEM image of a cross-link in a BN aerogel[29]

图5 泡沫状氮化硼材料的合成示意图[43]Fig.5 Schematic diagram of the synthesis of BN foam-like monoliths[43]
2.2水凝胶
水凝胶是一种三维网状结构的功能材料, 其质地柔软, 遇水溶胀而不溶解, 能保持一定的形状. 以纳米材料作为交联剂而制备的复合水凝胶呈现出优于传统水凝胶的机械和光学性能. 良好的水溶性是纳米材料作为交联剂的前提条件. 然而氮化硼是憎水性材料, 因此通过化学修饰在BNNSs 表面引入亲水性基团是将其用于水凝胶的关键. 常规修饰方法主要通过在BNNSs 表面引入大量表面活性剂或水溶性聚合物来提高其亲水性[23]. 但是引入的这些外来组分将作为“杂质”出现在BNNSs 样品中, 不利于凝胶的形成和性能的改善. 所以人们需要新的修饰方法来制备更为“洁净”的水溶性BNNSs 样品.
XIAO 等人剥离原始的h-BN 并对其进行功能化修饰, 使疏水的块状h-BN 转化成亲水的OH-BNNSs. 所得OH-BNNSs 在水和乙醇中具有良好的分散性, 能够有效地与聚(N-异丙基丙烯酰胺) (PNIPAM) 结合, 从而形成PNIPAM/OH-BNNSs复合水凝胶. 添加0.07 wt% OH-BNNSs 便能使凝胶的热导提高41%(图6)[44].
我们课题组用熔融的柠檬酸修饰BNNSs, 制备水溶性的ca-BNNSs. 根据光谱和热重分析数据得知, BNNSs 表面没有吸附或修饰大量柠檬酸分子. BNNSs 的亲水性可能来自于其B-N 键断裂产生的NH 和OH 等基团. 我们利用这种相对“洁净”的样品制备出ca-BNNSs/聚丙烯酰胺水凝胶(BNNS2.5/PAAm)[25]. 该水凝胶具有优异的柔韧性. 压缩应变为97%且应力超过8 MPa 时仍不破裂, 拉伸形变超过10 000% (图7);特别是保水性能突出, 在室温下长时间放置含水量仍高于94%.
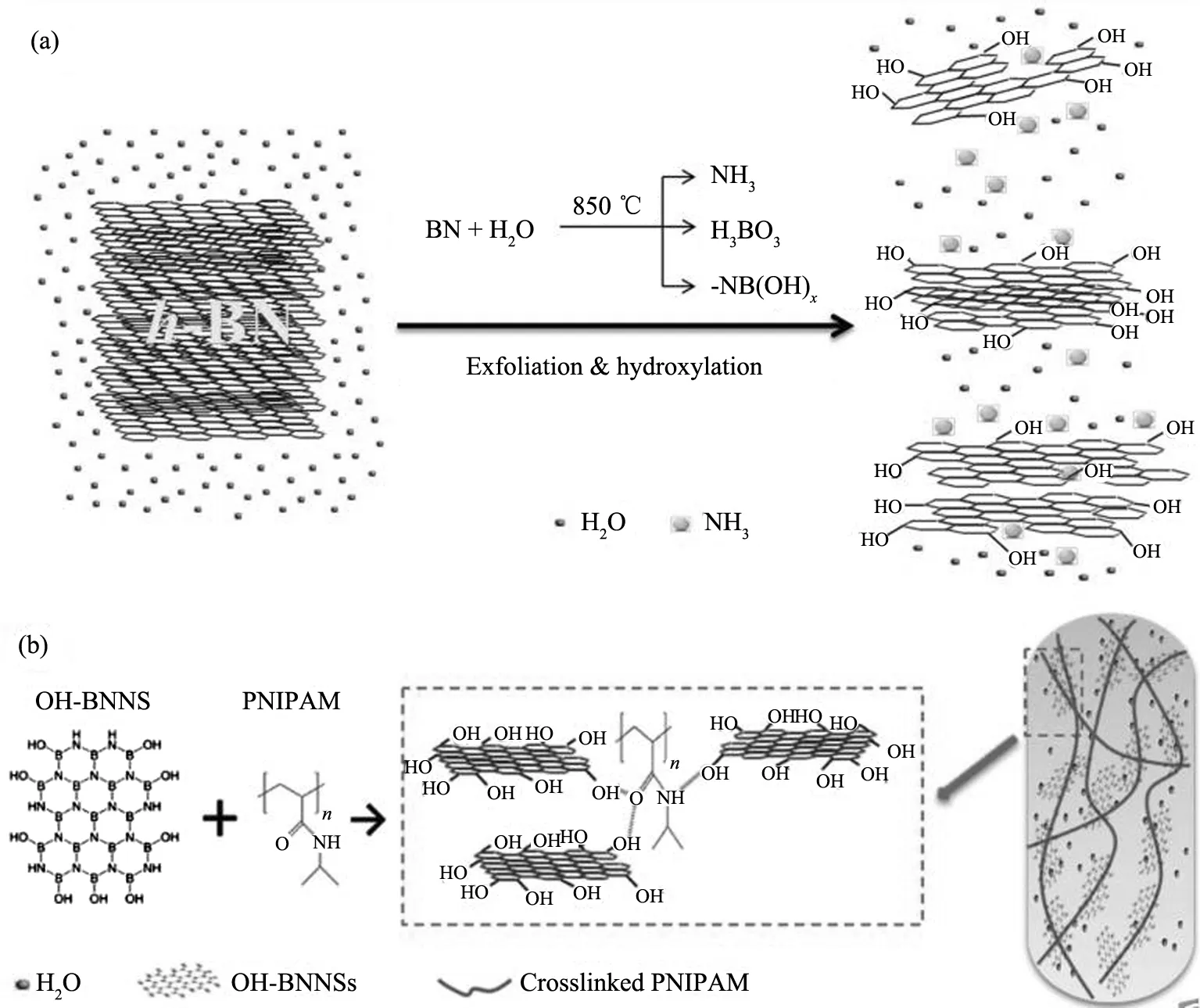
(a) 在热蒸汽中水解辅助剥离和h-BN粉末羟基化的示意图;(b) PNIPAM/OH-BNNSs水凝胶形成示意图.图6 PNIPAM/OH-BNNSs水凝胶的制备过程[44]Fig.6 Preparation of PNIPAM/OH-BNNSs hydrogel[44]

(a) BNNS2.5/PAAm水凝胶在经受大程度的压缩应变后完全恢复, 相较之下, (b) PAAm水凝胶样品容易碎裂;(c) BNNS2.5/PAAm水凝胶的拉伸测量并承受各种变形(d, e和f).图7 BNNS2.5/PAAm和PAAm水凝胶的柔韧性[25]Fig.7 Flexibility of BNNS2.5/PAAm and PAAm hydrogels[25]
水凝胶经过适当的干燥技术除去水分可直接转化为气凝胶[18,45-47]. 将BNNS2.5/PAAm 复合水凝胶冷冻干燥后观察其微观结构, 发现它具有多级孔结构(图8)[25], 大孔的尺寸一般在几百微米, 其孔壁由直径为几十微米的小孔组成, 构成相互贯通的三维网状结构. 这种特殊结构可能是BNNS2.5/PAAm 凝胶的良好柔韧性和保水性的起因. 而不含BNNSs 的传统PAAm 凝胶不具有这样的结构, 性能也急剧下降(图8)[25]. 在类似的研究中, LEI 等人利用球磨法制备高浓度BNNSs 水溶液, 静置两周直接转化为水凝胶(图1b), 将其冷冻干燥后得到在紫外光激发下发蓝光的BNNSs 气凝胶[18]. 除了冷冻干燥, 人们还尝试其他干燥技术. 如JUNG 等人利用胆酸钠(表面活性剂)剥离和修饰h-BN 粉末, 蒸发部分溶剂后得到水凝胶, 再用热水处理移除表面活性剂, 最终通过临界点干燥技术除去全部溶剂得到氮化硼气凝胶[45].

(a) 干凝胶的多级孔结构; (b) 是图(a)中选定区域的放大图; (c)和(d) 分别是PAAm 样品的不同放大倍数的图像.图8 冻干BNNS2.5/PAAm 凝胶的SEM 图[25]Fig.8 Typical SEM images of lyophilized xerogels[25]
3 氮化硼纳米片及其凝胶材料的应用
氮化硼凝胶材料的应用与它的性质和结构紧密相关. 基于它的电子结构和多孔性, 人们将其作为催化剂载体用于各种反应;基于它与H2之间的强结合能, 人们探索它的储氢性能;基于它的疏水性和吸附性, 人们采用它进行有机污染物的去除与净化. 虽然氮化硼凝胶的应用比较有限, 但是这些关键应用为氮化硼纳米片及相关材料的研究注入了新的活力.
3.1催化
氮化硼材料具有良好的化学稳定性和抗氧化性. 它在高温和氧化条件下表现出优于传统催化剂载体的性能. 而且理论计算显示过渡金属的dz2轨道与BNNSs 中B、N 的pz轨道有重叠, 因此BNNSs 负载的金属的催化活性可能与传统催化剂有差异[48-50]. 我们课题组在氮化硼纳米片表面负载了Pd 纳米粒子并用于硝基化合物的催化加氢反应, 性能优于商业化的Pd/C 催化剂(Sigma-Aldrich).而且催化剂可以循环使用15 次, 活性没有明显降低[22]. 氮化硼凝胶材料的多孔网状结构有利于反应底物和产物的扩散, 并更大程度地负载金属活性组分, 提高催化性能[51-53]. ZHAO 等人通过无模板合成法制备出三维氮化硼泡沫, 然后以其为载体负载Ag 纳米粒子得到Ag/3D BN 催化剂(图9). 相比于传统的Ag/γ-Al2O3, 这种催化剂在甲醇的氧化反应中表现出更高的稳定性和催化活性. 在转化率为50%和95%, Ag/3D BN 对应的起燃温度分别是50 ℃ 和110 ℃, 大约是Ag/γ-Al2O3对应值的一半[53]. 最近人们还将多孔氮化硼材料应用于光化学反应中. 如WENG 等人以氧化聚乙烯与硼酸的混合物为前驱体在1 000 ℃ 氨气氛围下焙烧合成了氮化硼泡沫. 由于其结构中存在的OH 官能团能缩小氮化硼的带隙, 从而表现出良好的可见光吸收能力. 这种泡沫与TiO2纳米粒子结合形成的复合物可作为光催化剂来降解有机物[54]. 有趣的是, 氮化硼材料自身也可以作为催化剂使用. 如PATIL等人制备了还原氧化石墨烯/氮化硼三维复合材料, 并作为无金属催化剂应用于氧气的电化学还原反应. 这种无金属催化剂同样呈现了高于商品化Pt/C 的稳定性[55].

图9 Ag/3D BN 催化甲醇氧化反应的机理图[53]Fig.9 Illustration of the reaction mechanism of Ag/3D BN catalytic methanol oxidation[53]
3.2储氢
开发高容量储氢材料是发展氢能源的关键步骤. 根据理论数据, H2分子与氮化硼表面的相互作用要大于H2分子与碳表面的相互作用[56-57]. 一个明显的例子, H2在氮化硼纳米管上比在碳纳米管上的结合能增加了40%[58]. 因此有望利用氮化硼纳米材料进行储氢. WENG 等人制备了一种比表面积高达1 900 m2/g, 孔隙率为1.070 cm3/g 的氮化硼海绵. 在-196 ℃ 和1 MPa 的条件下, 其储氢能力为2.57wt%[42]. 最近, 氮化硼与埃洛石纳米管或多壁碳纳米管结合制备的复合材料, 也表现出良好的储氢能力. 前者在50 ℃ 的条件下储氢能力为2.88 wt%[59], 后者在100℃ 下储氢能力为2.3 wt%[60]. 由此可知, 氮化硼材料不仅在低温, 而且在较高温条件下也具有良好的储氢能力.
3.3除污与净化
氮化硼凝胶材料(水凝胶类材料除外)通常具有亲油性、大比表面积和高孔隙率. 根据“相似相溶”的原理, 这些凝胶材料可以很好地吸附有机污染物. ZHAO等人制备的氮化硼泡沫, 能吸附自身重量190倍的有机污染物或油[61]. PHAM 等人制备的三维氮化硼气凝胶表现出良好的吸油能力(高达1 500 wt%)[31]. XUE 等人制备的泡沫状多孔氮化硼材料具有除去水溶液中染料和金属粒子的作用. 其对水溶液中罗丹明B 和Cd2+的移除能力分别是554 和561 mg/g[43]. 更重要的是, 氮化硼材料具有很好的抗氧化性和不可燃性, 因此吸附了有机污染物的多孔氮化硼材料可以通过焙烧的方式进行再生, 实现循环利用. 如LEI 等人制备的多孔氮化硼纳米片可以吸附自身重量29 倍的油, 且吸附饱和的多孔氮化硼材料经灼烧或加热后可循环使用(图10)[62]. 类似地, LIU 等人把吸附染料后的三维氮化硼材料经过简单的热处理(空气中500 ℃ 灼烧)即可重复使用, 且在15 次循环使用时仍能保持第一次吸附量的88%[63].

图10 (a) 多孔氮化硼纳米片的吸油测试装置; (b) 吸油2 分钟后饱和的多孔氮化硼纳米片, 插图是20 秒的吸油过程; (c) 燃烧法净化饱和的多孔氮化硼纳米片的除油图片, 插图是燃烧后多孔氮化硼纳米片颜色的变化; (d) 多孔氮化硼纳米片第二次吸油测试, 插图是2 分钟后吸油结果[62]Fig.10 (a) Photograph of the set-up for oil absorption tests with white porous BN nanosheets. (b) Photograph of porous BN nanosheets saturated with oil after 2 min of absorption, inset showing the absorption process after 20 s. (c) Photograph of burning oil-saturated porous BN nanosheets in air for cleaning purpose, inset showing the colour change after burning. (d) Photograph of the cleaned nanosheets for second oil absorption test, inset showing the absorption result after 2 min[62]
氮化硼凝胶材料在其他领域也有重要的应用. 如MABOUDIAN 等人把Pt 纳米粒子负载在氮化硼气凝胶上, 并将其应用于燃烧式气体传感器. 丙烷在Pt 纳米粒子表面燃烧释放出的热量, 经氮化硼气凝胶传递到多晶硅微加热器. 随着温度的升高, 多晶硅微加热器的阻抗也随之增加, 从而引起电流的变化, 实现量热式气体检测[64]. 此外, 水溶性的氮化硼材料具有较好的生物相容性, 可作为药物的运输工具[5]. WENG 等人将石墨结构的氮化碳(g-C3N4)和硼酸混合物置于马弗炉中焙烧, 通过置换反应使g-C3N4中的C 被B 取代得到具有良好水溶性的多孔氮化硼.它可装载抗癌药物阿霉素后通过内吞作用进入前列腺淋巴结癌细胞, 抑制癌细胞的扩散[65].
4 结语
尽管六方氮化硼材料具有很多优良的性质, 并且有长达半个多世纪的研究历史, 但是它相对于碳同系物来说还是远远落后. 近年来, 特别是2004 年石墨烯问世以后, 单层和少数层的氮化硼纳米片受到越来越多的研究者的关注. 人们已经采用CVD 法、机械剥离法或液相插层剥离法制备出克量级的氮化硼纳米片, 进而初步探索它们的各种应用, 包括催化剂载体、气体储存、光电子器件、传感器、导热材料和药物载带等. 另外, 人们也开发了多种方法构筑三维、多孔的氮化硼纳米材料, 以提高它们的适用范围和可操作性. 总体而言, 氮化硼纳米材料领域取得了一些重要研究成果, 但是它也有一些亟待解决的问题. 例如, 由于氮化硼层与层之间存在很强的“啮合”作用(lip-lip interations), 如何简便高效地获得大批量的氮化硼纳米片并进行化学修饰还是一个挑战;在氮化硼凝胶或其他三维多孔材料方面, 如何精确控制其结构(如孔径尺寸和孔径率)仍然存在困难;氮化硼纳米片及其凝胶材料的应用范围偏窄, 拓宽其应用范围是值得重视的课题. 对于后者, 一个可能的方案就是通过掺杂改变氮化硼材料的组分, 进而调控其性质. 例如, 通过碳或其他杂原子掺杂使绝缘的氮化硼转变为半导体型的, 将极大拓展它在光电子器件方面的应用, 同时也可以方便地进行化学修饰. 我们相信, 随着研究的日益深入, 氮化硼纳米片及其凝胶材料将呈现更广阔的前景.
[1] LI L H, CHEN Y. Atomically thin boron nitride: unique properties and applications [J]. Adv Funct Mater, 2016, 26(16): 2594-2608.
[2] 孟园, 陈继捷, 梁伟雄, 等. 六方氮化硼及其纳米片在催化领域的研究进展[J]. 西南民族大学学报: 自然科学版, 2015, 41(3): 331-337.
[3] 段小明, 杨治华, 王玉金, 等. 六方氮化硼(h-BN) 基复合陶瓷研究与应用的最新进展[J]. 中国材料进展, 2015, 34(10): 770-782.
[4] JIANG X F, WENG Q, WANG X B, et al. Recent progress on fabrications and applications of boron nitride nanomaterials: a review [J]. J Mater Sci Technol, 2015, 31(6): 589-598.
[5] LU F S, WANG F, CAO L, et al. Hexagonal boron nitride nanomaterials: advances towards bioapplications [J]. Nanosci Nanotechnol Lett, 2012, 4(10): 949-961.
[6] PAKDEL A, BANDO Y, GOLBERG D. Nano boron nitride flatland [J]. Chem Soc Rev, 2014, 43(3): 934-959.
[7] LIN Y, CONNELL J W. Advances in 2D boron nitride nanostructures: nanosheets, nanoribbons, nanomeshes, and hybrids with grapheme [J]. Nanoscale, 2012, 4(22): 6908-6939.
[8] BASCHE M. U.S. Pat., 3, 152, 006, 1964.
[9] RAND M J, ROBERTS J F. Preparation and properties of thin film boron nitride [J]. J Electrochem Soc, 1968, 115(4): 423-429.
[10] PAFFETT M T, SIMONSON R J, PAPIN P, et al. Borazine adsorption and decomposition at Pt (111) and Ru (001) surfaces [J]. Surf Sci, 1990, 232(3): 286-296.
[11] GAO Y, REN W, MA T, et al. Repeated and controlled growth of monolayer, bilayer and few-layer hexagonal boron nitride on Pt foils [J]. ACS Nano, 2013, 7(6): 5199-5206.
[12] SONG L, CI L, LU H, et al. Large scale growth and characterization of atomic hexagonal boron nitride layers [J]. Nano Lett, 2010, 10(8): 3209-3215.
[13] SHI Y, HAMSEN C, JIA X, et al. Synthesis of few-layer hexagonal boron nitride thin film by chemical vapor deposition [J]. Nano Lett, 2010, 10(10): 4134-4139.
[14] KIM G, JANG A R, JEONG H Y, et al. Growth of high-crystalline, single-layer hexagonal boron nitride on recyclable platinum foil [J]. Nano Lett, 2013, 13(4): 1834-1839.
[15] NOVOSELOV K S, JIANG D, SCHEDIN F, et al. Two-dimensional atomic crystals [J]. Proc Natl Acad Sci U S A, 2005, 102(30): 10451-10453.
[16] LI L H, CHEN Y, BEHAN G, et al. Large-scale mechanical peeling of boron nitride nanosheets by low-energy ball milling [J]. J Mater Chem, 2011, 21(32): 11862-11866.
[17] LI L H, GLUSHENKOV A M, HAIT S K, et al. High-efficient production of boron nitride nanosheets via an optimized ball milling process for lubrication in oil [J]. Sci Rep, 2014, 4: 07288.
[18] LEI W, MOCHALIN V N, LIU D, et al. Boron nitride colloidal solutions, ultralight aerogels and freestanding membranes through one-step exfoliation and functionalization [J]. Nat Commun, 2015, 6: 8849.
[19] CHEN X, DOBSON J F, RASTON C L. Vortex fluidic exfoliation of graphite and boron nitride [J]. Chem Commun, 2012, 48(31): 3703-3705.
[20] COLEMAN J N, LOTYA M, O’NEILL A, et al. Two-dimensional nanosheets produced by liquid exfoliation of layered materials [J]. Science, 2011, 331(6017): 568-571.
[21] ZHI C, BANDO Y, TANG C, et al. Large-scale fabrication of boron nitride nanosheets and their utilization in polymeric composites with improved thermal and mechanical properties [J]. Adv Mater, 2009, 21(28): 2889-2893.
[22] SUN W, MENG Y, FU Q, et al. High-yield production of boron nitride nanosheet and its uses as a catalyst support for hydrogenation of nitroaromatics [J]. ACS Appl Mater Interfaces, 2016, 8(15): 9881-9888.
[23] HAN W Q, WU L, ZHU Y, et al. Structure of chemically derived mono-and few-atomic-layer boron nitride sheets [J]. Appl Phys Lett, 2008, 93(22): 223103.
[24] LU F, WANG F, GAO W, et al. Aqueous soluble boron nitride nanosheets via anionic compound-assisted exfoliation [J]. Mater Express, 2013, 3(2): 144-150.
[25] HU X, LIU J, HE Q, et al. Aqueous compatible boron nitride nanosheets for high-performance hydrogels [J]. Nanoscale, 2016, 8(7): 4260-4266.
[26] VINU A, TERRONES M, GOLBERG D, et al. Synthesis of mesoporous BN and BCN exhibiting large surface areas via templating methods [J]. Chem Mater, 2005, 17(24): 5887-5890.
[27] HAN W Q, BRUTCHEY R, TILLEY T D, et al. Activated boron nitride derived from activated carbon [J]. Nano Lett, 2004, 4(1): 173-176.
[28] SURYAVANSHI U, BALASUBRAMANIAN V V, LAKHI K S, et al. Mesoporous BN and BCN nanocages with high surface area and spherical morphology [J]. Phys Chem Chem Phys, 2014, 16(43): 23554-23557.
[29] ROUSSEAS M, GOLDSTEIN A P, MICKELSON W, et al. Synthesis of highly crystalline sp2-bonded boron nitride aerogels [J]. ACS Nano, 2013, 7(10): 8540-8546.
[30] SONG Y, LI B, YANG S, et al. Ultralight boron nitride aerogels via template-assisted chemical vapor deposition [J]. Sci Rep, 2015, 5: 10337.
[31] PHAM T, GOLDSTEIN A P, LEWICKI J P, et al. Nanoscale structure and superhydrophobicity of sp2-bonded boron nitride aerogels [J]. Nanoscale, 2015, 7(23): 10449-10458.
[32] WANG Z, CAO X, PING J, et al. Electrochemical doping of three-dimensional graphene networks used as efficient electrocatalysts for oxygen reduction reaction [J]. Nanoscale, 2015, 7(21): 9394-9398.
[33] YIN J, LI X, ZHOU J, et al. Ultralight three-dimensional boron nitride foam with ultralow permittivity and superelasticity [J]. Nano Lett, 2013, 13(7): 3232-3236.
[34] ASHTON T S, MOORE A L. Three-dimensional foam-like hexagonal boron nitride nanomaterials via atmospheric pressure chemical vapor deposition [J]. J Mater Sci, 2015, 50(18): 6220-6226.
[35] PRATIK K C, NAMMARI A, ASHTON T S, et al. Saturated pool boiling heat transfer from vertically oriented silicon surfaces modified with foam-like hexagonal boron nitride nanomaterials [J]. Int J Heat Mass Tran, 2016, 95: 964-971.
[36] LOEBLEIN M, TAY R Y, TSANG S H, et al. Configurable three-dimensional boron nitride-carbon architecture and its tunable electronic behavior with stable thermal performances [J]. Small, 2014, 10(15): 2992-2999.
[37] XUE Y, YU D, DAI L, et al. Three-dimensional B, N-doped graphene foam as a metal-free catalyst for oxygen reduction reaction [J]. Phys Chem Chem Phys, 2013, 15(29): 12220-12226.
[38] ALAUZUN J G, UNGUREANU S, BRUN N, et al. Novel monolith-type boron nitride hierarchical foams obtained through integrative chemistry [J]. J Mater Chem, 2011, 21(36): 14025-14030.
[39] DAI J, WU X, YANG J, et al. Unusual metallic microporous boron nitride networks [J]. J Phys Chem Lett, 2013, 4(20): 3484-3488.
[40] DAI J, WU X, YANG J, et al. Porous boron nitride with tunable pore size [J]. J Phys Chem Lett, 2014, 5(2): 393-398.
[41] WENG Q, WANG X, ZHI C, et al. Boron nitride porous microbelts for hydrogen storage [J]. ACS Nano, 2013, 7(2): 1558-1565.
[42] WENG Q, WANG X, BANDO Y, et al. One-step template-free synthesis of highly porous boron nitride microsponges for hydrogen storage [J]. Adv Energy Mater, 2014, 4(7): 1301525.
[43] XUE Y, DAI P, JIANG X, et al. Template-free synthesis of boron nitride foam-like porous monoliths and their high-end applications in water purification [J]. J Mater Chem A, 2016, 4(4): 1469-1478.
[44] XIAO F, NAFICY S, CASILLAS G, et al. Edge-hydroxylated boron nitride nanosheets as an effective additive to improve the thermal response of hydrogels [J]. Adv Mater, 2015, 27(44): 7196-7203.
[45] JUNG S M, JUNG H Y, DRESSELHAUS M S, et al. A facile route for 3D aerogels from nanostructured 1D and 2D materials [J]. Sci Rep, 2012, 2: 849.
[46] ZENG X, YE L, YU S, et al. Facile preparation of superelastic and ultralow dielectric boron nitride nanosheet aerogels via freeze-casting process [J]. Chem Mater, 2015, 27(17): 5849-5855.
[47] ZENG X, YE L, SUN R, et al. Observation of viscoelasticity in boron nitride nanosheet aerogel [J]. Phys Chem Chem Phys, 2015, 17(26): 16709-16714.
[48] LASKOWSKI R, BLAHA P, SCHWARZ K. Bonding of hexagonal BN to transition metal surfaces: an ab initio density-functional theory study [J]. Phys Rev B, 2008, 78(4): 045409.
[49] GAO M, LYALIN A, TAKETSUGU T. Oxygen activation and dissociation on h-BN supported Au atoms [J]. Int J Quantum Chem, 2013, 113(4): 443-452.
[50] UOSAKI K, ELUMALAI G, NOGUCHI H, et al. Boron nitride nanosheet on gold as an electrocatalyst for oxygen reduction reaction: theoretical suggestion and experimental proof [J]. J Am Chem Soc, 2014, 136(18): 6542-6545.
[51] ZHENG M T, LIU Y L, GU Y L, et al. Synthesis and characterization of boron nitride sponges as a novel support for metal nanoparticles [J]. Sci China Chem, 2008, 51(3): 205-210.
[52] PERDIGON-MELON J A, AUROUX A, GUIMON C, et al. Micrometric BN powders used as catalyst support: influence of the precursor on the properties of the BN ceramic [J]. J Solid State Chem, 2004, 177(2): 609-615.
[53] ZHAO H, SONG J, SONG X, et al. Ag/white graphene foam for catalytic oxidation of methanol with high efficiency and stability [J]. J Mater Chem A, 2015, 3(12): 6679-6684.
[54] WENG Q, IDE Y, WANG X, et al. Design of BN porous sheets with richly exposed (002) plane edges and their application as TiO2visible light sensitizer [J]. Nano Energy, 2015, 16: 19-27.
[55] PATIL I M, LOKANATHAN M, KAKADE B. Three dimensional nanocomposite of reduced graphene oxide and hexagonal boron nitride as an efficient metal-free catalyst for oxygen electroreduction [J]. J Mater Chem A, 2016, 4(12): 4506-4515.
[56] LVOVA N A, ANANINA O Y. Theoretical study of the adsorption properties of porous boron nitride nanosheets [J]. Comp Mater Sci, 2016, 115: 11-17.
[57] ZHANG H, TONG C J, ZHANG Y, et al. Porous BN for hydrogen generation and storage [J]. J Mater Chem A, 2015, 3(18): 9632-9637.
[58] JHI S H, KWON Y K. Hydrogen adsorption on boron nitride nanotubes: a path to room-temperature hydrogen storage [J]. Phys Rev B, 2004, 69(24): 245407.
[59] MUTHU R N, RAJASHABALA S, KANNAN R. Synthesis, characterization of hexagonal boron nitride nanoparticles decorated halloysite nanoclay composite and its application as hydrogen storage medium [J]. Renew Energ, 2016, 90: 554-564.
[60] MUTHU R N, RAJASHABALA S, KANNAN R. Hexagonal boron nitride (h-BN) nanoparticles decorated multi-walled carbon nanotubes (MWCNT) for hydrogen storage [J]. Renew Energ, 2016, 85: 387-394.
[61] ZHAO H, SONG X, ZENG H. 3D white graphene foam scavengers: vesicant-assisted foaming boosts the gram-level yield and forms hierarchical pores for superstrong pollutant removal applications [J]. NPG Asia Mater, 2015, 7(3): e168.
[62] LEI W, PORTEHAULT D, LIU D, et al. Porous boron nitride nanosheets for effective water cleaning [J]. Nat Commun, 2013, 4: 1777.
[63] LIU D, LEI W, QIN S, et al. Template-free synthesis of functional 3D BN architecture for removal of dyes from water [J]. Sci Rep, 2014, 4: 4453.
[64] HARLEY-TROCHIMCZYK A, PHAM T, CHANG J, et al. Platinum nanoparticle loading of boron nitride aerogel and its use as a novel material for low-power catalytic gas sensing [J]. Adv Funct Mater, 2016, 26(3): 433-439.
[65] WENG Q, WANG B, WANG X, et al. Highly water-soluble, porous, and biocompatible boron nitrides for anticancer drug delivery [J]. ACS Nano, 2014, 8(6): 6123-6130.
[责任编辑:吴文鹏]
Research progress of boron nitride nanosheets and their gels
FU Qinrui, MENG Yuan, WANG Hailong, FANG Zilin, HU Quanqin, DUAN Chenghao, LU Fushen*
(DepartmentofChemistry,CollegeofScience,ShantouUniversity,Shantou515063,Guangdong,China)
Boron nitride sheets (BNNSs) possess high mechanical strength, ultimate chemical inertness and high thermal stability. BNNSs-based gels have large specific surface areas and porosities in addition to the distinct properties inherited from BNNSs. Therefore, BNNSs and their gels are promising materials for many technological applications such as catalysis, hydrogen storage, pollutant removal and gas adsorption. Here, we review the recent progress in the preparation and applications of boron nitride sheets and BNNSs-based gels.
boron nitride nanosheets; gels; catalysis; hydrogen storage; pollutant removal
1008-1011(2016)04-0403-11
2016-04-17.
国家自然科学基金项目(51272152)和广东省自然科学基金(S2013010014171).
付钦瑞(1990-),男,硕士生,研究方向为纳米功能材料.*通讯联系人,E-mail:fslu@stu.edu.cn.
TQ050.4
A
