细胞凋亡显像剂18F-ML-10前体合成及放射性标记
2016-08-15徐志宏张晓军李云刚张锦明
桂 媛,徐志宏, 张晓军,李云刚,刘 健,张锦明,*
1.华益科技有限公司,江苏 常熟 215522;2.中国人民解放军总医院 核医学科,北京 100853
细胞凋亡显像剂18F-ML-10前体合成及放射性标记
桂媛1,徐志宏1, 张晓军2,李云刚2,刘健2,张锦明2,*
1.华益科技有限公司,江苏 常熟215522;2.中国人民解放军总医院 核医学科,北京100853
摘要:18F-2-(5-氟-戊基)-2-甲基丙二酸(18F-ML-10)是一个有潜力的细胞凋亡显像剂。以5-溴-1-戊醇为原料,合成了前体:5-甲基磺酰基戊基-2-甲基丙二酸二乙酯,采用国产MF-2V-IT-1模块,经亲核取代及碱水解,合成了18F-ML-10;粗产品经HPLC纯化及固相萃取,得到18F-ML-10注射液。18F-ML-10的合成效率为(25.3±4.7)%(n=16, 不校正),产品的放射化学纯度大于99%,比活度为740 PBq/mol,K2.2.2含量低于10 mg/L,有机溶剂乙腈残留量为(0.015±0.01)%(质量分数),无菌、无热原符合要求,产品满足临床研究需求。
关键词:18F;放射性合成;放射药物;细胞凋亡;PET
肿瘤细胞凋亡显像是早期评价肿瘤放化疗疗效的方法之一, 影像学评价细胞凋亡的方法很多, 但特异性方法较少。第一个特异性肿瘤细胞凋亡显像剂是99Tcm标记的Annexin V,临床研究表明:肿瘤摄取99Tcm-Annexin V与其凋亡正相关[1-2]。18F-ML-10(2-(5-fluoro-pentyl)-2-methyl malonic acid)是近年来第一个应用于临床研究的凋亡显像的正电子药物, 用于脑胶质瘤放疗后疗效早期评价, 临床初步验证:胶质瘤经放疗后24 h,肿瘤摄取18F-ML-10与治疗后8周的核磁共振成像(MR)图像改变正相关,说明18F-ML-10是一个有潜在临床价值的细胞凋亡显像剂[3-5]。Sobrio等[6]报导了以丙二酸二叔丁基酯为起始原料,合成18F-ML-10的前体:5-对甲苯磺酰基戊基-2-甲基丙二酸二叔丁基酯;该前体的保护基团为叔丁基酯,脱保护需用强酸。Dewkar等[7]报导了以2-甲基丙二酸二乙酯为起始原料,合成了另一个前体:5-甲基磺酰基戊基-2-甲基丙二酸二乙酯,该前体的保护基团为乙酯,较容易脱保护。本研究在文献[6—7]的基础上改变原料,合成较容易脱保护的前体:5-甲基磺酰基戊基-2-甲基丙二酸二乙酯,采用国产氟多功能模块合成18F-ML-10,并进行质量控制,以便将18F-ML-10应用于临床研究。
1 试剂和仪器
甲苯磺酸吡啶盐、5-溴-1-戊醇、碘化钾(KI)、 对甲苯磺酸吡啶盐、 3,4-二氢吡喃、甲基丙二酸二乙酯、 氢化钠、二甲基甲酰胺(DMF)、对甲苯磺酰氯,均为分析纯,购自阿拉丁试剂;K2.2.2、氧-18水(丰度大于97%),江苏华益科技有限公司;SEP-PAK QMA,美国Waters公司;无水乙腈,美国Aldrich公司。
Agilent 6120型质谱仪,美国安捷伦公司;Bruker 300M核磁共振仪,美国布鲁克公司;SGWX-4熔点仪,上海精密仪器厂;Sumitomo HM-20S 回旋加速器,日本住友公司;MF-2V-IT-1型氟多功能合成仪,派特(北京)科技有限公司;高效HPLC分析仪,美国Waters公司,配有515泵、2487紫外分析仪、BioScan流动放射性检测器;GC7890型气相色谱,上海天美公司。上海三爱思精密试纸(pH=5.5~9.0)。
2 实验方法
18F-ML-10前体及ML-10标准品合成路线示于图1。
2.15-溴-1-戊-1-二氢吡喃醚(1)的合成
氮气保护下,在500 mL三颈瓶中加入4 g对甲苯磺酸吡啶盐(PPTS,16 mmol)、13.36 g 5-溴-1-戊醇(80 mmol)和200 mL二氯甲烷,滴加10.08 g 3,4-二氢吡喃(120 mmol)的200 mL二氯甲烷的溶液。滴完后,室温下反应过夜。停止反应,用水洗涤,有机相用无水硫酸镁干燥,过滤得粗品m=25 g,粗品过300~400目的硅胶柱分离(V(乙酸乙酯)∶V(正己烷)从5∶1到2∶1梯度洗脱)。
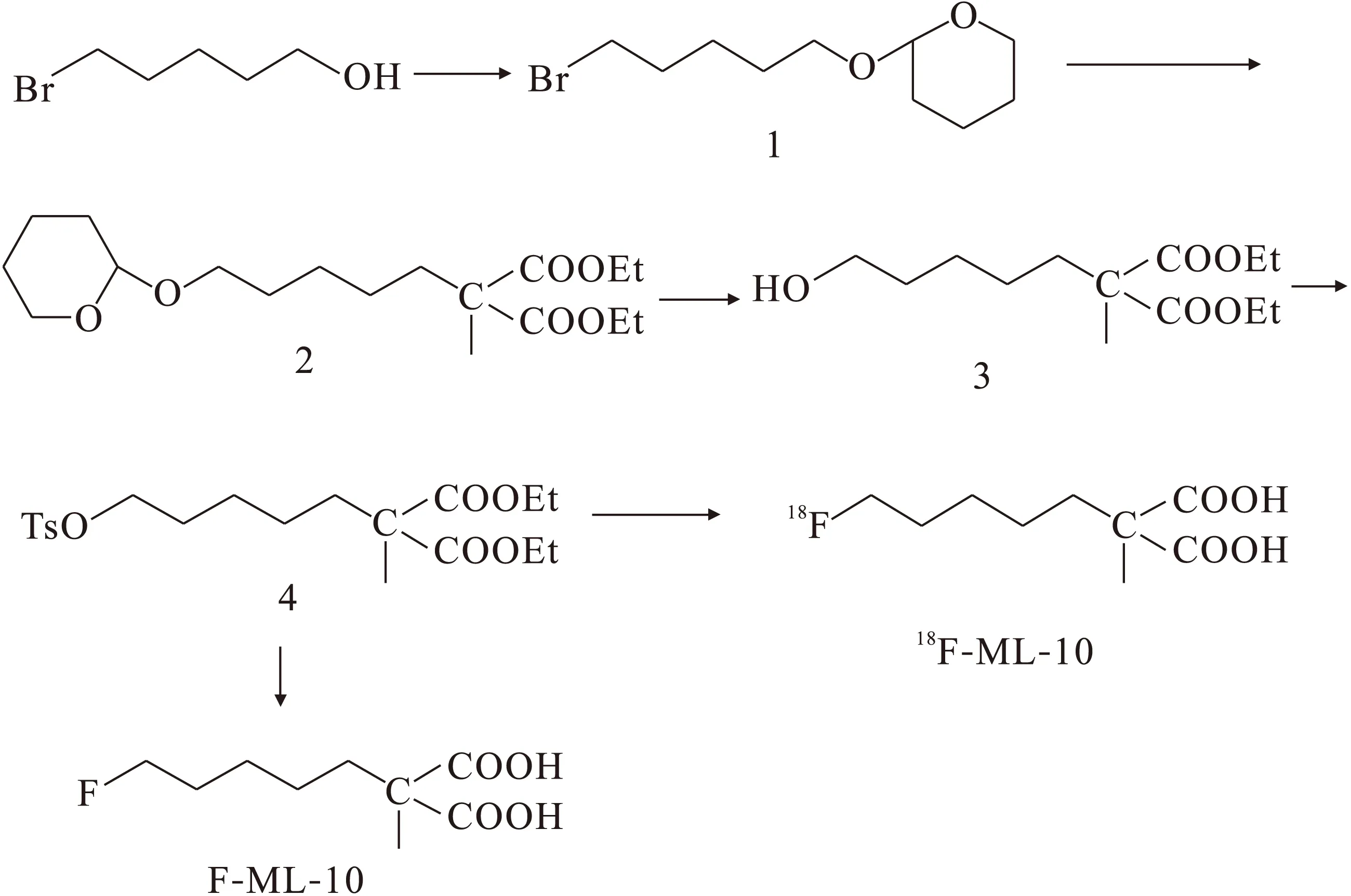
图1 18F-ML-10前体及ML-10标准品合成路线Fig.1 Reaction scheme for precursor of 18F-ML-10 and ML-10 reference standards
2.25-二氢吡喃醚-戊基-2-甲基丙二酸二乙酯(2)的合成
装置氮气保护,加入7 g甲基丙二酸二乙酯(40 mmol),50 mL无水DMF,冷至0 ℃,分批加入1.5 g 氢化钠(质量分数80%,48 mmol),加完后在0 ℃反应0.5 h; 0 ℃下,加入0.6 g KI(3.6 mmol),后滴加10 g 物质1(40 mmol)的50 mL无水DMF的溶液,加完后升至50 ℃反应过夜。加入饱和氯化铵溶液,调节pH值至中性,加入乙酸乙酯萃取,有机相用饱和食盐水洗涤,干燥,产品2可直接进行下一步反应。
2.35-戊醇-2-甲基丙二酸二乙酯(3)的合成
500 mL单颈瓶中依次加入13.7 g 物质2、1.6 g PPTS(6.4 mmol)、180 mL乙醇,在55 ℃下回流反应2 h。停止反应,旋干溶剂,柱分离可得产品(柱分离洗脱剂V(乙酸乙酯)∶V(正己烷)=2∶1)。
2.45-甲基磺酰基戊基-2-甲基丙二酸二乙酯(4)的合成
装置氮气保护,依次加入10 g 物质3、5.76 g 三乙胺(57 mmol)和100 mL二氯甲烷,冷至0 ℃,滴加10.86 g对甲苯磺酰氯(57 mmol)溶于100 mL二氯甲烷的溶液,约1 h滴完,滴完后室温下反应过夜。停止反应,反应液用饱和食盐水洗涤后,有机相用无水硫酸镁干燥,过滤,旋干得粗品,粗品柱分离可得产品(柱分离洗脱剂V(乙酸乙酯)∶V(正己烷)=4∶1),产物为无色透明液体,纯度大于98%。
2.52-(5-氟-戊基)-2-甲基丙二酸(标准品)的合成
装置氮气保护,250 mL三颈瓶中依次加入5 g物质4、100 mL乙腈和3.9 g无水四丁基氟化铵(TBAF,15 mmol),回流反应2 h。停止反应,减压旋去溶剂,加入约100 mL二氯甲烷然后用2×30 mL水洗涤。有机相干燥,过滤,旋干得粗品。粗品过柱分离可得纯品5-氟-2-甲基丙二酸二乙酯(ML-6)(柱分离洗脱剂V(乙酸乙酯)∶V(正己烷)=10∶1)。
100 mL反应瓶中依次加入0.5 g ML-6(1.9 mmol)、0.76 g氢氧化钠(19 mmol)和20 mL乙醇回流反应约2 h,停止反应,用盐酸调节pH值至强酸性,过滤,滤饼用少量乙醇洗涤,滤液旋干,残渣加约10 mL乙酸乙酯,过滤掉不溶性的无机盐,滤液再次旋干得粗品,粗品用正己烷和乙酸乙酯重结晶可得产品。
2.618F-ML-10的自动化合成
由Sumitomo HM-20S 回旋加速器20 MeV质子轰击丰度为98%的氧-18水,经18O(p,n)18F反应生成18F离子,将18F离子传到QMA柱,以下由MF-2V-IT-1型氟多功能合成器自动化合成。依序将安装在合成器的液体加入,加入1号瓶液体(1 mL的乙腈水溶液,含15 mg K2.2.2和 3 mg K2CO3),将18F(40~60 GBq)从QMA柱上淋洗入反应管,加热反应管并通入110 mL/min的氮气,将反应管中溶液蒸发至干;加2号瓶内液体(2 mL乙腈), 重复以上步骤,将反应管中溶液蒸发至干;加入3号瓶液体(1 mL乙腈溶解10 mg的5-甲基磺酰基戊基-2-甲基丙二酸二乙酯),83 ℃加热反应管5 min ;加入4号瓶液体(0.6 mL 2 mol/L NaOH)115 ℃加热反应管水解10 min,加入5号瓶液体(4 mL 1 mol/L HCl)中和, 最后加入6号瓶液体(2 mL含1%三氟乙酸(TFA)的20%(体积分数,下同)乙腈)。最终约4 mL的反应液自动移到半制备HPLC上分离,半制备分离柱为:Grace Attach C-18 柱(250 mm×10 mm),流动相为含1%TFA的20%乙腈,流速为12 mL/min。收集9~10 min的放射性峰,经合成器上固相萃取系统,将含20%乙腈的溶液转化成含8%乙醇的注射液。
2.718F-ML-10的质量控制
18F-ML-10应为无色透明的溶液,用精密pH试纸测其pH应在6.0~7.0。
取10 μL的18F-ML-10注射液,于美国Waters公司的高效HPLC分析仪上分析,HPLC分析柱为反相C-18柱(Nova ParK C-18,150 mm×3.9 mm),流动相为含1%TFA的20%乙腈,流速为1 mL/min。氟离子的tR=1.9 min,18F-ML-10的tR=5.8 min,产品的放化纯应大于95%。产品与ML-10标准品共注射进样(1 g/L),紫外波长为254 nm,18F-ML-10放射性峰应与ML-10的紫外吸收峰一致。
取衰变后的18F-ML-10注射液与等体积的标准K2.2.2(100 mg/L)溶液混合,取3 μL点样于经氯铂酸和碘化钾染色的TLC硅胶板上得到A点,同时另取3 μL标准K2.2.2(50 mg/L)、标准K2.2.2(10 mg/L)溶液点样硅胶板上得到B点、C点, 取3 μL衰变后的18F-ML-10注射液点样于硅胶板上得到D点。硅胶板上的A点和B点的深蓝色斑块应一致,同时D点的蓝色斑块应小于B点[8]。
取已完全衰变的5 μL18F-ML-10注射液,按文献[8]方法测残留乙腈的含量,乙腈含量应不高于0.04%(质量分数)。
按中国药典 2015 年版二部附录Ⅺ E和H检查注射液的内毒素和无菌性,应符合要求。
3 结果与讨论
3.1ML-10标准品和前体合成与表征
本研究以5-溴-1-戊醇为原料,最终合成了ML-10标准品和前体。
其中化合物1:纯品m=13.7 g,合成产率68%; LC-MS[M+1]+=251(100%),253(97%);1H NMR(300 MHz,CDCl3):δ=4.55~4.60(m,1H),3.81~3.92(m,1H),3.69~3.80(dt,1H,J=6.4 Hz、9.7 Hz),3.46~3.55(m,1H),3.35~3.45(dt,1H,J=6.4 Hz、9.7 Hz),3.39~3.45(t,2H,J=6.8 Hz),1.86~1.97(m,2H),1.46~1.85(m,10H)。化合物2:粗产品m=2.3 g,产率72.8%, LC-MS:[M+1]+=345,由于直接用于下步反应,没有做核磁鉴定。化合物3:m=6.4 g,化合物2和3两步总产率61.5%; LC-MS:[M+1]+=261;1H NMR(300 MHz,CDCl3):δ=4.12~4.23(q,4H,J=7.3 Hz),3.56~3.69(t,2H,J=6.1 Hz),1.76~1.92(m,2H),1.46~1.65(m,3H),1.32~1.46(m,2H),1.40(s,3H),1.17~1.31(m,2H),1.21~1.27(t,6H,J=7.3 Hz)。化合物4:m=12.4 g,合成收率78.9%;LC-MS:[M+1]+=339;1H NMR(300 MHz,CDCl3):δ=4.12~4.26(m,6H),3.00(s,3H),1.81~1.90(m,2H),1.69~1.80(m,2H),1.36~1.49(m,2H),1.40(s,3H),1.20~1.35(m,2H),1.20~1.28(t,6H)。化合物5:m=250 mg,合成收率47%;LC-MS:[M+1]+=415;1H NMR(300 MHz,CDCl3):δ=7.74~7.82(d,2H,J=8.3 Hz),7.29~7.39(d,2H,J=8.3 Hz),4.11~4.21(q,4H,J=7.1 Hz),3.96~4.04(t,2H,J=6.3 Hz),2.45(s,3H),1.74~1.84(m,2H),1.61~1.70(m,2H),1.36(s,3H),1.19~1.27(t,6H,J=7.1 Hz),1.12~1.38(m,4H)。化合物6:LC-MS:[M+1]+=207;1H NMR(300 MHz,CDCl3):δ=4.31~4.56(dt,2H,J=6.0、47.4 Hz),1.86~1.98(m,2H),1.61~1.82(m,2H),1.50(s,3H),1.29~1.55(m,4H)。
Sobrio等[6]采用丙二酸二叔丁基酯与5-溴戊苄醚反应,再经甲基化后,在钯碳催化下还原苄醚生成5-羟基-戊基-2-甲基丙二酸二叔丁基酯,合成步骤多,所用催化剂价格贵[6]。Dewkar等[7]采用2-甲基丙二酸二乙酯与1,5-二溴戊烷直接反应,生成5-溴-戊基-2-甲基丙二酸二乙酯,经甲基磺酸银将其转化成5-羟基-戊基-2-甲基丙二酸二乙酯,同样使用了贵金属试剂。本研究综合了二种方面的特点,用3,4-二氢吡喃替代苄基保护,用PPTS可以较容易脱保护,降低了合成成本。本研究从原料到前体共4步,合成总收率为33.4%,高于文献[6]的28%。
3.218F-ML-10的自动化合成结果
采用MF-2V-IT-1型多功能模块,单个反应管即能全自动合成18F-ML-10,并完成半制备HPLC的分离和HPLC流动相的溶剂转换得到注射液。 图2为半制备HPLC的放射性色谱图,仅见二个峰,一个是未反应的氟离子峰,另一个即为产品18F-ML-10的峰,说明本反应较单一,没有其它副反应。从氟离子到产品18F-ML-10花费时间40 min, 合成效率为(25.3±4.7)%(n=16,未衰减校正),衰减校正后的合成效率为32.6%,该效率低于文献[6]的39.8%。但文献[6]为小剂量合成,起始18F量为35~70 MBq,低于本研究18F量三个数量级,本研究的产品活度为10~15 GBq,满足临床使用要求。
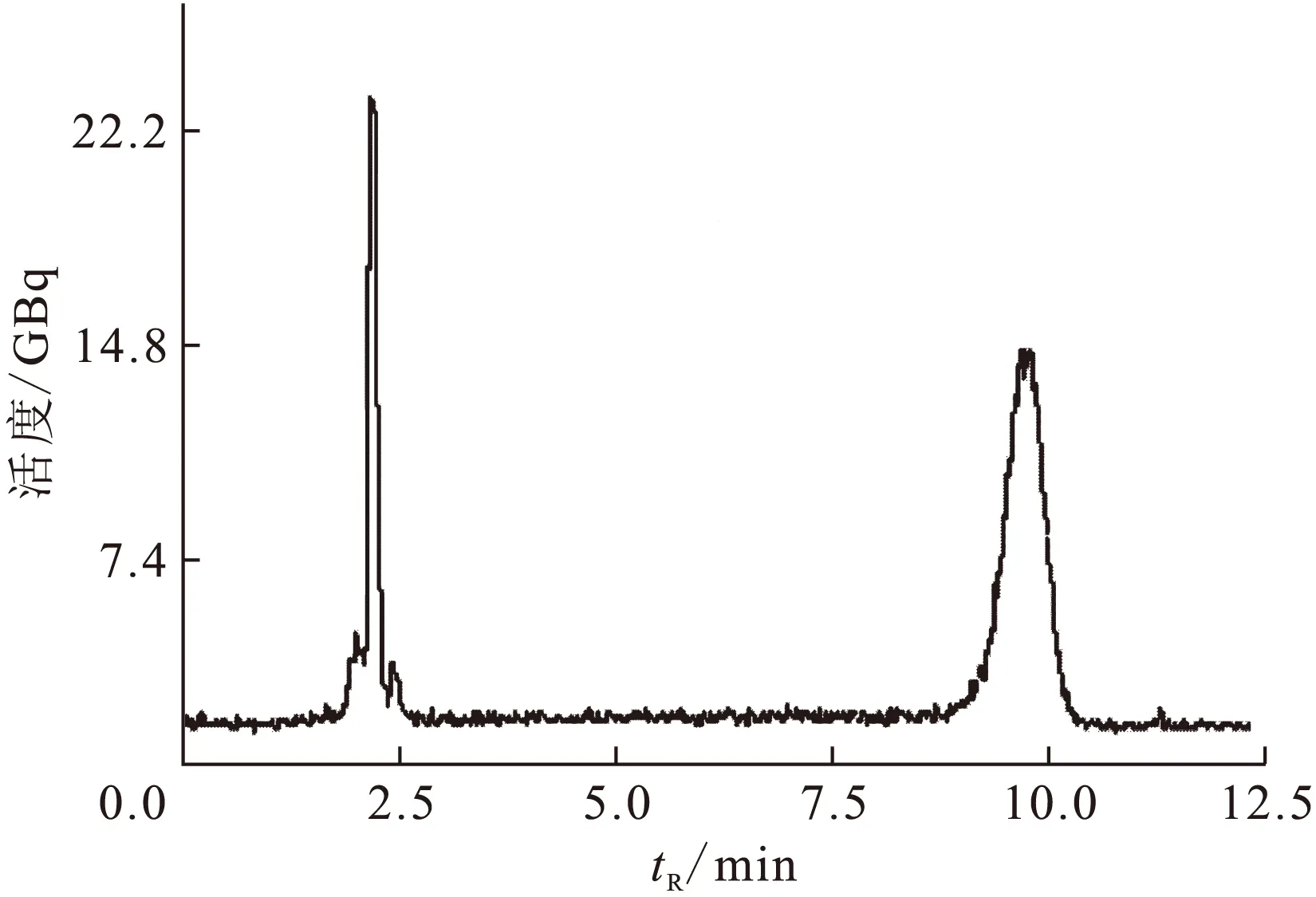
图2 半制备HPLC的18F-ML-10放射性色谱图Fig.2 Semipreparative radioactive HPLC traces for 18F-ML-10
3.318F-ML-10的质量控制结果
经溶剂转换后的含w=8%乙醇的18F-ML-10注射液为无色透明的液体,溶液pH=6.5。
产品的活度为10~15 GBq,活度浓度为1.0~1.5 TBq/L。
完全衰变后的18F-ML-10注射液点样于硅胶板上得到D点没有斑点形成,基本无色、无色环,低于标准K2.2.2( 10 mg/L)溶液的色斑C点。符合我国关于18F-FDG注射液中K2.2.2含量低于50 mg/L的要求[9]。
经分析型HPLC分析表明,在HPLC柱上仅一个放射性主峰,该峰的保留时间与ML-10标准品的紫外吸收峰保留时间一致(图3),18F-ML-10的放射化学纯度大于99%, 比活度为740 PBq/mol。
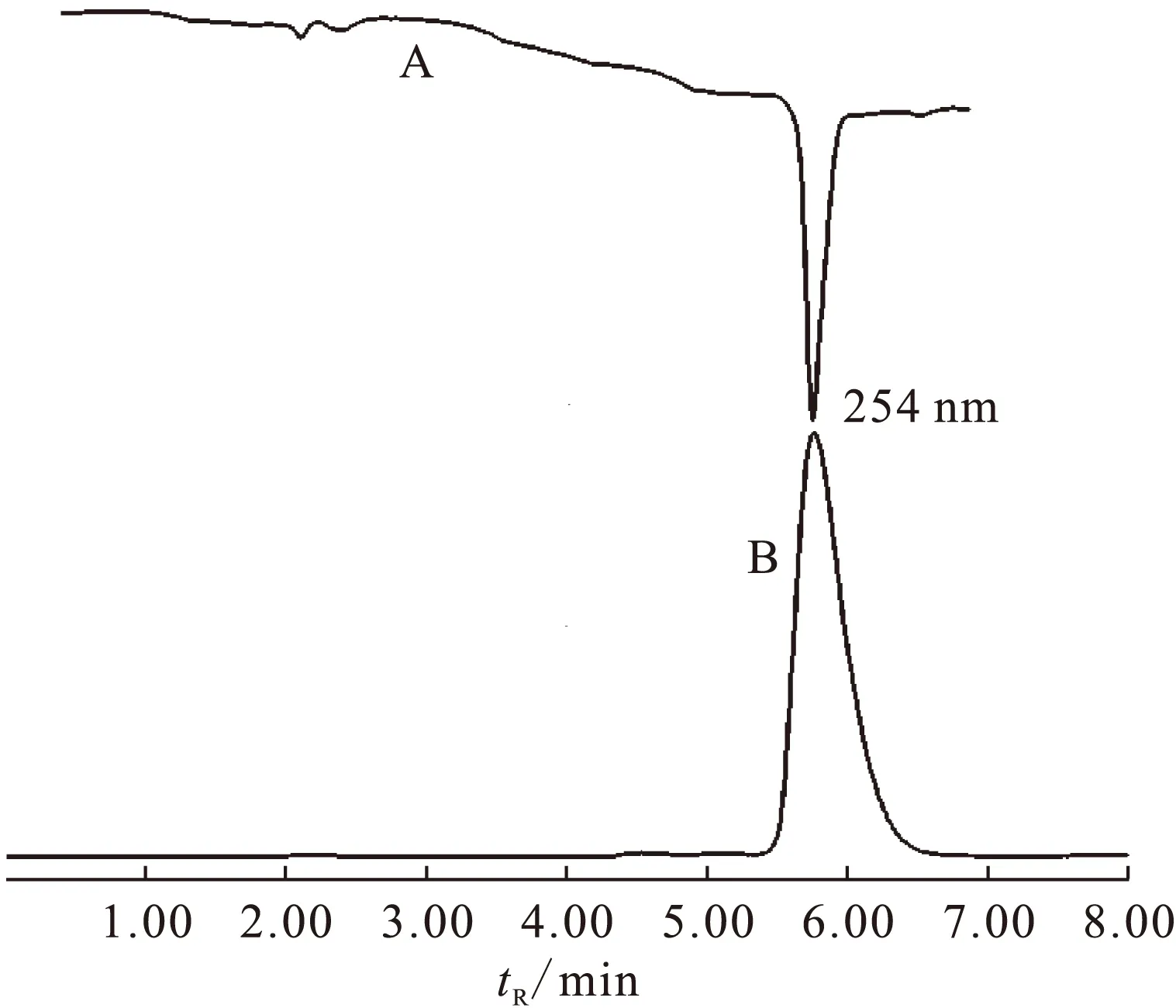
图3 18F-ML-10的分析型HPLC放射性(B)和ML-10标准品的紫外色谱图(A)Fig.3 18F-ML-10 radioactivity(B) and ML-10 UV traces(A)
经GC分析表明,有机溶剂乙腈的残留为(0.015±0.01)%(质量分数)。
注射液的内毒素和无菌性,符合要求。
4 结 论
本研究以5-溴-1-戊醇为原料,合成了前体5-甲基磺酰基戊基-2-甲基丙二酸二乙酯和标准品F-ML-10,用3,4-二氢吡喃替代苄基保护,用PPTS可以较容易脱保护,降低了合成成本。同时采用国产氟多功能模块,自动合成了18F-ML-10,合成效率为(25.3±4.7)%,18F-ML-10放射化学纯度大于99%,K2.2.2含量低于10 mg/L,
乙腈含量低于0.04%(质量分数),产品满足临床研究的需求。
参考文献:
[1]Kuge Y, Zhao S, Takei T, et al. Molecular imaging of apoptosis with radio-labeled Annexin A5 focused on the evaluation of tumor response to chemotherapy[J]. Anticancer Agents Med Chem, 2009, 9(9): 1003-1011.
[2]Hoebers F J, Kartachova M, de Bois J, et al.99TcmHynic-rh-Annexin V scintigraphy forinvivoimaging of apoptosis in patients with head and neck cancer treated with chemoradiotherapy[J]. Eur J Nucl Med Mol Imaging, 2008, 35(3): 509-518.
[3]Hoglund J, Shirvan A, Antoni G, et al.18F-ML-10, a PET tracer for apoptosis: first human study[J]. J Nucl Med, 2011, 52: 720-725.
[4]Allen A M, Ben-Ami M, Reshef A, et al. Assessment of response of brain metastases to radiotherapy by PET imaging of apoptosis with18F-ML-10[J]. Eur J Nucl Med Mol Imaging, 2012, 39: 1400-1408.
[5]Oborski M J, Laymon C M, Lieberman F S, et al. First use of18F-labeled ML-10 PET to assess apoptosis change in a newly diagnosed glioblastoma multiforme patient before and early after therapy[J]. Brain and Behavior, 2014, 4(2): 312-315.
[6]Sobrio F, Médoc M, Martial L, et al. Automated radiosynthesis of [18F]ML-10, a PET radiotracer dedicated to apoptosis imaging, on a TRACER Lab FX-FN module[J]. Mol Imaging Biol, 2013, 15: 12-18.
[7]Dewkar G K, Sundaresan G, Lamichhane N, et al. Microfluidic radiosynthesis and biodistribution of [18F] 2-(5-fluoro-pentyl)-2-methyl malonic acid[J]. J Label Compd Radiopharm, 2013, 56: 289-294.
[8]李云钢,张晓军,刘健,等.气相色谱法测量正电子放射性药物中有机溶剂残留及原因分析[J].同位素,2013,26(3):152-157.
[9]国家药典委员会.中华人民共和国药典2015年版[M].北京:中国医药科技出版社,2015:1559-1660.
收稿日期:2015-04-21;
修订日期:2015-11-19
基金项目:国家自然科学基金资助项目(81371593)
作者简介:桂媛(1981—),女,江西九江永修人,博士,高级工程师,从事有机合成工作 *通信联系人:张锦明(1965—),男,江苏南通人,博士,研究员,从事核医学工作,E-mail: zhangjm301@163.com
中图分类号:R817
文献标志码:A
文章编号:0253-9950(2016)03-0188-05
doi:10.7538/hhx.2016.38.03.0188
Synthesis Precursor of Apoptosis Imaging Agent18F-ML-10 and Its Radiolabing With18F
GUI Yuan1, XU Zhi-hong1, ZHANG Xiao-jun2, LI Yun-gang2, LIU Jian2, ZHANG Jin-ming2,*
1.Huayi Science & Technology Co. Ltd., Changshu 215522, China;2.Department Nuclear Medicine, The PLA General Hospital, Beijing 100853, China
Abstract:18F-2-(5-fluoro-pentyl)-2-methyl malonic acid(18F-ML-10) is one of the competitive candidate for apoptosis imaging with PET. ML-10 as reference and its OTs derivative (diethyl 2-methyl-2-(5-(tosyloxy)pentyl) malonate) as precursor for labeling with fluorine-18 were prepared.18F-ML-10 was synthesized via nucleophilic substitution and base hydrolysis. The18F-ML-10 injection was got by semi-HPLC and solid-extraction-preparation via home MF-2V-IT-1 module. The synthesis yield of18F-ML-10 is (25.3±4.7)%(n=16, no corrected decay), and the specific activity is 740 PBq/mol. The radiochemical purity is over 99%. The residuary acetonitrile in the injection is (0.015±0.01)%(w). The K2.2.2 mass concentration in the injection is low than 10 mg/L. The injection is free of bacteria and pyrogen. It can be used for clinical research.
Key words:18F; radiosynthesis; radiopharmaceuticals; apoptosis; PET
