CuFC吸附-微滤工艺处理含137Cs废水
2016-08-15肖湘竹
王 露,赵 军,*,胥 要,肖湘竹,邓 玥,杨 杨
1.中国工程物理研究院 核物理与化学研究所,四川 绵阳 621900;2.天津大学 环境科学与工程学院,天津 300072
CuFC吸附-微滤工艺处理含137Cs废水
王露1,赵军1,*,胥要2,肖湘竹1,邓玥1,杨杨1
1.中国工程物理研究院 核物理与化学研究所,四川 绵阳621900;2.天津大学 环境科学与工程学院,天津300072
摘要:采用单级亚铁氰化铜(CuFC)吸附-微滤工艺去除实验模拟废水中的137Cs,研究废水中137Cs初始活度浓度(C0)、吸附时间、pH值、竞争离子以及CuFC投加量对去污因子的影响。分别用去离子水、地表水和海水配制模拟废水,当模拟废水中137Cs的初始活度浓度分别为4.24×105、2.84×105、2.84×105 Bq/L,吸附时间为90 min,pH值为7,CuFC投加量为80 mg/L,不投加竞争离子时,本工艺的去污因子分别达到2.06×104、1.62×104和9.36×101,说明CuFC吸附-微滤工艺是一种高效的含137Cs废水处理工艺,且具有可观的应用前景。
关键词:CuFC;137Cs;吸附;微滤
随着我国原子能科学技术的发展,产生的含137Cs废水量也越来越大。含137Cs废水的水质体系一般为去离子水(例如反应堆出水)、地表水(例如受到137Cs污染的地表水)和海水(例如因137Cs泄露受到污染的海水)。137Cs半衰期较长,可长期在环境中存在,其放射出的β粒子及伴随的γ射线可对人体造成较大伤害,并对自然环境产生严重威胁,将含137Cs的废水处理后达标排放,对人类和环境均具有积极的意义。

膜分离法由于具有固液分离效率高和适应性强等特点,可将吸附后的金属亚铁氰化物从液相中分离出来。因此可将金属亚铁氰化物吸附与膜分离技术相结合用于含137Cs废水的处理。Rao等[5]用亚铁氰化铜(CuFC)吸附结合超滤工艺去除地表水中的137Cs,当水中137Cs的初始活度浓度为1.258×105Bq/L时,去污因子为1.99×102;文献[6]用亚铁氰化钾锌吸附+微滤工艺去除模拟废水中的137Cs,当废水中137Cs初始活度浓度为5.10×104Bq/L、亚铁氰化钾锌投加量为83 mg/L时,单级无机吸附微滤段的去污因子为5.87×101。
韩非等[7]采用单级亚铁氰化铜(CuFC)吸附-微滤工艺去除实验废水(用天津自来水配制,水质参数列于表1)中的133Cs,当CuFC投加量为20~40 mg/L时,平均去污因子达2.87×102~4.63×102。由于在韩非等的实验中,废水的初始Cs+质量浓度高达100 μg/L,达到了实际含137Cs的低放射性废水中Cs+的质量浓度(<10-1μg/L)的1 000倍以上,且废水水质不同(实际含137Cs的低放射性废水普遍为去离子水体系),为更好地考察CuFC吸附-微滤工艺对含137Cs的低放射性废水的处理效果,分别用去离子水、地表水和海水,加入放射性137Cs配制实验模拟废水,并采用单级吸附-微滤工艺去除模拟废水中的137Cs,研究废水中137Cs初始活度浓度、CuFC投加量、吸附时间、废水pH值、竞争离子投加量对去污因子的影响,以期为采用CuFC吸附-微滤组合工艺处理含137Cs放射性废水提供借鉴。
表1天津自来水水质
Table 1Quality of tapwater of Tianjin
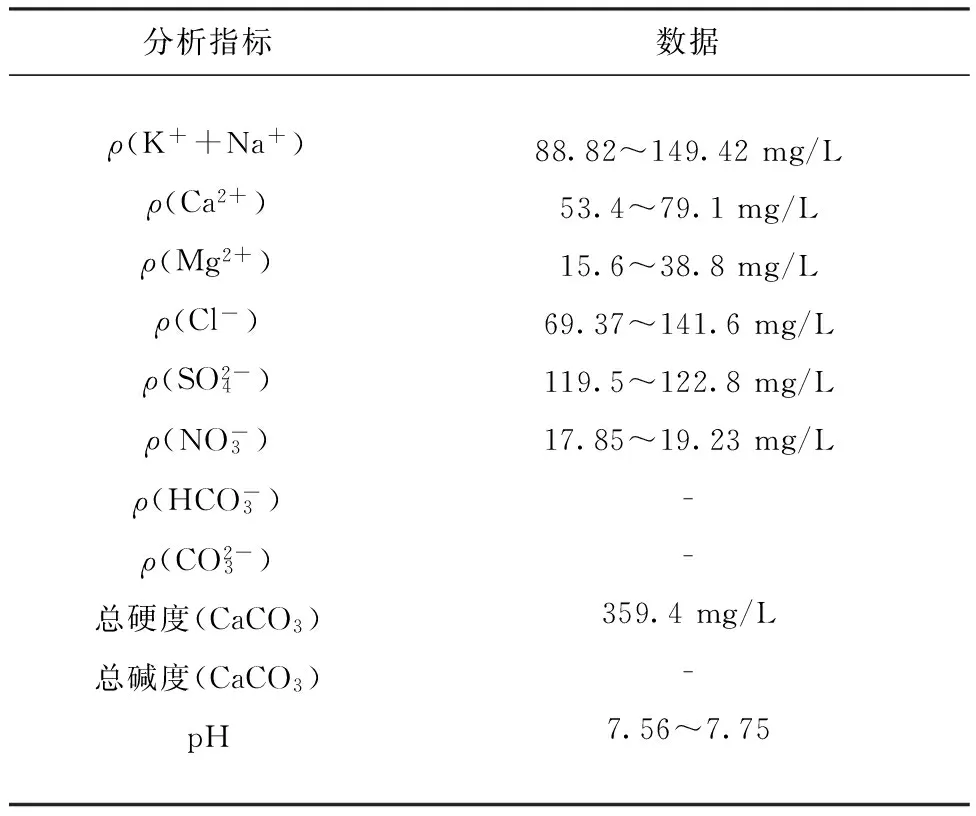
分析指标数据ρ(K++Na+)ρ(Ca2+)ρ(Mg2+)ρ(Cl-)ρ(SO2-4)ρ(NO-3)ρ(HCO-3)ρ(CO2-3)总硬度(CaCO3)总碱度(CaCO3)pH88.82~149.42mg/L53.4~79.1mg/L15.6~38.8mg/L69.37~141.6mg/L119.5~122.8mg/L17.85~19.23mg/L--359.4mg/L-7.56~7.75
1 实验部分
1.1试剂、材料及仪器
实验所用主要试剂纯度均为分析纯,各试剂除了溶解稀释外不经过其他预处理。氯化氢、氢氧化钠、氯化钠、氯化钾、氯化钙均为成都市科龙化工试剂厂生产。
WX型混合纤维素酯微孔滤膜(孔径0.22 μm,直径φ50 mm)用于混合液过滤。
富华79-1磁力搅拌仪,上海富华实验仪器有限公司,用于搅拌CuFC悬浊液;HNY-2102恒温培养振荡器,天津市欧诺仪器仪表有限公司,用于振荡目标溶液;AP-01P真空抽滤机、天津奥特赛恩斯仪器有限公司,溶剂过滤器、500 mL、杭州常胜科教器具厂,用于混合液抽滤;CANBERRA BE5030高纯锗伽马谱仪,美国CANBERRA公司,用于检测溶液中137Cs的活度浓度;PHS-2F pH计,上海精科公司,用于测废水的pH值;METTLER TOLEDO电子天平,精度为0.000 1 g,用于称量固体药品。所有测量仪器均在检定有效期内。
1.2实验方法
(1) 模拟废水的配制
在250 mL锥形瓶内加入一定量的137Cs标准溶液(用北京同辐同位素公司生产的137Cs原液加去离子水配制,活度浓度为4.24×107Bq/L),然后加入150 mL去离子水或地表水或海水,配制模拟废水。去离子水用Millipore纯水发生器制备,电导率为0.7 μs/cm;地表水、海水的水质参数列于表2。
表2实验用水水质
Table 2Quality of water used in the experiment
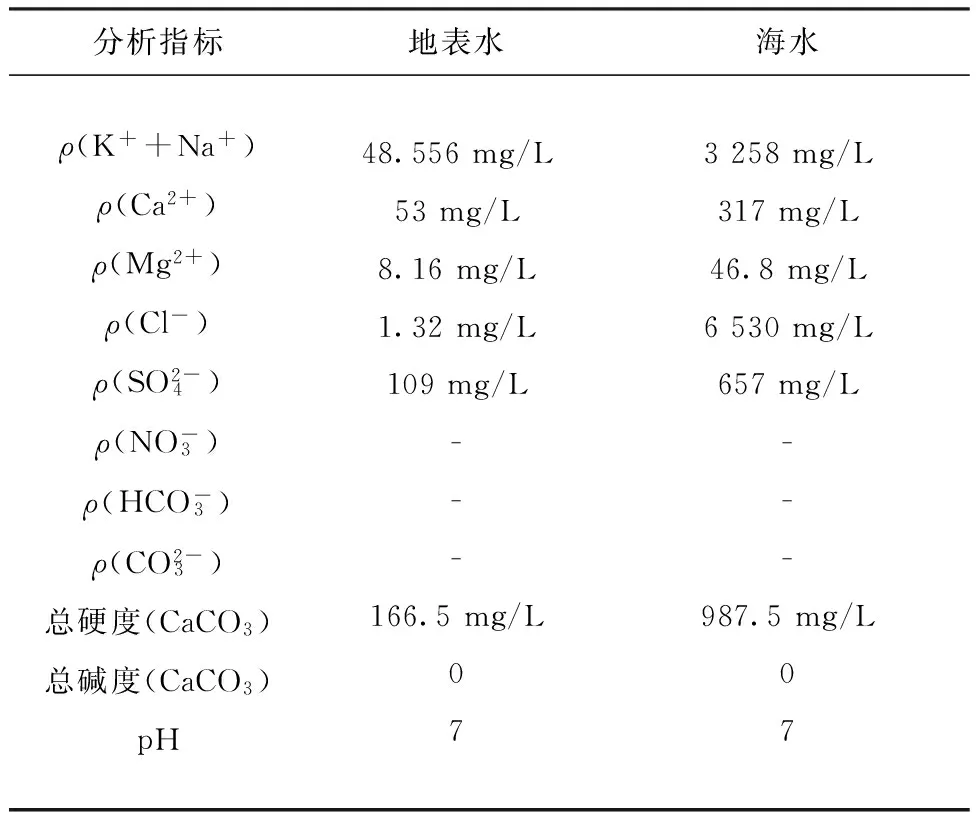
分析指标地表水海水ρ(K++Na+)ρ(Ca2+)ρ(Mg2+)ρ(Cl-)ρ(SO2-4)ρ(NO-3)ρ(HCO-3)ρ(CO2-3)总硬度(CaCO3)总碱度(CaCO3)pH48.556mg/L53mg/L8.16mg/L1.32mg/L109mg/L---166.5mg/L073258mg/L317mg/L46.8mg/L6530mg/L657mg/L---987.5mg/L07
(2) 吸附剂的制备
用Na4Fe(CN)6和Cu(NO3)2进行沉淀反应,制备CuFC(分子式为Cu2Fe(CN)6·7H2O),制备得到CuFC的悬浊液,其沉降性能良好,悬浊液颗粒粒径最小为0.55 μm,最大为45 μm,粒径为0.55~11.24 μm的颗粒体积分数为50%。大于实验用微滤膜的孔径(0.22 μm),过滤时颗粒不会穿过滤膜。
(3) 实验步骤
调节模拟废水的pH值为7.0(2.3节实验中分别调节模拟废水pH值为2.2~11.2),在模拟废水中加入一定量的吸附剂CuFC(2.4节及2.5节实验中先加入一定量的K+、Na+、Ca2+或腐殖酸),在25 ℃和200 r/min下,震荡一定时间(吸附时间)后,用抽滤装置抽滤,滤液制样后用γ谱仪测量137Cs的活度浓度。
1.3去污因子的计算
去污因子(DF)按公式(1)计算:
DF=C0/C1
(1)
式中:C0,模拟废水中137Cs的初始活度浓度,Bq/L;C1,滤液中137Cs的活度浓度,Bq/L。
2 结果和讨论
2.1137Cs初始活度浓度的影响
用去离子水配制三组不同C0的模拟废水,各投加不同量的CuFC进行废水处理实验,结果示于图1。由图1可知:当废水中CuFC投加量一定时,DF随C0增大而增大。这是因为在这三组废水中,Cs+的初始质量浓度均很低(分别为5.40×10-4μg/L、5.40×10-3μg/L和8.06×10-2μg/L),远达不到CuFC的饱和吸附容量,在废水中CuFC投加量一定时,随着C0的增大,C1的增加很小,因此DF随C0的增大而增大。
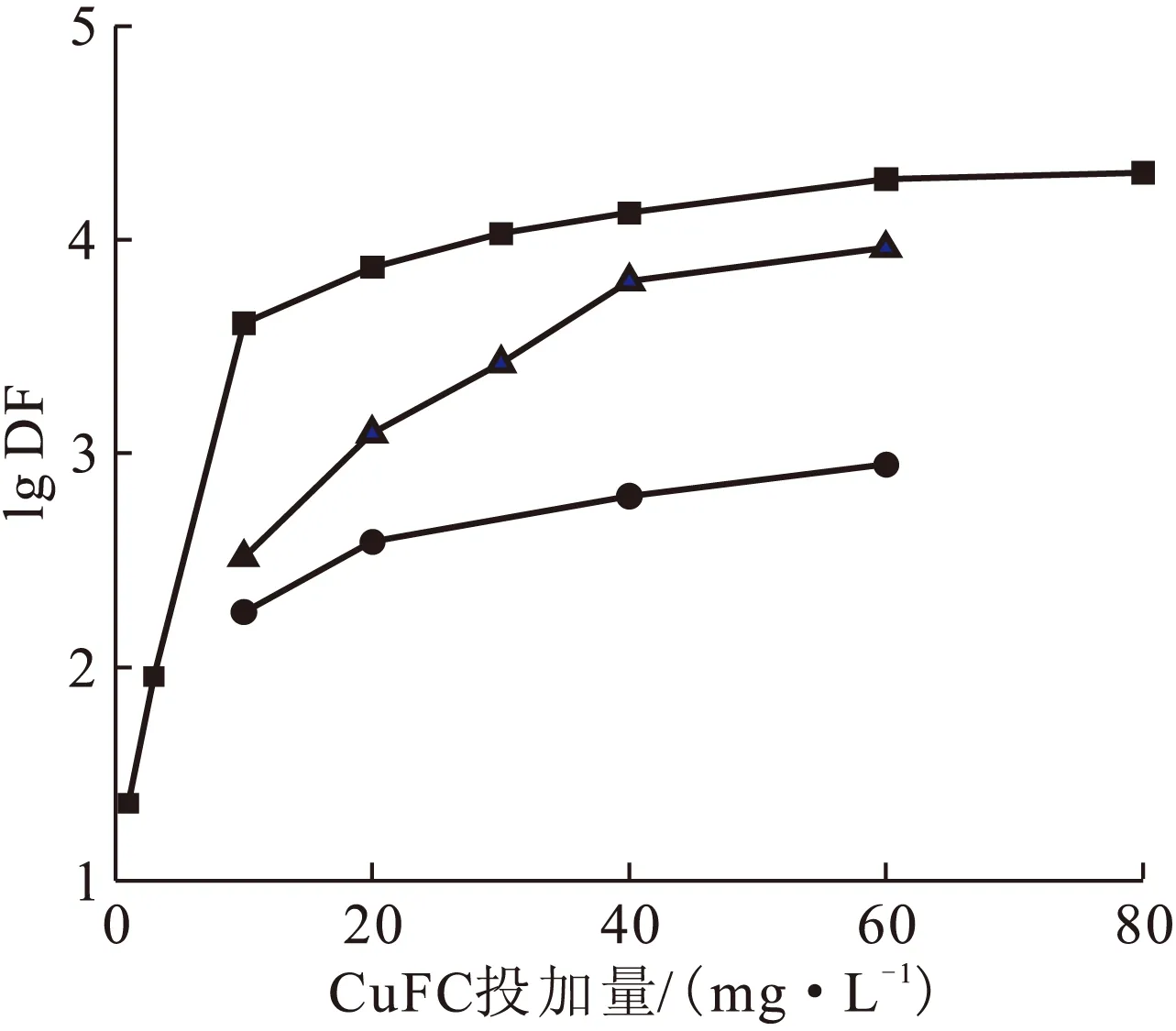
C0,Bq/L:■——4.24×105,▲——2.84×104,●——2.84×103图1 C0对DF的影响Fig.1 Influence of C0 on DF
2.2吸附时间的影响
用去离子水配制一组C0为2.84×105Bq/L的模拟废水,各投加40 mg/L的CuFC后,进行不同吸附时间下的废水处理实验,结果示于图2。由图2可知:DF随吸附时间的增加而增大,在最初20 min内,DF迅速增大,达到5.44×103;在20 min到80 min内,DF缓慢增大,80 min时,DF达到5.73×103,比20 min时增加了5.3%,增加量很小。综合考虑137Cs去除效果及处理成本,采用单级CuFC吸附-微滤工艺处理含137Cs的低放射性废水时,合适的水力停留时间约为20 min。
韩非等[8]研究发现,采用CuFC吸附-微滤工艺处理含Cs+废水时,吸附平衡时间约为90 min,与本实验的吸附平衡时间有差异。这是因为本实验模拟废水中,C0对应的Cs+初始质量浓度(8.06×10-2μg/L)比韩非实验溶液中Cs+初始质量浓度(100 μg/L)低了3个数量级,远达不到CuFC的饱和吸附容量,使本实验的表观吸附平衡时间仅为20 min。
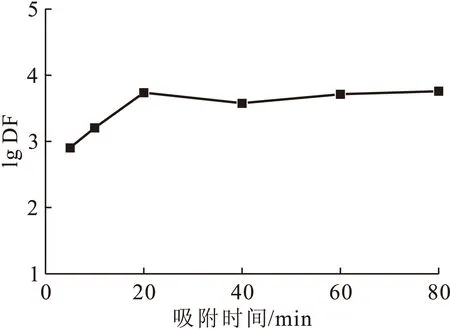
C0=2.84×105 Bq/L, ρ(CuFC)=40 mg/L图2 吸附时间对DF的影响Fig.2 Influence of adsorption time on DF
2.3pH值的影响
用去离子水配制一组C0为4.24×105Bq/L的模拟废水,用氯化氢或氢氧化钠溶液将其调为不同的pH值后,各投加40 mg/L的CuFC进行废水处理实验,结果示于图3。图3表明:当pH值从2.2增加到9.6时,DF缓慢增大;当pH值从9.6增加到10.9时,DF迅速减小。
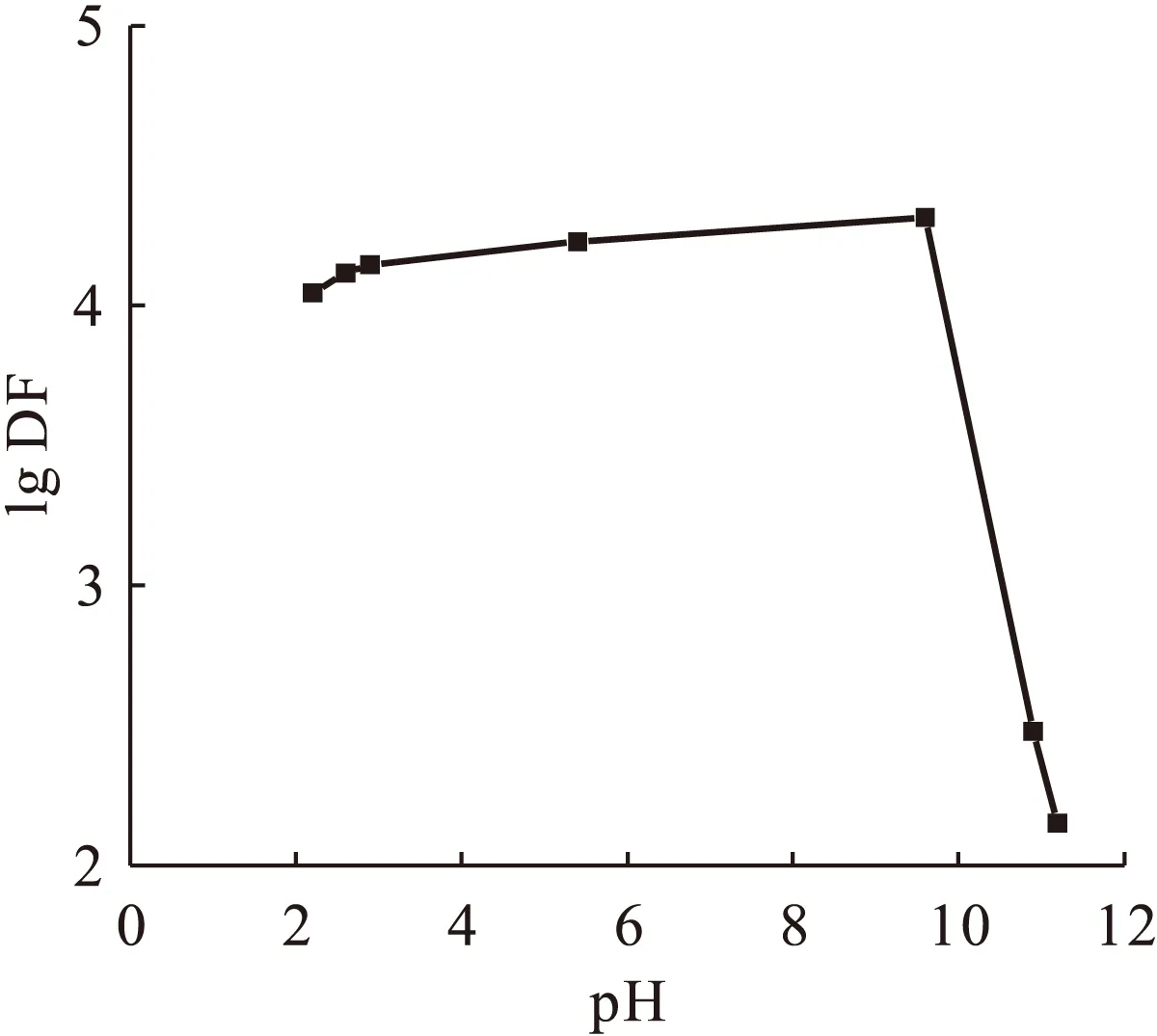
C0=4.24×105 Bq/L, ρ(CuFC)=40 mg/L图3 pH值对DF的影响Fig.3 Influence of pH on DF
废水中的Cs+和H+都可以被CuFC吸附[9],当pH值从2.2增加到9.6时,废水中H+浓度减少,CuFC表面的活性点位被H+占据的少,被Cs+占据的多,使废水中更多的Cs+有机会转移到CuFC固相中,导致DF增大,但DF增加量很小,这是因为本实验废水初始Cs+质量浓度非常小,废水中的H+远远过量于Cs+,当pH值从2.2增加到9.6时H+浓度的减少不足以使Cs+占据更多的吸附活性点位,因此DF缓慢增大。当废水pH值大于10.9后,DF迅速减小,并观察到废水由红棕色变为浅蓝色,是因为CuFC或其吸附Cs+后的产物在碱性条件下发生分解产生了Cu(OH)2所致,而Cu(OH)2不能吸附Cs+[10],废水中的Cs+只能被少量未分解的CuFC所吸附,导致DF迅速减小。韩非等[8]研究也发现,CuFC在pH>11后会分解,与本文研究结果一致。
2.4竞争离子的影响
用去离子水配制三组C0为2.84×105Bq/L的模拟废水,分别向每组投加不同量的竞争离子Ca2+、Na+、K+后,各投加40 mg/L的CuFC进行废水处理实验,结果示于图4。图4表明:废水中投加竞争离子Ca2+、Na+、K+后,DF迅速减小。这三种竞争离子对CuFC吸附Cs+的影响大小顺序为:K+>Na+>Ca2+。这一结果与翁皓珉等[11]的研究结果相吻合。
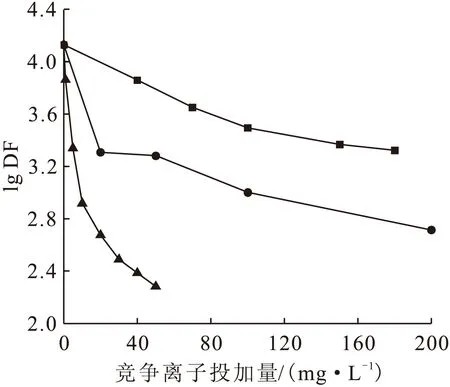
C0=2.84×105 Bq/L, ρ(CuFC)=40 mg/L■——Ca2+,●——Na+,▲——K+图4 竞争离子对DF的影响Fig.4 Influence of compete ions on DF
竞争离子对CuFC吸附Cs+的过程的影响机理主要体现在两方面:(1) 与Cs+抢占吸附空位;(2) 聚集在吸附空位周围通过静电斥力作用阻碍Cs+被吸附。机理(1)主要取决于竞争离子的半径;机理(2)主要取决于竞争离子的浓度。Cs+、Ca2+、Na+、K+的离子半径分别为0.169、0.099、0.102、0.138 nm[12-13],可以看出,离子半径越接近Cs+半径的离子,其竞争能力越强,对DF影响也越大。
韩非等[8]研究发现,当K+、Na+的投加量分别在30 mg/L和1 000 mg/L以内时,DF几乎不受影响,当K+、Na+投加量分别大于30 mg/L和1 000 mg/L时,DF才迅速减小。而本实验发现,当K+、Na+的投加量分别在3~50 mg/L和20~200 mg/L时,DF即迅速减小,本实验中竞争离子对DF的影响更加显著。本实验与韩非等[8]实验的条件几乎完全一致(137Cs、133Cs的化学性质相同),唯一不同的是本实验废水中Cs+初始质量浓度小3个数量级。由此可以推断,尽管CuFC对Cs+有很强的亲和力和高选择性,但质量浓度的不足会使Cs+在与其他离子竞争的过程中处于劣势。
2.5CuFC投加量的影响
分别用去离子水、地表水和海水配制三组模拟废水,使其C0分别为4.24×105Bq/L、2.84×105Bq/L和2.84×105Bq/L,分别向每组投加不同量的CuFC后进行废水处理实验,结果示于图5。由图5可知:DF随CuFC投加量的增大而增大,当CuFC投加量小于30 mg/L时,DF迅速增大;CuFC投加量从30 mg/L增加到80 mg/L时,DF缓慢增大,当CuFC投加量达到80 mg/L时,对于分别用去离子水、地表水和海水配制的模拟废水,DF分别达到2.06×104、1.62×104和9.36×101。综合考虑137Cs去除效果及药剂成本,采用单级CuFC吸附-微滤工艺处理含137Cs废水时,合适的CuFC投加量为30~60 mg/L。
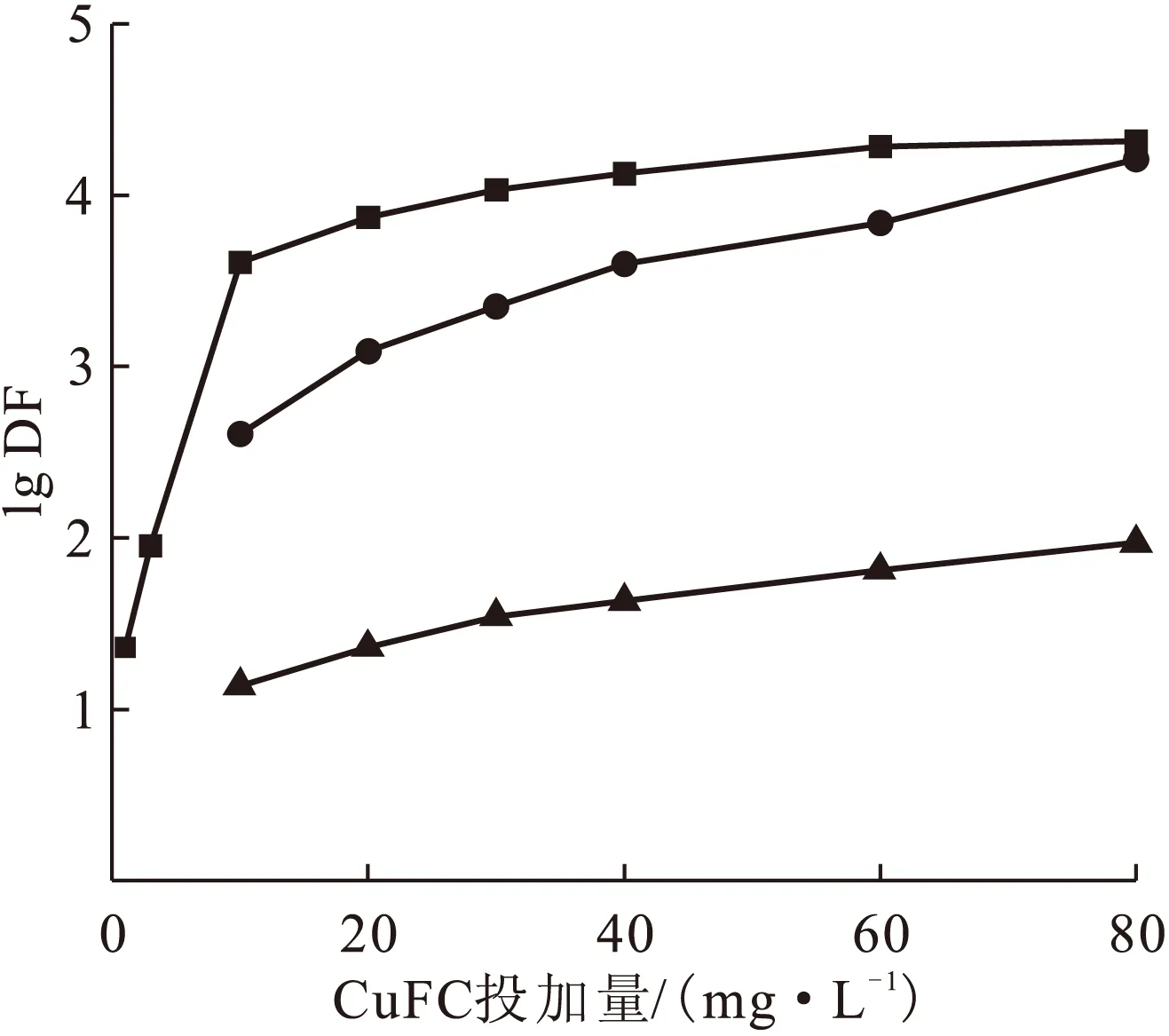
■——去离子水,C0=4.24×105 Bq/L;●——地表水,C0=2.84×105 Bq/L;▲——海水,C0=2.84×105 Bq/L图5 CuFC投加量对DF的影响Fig.5 Influence of the dosage of CuFC on DF
在相同的CuFC投加量下,对于分别用去离子水、地表水、海水配制的三种模拟废水,DF的大小顺序为:去离子水>地表水>海水,这是因为三种废水中竞争离子浓度的大小顺序为:去离子水<地表水<海水。对于用地表水配制的模拟废水,当CuFC投加量为20~40 mg/L时,DF达1.23×103~3.96×103,而韩非等[7]的研究中,DF仅为2.87×102~4.63×102,两次研究中DF的差异主要是由实验模拟废水中离子种类及浓度的差别(见表1和表2)所致。
本实验中,对于用地表水配制的模拟废水,当CuFC投加量为80 mg/L时,DF达1.62×104。而邓玥等[6]的研究中,当亚铁氰化钾锌投加量为83 mg/L时,DF仅为5.87×101。可见,用单级吸附-微滤工艺处理含137Cs废水时,采用CuFC作吸附剂的处理效果远优于采用亚铁氰化钾锌作吸附剂。
叶明吕等[14]用斜发沸石去除模拟地下水中的Cs,当沸石投加量为105mg/L(固液比为1∶10 g/mL)、吸附时间为10 d时,DF为103;可见,采用CuFC作吸附剂处理含137Cs废水的处理效果也优于沸石,且吸附平衡时间仅为90 min。福岛核事故后,采用沸石填充柱结合加压上浮装置、絮凝沉降三级组合工艺处理含高浓度137Cs的海水,DF为106[2];本实验中采用单级CuFC吸附-微滤工艺处理含137Cs的模拟海水(CuFC投加量为80 mg/L),DF接近102(DF为96)。综上所述,CuFC吸附-微滤工艺对于含137Cs废水有较高的去污因子,且当废水含盐量较高时,仍具有较好的去污效果。因此可用于核燃料后处理废水及海水等高含盐量的含137Cs废水处理,应用前景非常可观。
3 结 论
(1) 采用单级CuFC吸附-微滤工艺处理含137Cs废水时,当吸附时间大于20 min,pH值为2.2~9.6,CuFC投加量为30~60 mg/L时,对137Cs的去除效果较好。且模拟废水中137Cs的初始活度浓度越大、竞争离子投加量越小时,对137Cs的去除效果越好。
(2) 采用单级CuFC吸附-微滤工艺处理含137Cs的模拟海水时,去污因子接近102,表明CuFC吸附-微滤工艺可用于核燃料后处理废水及海水等高含盐量废水中137Cs的去除,具有可观的应用前景。
参考文献:
[1]黄明犬.放射性废水中低放射性废水处理现状与发展[J].西南给排水,2003,25(6):29-32.
[2]Hsu C W, DiPrete D P, Eibling R E, et al. Organic analyses of highly radioactive solutions requiring pretreatment by137Cs removal[J]. J Radioanal Nucl Chem, 2001, 250(2): 223-229.
[3]余少青,张春明,陈晓秋.日本福岛核电站事故后高浓度放射性废水处理系统介绍及其应用启示[J].辐射防护,2013,33(5):294-299.
[4]Roque M R, Carballo E, Polanco R, et al. Structure and adsorption properties of a porous cooper hexacyanoferrate polymorph[J]. J Phys Chem Solids, 2015, 86(1): 65-73.
[5]Rao S V S, Paul B, Lal K B, et al. Effective removal of cesium and strontium from radioactive wastes using chemical treatment followed by ultra filtration[J]. J Radioanal Nucl Chem, 2000 (246): 413-418.
[6]邓玥,赵军,刘学军.含铯废水膜处理工艺中吸附剂的选择[J].原子能科学技术,2010,44(增刊):143-147.
[7]Han Fei, Zhang Guang-hui, Gu Ping. Removal of cesium from simulated liquid waste with countercurrent two-stage adsorption followed by microfiltration[J]. J Hazard Mater, 2012 (225-226): 107-113.
[8]Han Fei, Zhang Guang-hui, Gu Ping. Adsorption kinetics and equilibrium modeling of cesium on copper ferrocyanide[J]. J Radioanal Nucl Chem, 2011, 293(1): 572-580.
[9]Nilchi A, Saberi R, Moradi M, et al. Adsorption of cesium on copper hexacyanoferrate-PAN composite ion exchanger from aqueous solution[J]. Chem Eng J, 2011, 172(1): 572-580.
[10]Haas P A. A review of information on ferrocyanide solids for removal of cesium from solutions[J]. Sep Sci Technol, 1993, 28(17-18): 2479-2506.
[11]翁皓珉.无机离子交换剂及其应用[M].北京:原子能出版社,1998:221.
[12]Park Y, Lee Y C, Shin W S, et al. Removal of cobalt, strontium and cesium from radioactive laundry wastewater by ammonium molybdophosphate-polyacrylonitrile(AMP-PAN)[J]. Chem Eng J, 2010, 162(2): 685-695.
[13]Ofomaja A E, Pholosi A, Naidoo E B. Kinetics and competitive modeling of cesium biosortion onto chemically modified pine cone powder[J]. Journal of the Taiwan Institute of Chemical Engineers, 2013, 44(6): 943-951.
[14]叶明吕,陆誓俊,秦春扣.放射性铯在沸石中的吸附与迁移的研究[J].核科学与工程,1994,14(1):72-77.
收稿日期:2015-01-19;
修订日期:2016-03-28
基金项目:国家自然科学基金资助项目(51178301)
作者简介:王露(1991—),女,陕西乾县人,研究实习员,环境工程专业,主要从事放射性“三废”处理及核设施退役等相关研究工作
中图分类号:O657.4
文献标志码:A
文章编号:0253-9950(2016)03-0176-06
doi:10.7538/hhx.2016.38.03.0176
CuFC Adsorption-Microfiltration Craft Deal With Wastewater Containing137Cs
WANG Lu1, ZHAO Jun1,*, XU Yao2, XIAO Xiang-zhu1, DENG Yue1, YANG Yang1
1.Institute of Nuclear Physics and Chemistry, China Academy of Engineering Physics, Mianyang 621900, China;2.Environmental Science and Engineering Institute of Tianjin University, Tianjin 300072, China
Abstract:The craft of single grade CuFC adsorption+microfiltration was used to treat the simulative wastewater containing137Cs. The affects of the initial activity concentration of137Cs, the adsorption time, pH, competing ions and the dosage of CuFC on decontamination fator(DF) were studied. The results indicate that when the adsorption time is 90 min, pH is 7, the dosage of CuFC is 80 mg/L, and add no competing ions, DF reach 2.06×104, 1.62×104 and 9.36×101 respectively for simulative wastewater made up of pure water (C0=4.24×105 Bq/L), surface water(C0=2.84×105 Bq/L ) and seawate(C0=2.84×105 Bq/L ). It indicates that the craft of CuFC adsorption-microfiltration is a high-efficiency craft to treat wastewater containing137Cs, and has considerable application prospect.
Key words:CuFC;137Cs; adsorption; microfiltration
*通信联系人:赵军(1968—),男,四川古蔺人,副研究员,先后从事放化分析、放射性“三废”处理及核设施退役等相关研究工作
