原电池电极反应的书写技巧
2016-08-15何礼奎陕西省西乡县第二中学
何礼奎(陕西省西乡县第二中学)
原电池电极反应的书写技巧
何礼奎
(陕西省西乡县第二中学)
书写原电池的电极反应式是原电池教学的重要内容,又是化学试题命题的一个热点,也是学生感到疑惑、难度较大的知识点。分析和书写电极反应式是对原电池原理认识的进一步深化和发展,能够促进学生对原电池原理的掌握。
一、判断原电池电极(正极、负极)的依据
1.多数情况下不活泼金属或非金属导体材料做正极,活泼金属做负极;
2.电子流入的极为正极,电子流出的极为负极;
3.电流方向由正极流向负极;
4.发生还原反应的为正极,发生氧化反应的为负极;
5.从电极上发生的现象可以确定,电极增重或产生气体的为正极,电极减轻的为负极。
二、书写原电池电极反应式的方法
1.双线桥法
原电池反应是自发的氧化还原反应,根据所给条件,写出原电池反应的离子方程式。分析化合价变化,还原剂为负极的反应物,氧化剂为正极的反应物,确定对应的产物,写出电极反应式。负极:还原剂-ne-=氧化产物(氧化反应);正极:氧化剂+ne-=还原产物(还原反应)。
2.运算法
依据条件写出原电池反应的离子方程式和其中一个较为简单的电极反应式;另一个复杂的电极反应式等于原电池的离子反应方程式减去其中简单的电极反应式。结合反应的环境,依据电荷守恒和质量守恒、得失电子守恒来配平电极反应式。电极产物在电解质溶液的环境中,应能稳定存在。溶液中不存在O2-,在酸性溶液中它与H+结合成H2O,在碱性溶液中它与H2O结合成OH-。碱性介质中生成的H+结合OH-生成水。+4价的C在酸性溶液中以CO2形式存在,在碱性溶液中以CO32-存在。书写电极反应式需要根据实际反应环境熟练应用这些规律。
三、电极反应的类型
1.简单原电池的电极反应
例1.锌片、铜片与硫酸铜溶液构成原电池(如图),写出电极与总反应式。
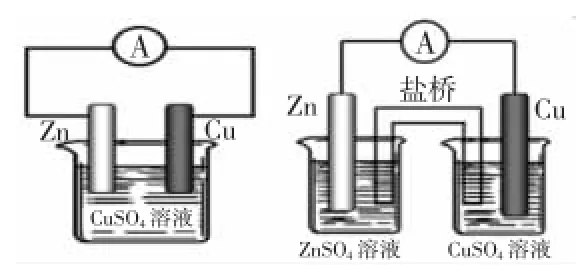
解析:单液原电池和双液原电池,原理相同,这种原电池属于简单原电池。原电池反应的离子方程式为,利用双线桥法,写出正、负极反应式。Zn片为负极失去电子生成Zn2+。Cu片为正极,溶液中Cu2+得到电子生成Cu。即负极:Zn-2e-=Zn2+;正极:Cu2++2e-=Cu。
2.复杂原电池的电极反应
例2.人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是()
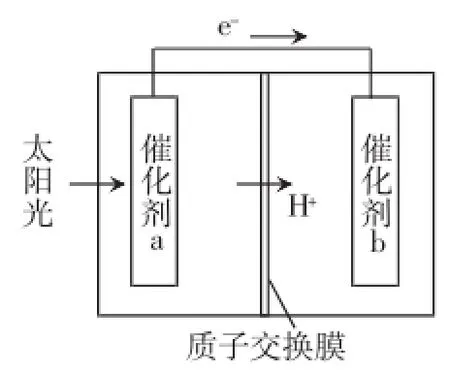
A.该过程是将太阳能转化为化学能的过程
B.催化剂a表面发生氧化反应,有O2产生
C.催化剂a附近酸性减弱,催化剂b附近酸性增强
D.催化剂b表面的反应是CO2+2H++2e-=HCOOH
解析:根据题给信息和反应特点,该电池中发生反应的化学方程式为:2CO2+2H2O=2HCOOH+O2↑;故其将太阳能转化为了化学能,A正确;氢离子的转移方向和电子转移的方向说明,催化剂a为负极,其表面发生的反应为:2H2O-4e-=4H++O2↑,氧元素化合价升高被氧化,B正确;催化剂a表面产生氢离子,酸性增强,C错误;催化剂b为正极,其表面发生的反应为:CO2+2H++2e-=HCOOH,D正确。答案为C。
3.燃料电池的电极反应
燃料电池正极上发生反应的物质是O2,电解质溶液有四种情况,正极反应式有四种写法。
(1)熔融固体氧化物电解质(高温下能传到O2-),正极:O2+ 4e-=2O2-;
(2)酸性电解质溶液,联系反应Na2O+2HCl=2NaCl+H2O,正极:O2+4e-+4H+=2H2O;
(3)碱性电解质溶液,联系反应Na2O+H2O=2NaOH,正极:O2+ 4e-+2H2O=4OH-
(4)熔融碳酸盐电解质,联系反应Na2O+CO2=Na2CO3,正极:O2+4e-+2CO2=2CO32-。
分别写出燃料电池的离子反应方程式和正极反应式,而负极反应式用燃料电池的离子反应方程式减去正极反应式得到。
例3.燃料电池(如图),电解质为KOH,在两极分别通入CH3OH和O2,有关此电池判断正确的是()
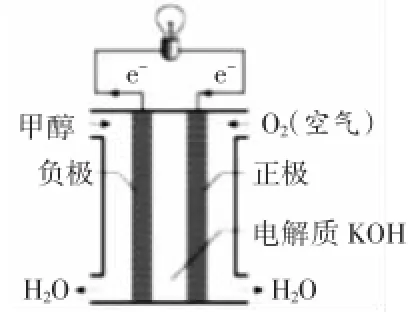
A.正极反应式:2CH3OH+2H2O-12e-=2CO2↑+12H+
B.放电一段时间后,负极的PH值升高
C.放电一段时间,阳离子向负极移动,阴离子向正极移动
D.该电池在工作时,每消耗32gCH3OH,外电路中通过6mole-
解析:碱性环境下,O2在正极反应:3O2+6H2O+12e-=12OH-,A错误;燃料电池的反应式为2CH3OH+3O2+4OH-=2CO32-+6H2O,减去正极反应式3O2+6H2O+12e-=12OH-,得到负极反应2CH3OH-12e-+16OH-=2CO32-+12H2O,负极区PH值下降,B错误;原电池放电时,阳离子向正极移动,阴离子向负极移动,C错误;负极:2CH3OH-12e-+16OH-=2CO32-+12H2O,32gCH3OH为1mol,转移电子6mol,D正确。答案为D。
彭以勇,浅析原电池电极反应式的书写及应用[J].理科考试研究,2013(7).
·编辑武慧慧
何礼奎,高级教师(五级),本科、学士。在全国杂志、报纸上发表教学论文50多篇。
