Ni-CeO2/γ-Al2O3电催化间甲基苯酚水蒸气重整的实验研究
2016-08-10冉泽朋董长青
冉泽朋, 陆 强, 王 昕, 胡 斌, 董长青
(华北电力大学 生物质发电成套设备国家工程实验室,北京 102206)
Ni-CeO2/γ-Al2O3电催化间甲基苯酚水蒸气重整的实验研究
冉泽朋, 陆 强*, 王 昕, 胡 斌, 董长青
(华北电力大学 生物质发电成套设备国家工程实验室,北京 102206)
摘要:以间甲基苯酚为生物质气化焦油含氧模型化合物,采用Ni-CeO2/γ-Al2O3催化剂开展了电催化水蒸气重整实验研究,考察了电流强度和重整温度对间甲基苯酚转化率、产气组成以及催化剂积碳的影响,并在600 ℃下,考察了催化剂的稳定性以及电流对催化剂稳定性的改善作用。结果表明:采用电催化方法能够显著提高间甲基苯酚的重整效率,在使用2.4 g催化剂和立式管式炉的条件下,重整温度为700 ℃以及电流强度为3 A时,转化率达到99.7 %;提高温度和电流能够显著提高产气中CO的体积分数,同时在一定程度上降低了CO2和H2的体积分数;此外,电流的引入也能够减少催化剂表面积碳的形成并显著提高催化剂的稳定性。
关键词:焦油;电催化水蒸气重整;间甲基苯酚;Ni-CeO2/γ-Al2O3
热解气化是一种高效的生物质资源利用方式,但气化过程中产生的焦油成分复杂、性状黏稠,容易阻塞管路,影响设备运行,同时焦油所含能量难以利用,严重限制了气化技术的大规模推广应用[1-3]。催化水蒸气重整是一种极为有效的焦油转化技术,核心在于催化剂[4-5]。前期研究已经证实镍基催化剂是一类有效的焦油水蒸气重整催化剂,但是其催化活性以及抗积碳能力仍有待提高[6-8]。由于焦油成分极其复杂且多变,为测试不同催化剂的性能,现有研究大多采用特定的焦油模型化合物,主要为苯、甲苯和萘等芳香烃类物质。Park等[9]以苯为原料开展水蒸气重整实验,研究了镍的前驱物和负载量等因素对Ni/CeO2(75 %)-ZrO2(25 %)催化剂活性的影响,发现镍负载量为15 %、硝酸镍作为镍的前驱物时催化剂活性最高。Ashok等[10]针对甲苯开展水蒸气重整实验,探究了Ce改性的Ni/CaO-Al2O3催化剂的催化活性,发现催化剂的活性随着铈负载量的增加先升高后降低,且Ni/Ca-Al-Ce(0.2)的催化活性最高。Ferella等[11]研究了基于ZrO2和Al2O3载体以及不同活性组分(如Co、Ni、Fe、Cr、Ce、Pt)的催化剂对萘水蒸气重整的催化效果,发现以ZrO2为载体且同时负载Fe/Ni/Pt的催化剂活性最高。实际上,生物质气化所形成的焦油,除了芳香烃外,还包括酚类衍生物等多种含氧有机物,但现阶段很少有针对这些物质的研究[12]。和芳香烃类物质相比,含氧有机物的热稳定性较差,极易在催化剂表面积碳,导致催化剂失活。因此,极有必要选取合适的含氧有机物作为焦油模型化合物,考察其在水蒸气重整过程中的反应以及积碳特性。近年来,针对生物油及其模型化合物的催化重整制氢,中国科学技术大学的李全新教授课题组提出了电催化重整的概念,在催化重整过程中引入一定的电流,依靠电流产生的热电子促进有机物的分解,能够显著提高重整效率[13-14]。本课题组将该技术应用于生物质气化焦油的催化重整,利用助剂CeO2和不同载体(SBA-15或γ-Al2O3)改性的镍基催化剂,对芳香烃模型化合物(甲苯、苯和1-甲基萘),在电催化作用下进行重整,可有效提高重整效率并抑制焦油组分在催化剂表面的积碳[15]。在此基础上,本研究选择间甲基苯酚为焦油含氧模型化合物,利用Ni-CeO2/γ-Al2O3作为催化剂,开展电催化水蒸气重整实验研究,考察了温度和电流强度对间甲基苯酚转化率、产物分布以及催化剂积碳的影响,并开展了长时间稳定性测试,考察电催化方式对催化剂稳定性的影响,来综合评价电催化方式较普通催化的优势。
1实 验
1.1催化剂制备
实验所用的催化剂为Ni-CeO2/γ-Al2O3,采用一步等体积浸渍法制备[16]。制备方法如下:首先将14.9 g硝酸镍(Ni(NO3)2·6H2O)和7.6 g硝酸铈(Ce(NO3)3·6H2O)溶于一定量的去离子水中配制成混合溶液,之后将94.0 g的γ-Al2O3浸渍到上述混合溶液中,充分搅拌并置于超声仪中超声分散24 h,然后将混合物转移至干燥箱,在105 ℃空气氛围中干燥12 h,而后保存备用,并在使用之前置于H2和N2的混合气氛中原位煅烧还原,由此获得高活性的催化剂[17],其中金属镍和CeO2铈的质量分数均为3 %。
1.2催化剂表征
催化剂的晶型结构由Rotaflex型X射线衍射仪测定,采用Cu Kα射线(λ=0.154 06 nm),扫描角2θ的范围为10~90 °,扫描速度为4 (°)/min。反应后催化剂的积碳率由Vario Macro Cube元素分析仪进行测定。
1.3电催化水蒸气重整实验
1.3.1反应过程间甲基苯酚的电催化水蒸气重整过程中会发生水蒸气重整反应(式(1)和(2)的水/碳比值,即反应物中水分子与间甲基苯酚所含碳原子的物质的量比值,分别为1和2)、水煤气变换反应(式(3))、干重整反应(式(4))、甲烷化反应(式(5))等[6,18-19],各反应受催化剂以及重整反应条件的影响,反应式如下:
C7H8O + 6H2O → 7CO + 10H2
(1)
C7H8O + 13H2O → 7CO2+ 17H2
(2)
CO +H2O ↔ CO2+H2
(3)
C7H8O + 6CO2→ 13CO + 4H2
(4)
CO + 3H2↔ CH4+H2O
(5)
1.3.2实验装置实验装置如图1所示,由微量注射泵、蠕动泵、预热器(上端石英管)、反应器(下端石英管)、电流控制器、冷凝器、干燥器和在线气相色谱分析仪(Micro GC 3000)组成。间甲基苯酚和水分别通过微量注射泵和蠕动泵注入反应器;上端的预热器用于气化间甲基苯酚和水,使其充分混合;下端的反应器内倒置一支U型石英棒,其上缠有电阻丝(Ni-Cr材质,电阻为15 Ω),而催化剂则装填在石英棒和电阻丝周围。
1.3.3操作流程实验前首先将2.4 g催化剂在H2和N2(体积比为1∶1)的混合气中800 ℃焙烧6 h(升温速率为2 ℃/min),完成催化剂的原位煅烧还原。然后以N2作为实验载气,调节预热器和反应器温度,其中预热器温度控制在300 ℃,目的在于保证反应物快速气化,同时防止其提前发生反应,反应器温度根据实验需要控制在500~700 ℃,控制电阻丝中通入的电流为0~3 A。待温度及电流强度达到设定值后通入间甲基苯酚(7.6 μL/min)和水(27.5 μL/min),开始实验。实验中,催化剂床层的空速为2 000 h-1,间甲基苯酚在混合气中的质量浓度为45 g/m3,水/碳比值为3。
反应出口气体首先经过冷凝器,使未反应的间甲基苯酚和水等可冷凝组分充分冷凝,不可冷凝气体经干燥后进入在线气相色谱分析仪进行分析。由于在线气相色谱仪可在2.8 min内完成一次气体组分的分析,因此每组实验中均采集多组数据。实验结束后,停止通入反应物,待反应器冷却至室温后停止通入N2,收集催化剂用于后续表征。催化剂的稳定性测试参照以上实验过程,根据测试条件调整实验温度和实验电流强度,两组测试条件分别为温度600 ℃、电流0 A和温度600 ℃、电流3 A,测试时长均为30 h。
1.4数据分析
在线气相色谱分析仪能够检测N2、H2、CO、CO2以及C1~C4的气态烃类物质,实验过程中只检测到N2、H2、CO、CO2和CH45种气体,没有检测到C2及以上气态烃类物质。由于实验中N2流量保持恒定,所以根据N2的流量以及混合气中N2的体积分数平均值,可以计算H2、CO2、CO与CH4的体积分数、单位时间产量以及间甲基苯酚的转化率。
1.4.1气体产物的体积分数及单位时间产量计算基于实验中采集的85组数据,计算各气体体积分数的平均值。气体组分的单位时间产量(Mi),即单位时间内产生气体组分的物质的量,可根据每次试验中恒定的N2流量与在线气相色谱仪直接分析得到的反应出口处不同气体的体积分数(μi)计算得到。产物气体组分的体积分数(Vi)定义为每种气体组分(H2、CO、CO2、CH4)的物质的量与产气中各气体组分物质的量之和的比值。具体的计算公式如下:
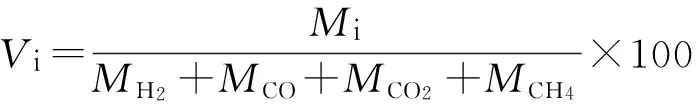
式中:Mi—i物质的单位时间产量,i=H2、CO、CO2、CH4,μmol/min;μi—i物质在反应出口气体中的体积分数,%;μN2—N2在反应出口气体中的体积分数,%;MN2—N2的物质的量流量,μmol/min;Vi—i物质在反应产物中的体积分数,%。
1.4.2转化率计算间甲基苯酚的转化率(X)定义为气体产物中的碳的物质的量与通入的间甲基苯酚中的碳的物质的量的比值。计算公式如下:

式中:X—间甲基苯酚的转化率,%;MC7H8O—间甲基苯酚的物质的量流量,μmol/min。
1.4.3催化剂积碳率计算催化剂的积碳率定义为测试后催化剂中碳的质量占催化剂质量的百分数,由元素分析仪直接测定。
2结果与讨论
2.1催化剂表征
图2给出了γ-Al2O3载体和新鲜Ni-CeO2/γ-Al2O3催化剂的XRD谱图。两张谱图中均有典型的γ-Al2O3的特征衍射峰(JCPDS # 10-0425)[20]。在Ni-CeO2/γ-Al2O3催化剂的XRD谱图中,衍射角44.6°、51.9°和76.6°所对应的衍射峰为金属镍的特征衍射峰(JCPDS # 04-0850)[21]。但在XRD谱图中未检测到CeO2的衍射峰,这可能是由于其含量低且高度分散在载体表面。
2.2电流强度与重整温度对反应的影响
2.2.1对转化率的影响图3给出了在不同电流强度和重整温度下间甲基苯酚的转化率。由图可知,随着电流强度的增加和重整温度的升高,间甲基苯酚的转化率显著提高。在电流为0 A、温度为500 ℃时,间甲基苯酚的转化率只有65.2 %;当电流增至3 A并且温度达到700 ℃时,间甲基苯酚的转化率达到99.7 %。在较低的反应温度下,电流对间甲基苯酚转化率的影响极为显著,随着温度的升高,电流的影响相对减弱,但仍然有较明显的作用。电流的存在能够显著提高间甲基苯酚转化率的原因在于:首先,电流通过电阻丝时会产生一定的热量,提高催化剂床层的局部温度,使部分催化剂活性提高;更主要的是,通电后电阻丝会发射出热电子,热电子能促进水和有机分子解离成离子碎片,使有机分子更易于被重整,从而提高间甲基苯酚的转化率[13-15]。综上,电催化的方式能够显著提高间甲基苯酚的转化率。
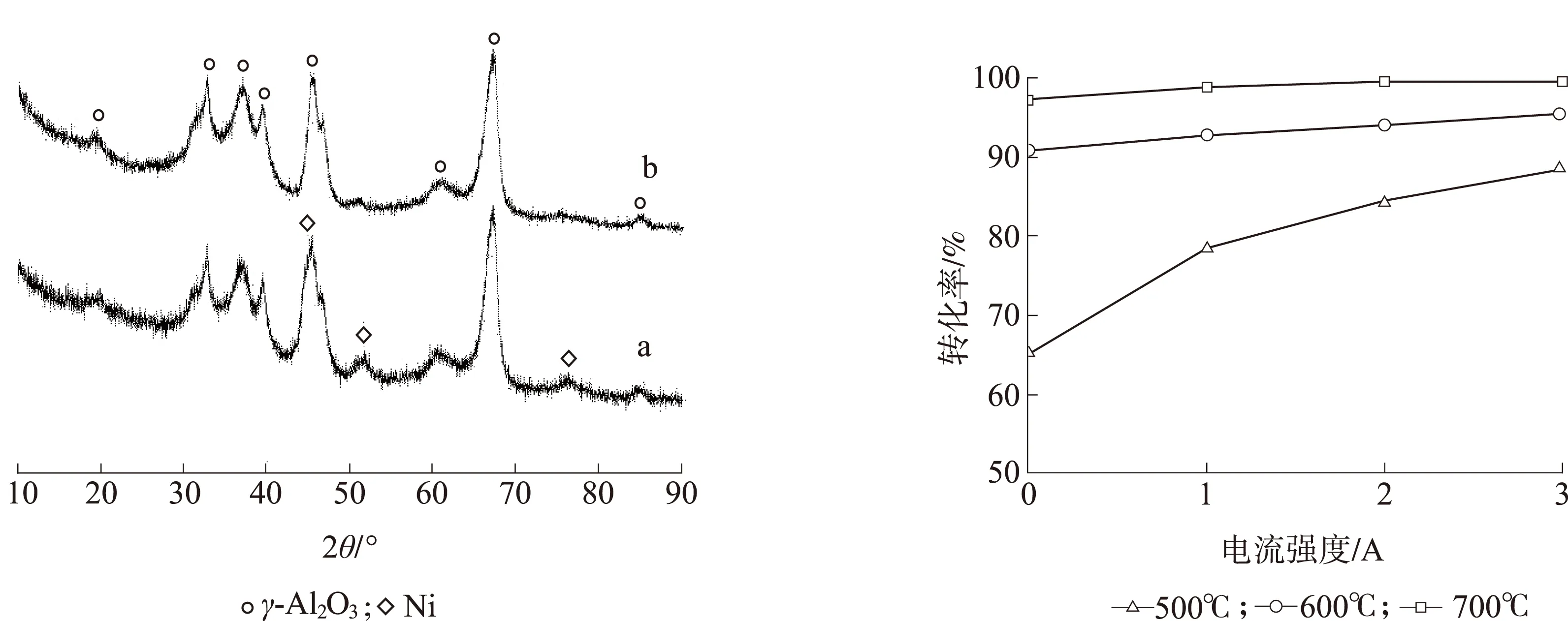
图 2γ-Al2O3(a)和新鲜Ni-CeO2/γ-Al2O3(b)的XRD谱图
图 3电流强度与重整温度对间甲基苯酚转化率的影响
Fig. 2XRD spectra ofγ-Al2O3(a) and
Fig. 3Effects of electric current intensity and reforming fresh Ni-CeO2/γ-Al2O3(b)temperature on them-cresol conversion
2.2.2对产物组成的影响表1给出了不同电流强度和重整温度条件下的产气组成和各气体的单位时间产量。重整产物中H2是主要产物,另外还有一定量的CO和CO2以及少量的CH4。由表可知:电流强度和重整温度对气体组分的体积分数的影响规律相似,其中温度的影响更为显著。当电流为3 A时,随着温度由500 ℃升到700 ℃,H2和CO2的体积分数分别由68.2 %和21.7 %降至66.6 %和17.3 %,而CO的体积分数则由9.6 %增至16.1 %,这可能是由于水煤气变换反应(式(3))为放热反应,升高温度会促进水煤气变换反应逆向进行[22],因此随着温度升高,H2和CO2的体积分数降低,而CO的体积分数增加。气体产物的单位时间产量主要由间甲基苯酚的转化率和产气的组成决定。在电流强度和重整温度较低的情况下,随着电流强度的增加和重整温度的提高,间甲基苯酚的转化率大幅提升,而产气组成的变化幅度相对较小,综合表现为CO、CO2和H2的单位时间产量增加;随着转化率变化幅度下降,产气组成的变化成为影响产量的主要因素,这也导致在电流和温度较高的条件下CO2和H2的单位时间产量出现下降。而CH4的含量及产量很低,随着反应条件加强CH4体积分数和单位时间产量逐渐减少,当温度为700 ℃,产物中已经检测不到CH4,这可能是提高温度和电流促进了CH4分解所致。
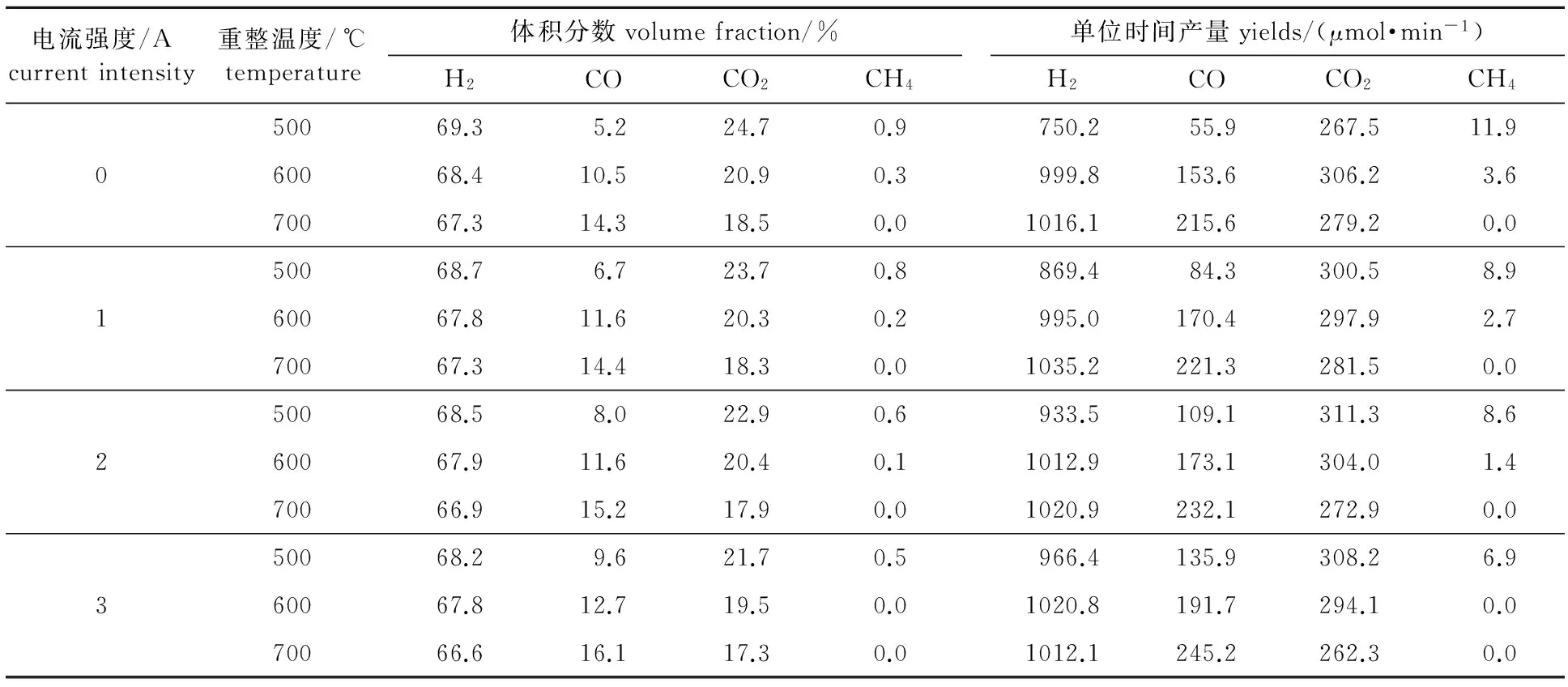
表 1 电流强度与重整温度对产气组成及单位时间产量的影响
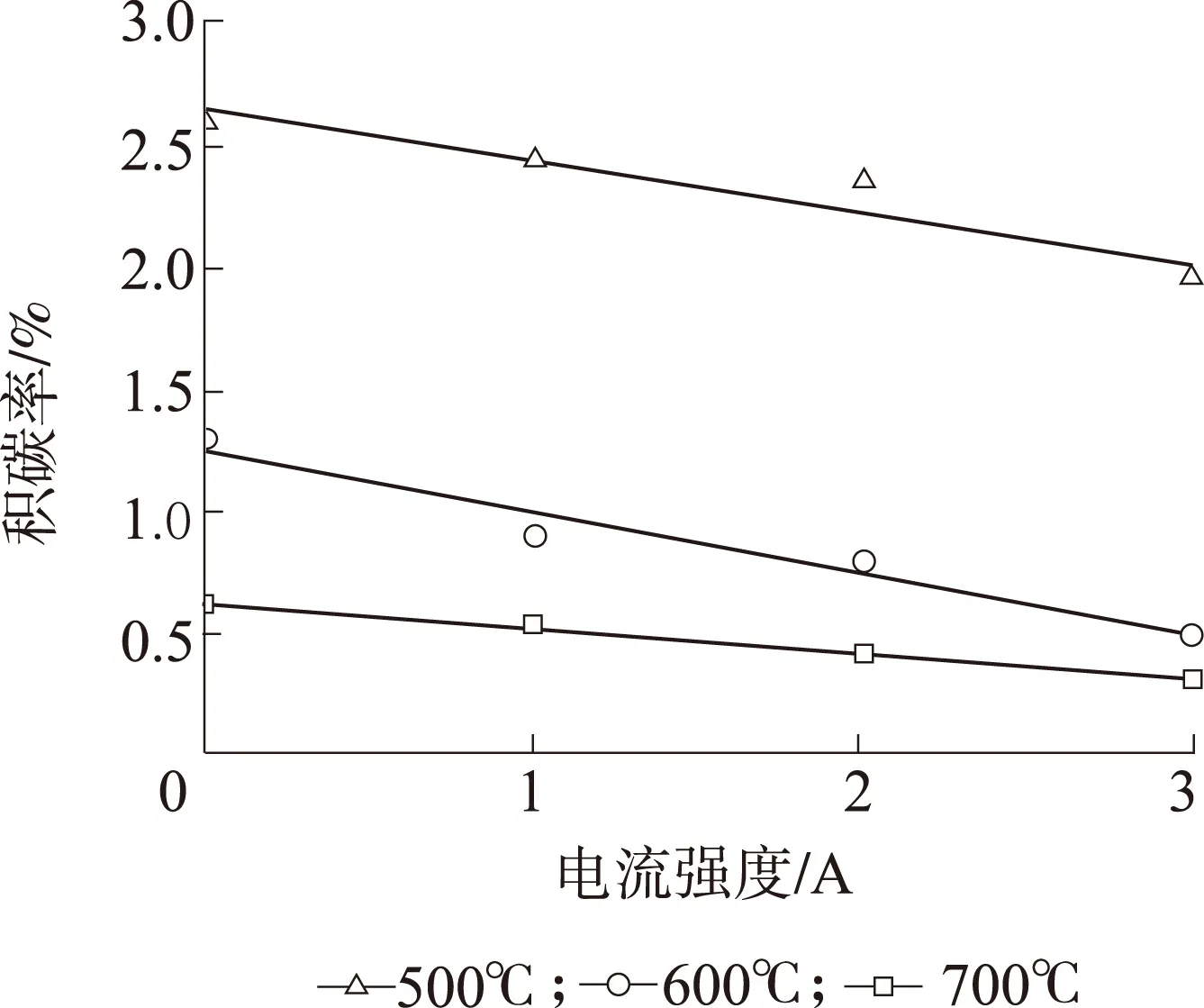
图 4 电流强度与重整温度对催化剂积碳的影响Fig. 4 Effects of electric current intensity and reforming temperature on the catalyst carbon deposit
2.2.3对积碳率的影响图4给出了不同实验条件下催化剂的积碳率。随着重整温度的提高和电流强度的增加,催化剂的积碳率逐渐下降。温度的提升对减少积碳作用明显,当电流为0 A时,温度由500 ℃升高到700 ℃,积碳率由2.6 %下降至0.6 %,可能是因为实验中水蒸气的加入,通过水与碳的反应C+H2O → CO+H2能够有效减少积碳,且该反应为吸热反应;而对于常规的焦油催化裂解,未添加水蒸气时,一定程度上提高温度往往会使得积碳更加严重[23-24]。在温度为500 ℃时,随着电流由0 A增至3 A,催化剂的积碳率由2.6 %降至1.9 %。说明在相同的温度条件下,增大电流能够在一定程度上减少积碳率。
2.3催化剂稳定性测试
为了测试催化剂的稳定性,在600 ℃电流为0 和3 A的条件下分别进行了30 h的稳定性测试,结果如图5所示。由图可知:在电流为0 A的条件下,间甲基苯酚的转化率仅在反应初期保持稳定,随着反应时间的延长,转化率逐渐降低,由初始的90 %降至30 h后的76 %,这一结果清楚地说明,由于间甲基苯酚的热稳定性差,容易在催化剂表面积碳使催化剂活性降低。而在电流为3 A的条件下,间甲基苯酚的转化率在很长一段时间内维持在94 %左右,在反应25 h后才稍有下降;由此可见,电流的引入能够明显提高催化剂的稳定性。此外,稳定性测试过程中,随着反应时间的延长,H2和CO的体积分数略微有下降,而CO2的体积分数稍有上升,CH4的体积分数略微上升,说明产气组成基本保持稳定,电催化方式能够显著提高催化剂的稳定性。

a.0 A; b.3 A图 5 催化剂稳定性测试Fig. 5 Catalytic stability tests
3结 论
3.1采用Ni-CeO2/γ-Al2O3催化剂,对生物质气化焦油含氧模型化合物间甲基苯酚进行电催化水蒸气重整实验。研究表明:采用电催化方式能够显著提高间甲基苯酚的转化率,在使用2.4 g催化剂和立式管式炉的条件下,重整温度为700 ℃、电流为3 A时,间甲基苯酚的转化率达到99.7 %,重整气体产物以H2为主,另外还有一定量的CO和CO2以及少量的CH4。
3.2电流的引入也能够在一定程度上调节产气组成,提高电流强度能够提高产气中CO的体积分数以及单位时间产量、降低催化剂的积碳,并且显著提高催化剂的稳定性。
参考文献:
[1]MILNE T A,ABATZOGLOU N,EVANS R J. Biomass gasifier “Tars”:Their nature,formation,and conversion,NREL/TP-570-25357[R]. Golden:U.S. Department of Engrgy,1998.
[2]PALMA C F. Modelling of tar formation and evolution for biomass gasification:A review[J]. Applied Energy,2013,111(4):129-141.
[3]SHEN Y,YOSHIKAWA K. Recent progresses in catalytic tar elimination during biomass gasification or pyrolysis:A review[J]. Renewable & Sustainable Energy Reviews,2013,21(5):371-392.
[4]江俊飞,应浩,蒋剑春,等. 生物质催化气化研究进展[J]. 生物质化学工程,2012,46(4):52-57.
[5]王夺,刘运权. 生物质气化技术及焦油裂解催化剂的研究进展[J]. 生物质化学工程,2012,46(2):39-47.
[6]BAMPENRAT A,MEEYOO V,KITIYANAN B,et al. Naphthalene steam reforming over Mn-doped CeO2-ZrO2supported nickel catalysts[J]. Applied Catalysis A: General,2010,373(1):154-159.
[7]SEKINE Y,MUKAI D,MURAI Y,et al. Steam reforming of toluene over perovskite-supported Ni catalysts[J]. Applied Catalysis A:General,2013,451(2):160-167.
[8]谢登印,张素平,陈志远,等. Ni/Al2O3改性催化剂催化重整生物油模拟物制氢研究[J]. 燃料化学学报,2015,43(3):302-308.
[9]PARK H J,PARK S H,SOHN J M,et al. Steam reforming of biomass gasification tar using benzene as a model compound over various Ni supported metal oxide catalysts[J]. Bioresource Technology,2009,101(S1):101-103.
[10]ASHOK J,KAWI S. Steam reforming of toluene as a biomass tar model compound over CeO2promoted Ni/CaO-Al2O3catalytic systems[J]. International Journal of hydrogen Energy,2013,38(32):13938-13949.
[11]FERELLA F,STOEHR J,MICHELIS I D,et al. Zirconia and alumina based catalysts for steam reforming of naphthalene[J]. Fuel,2013,105(2):614-629.
[12]GÜELL B M,BABICH I V,LEFFERTS L,et al. Steam reforming of phenol over Ni-based catalysts:A comparative study[J]. Applied Catalysis B:Environmental,2011,106(3/4):280-286.
[13]YUAN Li-xia,YE Tong-qi,GONG Fei-yan,et al. Hydrogen production from the current-enhanced reforming and decomposition of ethanol[J]. Energy & Fuels,2009,23(6):3103-3112.
[14]TAO Kan,XIONG Jia-xing,LI Xing-long,et al. High efficient production of hydrogen from crude bio-oil via an integrative process between gasification and current-enhanced catalytic steam reforming[J]. International Journal of hydrogen Energy,2010,35(2):518-532.
[15]TAO Jun,LU Qiang,DONG Chang-qing,et al. Effects of electric current upon catalytic steam reforming of biomass gasification tar model compounds to syngas[J]. Energy Conversion and Management,2015,100:56-63.
[16]TAO Jun,ZHAO Lei-qiang,DONG Chang-qing,et al. Catalytic steam reforming of toluene as a model compound of biomass gasification tar using Ni-CeO2/SBA-15 catalysts[J]. Energies,2013,6(7):3284-3296.
[17]BARTHOLOMEW C H,FARRAUTO R J. Chemistry of nickel-alumina catalysts[J]. Journal of Catalysis,1976,45(1):41-53.
[18]SWIERCZYNSKI D,COURSON C,KIENNEMANN A. Study of steam reforming of toluene used as model compound of tar produced by biomass gasification[J]. Chemical Engineering and Processing:Process Intensification,2008,47(3):508-513.
[19]TRANE R,DAHL S,SKJØTH-RASMUSSEN M S,et al. Catalytic steam reforming of bio-oil[J]. International Journal of hydrogen Energy,2012,37(8):6447-6472.
[20]ZANUTTINI M S,LAGO C D,QUERINI C A,et al. Deoxygenation ofm-cresol on Pt/γ-Al2O3catalysts[J]. Catalysis Today,2013,213(7):9-17.
[21]LU You-jun,LI Sha,GUO Lie-jin. Hydrogen production by supercritical water gasification of glucose with Ni/CeO2/Al2O3:Effect of Ce loading[J]. Fuel,2013,103(1):193-199.
[22]ZHAO Bao-feng,ZHANG Xiao-dong,CHEN Lei,et al. Steam reforming of toluene as model compound of biomass pyrolysis tar for hydrogen[J]. Biomass and Bioenergy,2010,34(1):140-144.
[23]WU Ceng,LIU Rong-hou. Carbon deposition behavior in steam reforming of bio-oil model compound for hydrogen production[J]. International Journal of hydrogen Energy,2010,35(14):7386-7398.
[24]MENDIARA T,JOHANSEN J M,UTRILLA R,et al. Evaluation of different oxygen carriers for biomass tar reforming (I): Carbon deposition in experiments with toluene[J]. Fuel,2011,90(3):1049-1060.
doi:10.3969/j.issn.1673-5854.2016.04.002
收稿日期:2015-12-28
基金项目:国家自然科学基金资助项目(51576064);中央高校基本科研业务费专项基金(2016YQ05,2015ZZD02)
作者简介:冉泽朋(1990— ),男,河北保定人,硕士生,研究方向:生物质热解气化焦油催化转化研究 *通讯作者:陆 强(1982— ),男,副教授,博士,硕士生导师,研究方向:生物质高效热解转化;E-mail:qianglu@mail.ustc.edu.cn。
中图分类号:TQ35;TK6
文献标识码:A
文章编号:1673-5854(2016)04-0006-07
Electrochemical Catalytic Steam Reforming of m-Cresol with Ni-CeO2/γ-Al2O3Catalyst
RAN Ze-peng, LU Qiang, WANG Xin, HU Bin, DONG Chang-qing
(National Engineering Laboratory for Biomass Power Generation Equipment,North China Electric Power University, Beijing 102206, China)
Abstract:m-Cresol was selected as the oxygenated model compound of biomass gasification tar to study the electrochemical catalytic steam reforming using the Ni-CeO2/γ-Al2O3 as catalyst. Experiments were carried out to reveal the effects of electric current intensity and reforming temperature on the m-cresol conversion,product gas composition and carbon deposition of the catalyst. In addition,the stability tests at 600 ℃ were conducted to evaluate the stability of the catalyst and the improving effect of the electric current on the catalyst stability.The results indicated that the electrochemical catalytic method significantly improved the reforming efficiency of the m-cresol.The conversion rate reached as high as 99.7 % at 700 ℃ and electric current of 3 A with 2.4 g catalyst in the vertical tube furnace.The elevation of the temperature and current intensity could increase the CO volume fraction,and decrease the concentrations of CO2 and H2.Furthermore,the presence of the electric current also reduced the carbon deposition on the catalyst and enhanced the stability of the catalyst.
Key words:tar;electrochemical catalytic steam reforming;m-cresol;Ni-CeO2/γ-Al2O3
·研究报告——生物质能源·
