果胶基载体材料胃靶向载药微丸的制备及应用
2016-08-06李坚斌李辰杨勇何中伟杭方学广西大学轻工与食品工程学院广西南宁530004
李坚斌,李辰,杨勇,何中伟,杭方学(广西大学轻工与食品工程学院,广西南宁530004)
果胶基载体材料胃靶向载药微丸的制备及应用
李坚斌,李辰,杨勇,何中伟,杭方学
(广西大学轻工与食品工程学院,广西南宁530004)
为了使药物在胃靶向长时间的释放,以达到增强局部治疗效果,降低全身毒副作用,起到保健作用。利用低甲氧基果胶,采用滴定法结合果胶钙化改性技术研究制备了胃靶向载药微丸。结果表明:制泡剂CaCO3∶CH3COOH为2∶5(质量比)时,制备的微丸性能最好;SEM观察可知,钙化后的果胶分子,颗粒尺寸减小,颗粒表面有更多的凹槽,有大量的片状层叠和微孔,生成的蛋格结构物使分子更加致密,以使微丸效果更加明显。
果胶;靶向给药系统;胃;控释调控
果胶是一种酸性多糖,由甲酯化的半乳糖醛酸聚合而成,在食品保健工业中常被用作胶凝剂、增稠剂、乳化剂和稳定剂。在药剂学领域,它可用作亲水性乳化剂。目前,药物的研发进入了一个崭新的时代,药物递送系统(drug delivery system,DDS)是药物制剂发展的大势所趋。DDS能够利用特别的载体将药物有效的递送至靶向部位,药物除了能以常规速率释放外,还可以实现定时、定速、定位和靶向释放[1]。靶向给药制剂是目前国内外医药工业发展的重要方向,因为开发周期短,投入少,疗效好,毒副作用小,经济风险低,产品技术含量高且能增强患者用药依从性等优点而被制药企业所青睐[2-4]。
口服胃靶向给药系统是利用制剂的物理化学性质以及胃肠道部位pH、胃肠道酶、制剂在胃肠道的转运机制等生理学性质,使药物在胃特定部位释放的给药系统,有保健的作用。用于载药或营养物微丸的物质有,壳聚糖[5-6],淀粉[7],果胶等,其中果胶较为普遍。刘文利,张良珂等[8]研究了阿西美辛果胶铋凝胶微丸的制备及体外释放,并考察果胶铋凝胶微丸的溶胀及释药性质。WUWenjie等[9]制备了卵磷脂/锌果胶复合微球并研究了其特性。Veronovski A等[10]制备了可降解凝胶,并研究了其在载体材料方面的应用。这些载体材料能够把保健药物及营养物质运送到胃部,对胃健康有重要作用,例如,可将DA-6034[11]和vitamin E[12]等包裹在载体微丸中,运送到特定部位,起到靶向治疗或补充营养的效果。本研究主要采用滴定法对果胶载体材料进行钙化改性,探讨了其基本特性,并利用钙化改性后的果胶载体材料,制备了适合胃靶区的载药微丸,为进一步制备胃靶区给药制剂提供了理论基础。
1 材料与方法
1.1材料与设备
1.1.1材料
果胶(酯化度为15%~25%,食品级):衢州果胶有限公司;VB1(药用级):上海伯奥生物科技有限公司。
1.1.2设备
HJ-3数显恒温磁力搅拌器:上海鸿都电子科技有限公司;DHG-9070A电热恒温鼓风干燥箱:上海精宏实验设备有限公司;RCZ-1A溶出度测定仪:上海黄海药检仪器有限公司;UV-2802S紫外可见分光光度计:尤尼柯(上海)仪器有限公司。
1.2方法
1.2.1钙化果胶的制备
配制果胶溶液,加入制泡剂,搅拌,使其充分分散,得到果胶混悬液。配制CaCl2溶液,加入适量的CH3COOH,搅拌均匀。把果胶混悬液缓慢滴入快速搅拌的CaCl2溶液中,反应成微丸。继续搅拌30 min,减压过滤,充分洗涤3次,40.0℃下真空干燥。
1.2.2钙化果胶漂浮率的测定
取钙化果胶于具塞瓶中,取200.0 mL人工胃液(pH为1.0)为漂浮介质,置于恒温震荡仪中(转速为100 r/min),于第0、5、15 min及0.5、1、2、3、4、5、6、7、8、10、12、20、24 h观察微丸漂浮数目,漂浮率按下公式计算:

1.2.3表面形貌(SEM)
在红外灯照射下,将干燥的样品固定在双面导电胶上。在真空下,对样品进行离子溅射喷金处理,用日本HITACHI S-3400N型扫描电子显微镜观察样品表面形貌。
1.2.4微丸中VB1的体外释放研究
采用《中华人民共和国药典》2010年版二部体外释放度试验方法第一法测定,将不同处方制备的果胶微丸置于500 mL的溶出介质中,温度为(37.5±0.5)℃,调节转速为100 r/min。每0.5 h取样1次,在30 s内完成取样和补充等体积同温释放溶液。样液经0.5 μm微孔滤膜过滤后,以释放溶液做参比溶液,测定其在波长为279 nm时的吸光度。
各时间点校正后的累积溶出百分数为:

式中:AR为药物在t时间内的累积释放率,%;Mt为t时间内药物在缓冲液中的累积浓度,μg/mL;M∞为药物100%释放时缓冲液中的浓度,μg/mL。
2 结果与讨论
2.1钙化果胶胃漂浮微丸
干燥前后微丸形状对比图如图1所示。

图1 干燥前后微丸形状对比Fig.1 Images of microspheres before and after drying
图1左是滴定法制备的果胶钙化胃漂浮微丸,图1右是在40.0℃真空干燥后的微丸。依图1可知,干燥前的微丸比较圆整,干燥后,水分散失,其圆整度降低。不同的干燥方式对微丸的形状有一定影响,对比真空干燥、室温放干、和气流干燥,发现真空干燥得到的微丸的圆整度最好,所以采用真空干燥。
2.2制泡剂配比对微丸外观形态的影响
制泡剂对微丸的圆整度、硬度、气泡数及内部固化程度均有一定的影响,选用CaCO3与CH3COOH(质量比)为制泡剂,由电镜扫描图来研究不同配比对微丸的影响。结果如表1。

表1CaCO3对微丸外观的影响Table 1 Effects on micro pill appearance of CaCO3
据表1可知,(a)制备的微丸,CH3COOH浓度较低,气泡数较少;(c)制备的微丸,CH3COOH浓度较高,气泡数较多,内部固化不完全,微丸硬度差,圆整度差;(b)气泡数适量,内部固化完全,硬度好,圆整度好。经过对比,(b)处方制备的微丸,优于(a)和(c)。
2.3制泡剂配比对微丸漂浮率的影响
制泡剂配比对微丸的漂浮率有一定的影响。不同制泡剂配比制备微丸,测定漂浮率。结果如图2。
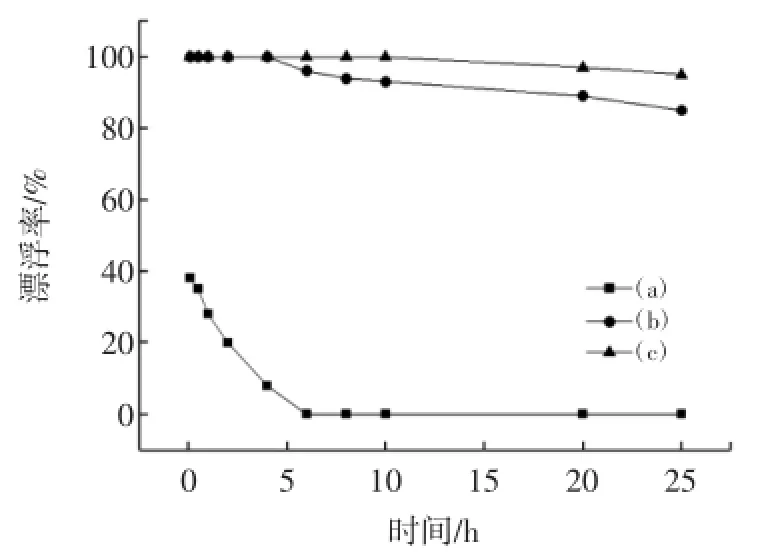
图2CaCO3微丸在人工模拟胃液中的漂浮曲线Fig.2 Floating curve of CaCO3pellet in SGF
依图2可知,CH3COOH浓度较低时,漂浮率很小,如(a)CaCO3/CH3COOH=2∶2,这是因为微丸产生的气泡不足,无法提供足够的浮力供微丸漂浮。随着CH3COOH浓度的增加,微丸的漂浮性能提高,如(b)CaCO3/CH3COOH=2∶5和(c)CaCO3/CH3COOH=2∶10,24 h的漂浮率仍保持在90%以上。CaCO3作制泡剂,不仅能与CH3COOH反应产生气泡,减小微丸的密度达到漂浮,并且在微丸内部产生的Ca2+还可以与果胶发生内部固化,提高微丸的机械强度与气泡存留时间,提高微丸的漂浮性能。
对比(a)、(b)、(c)3个配方制备微丸的外观形态和漂浮率,可知(b)为最佳,选择(b)为胃漂浮微丸的制泡剂。
2.4表面形貌(SEM)
选取果胶、钙化果胶,进行电镜扫描,结果如图3所示。

图3 果胶的电镜扫描图Fig.3 The SEM of pectin
A(a)和A(b)为果胶的扫描电镜图,B(a)和B(b)为钙化果胶的扫描电镜图。依图3可知,果胶钙化后,颗粒尺寸减小,颗粒表面具有更多的凹槽、有大量的片状层叠和微孔,这是因为果胶与金属离子交联之后,生成蛋格结合的金属配合物。
2.5钙化时间对VB1体外释放度的影响
钙化时间对微丸释放度有一定的影响。选择不同的钙化时间的钙化果胶,制备微丸,测定释放度,结果如图4所示。
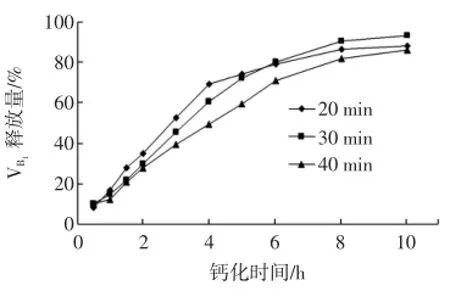
图4 钙化时间对钙化果胶微丸体外释放度的影响Fig.4 Effect of reaction time on the release of pectin-based pellet
依图4可知,钙化时间越长,药物释放越缓慢,控释效果越好。因为钙化时间越长,果胶钙化程度越大,微球内部果胶中游离的羧基与溶液中的钙离子交联的越充分,有助于增强微球的机械强度,所形成的Egg-box结构越紧密,粒径也越小。
3 结论
根据胃靶向漂浮给药系统对载体材料的要求,选择果胶钙化改性技术,考察钙化果胶的水溶性、溶胀度、漂浮性能、结构特征。选择VB1为模型药物,钙化果胶为载体材料,用滴定法制备胃漂浮微丸。研究结果表明,制泡剂CaCO3∶CH3COOH为2∶5(质量比)时,制备的微丸性能最好。SEM观察可知,钙化后的果胶分子,颗粒尺寸减小,颗粒表面有更多的凹槽,有大量的片状层叠和微孔,生成的蛋格结构物使分子更加致密。体外模拟实验表明,钙化时间为30 min时,制备的微丸具有胃靶向释药特性,药物可在胃内持续漂浮10 h,释放度达到90%以上,效果最佳。
[1]梅兴国.把握创新制剂推动我国药业发展新机遇[J].国际药学研究杂志,2010,37(2):89-91
[2]郁丹红.丹参二萜醌组分整体药剂学性质表征及其固体分散体微丸的研究[D].南京:南京中医药大学,2013
[3]陈斌,萧伟,黄洋,等.通脉复方微丸多元释药系统中葛根黄酮速释单元的制备工艺研究[J].中国医院药学杂志,2012,36(12):1243-1248
[4]孙晓英.靶向给药-药剂学研究的热点[J].基础医学论坛,2010,14(16):563-565
[5]Tsai R Y,Chen P W,Kuo T Y,et al.Chitosan/pectin/gum Arabic polyelectrolyte complex:Process-dependent appearance,microstructure analysis and its application[J].Carbohydrate polymers,2014,101(1):752-759
[6]Krum K,Alexander H,Krauland M.Synthesis and in vitro evaluation of a novel thiolated chitosan[J].Biomaterials,2005,269(7):819-826
[7]黄嫣然.淀粉载体材料在模拟人体消化道不同部位的靶向控释调控[D].广州:华南理工大学,2008
[8]刘文利,张景勍,张良珂,等.阿西美辛果胶铋凝胶微丸的制备及体外释放[J].中国医院药学杂志,2010,30(19):1630-1634
[9]WUWenjie,LIWeishuang,ZHAO Yuanhang,et al.Preparation and properties of lecithin/zinc pectin composite microspheres[J].Fuhe Cailiao Xuebao/Acta Materiae Compositae Sinica,2013,30(4):142-147
[10]Veronovski A,Tkalec G,Knez Zˇ,et al.Characterisation of biodegradable pectin aerogels and their potential use as drug carriers[J].Carbohydrate polymers,2014,113:272-278
[11]Jang S W,Lee J W,Park S H,et al.Gastroretentive drug delivery system of DA-6034,a new flavonoid derivative,for the treatment of gastritis[J].Int J Pharm,2008,356(1/2):88-94
[12]Somabarapul S,Pandit S,Gradassi G,et al.Effect of vitamin E TPGS on immune response to nasally delivered diphtheria toxoid loaded Poly(caprolactone)microparticles[J].Int J pharm,2005,298 (2):344-347
Preparation and Application of Pectin-based Carrier Drug Pellets
LI Jian-bin,LI Chen,YANG Yong,HE Zhong-wei,HANG Fang-xue
(Light Industry and Food Engineering Institute,Guangxi University,Nanning 530004,Guangxi,China)
In order to make the drug in the stomach prolonged release of the drug targeting to achieve enhanced local therapeutic effect,reduce systemic side effects,the use of low-methoxy pectin,using the titration method combined with calcification of modified pectin were prepared stomach target to the drug-loaded pellets.The results showed that:the system foam agent CaCO3∶CH3COOH was 2∶5(mass ratio),and performance of the pellets was preferably;SEM observation showed that the pectin molecule calcification after particle size reduction,particle surface more grooves,a large number microporous sheet stack and the resulting egg cell structure of the molecule was more compact,so that the pellets effect was more pronounced.
pectin;targeted drug delivery system;stomach;controlled-release regulation
10.3969/j.issn.1005-6521.2016.10.004
国家自然科学基金项目(20864001;31160326);广西科学研究与技术开发项目(桂科能10100025)
李坚斌(1970—),女(汉),教授,博士生导师,博士,研究方向:糖类物质生物利用及其污染控制。
2015-04-05
