一例暴露因素不明的狂犬病病例的分子流行病学溯源
2016-07-28李幸乐李凤丽孙建伟黄学勇许汴利
李幸乐, 李凤丽, 李 懿, 孙建伟, 黄学勇,许汴利
一例暴露因素不明的狂犬病病例的分子流行病学溯源
李幸乐, 李凤丽, 李懿, 孙建伟, 黄学勇,许汴利
河南省疾病预防控制中心,河南省医学病原生物学重点实验室,郑州450016
摘要:目的对一例暴露因素不明的人狂犬病病例进行实验室确诊,通过分子流行病学分析探索其可能的感染来源。方法通过对存活疑似人狂犬病病例的唾液、脑脊液、血清标本采用直接免疫荧光试验、反转录-聚合酶链式反应和快速荧光灶抑制试验进行实验室确诊;通过时空进化分析探索该病例可能的感染来源。结果病例唾液标本直接免疫荧光试验结果呈阳性,病例血清标本经快速荧光灶抑制试验检测抗狂犬病病毒中和抗体呈阳性。病例唾液标本经反转录-聚合酶链式反应获得狂犬病病毒核蛋白基因预期扩增片段,序列测定进一步证实为狂犬病病毒。该狂犬病病毒株与2011年安徽省一株犬源狂犬病病毒株核苷酸序列同源性最高,为98.4%。结论该疑似狂犬病病例可确诊为狂犬病病例。其发病源于至少2011年以来的某次不自觉的狂犬病病毒感染。
关键词:狂犬病;反转录-聚合酶链式反应;分子流行病学
狂犬病是由狂犬病病毒感染导致的急性致死性疾病,是一种人兽共患病。狂犬病多见于犬、狼、猫等食肉动物和蝙蝠,人类狂犬病绝大多数由病犬咬伤所致,潜伏期长短不一,与伤者年龄、伤口部位、伤口深浅、入侵病毒的数量和毒力等因素有关,多数潜伏期在3个月以内。本研究经过系统的实验室诊断确诊了1例临床典型、暴露因素不明的狂犬病病例,并对该狂犬病病例可能的感染途径进行了探索性分析。现将结果报告如下。
1材料与方法
1.1个案信息及标本采集患者ZXQ, 男,汉族,48岁,农民,河南省新乡市辉县北云门乡南桃固村人。2013年10月2日发病,表现为烦躁、怕风、吞咽困难、不能进水。病症呈反复进行性加重。2013年10月12日因呼吸衰竭死亡。患者入院时神志清醒,自述近期无狂犬病暴露史。查体未发现肉眼可见外伤。河南省疾病预防控制中心于2013年10月7日收集病人唾液混合液标本1份(每间隔3小时采集一次,采集3次);脑脊液标本1份。于2013年10月8日收集血清标本1份。所有标本冷冻保存,备检。
1.2病例标本的直接免疫荧光法检测患者的唾液标本4 ℃ 2 000 r/min 离心20 min,取出上清,唾液沉渣采用PBS制成30%悬液,制片备用。取10 μL唾液沉渣制成的悬液推片,干燥后丙酮固定30 min,弃丙酮,室温干燥5 min;加50 μL以PBS 1∶100稀释的异硫氰酸荧光素标记抗狂犬病病毒核蛋白单克隆抗体(FITC Anti-Rabies Monoclonal Globulin, 含0.1%的1% EVAN's Blue)覆盖玻片上的唾液沉渣,37 ℃湿盒孵育30 min;缓流冲洗弃荧光标记抗狂犬病病毒核蛋白单克隆抗体,PBS振洗2次,水洗1次;干燥后加10 μL 80% 甘油覆盖唾液沉渣;荧光显微镜下观察结果。同时以健康人唾液标本设立阴性对照。
1.3病例标本的反转录-聚合酶链式反应检测采用Qiagen公司(Düsseldorf, NordrheinWestfalen, German)QIAamp Viral RNA Mini Kits病毒RNA提取试剂盒依据说明书操作提取患者唾液、脑脊液标本的病毒RNA。病毒RNA采用Invitrogen公司(Carlsbad, California, USA)SuperScript®III 1st Strand cDNA Synthesis Kits反转录试剂盒依据说明书操作反转录合成cDNA。采用Promega公司(Madison, Wisconsin, USA)GoTaqR Green Master Mix试剂进行巢式聚合酶链式反应,分别针对狂犬病病毒N蛋白进行目的基因片段扩增[1],引物见表1。扩增N蛋白基因时,外引物为PN1-1和PN1-2,内引物为PN2-1和PN2-2。外引物反应条件为:94 ℃预变性3 min;94 ℃变性30 s,56 ℃退火30 s,72 ℃延伸1 min 40 s,共35个循环;72 ℃延伸10 min。内引物反应条件为:94 ℃预变性3 min;94 ℃变性30 s,56 ℃退火30 s,72 ℃延伸40 s,共35个循环;72 ℃延伸10 min。PCR终产物长度约250 bp。
表1病例标本RT-PCR检测用引物
Table.1Primers used in RT-PCR for the samples of patient
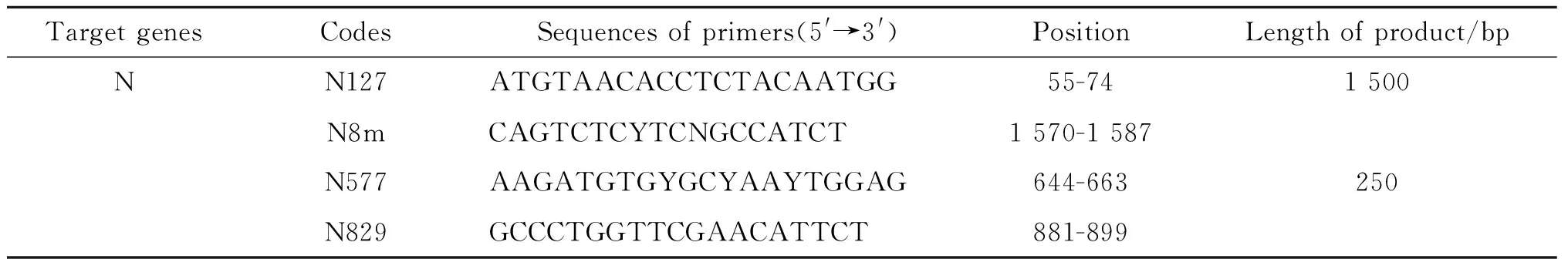
TargetgenesCodesSequencesofprimers(5'→3')PositionLengthofproduct/bpNN127ATGTAACACCTCTACAATGG55-741500N8mCAGTCTCYTCNGCCATCT1570-1587N577AAGATGTGYGCYAAYTGGAG644-663250N829GCCCTGGTTCGAACATTCT881-899
Note: Rabies virus vaccine strain PV2061 (GenBank ID: NC_001542) was used as the template to design primers by the Primer 5.0 software.
1.4核酸序列测定与分析扩增产物送南京金斯瑞生物技术有限公司测序。采用BioEdit 5.0.6版本软件进行序列拼接,采用Clustal X 2.1软件进行序列排列,采用MEGA 4.1软件进行系统进化分析,所有操作按照软件使用说明进行。
1.5病例标本的快速荧光灶抑制试验以96孔细胞培养板作为检测板,每行对应一份样本。按照预先设计的方案于相应行每孔加入100 μL含10% FBS 的DMEM培养液,取病例血清、病例脑脊液、国家标准品(21.4 IU/mL)、阴性血清(0.0 IU/mL)各50 μL分别加入相应行第一孔内,连续进行1∶3倍比稀释,每行最后一孔弃去50 μL混合液,同时设立细胞对照和CVS-11病毒对照;除细胞和病毒对照孔以外每孔加入稀释至80%细胞感染量的CVS-11毒种50 μL,37 ℃中和作用1 h;中和作用结束后每孔加入1×106/mL的BSR细胞悬液50 μL,37 ℃ 5% CO2孵箱培养24 h。然后进行常规的FAT检测,在倒置荧光显微镜下观察检测结果,在记录表中详细记录各样品50%分界点前后孔内荧光染色细胞百分比,代入计算公式内求取各样品中和抗体效价值,单位为IU/mL。
2结果
2.1直接免疫荧光检测结果病例唾液标本检测结果如图1。病例唾液标本和健康人唾液标本区分明显。健康人唾液标本仅见伊文思蓝底染红色正常上皮细胞,无特异性苹果绿染。病例唾液标本除可见伊文思蓝底染以外,几乎在所有视野中都观察到大小、形状不一的特异性性的呈苹果绿色的狂犬病病毒抗原抗体结合物。

1:DFA production of healthy control;2:DFA production of rabies case;3:DFA production of rabies case.图1 狂犬病病例DFA检测结果Fig.1 DFA production of rabies case
2.2反转录-聚合酶链式反应检测结果病例标本检测结果如图2。病例唾液标本经RT-PCR扩增N蛋白,在预期位置获得特异性条带,唾液标本呈阳性反应。
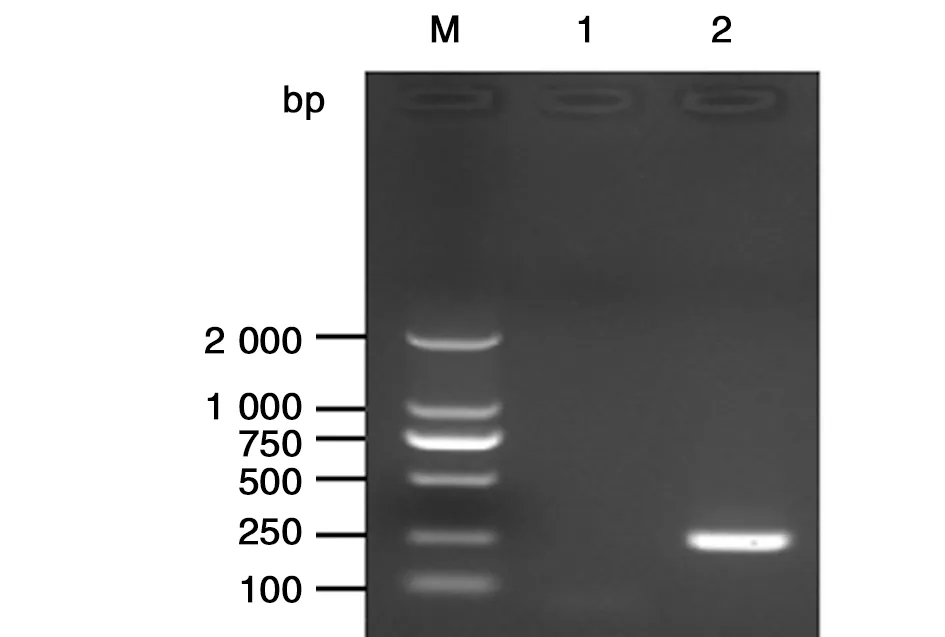
M:DL2000 Marker; 1:RT-PCR production of healthy control;2:RT-PCR production of rabies case.图2 狂犬病病例RT-PCR检测结果Fig.2 RT-PCR production of rabies case
2.3狂犬病病毒N基因系统进化分析及同源性比较病例唾液标本RT-PCR产物经核苷酸序列测定获得狂犬病病毒N蛋白部分核苷酸序列,共250 bp。经NCBI网站BLAST比对显示与2011年安徽省犬源狂犬病病毒株11AF60(GenBank序列号:JQ798953)核苷酸同源性最为接近,为98.4%。在NCBI网站筛选背景清晰的、具有代表性的狂犬病病毒N蛋白基因序列共同进行系统进化分析(如图3)。进化分析结果显示:狂犬病病毒株存在时间、空间和物种聚集性。来自浙江省和江苏省的人源和犬源狂犬病病毒株形成一个相对独立的分支;浙江省和江西省的鼬獾源的狂犬病病毒形成一个相对独立的分支;河南省狂犬病病毒株形成两个相对独立的分支,河南省人源狂犬病病毒株和部分犬源狂犬病病毒株与安徽省犬源狂犬病病毒株亲缘关系接近,河南省部分犬源狂犬病病毒株也形成一个独立分支。
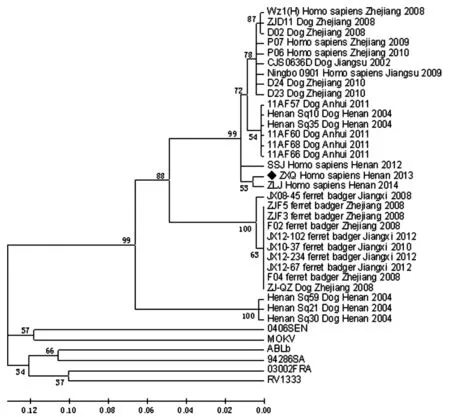
图3 狂犬病病毒N蛋白基因时空进化分析Fig.3 Phylogenetic analysis of N protein genes of rabies viruses
2.4病例抗狂犬病病毒中和抗体检测结果病例脑脊液标本为发病后第6 d脑脊液标本,抗狂犬病病毒中和抗体效价为0.0 IU/mL(<0.05 IU/mL),为阴性。病例血清标本为发病后第7 d的血清标本,抗狂犬病病毒中和抗体效价为0.85 IU/mL(≥0.05 IU/mL),为阳性。
3讨论
该狂犬病病例临床症状典型。实验室检测抗原、核酸均为阳性;病例没有确切的狂犬病暴露史,因此也没有进行狂犬病暴露后免疫,病例血清中的抗狂犬病病毒中和抗体为阳性。所有这些证据均表明该病例为狂犬病病例。该狂犬病病例的特殊性在于没有确切的狂犬病暴露史。病例在病程初期自述近期无狂犬病暴露史。流行病学调查显示病例发病半年前家中开始养犬,拴养,家犬至病例发病一直存活,无异常表现。根据国际社会公认的十日观察法判断,可以排除家犬作为感染来源的可能。病例家属及同村村民因此坚持认为病例的发病源于20多年前一次未经处理的严重犬伤。
狂犬病病毒是一种高度保守的病毒,尤其以狂犬病病毒基因组中的N蛋白核苷酸序列最为保守,大多数毒株N蛋白基因核苷酸序列的同源性大于98%[2]。这种情况下采用分子生物学手段对狂犬病病毒进行溯源似乎并不乐观。中国人狂犬病感染途径单一,狂犬病病毒基因型稳定[3],这种情况则使分子流行病学溯源具有一定的可能性。研究筛选时间、空间和物种等背景清晰的、具有代表性的狂犬病病毒N蛋白基因序列进行时空进化分析。进化分析显示:中国的狂犬病病毒株存在物种聚集性、时间和空间聚集性。这种聚集性是由于同种野生物种在同一时间和空间接触机会多,相互感染导致的结果。犬源狂犬病病毒株除体现一定的物种聚集性以外,与同一时间和空间的其他物种(尤其是人)的亲缘关系存在一定交叉。这恰好证实了在中国,犬是狂犬病感染的几乎唯一来源。经过NCBI网站BLAST比对发现该病例感染的狂犬病病毒株与2011年安徽省犬源狂犬病病毒株11AF60核苷酸同源性最为接近。综合考虑以上两点,我们有理由认为该病例的发病源于至少2011年以来的某次不自觉的狂犬病病毒感染。这也意味着该病例的最长潜伏期不超过两年,与二十多年前的犬伤并无关联。考虑到病例来自犬只管理相对混乱的农村地区[4],因此犬作为感染来源的可能性非常大。
研究在一定程度上解释了病例可能的感染来源和感染时间,但是并没有直接证据。在目前阶段,即使是暴露史明确的狂犬病病例,未必能获得完整的证据链。这在一定程度上是由于狂犬病监测数据的缺失导致的。这种缺失与狂犬病的特殊性以及现阶段公众对狂犬病的认识相关:多数狂犬病病例临床症状典型,无须实验室确诊。同时,实验室诊断只有在病程中晚期才能介入,此时已经失去了狂犬病暴露后预防的最后机会,而且几乎没有治愈的希望。实验室诊断对狂犬病病例似乎没有意义可言。事实上,狂犬病病例的实验室诊断有助于指导犬的免疫和人的免疫[5-6]。狂犬病实验室诊断更为长远的意义在于,通过实验室诊断不断提高狂犬病实验室诊断的能力和水平,完善狂犬病实验室诊断数据。尤其是分子水平的数据。使实验室诊断在狂犬病的预防和治疗中发挥更加重要的作用。由中国科学家研发的重组狂犬病病毒可以阻止狂犬病病毒野毒株感染小鼠的病情进一步发展恶化[7-8]。狂犬病的治疗正在艰难而积极的推进。中国政府已经认识到狂犬病实验室诊断的重要性,将在新的全国狂犬病监测方案中对狂犬病病例的实验室诊断提出要求。力求从各个方面包括实验室诊断方面提高狂犬病的防治水平。
参考文献:
[1] Li XL, Huang XY, Sun JW, et al. Laboratory diagnosis of a human rabies case and its significance[J].survei 11.2014, 29 (3) : 186-190. (in Chinese)
李幸乐, 黄学勇, 孙建伟, 等. 一例狂犬病病例的实验室诊断及其启示[J]. 疾病监测, 2014, 29 (3) : 186-190. DOI:10.3784/j.issn.2014.03.006
[2] Jin Q.Medical molecular virology[M].Version 1 Beijing Science press,2001,619.
金奇. 医学分子病毒学[M]. 北京:科学出版社, 2001,619.
[3] Jiao W, Li H, Tao X, et al. Investigation and analysis of rabies viral infection and distribution in China in 2005-2012[J]. Virol Sin,2013, 28 (3): 183-185. DOI: 10.1007/s12250-013-3324-7
[4] Wang C, Wang Y, Du X, et al. Rabies immunization status of dogs, Beijing, China[J]. Emerg Infect Dis,2011, 17 (6): 1129-1130. DOI: 10.3201/eid/1706.101590
[5] Zhao J, Liu Y, Zhang S, et al. Analysis of an outbreak of human rabies in 2009 in Hanzhong District, Shaanxi province, China[J]. Vector Borne Zoonotic Dis,2011, 11 (1): 59-68. DOI: 10.1089/vbz.2009.0190
[6] Gao LD, Zhang H, Cai L,et al. Epidemic of rabies and effect of its vaccine against a dog that consecutively attacked ten people in one day[J]. Biomed Environ Sci,2014, 27(1):60-64. DOI: 10.3967/bes2014.017
[7] Wang H, Zhang G, Wen Y, et al. Intracerebral administration of recombinant rabies virus expressing GM-CSF prevents the development of rabiesafter infection with street virus[J]. PLoS One,2011,6(9): 1-13. DOI: 10.1371/journal.pone.0025414
[8] Zhou M, Zhang G, Ren G, et al. Recombinant rabies viruses expressing GM-CSF or flagellin are effective vaccines for both intramuscular and oral immunizations[J]. PLoS One,2013,8(5):1-12. DOI: 10.1371/journal.pone.0063384
DOI:10.3969/j.issn.1002-2694.2016.05.011
通讯作者:许汴利,Email:bianlixu@163.com
中图分类号:R373.9
文献标识码:A
文章编号:1002-2694(2016)05-473-04
Corresponding author:XU Bian-li, Email:bianlixu@163.com
收稿日期:2015-11-26修回日期:2016-02-17
Molecular epidemiology analysis of a unknown exposure human rabies
LI Xing-le,LI Feng-li, LI Yi, SUN Jian-wei, HUANG Xue-yong,XU Bian-li
(InstituteforInfectiousDiseaseControlandPrevention,HenanCentersforDiseaseControlandPrevention,Zhengzhou450016,China)
Abstract:Direct immunofluorescence assay (DFA), reverse transcription polymerase chain reaction (RT-PCR), rapid fluorescent focus inhibition test (RFFIT) were used to detect the samples of saliva, cerebrospinal fluid (CSF), serum of a living patient for rabies laboratory diagnosis. The infection source of the unknown exposure of human was analyzed with molecular epidemiology method rabies. Results showed that the rabies virus antigen of the saliva samples of patient was positive. The predicted segments of the nucleoprotein (N) genes of rabies virus was amplified from the saliva samples of patient. Rabies virus neutralizing antibody (RVNP) was proved positive in the serum sample of patient. The rabies virus had the highest nucleotide homology with 11AF60(98.4%).In clusion the suspected human rabies case was diagnosed in laboratory as defined rabies case,and have been infected by rabies virus since 2011.
Key words:rabies; reverse transcription-polymerase chain reaction (RT-PCR); molecular epidemiology analysis This study was supported by the Science and Technology Research Programs in Henan Province-Provincial Program(No. 42102310389)
河南省科技攻关项目(No.42102310389)资助
