儿童华法林药动和药效相关基因型频率和通路富集研究
2016-05-09琳董辰王慧君卢宇蓝周文浩
杨 琳董 辰王慧君 卢宇蓝 周文浩
儿童华法林药动和药效相关基因型频率和通路富集研究
杨琳1董辰1王慧君卢宇蓝周文浩
摘要目的探讨华法林药动和药效相关基因位点的人群频率差异,为华法林药物基因组学研究提供基础数据。方法利用复旦大学附属儿科医院(我院) 620例全外显子测序(WES)数据,对公共数据库中已报道的华法林药物相关位点计算等位基因频率。与千人基因组东亚人和欧洲人的等位基因频率进行比较。结果我院620例WES数据共检测到27个药物相关的多态性位点,涉及12个基因。27个华法林药物相关位点中,3个位点在这3组人群间差异无统计学意义(P≥0.01) ; 10个位点在我院WES数据与千人基因组东亚人等位基因频率差异无统计学意义(P≥0.01)、与千人基因组欧洲人等位基因频率差异有统计学意义(P<0.01) ; 1个位点我院WES数据与千人基因组东亚人等位基因频率差异有统计学意义(P<0.01)、与千人基因组欧洲人等位基因频率差异无统计学意义(P≥0.01) ; 13个位点在我院WES数据与千人基因组东亚人、欧洲人等位基因频率差异均有统计学意义(P<0.01)。结论华法林已报道的药物相关位点存在明显种族差异性,明确其变异为制定华法林个体化给药的精准医疗提供了基础数据。
关键词药物基因组学;全外显子组测序;千人基因组;种族差异;华法林
作者单位复旦大学附属儿科医院分子诊断中心上海,201102; 1共同第一作者
药物基因组学是在药物遗传学基础上,将分子药理学和分子生物学相结合,研究人群对药物产生差异反应的学科[1]。从基因水平揭示个体间遗传特征的差异,将基因测序、遗传学统计和基因表达分析等方法,运用于个体化用药和药物不良反应监测。华法林属于香豆素类口服抗凝药物,通过特异性抑制维生素K环氧化物还原酶(VKOR)的催化反应而发挥抗凝作用[2]。其治疗窗狭窄且剂量个体差异大[3]。华法林的剂量受多重因素(如年龄、性别、药物、饮食、药动和药效相关基因)的影响[4]。目前细胞色素P450 2C9(CYP2C9)和维生素K环氧化物还原酶复合体1 (VKORC1)基因多态性为华法林药物基因组学的研究重点[5,6]。多个成年人华法林剂量预测公式涉及这2个基因的多态性位点[3,7,8]。相比于成人,儿科临床实践中对于个体化用药的需求和药物不良反应的预警更为迫切。
本研究针对华法林已知药动和药效相关基因位点,基于复旦大学附属儿科医院(我院)全外显子组测序(WES)数据,对比千人基因组欧洲人数据和东亚人数据[9],进行相关基因型频率比较,并通过药物相关基因所属通路的富集分析,为华法林药物基因组学研究提供基础数据。
1 方法
1.1纳入标准同意并在我院行WES检测的病例。
1.2DNA提取及全外显子组捕获采用QIAGEN公司mini blood全血试剂盒及其标准DNA抽提方法提取基因组DNA(gDNA),用美国Thermofisher公司生产的NanoDrop紫外分光光度仪测定样本的浓度及定量。参照SureSelct Human All Exon试剂盒说明书,基因组DNA经过超声打断、末端修复、接头连接和杂交捕获。捕获文库采用Illumina HiSeq 2000平台进行序列检测。
1.3测序数据初步分析原始图像文件经Illumina base calling Software 1.7进行图像识别(Base calling),去除污染及接头序列处理后。Clean reads采用Burrows-Wheeler Aligner (BWA)软件v.0.5.9-r16,以人类基因组hg19 (GRCh37)为参考序列进行比对。采用SAMtools软件v.0.1.16,对生成的BAM文件进行排序、合并和去除重复。生成初步分析数据,包括: reads长度分析、数量及总产量、reads比对到参考序列的总序列在基因组中的覆盖度(Coverage)与测序深度(Depth)等。采用GATK软件v.3.2.2进行SNV分析。排除低可信度SNPs:①测序深度<4;②对于一致性的质量评分<20;③邻近区域平均拷贝数>2;④与前1个SNV距离<5 bp。
1.4已知药物敏感位点华法林遗传多态性位点和药物不良反应的关联注释来自PharmGKB数据库,来源为数据库人工整理的具有临床显著意义的变异-药物关联对(Clinical Annotation)。共涉及的变异包括27个多态性位点,关联到12个基因。
1.5统计学方法等位基因频率的统计学差异检验由R软件(版本3.2.1)完成。我院WES数据和千人基因组数据库东亚人和欧洲人等位基因频率的比较采用比率检验(proportion test,对应函数prop.test() )来获取P值。所有检验的P值行Bonferroni矫正(对应函数p.adjust() ),P<0.01为2组位点等位基因频率差异有统计学意义。
2 结果
我院620例行WES检测病例,男325例,女295例。
2.2华法林药物相关位点与千人基因组的比较结果将华法林药物相关位点在我院WES数据分别与千人基因组东亚人、欧洲人等位基因频率进行比较。图1显示,在27个位点中,3个(rs1057910、rs2592551、rs2108622)在这3组人群间差异无统计学意义(P≥0.01) ; 10个位点(rs1131873、rs1799853、rs699664、rs10509680、rs11150606、rs1800566、rs7196161、rs7294、rs339097、rs8050894)在我院WES数据与千人基因组中东亚人等位基因频率差异无统计学意义(P≥0.01)、与千人基因组欧洲人等位基因频率差异有统计学意义(P<0.01) ; 1个位点(rs7900194)在我院WES数据与千人基因组东亚人等位基因频率差异有统计学意义(P<0.01)、与千人基因组欧洲人等位基因频率差异无统计学意义(P≥0.01) ; 13个位点(rs9923231、rs12777823、rs1042580、rs10871454、rs10517、rs61162043、rs1877724、rs12714145、rs2359612、rs2189784、rs2501873、rs3212198、rs4917639)在我院WES数据与千人基因组东亚人、欧洲人等位基因频率差异均有统计学意义(P<0.01)。
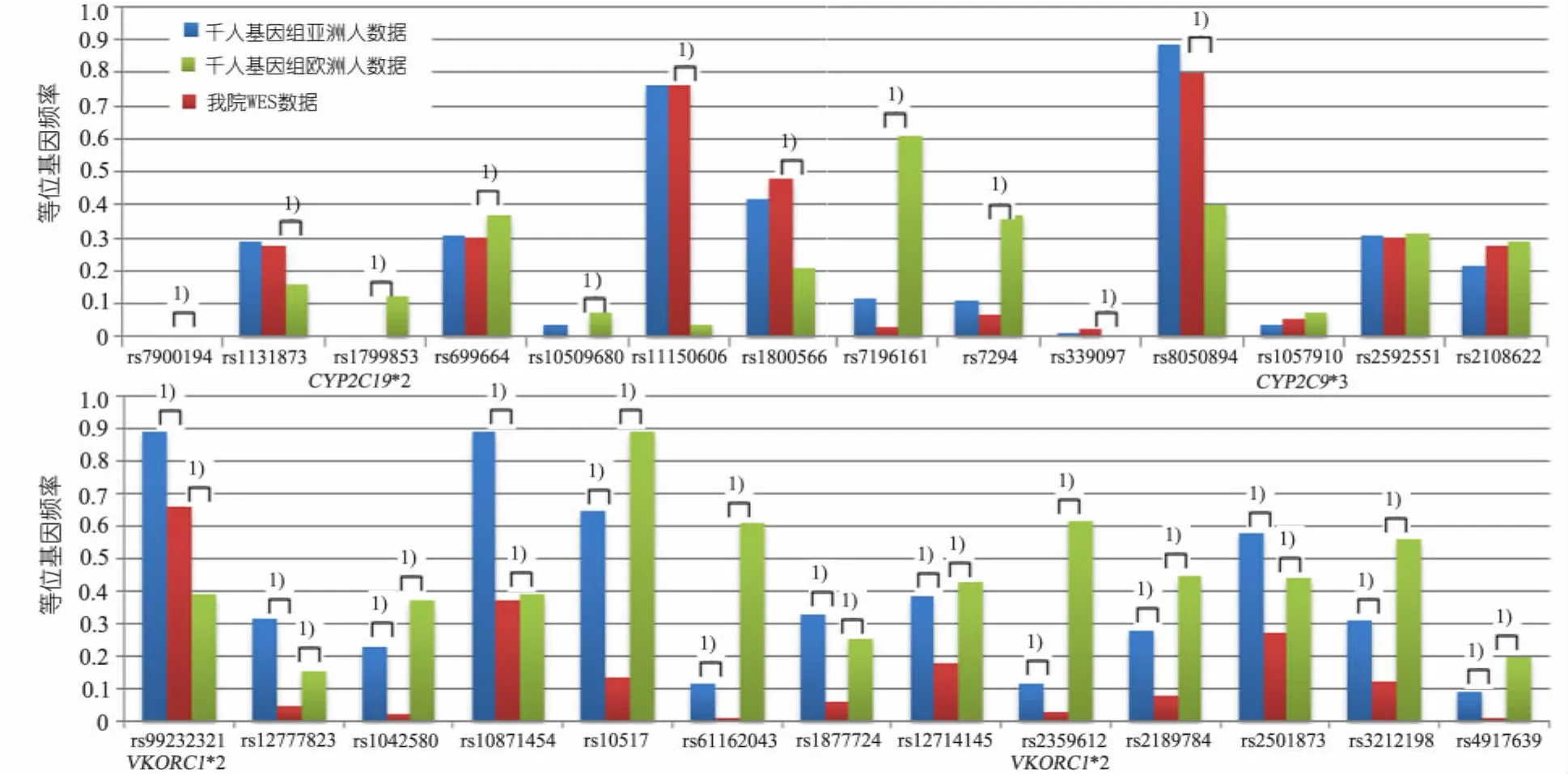
图1 华法林药物相关位点在我院620例WES、千人基因组亚洲人、欧洲人等位基因频率比较注 1)差异有统计学意义,P<0.01
2.3华法林药物相关位点涉及基因分析与华法林相关的变异位点分布在12个基因上,进一步研究这些基因在功能上的联系。String通路富集分析(http: / /string.embl.de)显示,共有9个基因显著地集中到了5个生物通路中。其中主要涉及凝血、出血、体液调节、创伤及外源性物质的代谢(图2)。

图2 华法林药物相关基因的通路富集示意图
3 讨论
临床使用的华法林是两种不同活性的消旋异构体的混合物,S型较R型效能强,占全部效应的60%~70%[10]。图3显示,华法林经口服后,在肠道吸收,肝脏代谢。S型由CYP2C9代谢,R型由CYP1A1、CYP1A2和CYP3A4代谢。由于S型华法林的药理活性更强,且代谢仅依靠CYP2C9通路,所以该基因对于华法林剂量影响较大。CYP2C9基因的多态性主要取决于编码区的SNPs。人类细胞色素P450等位基因命名委员会(http: / /www.cypalleles.ki.se/cyp2c9.htm)已经命名58种SNPs,分别为CYP2C9* 1~CYP2C9* 58。VKORC1基因编码的维生素K环氧化物还原酶(VKOR)是华法林的作用靶点。VKOR催化维生素K从环氧化物到还原型,还原型维生素K是谷氨酰基羧化酶(GGCX)的辅助因子,共同作用下可以激活维生素K依赖的凝血因子及蛋白,通过一系列级联反应启动血液凝固[5,11]。华法林药物剂量计算公式中,主要涉及CYP2C9基因和VKORC1基因。
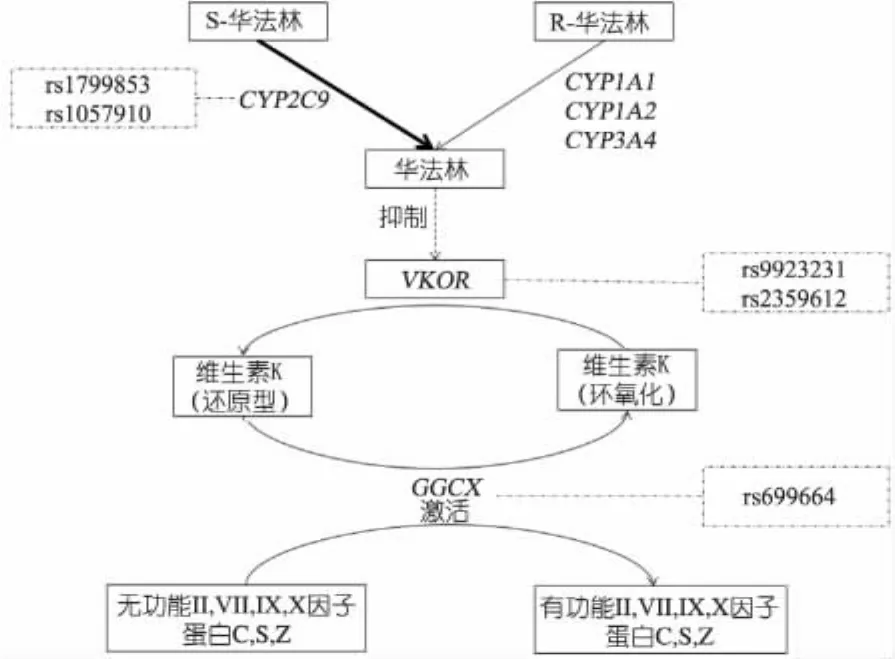
图3 华法林代谢示意图
将华法林药物相关位点在我院WES数据分别与千人基因组东亚人和欧洲人等位基因频率进行比较。在27个位点中,3个位点在这3组人群间差异无统计学意义,证明在不同种族中,这3个位点的基因频率较为一致,其中包括rs1057910,该位点即CYP2C9* 3。这3个位点可能具重要功能而相对保守性较高。
10个位点在我院WES数据与千人基因组东亚人等位基因频率差异无统计学意义,与千人基因组欧洲人数据差异有统计学意义。说明在10个位点中,东亚人与欧洲人可能存在种族差异。其中包括rs1799853(即CYP2C9* 2),说明该位点东亚人与欧洲人存在明显频率差异。该位点在千人基因组中T等位基因频率为东亚人群0.001、欧洲人群0.124、我院WES为0; HapMap数据库中亚洲人群HCB及JPT均为0; AoD数据库中高加索人0.17,HapMap数据库中欧洲人0.104。均提示亚洲人T等位基因频率低于其他人群。因为该位点TT基因型提示需要较低的华法林剂量,而东亚人群T等位基因低频,所以较欧洲人群而言,具有该位点的东亚人群需要较高的华法林剂量。该位点为目前华法林剂量预测公式中的常用位点,但该位点频率在我院WES数据及多个东亚人数据中均为0,该位点作为剂量计算位点对于亚洲人意义不大,故而,目前的华法林公式在进行跨种族人群推广中应特别注意。
仅1个位点(rs7900194)在我院WES数据与千人基因组中东亚人等位基因频率差异有统计学意义,与千人基因组欧洲人数据差异无统计学意义。该位点位于基因CYP2C9。该位点在我院WES数据中频率偏低,接近于千人基因组中欧洲人群数据,可能是由于样本量及位点位置有关。
13个位点在我院WES数据与千人基因组东亚人、欧洲人等位基因频率差异均有统计学意义。其中包括VKORC1基因的rs9923231和rs2359612。rs9923231位点T等位基因频率在千人基因组东亚人群0.88、欧洲人群0.39、我院WES数据为0.66; HapMap数据库东亚人群数据HCB为0.94,JPT为0.90,欧洲人为0.40。均提示东亚人T等位基因频率高于欧洲人群。因为该位点AA基因型提示需要较低的华法林剂量,而东亚人群T等位基因高频,所以较欧洲人群而言,具有该位点的东亚人群需要较低的华法林剂量。rs2359612位点G等位基因频率千人基因组东亚人群为0.12、欧洲人群0.61、我院WES数据为0.026; HapMap数据库中东亚人群HCB为0.058,JPT为0.099,欧洲人为0.60。均提示东亚人G等位基因频率低于欧洲人群。因为该位点AA基因型提示需要较低的华法林剂量,而东亚人群G等位基因低频,所以较欧洲人群而言,具有该位点的东亚人群需要较低的华法林剂量。但需要注意的是,该位点位置为NM_024006.5: c.283 + 837T>C,为内含子区域,WES数据可能会受到捕获区域设定的影响,而影响最终的基因型确定。
华法林药动及药效相关基因富集分析发现(图2),其中7个基因富集到了血液凝固和出血生理过程,包括VKORC1、GGCX、HNF4A、STX4、THBD、CYP4F2和CALU; 7个基因富集到了循环复合物形成的生理过程,包括NR1I3、HNF4A、THBO、EPHX1、VKORC1、CALU和NQO1; 3个基因富集到了药物代谢生理过程,包括CYP4F2、VKORC1 和CYP2C9; 4个基因富集到了对外源刺激反应的生理过程,包括CYP4F2、HNF4A、NQO1和CYP2C9。既往的华法林药物剂量计算公式中,多涉及CYP2C9和VKORC1基因。但从通路富集中可以发现,涉及药物代谢生理过程中,除VKORC1和CYP2C9外,还包括CYP4F2。rs2108622位于CYP4F2基因,该位点等位基因频率在我院WES数据,千人基因组东亚人和欧洲人差异无统计学意义,为高度保守位点。已有研究发现,该位点与华法林剂量存在相关性[12]。是否应该将该位点纳入到华法林剂量公式中,有待进一步研究。已有多个研究报道GGCX基因多态性与华法林剂量相关。GGCX涉及参与血液凝固的维生素K依赖蛋白的活性,为参与凝血及华法林作用机制的重要基因[13]。rs699664位于GGCX基因,该位点我院WES数据与千人基因组中东亚人数据相似,同欧洲人存在显著差异。但该位点与华法林剂量相关文献多来自东亚,在进行剂量相关公式研究中,应考虑到该位点的种族差异性[14,15]。
华法林其处方量可达人口数的0.5%~1.5%[10]。华法林的剂量个体差异性一直是临床药理学的研究热点。多项研究做出了基于CYP2C9基因的多态性位点(rs1799853,rs1057910)和VKORC1基因的多态性位点(rs9923231,rs2359612)的华法林的剂量预测公式。但是目前研究多局限于成人,且由于药物剂量预测公式的外推性差,使这些公式都不能直接用于儿科用药指导。此外,各个剂量预测公式均仅能解释部分的剂量差异,一方面,可能与华法林药效影响因素的复杂性有关,没有将主要的影响因素纳入其中,如纳入预测的位点不足等;另一方面,随着遗传学对种族差异性的深入认识,不同种族中是否应纳入不同的药物相关位点,使用不同的预测公式,也值得深入研究。
综上,目前华法林在儿科的应用缺乏可靠的剂量预测方法,①需要基于大样本的华法林药物位点与疗效的相关性分析;②建立儿科华法林药效评估的可行、可靠方法及相关指标参考值范围;③通过多元线性回归方程对华法林抗凝治疗的个体化精准用药提供预测方法。
参考文献
[1]Johnson JA.Pharmacogenetics: potential for individualized drug therapy through genetics.Trends Genet,2003,19(11) : 660-666
[2]Hirsh J,Fuster V,Ansell J,et al.American Heart Association/American College of Cardiology Foundation guide to warfarin therapy.J Am Coll Cardiol,2003,41(9) : 1633-1652
[3]Limdi NA,McGwin G,Goldstein JA,et al.Influence of CYP2C9 and VKORC1 1173C/T genotype on the risk of hemorrhagic complications in African-American and European-American patients on warfarin.Clin Pharmacol Ther,2008,83 (2) : 312-321
[4]Mega JL,Giugliano RP.Genotype-guided dosing of warfarin.Clin Chem,2014,60(7) : 920-922
[5]Rost S,Fregin A,Ivaskevicius V,et al.Mutations in VKORC1 cause warfarin resistance and multiple coagulation factor deficiency type 2.Nature,2004,427(6974) : 537-541
[6]Sconce EA,Khan TI,Wynne HA,et al.The impact of CYP2C9 and VKORC1 genetic polymorphism and patient characteristics upon warfarin dose requirements: proposal for a new dosing regimen.Blood,2005,106(7) : 2329-2333
[7]Hillman MA,Wilke RA,Yale SH,et al.A prospective,randomized pilot trial of model-based warfarin dose initiation using CYP2C9 genotype and clinical data.Clin Med Res,2005,3(3) : 137-145
[8]Dervieux T,Bala MV.Overview of the pharmacoeconomics of pharmacogenetics.Pharmacogenomics,2006,7(8) : 1175-1184
[9]1000 Genomes Project Consortium,Abecasis GR,Auton A,et al.An integrated map of genetic variation from 1,092 human genomes.Nature,2012,491(7422) : 56-65
[10]Johnson JA,Gong L,Whirl-Carrillo M,et al.Clinical Pharmacogenetics Implementation Consortium Guidelines for CYP2C9 and VKORC1 genotypes and warfarin dosing.Clin Pharmacol Ther,2011,90(4) : 625-629
[11]Li T,Chang CY,Jin DY,et al.Identification of the gene for vitamin K epoxide reductase.Nature,2004,427(6974) : 541-544
[12]Ross KA,Bigham AW,Edwards M,et al.Worldwide allele frequency distribution of four polymorphisms associated with warfarin dose requirements.J Hum Genet,2010,55(9) : 582-589
[13]Wu SM,Cheung WF,Frazier D,et al.Cloning and expression of the cDNA for human gamma-glutamyl carboxylase.Science,1991,254(5038) : 1634-1636
[14]Tian L,Zhang J,Xiao S,et al.Impact of polymorphisms of the GGCX gene on maintenance warfarin dose in Chinese populations: Systematic review and meta-analysis.Meta Gene,2015(1),5: 43-54
[15]Sun Y,Wu Z,Li S,et al.Impact of gamma-glutamyl carboxylase gene polymorphisms on warfarin dose requirement: a systematic review and meta-analysis.Thromb Res,2015,135(4) : 739-747
(本文编辑:张崇凡)
Study on the enrichment of warfarin genotype frequency and pathway associated with its pharmacokinetics and drug effect in children
YANG Lin1,DONG Chen1,WANG Hui-jun,LU Yu-lan,ZHOU Wen-hao(Children's Hospital of Fudan University,Shanghai 201102,China; 1 Co-first author)
Corresponding Author: LU Yu-lan,E-mail: yulanlu@ fudan.edu.cn; ZHOU Wen-hao,E-mail: zwhchfu@126.com
AbstractObjective The study of pharmacogenomics focused on how mutations of essential enzyme genes would lead to different drug response.It would be of great importance to identify warfarin-response-related variants of the patients before clinical treatment,especially for pediatrics.Methods In this study,the allele frequencies of reported clinically significant warfarinresponse-related variants were evaluated based on 620 WES data collected from Children Hospital of Fudan University.Then the local allele frequencies were compared with public population-based databases,including 1000 Genomes project.Results 27 warfarin-response-related variants that have clinical significance were detected in the 620 WES data that we used.These variants were distributed in 12 genes.There were 27 warfarin-related variants,and the frequency of 3 variants in our data showed no difference with European and East Asian population of 1000 Genome project(P≥0.01),10 of them showed no difference with East Asian (P≥0.01) but were significantly different from European population (P<0.01),1 variant showed no difference with European and different fromh East Asian(P≥0.01),and 13 variants were different from both population frequency data(P<0.01).Conclusion Warfarin-response-related variants detected in our database also show population-specificity,which indicates that sufficient genome-wide data preparation are necessary for the personized drug usage and the practice of precise medicine.
Key wordsPharmacogenomics; Whole exome sequencing; 1000 Genome project; Population specificity; Warfarin
(收稿日期:2015-12-30修回日期: 2016-02-01)
通讯作者卢宇蓝,E-mail: yulanlu@ fudan.edu.cn;周文浩,E-mail: zwhchfu@126.com
基金项目市科委/医学领域重点项目子课题,14411950402;上海市卫计委课题:沪卫计科教(2013) 018号
DOI:10.3969/j.issn.1673-5501.2016.01.009
