Fe-MIL-101催化Paal-Knorr反应合成吡咯衍生物
2016-04-08王静静陶柳实
杨 明, 汤 甲, 王静静, 范 爽, 张 欢, 陶柳实, 谭 丽
(1. 北京科技大学材料科学与工程学院, 2. 新材料技术研究院, 北京 100083)
Fe-MIL-101催化Paal-Knorr反应合成吡咯衍生物
杨明1, 汤甲1, 王静静1, 范爽1, 张欢1, 陶柳实1, 谭丽2
(1. 北京科技大学材料科学与工程学院, 2. 新材料技术研究院, 北京 100083)
摘要以Fe-MIL-101为非均相催化剂, 通过多种伯胺与2,5-二甲氧基四氢呋喃进行Paal-Knorr反应, 高效合成相应的吡咯衍生物. 在Fe-MIL-101结构中, 裸露的Fe(Ⅲ)配位点作为催化活性中心参与吡咯衍生物的催化合成反应. 同时Fe-MIL-101的高比表面积和大的孔尺寸确保了底物分子与催化活性中心的充分接触以及产物的自由脱离, 从而促进了催化反应的快速进行. Fe-MIL-101在催化反应过程中具有很好的稳定性, 多次循环使用后仍能表现出良好的催化性能. 此外, 该催化剂在伯胺(包括脂肪胺、芳香胺)与2,5-己二酮的Paal-Knorr缩合反应中也具有优异的催化性能.
关键词Fe-MIL-101非均相催化剂; Paal-Knorr反应; 吡咯衍生物
吡咯及其衍生物作为一类重要的杂环化合物, 在有机合成、药物化学及材料化学等领域具有广泛的应用[1~4]. 目前合成该类化合物的方法很多, 主要包括Hantzsch反应[5,6]、1,3-偶极环加成反应[7]、环化反应[8]和Paal-Knorr反应[9,10]等. 其中, 1,4-二羰基化合物与胺的Paal-Knorr缩合反应是最常用的. 近年来, 均相催化剂如三氟甲基磺酸钪[11]、氨基磺酸[12]、方酸[13]及过渡金属铜盐[14,15]等在Paal-Knorr反应中具有优异的催化活性. 然而均相催化剂存在难以回收再利用、易造成环境污染等问题, 因此非均相催化剂的开发和利用成为解决上述问题的有效途径. 目前已报道的非均相催化剂如PEG-SO3H[16]、Nano-FGT[17,18]和沸石分子筛[19,20]等在Paal-Knorr反应中具有良好的催化效果, 但是上述非均相催化剂仍存在着一些不足, 如催化剂制备过程复杂、目标产物产率低及循环稳定性差等. 因此, 构筑具有活性高、毒性小且循环性能优异的新型非均相催化剂成为目前研究的主要趋势.
金属有机骨架(Metal organic frameworks, MOFs) 是一类由金属离子与有机配体之间通过配位键构筑而成的多孔材料[21~25]. 在MOFs结构中高度分散的金属离子具有不饱和的配位点, 这些具有不饱和配位点的离子可作为催化活性中心参与到催化反应中[26~28]. 同时该类材料还拥有较大的比表面积和孔体积, 有利于反应的快速进行. 目前MOFs在醇的氧化、醛的烃化、烯烃环氧化、缩醛反应、Suzuki偶联反应和硝基的还原等催化反应中均表现出优异的催化性能[22,28~30], 然而MOFs作为非均相催化剂应用于Paal-Knorr反应还较为少见[31].
本文利用Fe(Ⅲ)与有机配体构筑Fe-MOFs(Fe-MIL-101) 多孔材料, 并将其作为非均相催化剂用于Paal-Knorr反应催化合成吡咯及其衍生物. 在Fe-MIL-101的结构中, Fe(Ⅲ)中未饱和的配位点被溶剂分子占用, 通过去溶剂化, 使这些配位点得以裸露, 进而作为活性点位参与催化反应[32]. Fe-MIL-101制备简单, 同时具有较高的比表面积(2670.49 m2/g) 和较大的孔体积(0.75 cm3/g), 有利于Fe(Ⅲ)与底物的充分接触以及产物的脱离, 促进了催化反应的快速进行.
1实验部分
1.1试剂与仪器
对苯二甲酸(H2BDC)和FeCl356H2O, 分析纯, Alfa Aesar(北京) 化学有限公司; 其它试剂均为分析纯, 北京化学试剂公司.
ZEISS SUPRA55型扫描电子显微镜; M21X型X射线衍射仪(XRD), CuKα射线(λ=0.154178 nm); 6700 Thermo Scientific 型红外光谱仪(KBr压片); Agilent 7890A/5975C GCMS气质联用仪.
1.2实验过程
1.2.1Fe-MIL-101的制备将0.658 g(3.96 mmol) 对苯二甲酸和1.07 g(3.96 mmol) FeCl3·6H2O溶解于90 mL DMF中, 并向其中加入3.6 mL乙酸, 分散均匀, 在110 ℃下保温24 h. 反应结束后离心分离, 所得固体产物用DMF和甲醇分别洗涤3次, 最后在80 ℃条件下干燥24 h, 得到砖红色的固体产物Fe-MIL-101. 另外, 为了进一步验证所制材料是Fe-MIL-101, 根据文献[33]方法, 采用微波合成法制备出Fe-MIL-101, 记为MIL-101(Fe).
1.2.2吡咯及其衍生物的催化合成过程将Fe-MIL-101(0.2 mmol) 加入到含有胺(5 mmol)、2,5-二甲氧基四氢呋喃(6 mmol)、水(2 mL)以及以硝基苯(1 mmol)为内标物的混合溶液中, 在100 ℃下磁力搅拌50 min. 反应结束后, 加入适量乙醇稀释, 离心, 上清液通过气相色谱-质谱进行检测分析, 将回收后的催化剂, 用乙醇洗涤3次, 在90 ℃下干燥, 以备循环使用, 催化反应式如下:
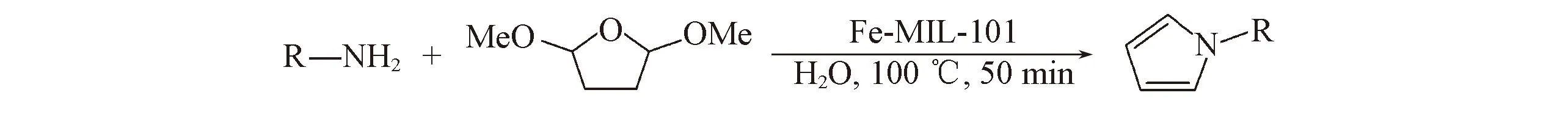
2结果与讨论
2.1催化剂的表征
从图1(A)的SEM照片可以看出, 所制备材料的形貌为正八面体结构, 晶体尺寸均一, 大小约为800 nm. 通过图1(B)的PXRD谱图可以看出, Fe-MIL-101的峰位置和峰型与MIL-101的模拟结构以及采用微波法所制备的MIL-101(Fe)相吻合. 由图1(C)的FTIR谱图可以看出, Fe-MIL-101的特征吸收峰与MIL-101(Fe)也基本吻合, 表明制备了Fe-MIL-101.

Fig.1 SEM image of Fe-MIL-101(A), PXRD patterns(B) of Cr-MIL-101-simulation(a), Fe-MIL-101(b), MIL-101(Fe)(c) and FTIR spectra(C) of Fe-MIL-101(a) and MIL-101(Fe)(b)
2.2不同催化剂对Paal-Knorr反应的影响
为了考察Fe-MIL-101在Paal-Knorr缩合反应中的催化活性, 研究了几种常见的铁源催化剂的催化性能, 结果列于表1. 可以看出, 在无催化剂条件下, 反应60 min后, 苯胺的转化率为20.4%(表1,Entry 1), 以FeCl3·6H2O, Fe(NO3)3·9H2O和Fe2(SO4)3为催化剂时, 苯胺的转化率得到了明显提升, 反应50 min后几乎所有的苯胺都转化成了相应产物(表1, Entries 2~4). 而以配位型的Fe(C5H5)2为催化剂时, 反应50 min后苯胺的转化率仅有13.3%(表1, Entry 5). 在相同反应条件下, 加入含有相同摩尔量Fe(Ⅲ)的Fe-MIL-101后, 苯胺的转化率高达98.9%(表1, Entry 6). Fe-MIL-101中不饱和配位的Fe(Ⅲ)作为催化活性中心能够高效催化Paal-Knorr缩合反应, 同时高的比表面积和大的孔体积保证了Fe(Ⅲ)与底物的充分接触以及产物的脱离. Fe-MIL-101作为一种新型的非均相催化剂, 有望替代传统的均相铁源催化剂高效催化Paal-Knorr缩合反应.
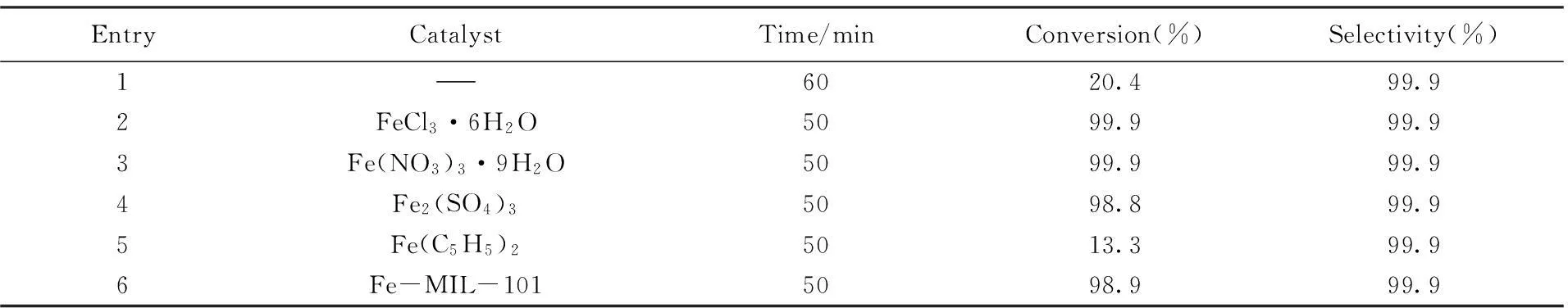
Table 1 Influence of Fe(Ⅲ)-catalysts on the Paal-Knorr reaction conversion*

2.3不同溶剂对Paal-Knorr反应的影响
在不同溶剂下考察Paal-Knorr催化反应, 结果示于表2. 在无溶剂或分别以乙醇、乙腈、三氯甲烷、四氢呋喃及二氯乙烷为溶剂条件下, 苯胺的转化率均比较低(表2, Entries 1~6). 以水为溶剂时, 苯胺转化率高达98.9%(表2中Entry 7), 这可能是由于水分子首先参与2,5-二甲氧基四氢呋喃的水解反应生成2,5-二羟基四氢呋喃, 然后进一步失水生成丁二醛, 进而在催化剂的作用下与苯胺反应生成吡咯产物(图2)[15]. 为了进一步验证水分子在该缩合反应中的重要作用, 在以二氯乙烷为溶剂的体系中引入适量水, 反应50 min后, 其转化率由原来的8.7%(表2中Entry 6) 提升至64.1%(表2中Entry 8), 延长反应时间至180 min, 几乎所有的苯胺转化为相应的产物(表2中Entry 9). 因此, 对于苯胺和2,5-二甲氧基四氢呋喃的Paal-Knorr反应, 水是一种优良的溶剂[34].

Table 2 Influence of different solvents on the Paal-Knorr reaction conversiona
a. Reaction conditions: Fe-MIL-101(0.2 mmol); aniline(5 mmol); tetrahydro-2,5-dimethoxyfuran(6 mmol); nitrobenzene(1 mmol); reaction temperature(100 ℃);b. 2 mL solvent;c. solvent: 2 mL C2H4Cl2+24 mmol water.
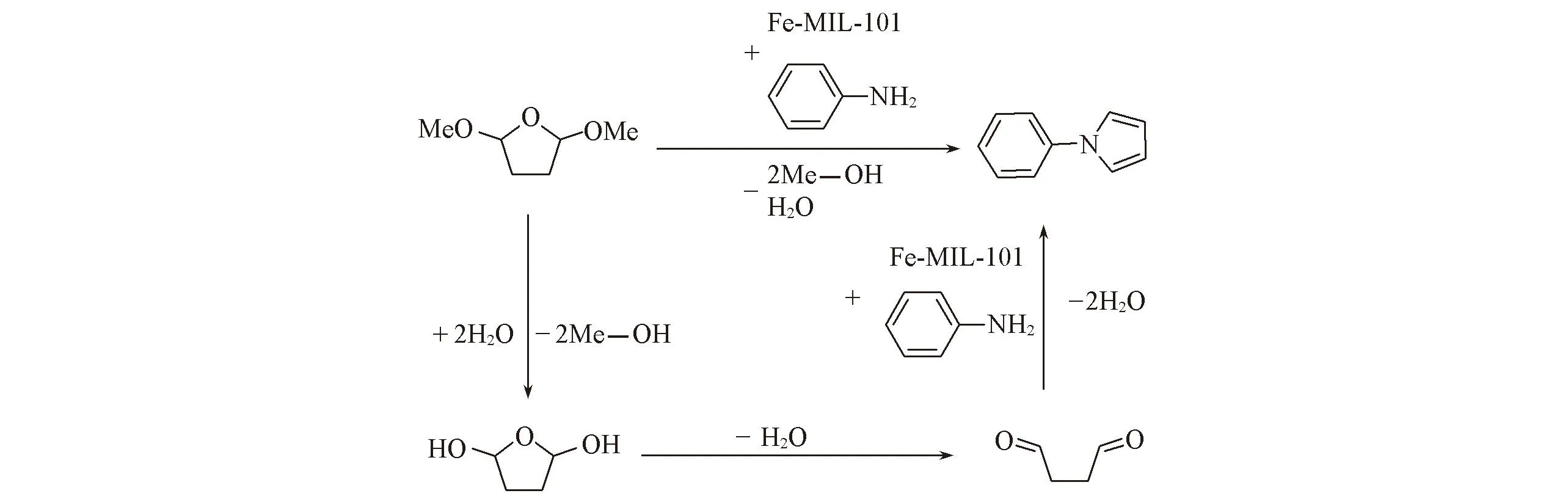
Fig.2 Water involved in the process of the Paal-Knorr reaction
2.4反应温度和时间对Paal-Knorr缩合反应的影响
在反应温度分别为60, 80和100 ℃时, 反应1 h后, 苯胺的转化率分别为1.91%, 37.1%和99.6%(表3中Entries 1, 3和7); 控制反应温度为60 ℃, 反应时间由1 h延长至24 h, 苯胺的转化率则由1.91%提升至46.8%(表3, Entries 1, 2); 当升高反应温度至80 ℃时, 6 h后, 苯胺几乎全部转化为相应产物(表3, Entry 5); 当反应温度升至100 ℃时, 仅需反应50 min, 苯胺的转化率便高达98.9%(表3, Entry 6). 因此, 在后续反应中, 反应温度和时间分别设定为100 ℃和50 min.

Table 3 Influence of temperature and time on the Paal-Knorr reaction conversion*
* Reaction conditions: Fe-MIL-101(0.2 mmol); aniline(5 mmol); tetrahydro-2,5-dimethoxyfuran(6 mmol); nitrobenzene(1 mmol); water(2 mL).
2.5Fe-MIL-101催化伯胺与2,5-二甲氧基四氢呋喃的Paal-Knorr反应
以Fe-MIL-101为催化剂, 催化多种结构的伯胺与2,5-二甲氧基四氢呋喃的Paal-Knorr缩合反应. 由表4可以看出, 取代基在苯环上的不同位置对目标产物的产率影响较微弱(表4, Entries 2~4). 无论芳香伯胺带有给电子基(表4, Entries 4, 5), 还是吸电子基(表4, Entries 6~8), Fe-MIL-101存在的条件下均可以与2,5-二甲氧基四氢呋喃进行Paal-Knorr缩合反应, 高效转化为相应的吡咯衍生物. 这可能是由于中间产物丁二醛较为活泼, 易与伯胺发生亲核-加成反应, 催化反应几乎不受空间位阻和电子效应的影响.
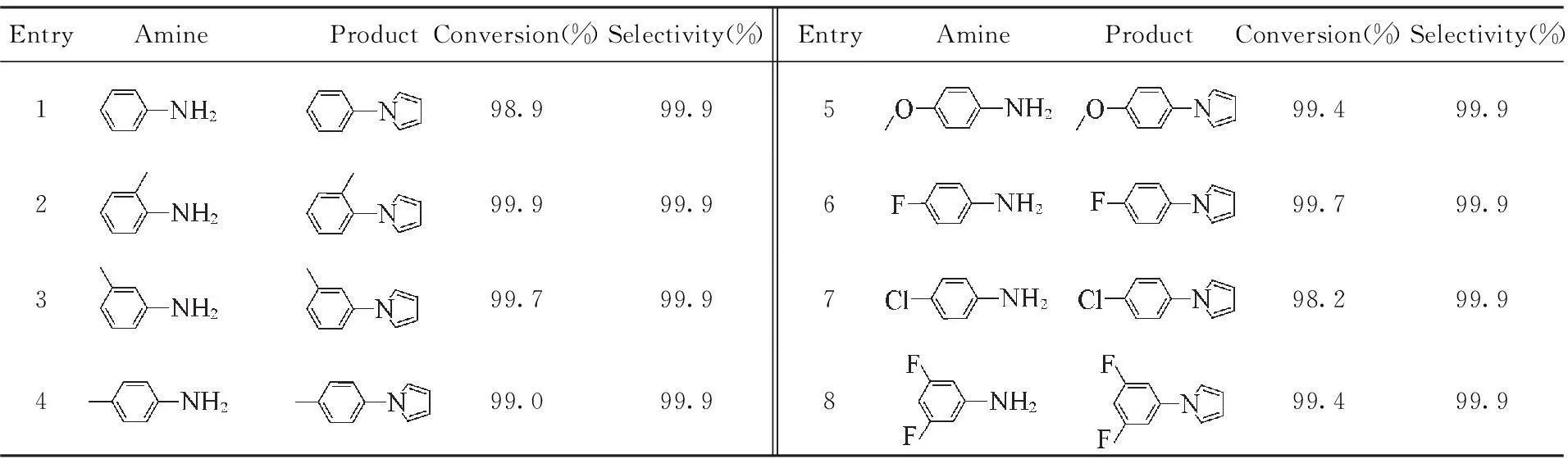
Table 4 Paal-Knorr reaction catalyzed by Fe-MIL-101 between tetrahydro-2,5-dimethoxyfuran and amines*
*. Reaction conditions: Fe-MIL-101(0.2 mmol), amine(5 mmol), tetrahydro-2,5-dimethoxyfuran(6 mmol), nitrobenzene(1 mmol), water(2 mL). Reaction temperature: 100 ℃, reaction time: 50 min.
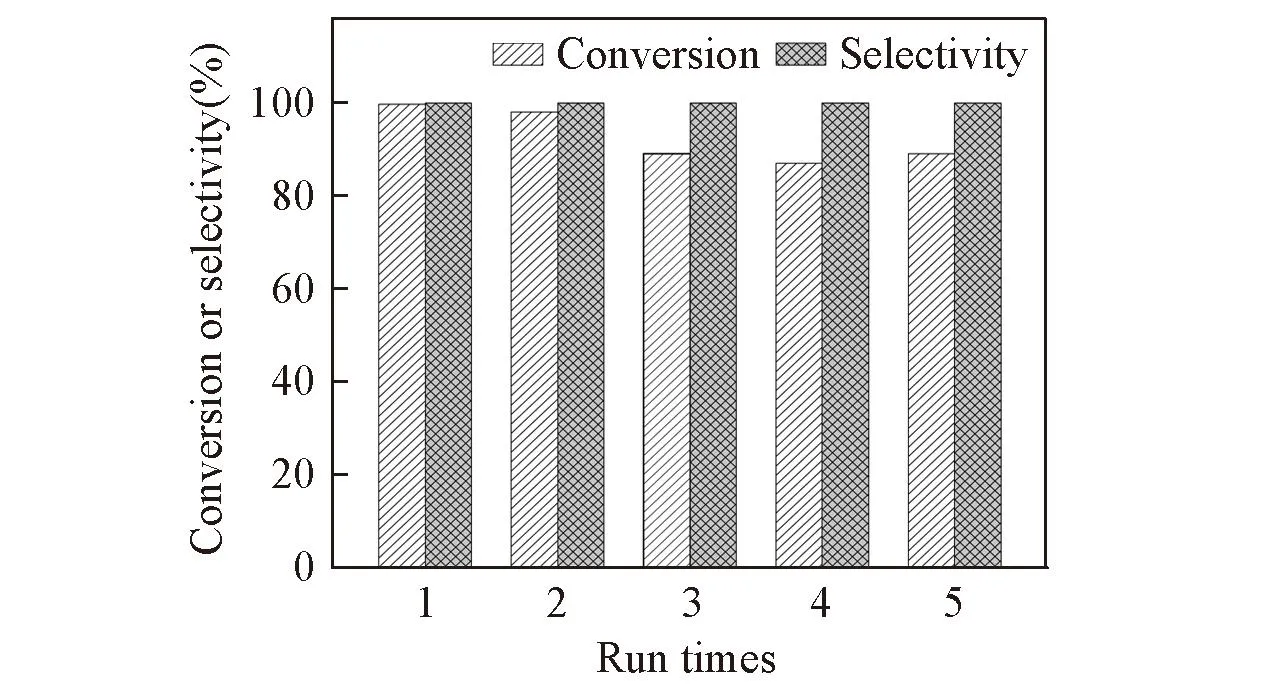
Fig.3 Recycling test of Fe-MIL-101
2.6催化剂的稳定性及循环性能
为了考察Fe-MIL-101在反应体系中的稳定性, 反应结束后, 将催化剂回收并对其进行PXRD和FTIR分析. 结果表明, 回收的催化剂与新制备的催化剂具有相同的衍射峰; FTIR显示催化反应前后的Fe-MIL-101特征吸收峰没有明显变化, 表明Fe-MIL-101具有很好的稳定性. Fe-MIL-101经过5次循环后, 仍然具有较好的催化活性(图3), 第5次催化反应苯胺的转化率仍高于80%.
2.7催化剂应用于伯胺与2,5-己二酮的Paal-Knorr反应体系
为了进一步拓展催化剂Fe-MIL-101在Paal-Knorr缩合反应中的应用, 我们将Fe-MIL-101应用于催化伯胺与2,5-己二酮的Paal-Knorr反应体系中. 由于伯胺和2,5-己二酮可直接发生缩合反应, 无水解过程, 因此该缩合反应可在无溶剂条件下进行. 由表5可知, 多种伯胺与2,5-己二酮均能高效生成相应的吡咯衍生物. 如苯胺与2,5-己二酮反应, 苯胺转化率可高达93.6%(表5, Entry 1). 然而当以邻位甲基苯胺为底物时, 其转化率只有53.2%(表5, Entry 2), 明显低于间位甲基苯胺(93.4%, 表5, Entry 3) 和对位甲基苯胺(99.0%, 表5, Entry 4) 的转化率, 这可能是受到空间位阻的影响; 通过对比带有给电子基芳香胺(表5, Entries 4, 5) 和吸电子基芳香胺(表5, Entries 6, 7) 的催化结果, 发现含有给电子基的芳香胺具有较高的产率[35]. 此外, 结果还表明, 相较于芳香族伯胺, 脂肪族伯胺与2,5-己二酮可更快速地反应生成相应的吡咯衍生物(表5, Entries 8, 9).
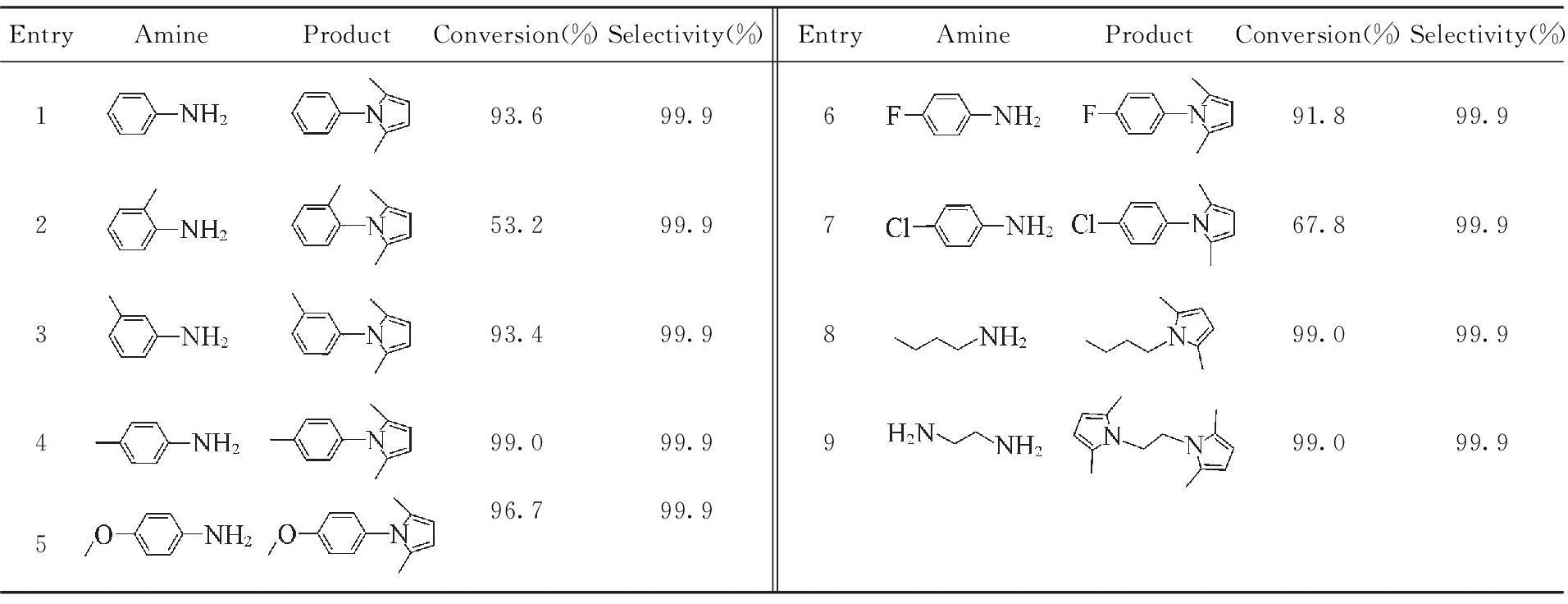
Table 5 Paal-Knorr reaction catalyzed by Fe-MIL-101 between acetonylacetone with amines*
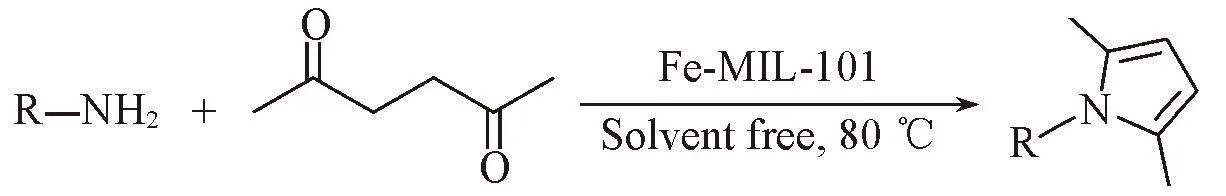
3结论
以Fe-MIL-101为非均相催化剂, 高效催化胺和2,5-二甲氧基四氢呋喃的Paal-Knorr反应, 合成了一系列吡咯衍生物. 不饱和配位的Fe(Ⅲ)高度分散于Fe-MIL-101结构中, 作为催化活性中心参与到吡咯衍生物的合成反应, 同时Fe-MIL-101的高比表面积和大的孔尺寸, 确保了底物分子与催化活性中心的充分接触以及产物的自由脱离, 从而促进了催化反应的快速进行. 该催化剂稳定性好, 多次循环后仍具有较高的催化活性. 此外, 该催化剂在伯胺与2,5-己二酮的Paal-Knorr反应中也表现出很好的催化活性. Fe-MIL-101作为一种新型的非均相催化剂在吡咯衍生物的催化合成中具有巨大的潜在应用价值.
参考文献
[1]Adhikari A., Radhakrishnan S., Vijayan M.,J.Appl.Polym.Sci., 2012, 125, 1875—1881
[2]Andersen R. J., Faulkner D. J., Cun-heng H., van Duyne G. D., Clardy J.,J.Am.Chem.Soc., 1985, 107(19), 5492—5495
[3]Fürstner A.,Angew.Chem.Int.Ed., 2003, 42, 308—311
[4]Dieter R. K., Yu H.,Org.Lett., 2000, 2, 2283—2286
[5]Hantzsch A., Dtsch Ber.,Chem.Ges., 1890, 23, 1474—1476
[6]Ferreira V. F., de Souza M. C. B. V., Cunha A. C., Pereira L. O. R., Ferreira M. L. G.,Org.Prep.Proced.Int., 2001, 33, 411—454
[7]Berree F., Marchand E., Morel G.,TetrahedronLett., 1992, 33, 6155—6158
[8]Lee C. F., Yang I. M., Hwu T. Y., Feng A. S., Tseng J. C., Luh T. Y.,J.Am.Chem.Soc., 2000, 122, 4992—4993
[9]Chiu P. K., Sammes M. P.,Tetrahedron, 1990, 46, 3439—3456
[10]Wang B., Gu Y., Luo C., Yang T., Yang L., Suo J.,TetrahedronLett., 2004, 45, 3417—3419
[11]Chen J. X., Wu H. T., Zheng Z. G., Jin C., Zhang X. X., Su W. K.,TetrahedronLett., 2006, 47, 5383—5387
[12]Luo H. T., Kang Y. R., Li Q., Yang L. M.,Heteroat.Chem., 2008, 19, 144—148
[13]Azizi N., Davoudpour A., Eskandari F., Batebi E.,Monatsh.Chem., 2013, 144, 405—409
[14]Monnier F., Taillefer M.,Angew.Chem.Int.Ed., 2009, 48, 6954—6971
[15]Deng H. J., Fang Y. J., Chen G. W., Liu M. C., Wu H. Y., Chen J. X.,Appl.Organomet.Chem., 2012, 26, 164—167
[16]Jafari A. A., Amini S., Tamaddon F.,J.Appl.Polym.Sci., 2012, 125, 1339—1345
[17]Polshettiwar V., Varma R. S.,Tetrahedron, 2010, 66, 1091—1097
[18]Polshettiwar V., Baruwati B., Varma R. S.,Chem.Commun., 2009, 1837—1839
[19]Sreekumar R., Raghavakaimal P.,Synth.Commun., 1998, 28(9), 1661—1665
[20]Song G. Y., Wang B., Wang G., Kang Y. R., Yang T., Yang L. M.,Synth.Commun., 2005, 35, 1051—1057
[21]Xie S. M., Zhang Z. J., Yuan L. M.,Chem.J.ChineseUniversities, 2014, 35(8), 1652—1657(谢生明, 张泽俊, 袁黎明. 高等学校化学学报, 2014, 35(8), 1652—1657)
[22]Song L. F., Zhang J., Sun L. X., Xu F., Li F., Zhang H. Z., Si X. L., Jiao C. L., Li Z. B., Liu S., Liu Y. L., Zhou H. Y., Sun D., Du Y., Cao Z., Gabelica Z.,EnergyEnviron.Sci., 2012, 5, 7508—7520
[23]Xu L., Chen C., Wang R., Luo J. H., Liu Y. L., Zhang N.,Chem.J.ChineseUniversities, 2013, 34(8), 1907—1912(徐力, 陈超, 王瑞, 罗家还, 刘云凌, 张宁. 高等学校化学学报, 2013, 34(8), 1907—1912)
[24]Furukawa H., Cordova K. E., O’Keeffe M., Yaghi O. M.,Science, 2013, 341, 1230444-1—12
[25]Song F. J., Zhang T., Wang C., Lin W. B.,Proc.R.Soc.A., 2012, 468, 2035—2052
[26]Zhang Y., Yang X. G., Wang Q. Y., Yao J., Hu J., Wang G. Y.,Chem.J.ChineseUniversities, 2014, 35(3), 613—618(张毅, 杨先贵, 王庆印, 姚洁, 胡静, 王公应. 高等学校化学学报, 2014, 35(3), 613—618)
[27]O’Keeffe M., Yaghi O. M.,Chem.Rev., 2012, 112, 675—702
[28]Lee J.Y., Farha O. K., Roberts J., Scheidt K. A., Nguyen S. B. T., Hupp J. T.,Chem.Soc.Rev., 2009, 38, 1450—1459
[29]Tang J., Dong W. J., Wang G., Yao Y. Z., Cai L., Liu Y., Zhao X., Xu J. Q., Tan L.,RSCAdv., 2014, 4, 42977—42982
[30]Tang J., Yang M., Yang M., Dong W. J., Wang G.,NewJ.Chem., 2015, 39, 4919—4923
[31]Phan N. T.S., Nguyen T.T., Luu Q. H., Nguyen L. T. L.,J.Mol.Catal.A:Chem., 2012, 363/364, 178—185
[32]Dhakshinamoorthy A., Alvaro M., Garcia H.,Adv.Synth.Catal., 2010, 352, 3022—3030
[33]Kathryn M. L., Pashow T., Rocca J. D., Xie Z. G., Tran S., Lin W. B.,J.Am.Chem.Soc., 2009, 131, 14261—14263
[34]Azizi N., Khajeh-Amiri A., Ghafuri H., Bolourtchian M., Saidi M. R.,Synlett., 2009, 14, 2245—2248
[35]Wang F. H., Zhu X. D., Miao H.,J.AnhuiPoly.Univ., 2014, 29(2), 26—30(王芬华, 朱贤东, 苗慧. 安徽工程大学学报, 2014, 29(2), 26—30)
Paal-Knorr Reaction Catalyzed by Fe-MIL-101 for
Efficient Synthesis of Pyrroles†
YANG Ming1, TANG Jia1, WANG Jingjing1, FAN Shuang1,
ZHANG Huan1, TAO Liushi1, TAN Li2*
(1.SchoolofMaterialsScienceandEngineering, 2.InstituteforAdvancedMaterialsandTechnology,
UniversityofScienceandTechnologyBeijing,Beijing100083,China)
AbstractA highly porous metal-organic frameworks(Fe-MIL-101) was synthesized as a heterogeneous catalyst for the Paal-Knorr reaction. The free coordination position of Fe(Ⅲ) in Fe-MIL-101 can be used as catalytic active sites for the Paal-Knorr reaction. The large surface area and pore size of Fe-MIL-101 contribute to offer an access for organic substrates to the active sites sufficiently, which ensure a high catalytic performance of Fe-MIL-101 for pyrroles. The catalyst could be reused five times without loss of its catalytic activity. In addition, the catalyst also exhibits high catalytic activity in other amines system with 2,5-hexane-dione for Paal-Knorr condensation reaction.
KeywordsFe-MIL-101 heterogeneous catalyst; Paal-Knorr reaction; Pyrrole derivative
(Ed.: V, Z)
† Supported by the Fundamental Research Funds for the Central Universities, China(No.FRF-TP-14-061A1).
doi:10.7503/cjcu20150450
基金项目:中央高校基本科研业务费专项资金(批准号: FTF-TP-14-061A1)资助.
收稿日期:2015-06-12. 网络出版日期: 2015-12-20.
中图分类号O643
文献标志码A
联系人简介: 谭丽, 女, 博士, 工程师, 主要从事催化材料研究. E-mail: tljw060606@163.com
