超高效液相色谱法同时测定食品塑料包装材料中的紫外吸收剂和抗氧化剂
2016-03-24陈立伟吴楚森吴玉銮罗海英
陈立伟,吴楚森,汪 毅,吴玉銮,王 莉,董 浩,王 斌,罗海英
(广州质量监督检测研究院,国家包装产品质量监督检验中心(广州),广东 广州 511447)
研究简报
超高效液相色谱法同时测定食品塑料包装材料中的紫外吸收剂和抗氧化剂
陈立伟,吴楚森,汪毅,吴玉銮*,王莉,董浩,王斌,罗海英
(广州质量监督检测研究院,国家包装产品质量监督检验中心(广州),广东广州511447)
摘要:超声萃取结合超高效液相色谱(UPLC)技术,建立了食品塑料包装材料中14种紫外吸收剂及抗氧化剂(UV-0,UV-9,UV-71,UV-329,UV-326,UV-327,UV-234,UV-360,抗氧化剂2246,抗氧化剂425,TH-1790,抗氧化剂3114,抗氧化剂1010和抗氧化剂1076)的高通量检测方法。样品经三氯甲烷-甲醇超声提取,C18色谱柱分离后,乙腈和0.1%甲酸水为流动相梯度洗脱,二极管阵列检测器测定。14种物质在一定的浓度范围内线性关系良好,相关系数(r2)均不低于0.999 2,方法定量下限(S/N=10)为 8.0~33.0 mg/kg,平均回收率为83.6%~116.2%,相对标准偏差(RSD,n=6)为1.3%~9.5%。方法具有前处理简单、净化效果好等特点,适用于食品塑料包装中14种紫外吸收剂及抗氧化剂的同时测定。
关键词:紫外吸收剂;抗氧化剂;食品塑料包装;超高效液相色谱法
紫外吸收剂是一种光稳定剂,添加到塑料和其他高分子材料中可选择性吸收高能量的紫外线,使之变成无害的能量而释放或消耗,进而延长材料的使用寿命。抗氧化剂是一种化学添加剂,常用来抑制和延缓聚合物材料氧化和降解[1]。研究表明,部分紫外吸收剂和抗氧化剂有毒有害,长期摄入将对机体的生殖、发育、神经系统、免疫系统等产生多方面影响[2-3],如酚类抗氧化剂具有弱雌激素效应,即使在摄入量很低的情况下,也可能会给人体健康带来危害[4]。紫外吸收剂(2-羟基-4-甲氧基苯基)苯基甲酮(UV-9)等含羟基的衍生物均具有雌激素活性,并且其雌激素活性强于双酚A[5]。GB9685-2008《食品容器、包装材料用添加剂使用卫生标准》[6]对UV-9,UV-71,UV-329,UV-326,UV-327,UV-234 和UV-360等紫外吸收剂,以及2246,425,TH-1790,3114,1010和1076等抗氧化剂均提出限量要求。因此,建立食品塑料包装材料中紫外吸收剂和抗氧化剂的快速、准确检测方法,有利于对食品塑料包装材料中可能超量使用的紫外吸收剂和抗氧化剂行为进行监管。
目前食品包装材料中紫外吸收剂和抗氧化剂的测定方法主要有液相色谱法[7-9]、气相色谱-质谱法[10-11]以及液相色谱-串联质谱法[12]等;前处理方法主要有索氏提取(SE)[13-14]、快速溶剂萃取(ASE)[15-16]、微波辅助提取(MAE)[17-18]、超临界流体萃取(SFE)[19]、超声萃取(UE)[20-21]等。UPLC法分离效率高和分析时间短的优点已在多残留分析中得到充分体现,超声萃取技术因成本低、溶剂消耗量小在样品前处理中也得到广泛应用。
本文利用UPLC和超声萃取技术的特点,通过对样品前处理以及色谱检测条件的优化,建立了食品塑料包装材料中UV-0,UV-9,UV-71,UV-329,UV-326,UV-327,UV-234,UV-360,抗氧化剂2246,抗氧化剂425,TH-1790,抗氧化剂3114,抗氧化剂1010和抗氧化剂1076(结构式见图1)等14种物质的UPLC同时测定方法。

图1 14种分析物的化学结构Fig.1 Chemical structures of 14 kinds of analytes
1实验部分
1.1仪器、试剂与材料
ACQUITYTM超高效液相色谱仪配二极管阵列检测器(UPLC,美国Waters公司),MS2 Minshaker涡旋振荡器(德国IKA公司),N-EVAP 112水浴氮吹仪(美国OA公司),KDC-400低速离心机(科大创新公司),KQ-500E超声波清洗器(昆山市超声仪器有限公司),Milli-Q去离子水发生器(美国Millipore公司)。
UV-0,UV-9,UV-71,UV-234,UV-326,UV-327,UV-329,UV-360,TH-1790,抗氧化剂1076,抗氧化剂2246,抗氧化剂425,抗氧化剂1010标准品(上海安谱科学仪器有限公司),抗氧化剂3114(瑞士Adamas Reagent公司),乙腈、丙酮、甲醇(色谱纯,美国Fisher公司),甲酸(色谱纯,上海安谱科学仪器有限公司),三氯甲烷(分析纯,广州化学试剂厂)。
分别准确称取各标准物质10.0 mg,配制成1 000 mg/L的标准储备溶液,置于4 ℃冰箱冷藏保存。其中UV-0,UV-9,TH-1790,抗氧化剂2246,抗氧化剂425用甲醇溶解并定容制得标准储备溶液;抗氧化剂1076和1010用少量丙酮溶解,甲醇定容制得标准储备溶液;UV-71,UV-327,UV-329和抗氧化剂3114用少量甲苯溶解,甲醇定容制得标准储备溶液;UV-234,UV-326和UV-360用少量二氯甲烷溶解,甲醇定容制得标准储备溶液。使用时,用甲醇稀释成所需浓度的混合标准工作液。
分析样品:食品包装塑料样品10个,均购自广州本地超市。
1.2超高效液相色谱条件
色谱柱:ACQUITY UPLC BEH C18(2.1 mm×50 mm,1.7 μm);流动相:A为0.1%甲酸水溶液,B为乙腈;梯度洗脱程序:0~4 min,60% B;4~7 min,60%~85% B;7~12 min,85% B;12~13 min,85%~100% B;13~25 min,100%B;25~26 min,100%~60%B;26~29 min,60%B;流速:0.2 mL/min;进样量:2.0 μL;紫外检测波长:275 nm;柱温:30 ℃。
1.3样品处理
将食品塑料包装样品剪碎(约5 mm×5 mm小片),混合均匀,准确称取0.5 g(精确至0.001 g)样品于25 mL具塞比色管中,加入5 mL三氯甲烷,涡旋振荡2 min使塑料溶解,边涡旋边缓慢加入20 mL甲醇,超声30 min,基质析出后,以4 000 r/min离心5 min,收集上清液10 mL于40 ℃水浴中氮气吹干,加入1.0 mL甲醇复溶,涡旋摇匀,过0.22 μm滤膜供UPLC测定。

图2 不同提取溶剂对食品塑料包装材料中14种待测物提取回收率的影响Fig.2 Effects of different solvents on recoveries of 14 analytes in plastic food packing materials
2结果与讨论
2.1萃取溶剂的选择
由于大多数食品塑料包装材料是结晶态聚合物,分子间相互作用力较强,溶剂分子不易渗入聚合物内部,因此在选择提取溶剂时,除要充分考虑溶剂对目标物质的溶解能力外,还要选择能溶胀高分子聚合物制品的溶剂。研究表明[22],采用主辅溶剂混合提取的效果较好,其中一种溶剂为高分子聚合物溶胀剂,打开溶剂的萃取通道,而另一种溶剂则对目标物质有着较好的溶解度,并对高分子聚合物有沉淀作用[4]。本文采用三氯甲烷将样品分散后,比较了极性由强到弱的乙腈、甲醇、乙酸乙酯、正己烷作为提取溶剂时对加标100 mg/kg的食品塑料包装样品中目标物的提取效果(见图2)。由图2可见,甲醇的提取回收率最高,对14种目标物的溶解性最好,乙腈、正己烷对目标物的提取能力较低,乙酸乙酯的溶解性最低,所以本文选用三氯甲烷和甲醇作为提取溶剂。由于甲醇为塑料高分子样品的沉淀剂,为避免高分子聚合物沉淀过快而将待测物重新包裹成胶块,对检测结果造成影响,因此应在涡旋振荡器操作下缓慢滴加甲醇。

图3 超声时间对食品塑料包装材料中14种待测物提取回收率的影响Fig.3 Effects of different ultrasonic extraction times on recoveries of 14 analytes in plastic food packing materials
2.2超声时间的选择
研究了超声时间对提取效率的影响,选择0.5 g塑料样品,加入1 000.0 mg/L的标准溶液250 μL,放置0.5 h至完全吸收后,用三氯甲烷-甲醇提取,在超声功率为250 W,超声温度为25 ℃的条件下,分别考察了超声5,10,20,30,40 min的提取效果,结果如图3所示。
由图3可以看出,当超声时间小于30 min时,14种待测物未能充分提取出;当超声时间大于30 min时,紫外吸收剂的回收率略有上升,但抗氧化剂的回收率有不同程度的下降或趋于平缓。这可能是因为随着提取时间的增加,抗氧化剂在提取过程中因氧化而造成的损失也增大,致使回收率下降。由于超声40 min时紫外吸收剂的回收率与超声30 min时差别不大,但抗氧化剂的回收率下降,因此实验选择超声提取时间为30 min。
2.3分离条件的优化
目前液相色谱法最常用的色谱柱为C18柱,为了满足不同样品分离分析的要求,主要通过改变流动相组成来调节色谱柱的保留范围和选择性[23]。常用的有机流动相为甲醇和乙腈,水相为超纯水或缓冲溶液。本文首先考察了乙腈-水作为流动相时的洗脱效果,发现先出峰的目标分析物色谱峰变形,峰形不对称,且抗氧化剂3114和UV-327不能较好的分离。而在水相中加入0.1%甲酸后,待测化合物的峰形变好,因此选用乙腈-0.1%甲酸水作为流动相。
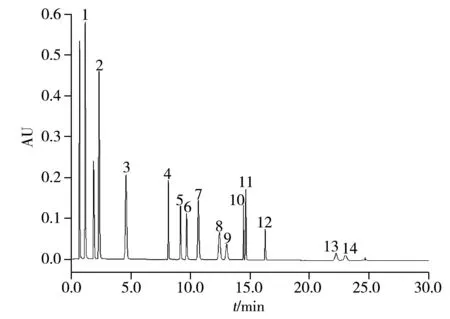
图4 14种目标化合物的色谱图(浓度100 mg/L,λ=275 nm)Fig.4 Chromatogram of 14 target analytes of 100 mg/L(λ=275 nm)1.UV-0,2.UV-9,3.UV-71,4.antioxidant 2246,5.antioxidant 425,6.TH-1790,7.UV-329,8.UV-326,9.UV-234,10.antioxidant 3114,11.UV-327,12.antioxidant 1010,13.UV-360,14.antioxidant 1076
本文研究的14种物质极性范围较宽,采用等度洗脱无法将结构和性质相似的苯并三唑类化合物UV-329,UV-326,UV-327,UV-234等分离开,为了提高极性相似化合物的分离度,改善化合物的峰形,比较了不同梯度洗脱程序对14种目标物质的洗脱效果。结果表明,当初始有机相比例为70%时,出峰时间快的目标物质不能有效分离;当初始有机相比例为60%,并延长有机相比例为85%的保持时间时,UV-327和抗氧化剂3114的峰重叠,14种待测物质不能完全分离开,抗氧化剂1076未出峰;当采用“1.2”所示的梯度洗脱程序时,14种目标物质得到了较好的分离,且响应较高,因此选用乙腈-0.1%甲酸水流动相体系梯度洗脱分离14种目标物。
在上述优化条件下,14种目标物质混合标准溶液的UPLC色谱图如图4所示,由图可见14种化合物获得了较好的分离。
2.4线性关系与检出限
按“1.1”方法配制14种待测物的系列混合标准工作液,其中UV-0,UV-9,UV-71,UV-329,UV-326,UV-327和UV-360的浓度分别为1.5,15.0,50.0,100.0,200.0 mg/L;抗氧化剂2246,425,TH-1790,3114和1010的浓度分别为3.0,10.0,50.0,100.0,200.0,300.0 mg/L;UV-234和抗氧化剂1076的浓度分别为5.0,20.0,50.0,100.0,200.0,500.0 mg/L。在优化条件下进行检测,以各待测物的峰面积为纵坐标(y),相应的质量浓度为横坐标(x,mg/L)作曲线,得到各待测物的线性方程。以各待测物3倍信噪比的响应值对应的浓度作为仪器的检出限(LOD,S/N=3),结合前处理条件的稀释倍数,确定方法的定量下限(MLOQ,S/N=10)。
14种待测物的线性回归方程、相关系数、仪器检出限和方法定量下限见表1。14种待测物在相应的浓度范围内线性关系良好,相关系数均不低于0.999 2,LOD为0.5~2.0 mg/L,MLOQ为8.0~33.0 mg/kg。

表1 14种待测物的线性方程、相关系数、仪器检出限和方法定量下限
2.5回收率与精密度
选取阴性塑料样品分别进行3个水平(MLOQ,2×MLOQ,10×MLOQ)的加标回收实验,6次平行实验的结果见表2。结果表明,在加标浓度范围内,14种待测物的平均回收率为83.6%~116.2%,相对标准偏差(RSD)为1.3%~9.5%,该方法具有良好的回收率与精密度。

表2 回收率和精密度测定结果(n=6)
2.6实际样品检测
使用本方法测定了PP,PS,PE等不同类型的10个食品塑料包装材料样品,结果见表3。从表3可以看出,有6个样品检出抗氧化剂2246,1010和1076,紫外吸收剂均未检出。其中4个样品中分别检出抗氧化剂1076和抗氧化剂2246,检出含量分别为42~70 mg/kg和20~37 mg/kg;3个样品中检出抗氧化剂1010,检出含量为134~175 mg/kg。各种样品中抗氧化剂的检出含量均符合GB9685-2008的安全要求。图5为检出目标物的塑料杯样品的色谱图。

表3 市售食品塑料包装材料中抗氧化剂的含量(mg/kg)
-:no detected

图5 市售塑料杯样品检出目标物的色谱图Fig.5 Chromatogram of the targets in a plastic bottle sample
3结论
建立了超声萃取结合UPLC测定食品塑料包装材料中UV-0,UV-9,UV-71,UV-329,UV-326,UV-327,UV-234,UV-360,抗氧化剂2246,抗氧化剂425,TH-1790,抗氧化剂3114,抗氧化剂1010和抗氧化剂1076等14种物质的高通量方法。优化了萃取溶剂种类、超声提取时间及色谱分离条件,得到最佳的实验条件。检出限、回收率和精密度等指标的研究表明,本方法准确、灵敏,具有良好的回收率和精密度,可为定性、定量分析食品塑料包装材料中紫外吸收剂和抗氧化剂提供一种准确有效的检测方法。
参考文献:
[1]Chen Z F,Pan J W,Chu X G,Kang Y Z.Food&Machinery(陈志锋,潘健伟,储晓刚,康英章.食品与机械),2006,22(2):3-7.
[2]Scholler D,Vergnaud J M,Bouquant J,Vergallen H,Feigenbaum A.Packag.Technol.Sci.,2003,16(5):209-220.
[3]Zhao M P,Li Y Z,Chang W B.Chin.J.Anal.Chem.(赵美萍,李元宗,常文保.分析化学),2003,31(1):103-109.
[4]Ai L F,Guo C H,Ge S H,Chen R C,Zhao A K.J.Instrum.Anal.(艾连峰,郭春海,葛世辉,陈瑞春,赵安康.分析测试学报),2011,30(1):13-17.
[5]Kawamura Y,Ogawa Y,Nishimura T,Kikuchi Y,Nishikawa J,Nishihara T,Tanamoto K.J.HealthSci.,2003,49(3):205-212.
[6]GB 9685-2008.Hygienic Standards for Uses of Additives in Food Containers and Packaging Materials.National Standards of the People’s Republic of China(食品容器、包装材料用添加剂使用卫生标准.中华人民共和国国家标准).
[7]Lin R,Lai Y,Lin W J,Dong Q M,Huang L,Ge X X,Lin H X,Huang Z P,Tu X P.J.Instrum.Anal.(林睿,赖莺,林伟靖,董清木,黄龙,葛秀秀,林海霞,黄宗平,涂星鹏.分析测试学报),2015,34(1):20-27.
[8]Suman M,Tegola S L,Catellani D,Bersellini U.J.Agric.FoodChem.,2005,53(26):9879-9884.
[9]Noguerol-Cal R,López-Vilario J M,González-Rodríguez M V,Barral-Losada L F.J.Sep.Sci.,2007,30(15):2452-2459.
[10]Zenker A,Schmutz H,Fent K.J.Chromatogr.A,2008,1202(1):64-74.
[11]Minuti L,Pellegrino R.J.Chromatogr.A,2008,1185(1):23-30.
[12]Negreira N,Rodríguez I,Ramil M,Rubí E,Cela R.Anal.Chim.Acta,2009,654(2):162-170.
[13]Molander P,Haugland K,Hegna D R,Ommundsen E,Lundanes E,Greibrokk T.J.Chromatogr.A,1999,864(1):103-109.
[14]Jiang X H.Chem.Anal.Meterage(姜晓辉.化学分析计量),2009,18(3):65-66.
[15]Garrido-López,Tena M T.J.Chromatogr.A,2005,1099(1/2):75-83.
[16]Paepe A D,Erlandsson B,Ostelius J,Gasslander U,Arbin A.J.Liq.Chromatogr.RelatedTechnol.,2006,(29):1541-1559.
[17]Dopico-García M S,López-Vilarió J M,González-Rodríguez M V.J.Agric.FoodChem.,2007,55(8):3225-3231.
[18]Marcato B,Vianello M.J.Chromatogr.A,2000,(869):285-300.
[19]Arias M,Penichet I,Ysambertt F,Bauza R,Zougagh M,Ríos A.J.Supercrit.Fluids,2009,(50):22-28.
[20]Zhou X J,Zhao Y Q,Li W,Xie J J.Sci.Technol.FoodInd.(周相娟,赵玉琪,李伟,谢精精.食品工业科技),2010,31(9):288-297.
[21]Li J,Zhang J Z,Shao D L,Jiang J S.J.Instrum.Anal.(李静,张居舟,邵栋梁,蒋俊树.分析测试学报),2011,30(4):435-438.
[22]Zhang F,Zhang Y Q,Huang Z Q,Li Z H,Fu S L,Yan H F.Chin.J.Anal.Lab.(张帆,张莹杞,黄志强,李忠海,付善良,颜鸿飞.分析试验室),2010,29(5):36-39.
[23]Zou H F,Zhang Y K,Lu P Z.HighPerformanceLiquidChromatography.Analytical Chemistry Series,Volume 3 Copies.Beijing:Science Press(邹汉法,张玉奎,卢佩章.高效液相色谱法 分析化学丛书 第三卷 第三册.北京:科学出版社),1998:38.
Determination of Ultraviolet Absorbers and Antioxidants in Plastic Food Packing Materials by Ultra High Performance Liquid Chromatography
CHEN Li-wei,WU Chu-sen,WANG Yi,WU Yu-luan*,WANG Li,DONG Hao,WANG Bin,LUO Hai-ying
(Guangzhou Quality Supervision and Testing Institute,National Center for Packing Products Quality Supervision and Testing(Guangzhou),Guangzhou511447,China)
Abstract:A new method was established to determine 14 kinds of ultraviolet absorbers and antioxidants(including UV-0,UV-9,UV-71,UV-329,UV-326,UV-327,UV-234,UV-360,antioxidant 2246,425,TH-1790,3114,1010 and 1076) in plastic food packing materials by ultrasonic extraction combined with ultra high performance liquid chromatography(UPLC).In the study,the plastic food packing materials were ultrasonically extracted with trichloromethane-methanol,and analyzed with C18column,employing acetonitrile -0.1% formic water as mobile phases by gradient elution.All of the samples were detected with diode-array detector.The 14 analytes presented good linearities in the respective linear ranges,with correlation coefficients(r2) not less than 0.999 2.The quantitation limits(S/N=10) were in the range of 8.0 -33.0 mg/kg,the average recoveries(n=6) ranged from 83.6% to 116.2%,with relative standard deviations(RSD,n=6) of 1.3%-9.5%.The developed method,characteristic by simple pre-treatment procedure and satisfactory purification,was suitable for the simultaneous determination of 14 kinds of ultraviolet absorbers and antioxidants in plastic food packing materials.
Key words:ultraviolet absorbers;antioxidants;plastic food packing materials;ultra high performance liquid chromatography(UPLC)
中图分类号:O657.72;TQ572.48
文献标识码:A
文章编号:1004-4957(2016)02-0206-07
doi:10.3969/j.issn.1004-4957.2016.02.012
*通讯作者:吴玉銮,博士,教授级高级工程师,研究方向:色谱质谱检测,Tel:020-82022303,E-mail:docwu@126.com
基金项目:国家质量监督检验检疫总局科技计划项目(2014QK056)
收稿日期:2015-08-28;修回日期:2015-09-23
