Meta-ANOVA方法在FTO基因rs9939609多态性位点遗传模式界定中的应用*
2016-02-23戚敏杰陈燕子詹芳芳平智广
戚敏杰,刘 莉,陈燕子,詹芳芳,平智广#
1)郑州大学公共卫生学院卫生统计学教研室 郑州 450001 2)郑州大学基础医学院组织学与胚胎学教研室 郑州 450001
Meta-ANOVA方法在FTO基因rs9939609多态性位点遗传模式界定中的应用*
戚敏杰1),刘莉2),陈燕子1),詹芳芳1),平智广1)#
1)郑州大学公共卫生学院卫生统计学教研室 郑州 4500012)郑州大学基础医学院组织学与胚胎学教研室 郑州 450001
关键词meta-ANOVA;遗传模式;关联研究;基因多态性;FTO基因
摘要目的:探索FTO基因rs9939609位点的遗传模式,综合评价该位点多态性与肥胖的遗传关联性。方法:全面检索国内外数据库,搜集符合纳入标准的研究资料,并按照排除标准排除。运用meta-ANOVA方法对FTO基因rs9939609位点AA、AT和TT 3种基因型携带者的体重指数(BMI)的平均水平进行比较,得到设定的参数λ判断该位点的遗传模式。 结果:共纳入文献48篇,按照年龄进行分层后,少年组9篇,成年组33篇,老年组6篇。3组的AA、AT和TT 3种基因型携带者BMI平均水平差异有统计学意义[少年组(P<0.001),λ=0.5,β=0.656,95%CI(0.489~0.823);成年组(P<0.001),λ=0.5,β=0.670,95%CI(0.562~0.778);老年组(P<0.001),λ=0.5,β=0.523, 95%CI(0.363~0.682)]。3组的验证遗传模式均为加性遗传。 结论:FTO基因rs9939609位点多态性与肥胖有关联性,A等位基因有使BMI增加的风险,该位点的遗传模式为加性遗传。 1.3文献筛选对检索到的文献进行初步筛选,通过阅读题目和判断是否纳入该次研究。然后对初筛纳入的文献搜集全文,无法获取全文的文章,向通信作者联系以取得全文,阅读全文进行二次筛选。 表1文献质量评价结果内容与主题条目评价描述题目与前言95.8%(46/48)的文献在题目和 首先利用STREGA声明对纳入文献进行质量评价,评价结果显示在题目和部分仅有少数研究未说明研究设计类型,其中队列研究共22篇,比重较大,队列研究在病因探索研究中论证性较强,使研究的结果更具有说服力。纳入文献方法学部分关于基因分型和Hardy-Weinberg平衡检验的报告较充分,仅有小部分文献明确描述了分析人群分层的方法,人群分层容易出现混杂效应,采取一定的方法对其进行调整,则会提高研究结果的可靠性。详细报告单体型变异的文献数量也较少,根据SNP位点间的连锁不平衡关系可以对单体型进行分析,进行单体型推断时,不同窗口数据有不同的定义,这样可能会导致不同的研究结果之间很难进行比较[20]。因此,该研究纳入的文献质量总体上较好,但相对于标准的遗传关联研究报告规范还有一些不足。 中使用常用的词汇说明研究设计类型背景原理所有文献均在前言部分解释问题的科学背景和研究原理研究目的所有文献均明确说明研究目的方法研究设计所有文献均阐明研究设计的要素研究现场31.3%(15/48)的文献报告了随访和数据收集的时间研究对象60.4%(29/48)的文献描述了研究对象的纳入和排除标准研究变量20.8%(10/48)的文献按照不同种族对人群进行分层,93.7%(45/48)的文献给出了DNA来源,91.6%(44/48)的文献报告了基因分型方法及相关技术平台,18.8%(9/48)的文献给出了基因分型的错误率和检出率偏倚68.8%(33/48)的文献说明了如何避免可能存在偏倚的方法样本量所有文献均解释了样本量的确定方法数量变量81.3%(39/48)的文献解释了数量变量的分析方法统计学方法66.7%(32/48)的文献说明考虑Hardy-Weinberg平衡及采用的统计分析方法,22.9%(11/48)的文献说明了连锁不平衡的关系结果研究对象10.4%(5/48)的文献完整报告了关联分析每个阶段研究对象的数目,6.3%(3/48)的文献说明了每个阶段无应答的情况并分析其原因,4.2%(2/48)的文献考虑了使用研究对象纳入和排除流程图报告拟进行基因分型的人数和分型成功的人数描述性数据所有文献均描述了研究对象的一般情况结局数据所有文献均报告了结局事件的数量主要结果43.8%(21/48)的文献报告了关联强度估计值和95%CI其他分析62.5%(30/48)的文献做了亚组或交互作用分析讨论关键结果所有文献均概括与研究假设有关的重要结果局限性所有文献均讨论研究的局限性解释所有文献均给出一个总体的结果解释可推广性43.8%(21/48)的文献讨论了研究结果的外推有效性其他信息资助75.0%(36/48)的文献给出当前研究的资助来源和资助者
AbstractAim: To explore the genetic model of rs9939609 in FTO gene, as well as evaluate the association of gene polymorphism and obesity.Methods: All studies on this subject were searched in the electronic databases of China and abroad. The inclusion and exclusion criteria were used to select proper studies. The average level of body mass index(BMI) was compared between groups of AA,AT and TT. Then a parameter λ was set to estimate the genetic model.Results: A total of 48 studies were included. They were stratified into 3 groups by age of subjects. Nine studies were in youth group, 33 were in adult group, and 6 were in old group. The difference of BMI between AA,AT and TT genotype in three groups were statistically significant[in youth group(P<0.001),λ=0.5,β=0.656,95%CI(0.489-0.823);in the adult group(P<0.001),λ=0.5,β=0.670,95%CI(0.562-0.778);in old group(P<0.001),λ=0.5,β=0.523,95%CI(0.363-0.682)].The genetic model in three groups were all proved to be additive inheritance.Conclusion: The SNP rs9939609 on FTO gene is significantly associated with obesity.Allele A increases the risk of high BMI. The genetic model is confirmed to be additive.
遗传关联研究在探讨遗传因素与疾病之间的关系时,往往试图从复杂的生物学和社会背景下探索出微弱的关联作用[1],这对于统计模型的高效运用无疑是一个严峻的考验。研究者[2]通过分析不同基因型的发病危险来评价基因与疾病之间的关联。通常采用的方法是假设遗传模式(如显性模式、隐性模式、加性模式)合并成2组,对于不同的遗传模型有不同的假设,分析时需要利用一定的专业知识来选择出较合理的遗传模式,以期能得出准确的结论。但是对于多基因疾病(复杂性疾病)而言,每个位点的遗传模式并不明确,并且将3组数据合并成2组不仅增加工作量,而且当结果出现矛盾时,研究结果的真实性也将受到质疑。Meta-ANOVA方法首先在忽略基因位点遗传模式的前提下进行多组间差异的比较,确定基因对疾病起作用,然后通过参数设定确定遗传模式,并利用基因型之间的差异来获取遗传效应。作者以FTO基因rs9939609多态性与肥胖的关联研究为例,探讨meta-ANOVA方法在关联分析及遗传模式界定中的有效运用。
1资料与方法
1.1资料来源与检索方法在PubMed、Springer、Web of Science、Elsevier、万方数据库、CNKI和重庆维普数据库中检索国内外公开发表的关于FTO基因rs9939609多态性与肥胖关系研究的文献。检索关键词中文为“肥胖、FTO、rs9939609”;英文为“obesity,FTO gene polymorphism,rs9939609”,发表时间为2008年1月至2014年10月,最后一次检索日期为2014年10月14日。
1.2纳入和排除标准纳入标准:①以论著形式发表并提供原始数据的文献。②研究对象为肥胖人群。③纳入文献研究设计为病例对照、队列研究或全基因组遗传关联研究。④提供FTO基因rs9939609位点3组基因型携带者的BMI均值、标准差和样本量。排除标准:①数据不完整,无明确基因型。②重复发表文献,选取最近发表的一篇。③文献类型为摘要、会议论文。
1.4文献质量评价工具采用STREGA声明[3]对纳入的文献进行质量评价。STREGA是在已有的STROBE声明的基础上, 结合遗传学关联研究的特点和进展制定而成[4],包括题目和摘要、前言、方法、结果、讨论和其他信息6部分内容共22个条目,对遗传学关联研究在报告时所应包含的内容提出了最基本的要求。
1.5统计学处理
1.5.1数据整理对相关数据进行整理后,对人群按照年龄进行分层,分成少年组(0~岁)、成年组(15~60岁)、老年组(60岁以上)。对3个年龄组数据进行两因素方差分析。文献研究为区组因素,基因型为处理因素,加权标准差,比较该位点突变纯合子(TT)、杂合子(AT)和野生纯合子(AA) 3种基因型携带者的BMI平均水平,运用Bonferroni法进行多重比较。
1.5.2遗传模式判定[5]设定参数λ=md1/md2,其中md1=AT-AA,表示AT基因型与AA基因型个体BMI平均水平的差值;md2=TT-AA,表示TT基因型与AA基因型个体BMI平均水平的差值。λ取0、0.5和1分别对应隐性、加性和显性遗传模式。依据λ取值判断遗传模式,并绘制散点图。
1.5.3遗传模式的验证当该位点的遗传模式为隐性遗传时,运用meta分析,异质性检验使用Q检验,数据合并选择随机效应模型,计算合并效应值及其95%CI,验证AT和AA基因型个体BMI之间差异无统计学意义;当为显性遗传时,方法同上,验证TT和AT基因型个体之间差异无统计学意义;当为加性遗传时,等位基因A和T的作用相同, TT-AT和AT-AA两组不存在差异,由于无法直接进行meta分析,则通过计算两组95%CI是否重叠进行验证。
以上数据整理及遗传模式判定部分用SPSS 21.0完成,遗传模式验证部分用Stata 12.0完成。
2结果
2.1基本情况根据上述检索策略共检索到361篇文献,其中英文文献259篇,中文文献102篇;去除重复文献152篇,初筛后纳入132篇,经二次筛选,最后共有48篇纳入该研究。包含英文文献43篇,中文文献5篇;按照年龄进行分层后,少年组纳入9篇,成年组33篇,老年组6篇。
2.2文献质量评价结果见表1。
2.3Meta-ANOVA分析结果
2.3.13个年龄组rs9939609位点多态性与BMI的相关性少年组、成年组以及老年组方差分析结果显示,3种基因型所对应的BMI平均水平差异有统计学意义(F分别为21 621.683、79 051.448和68 722.804,P均<0.001);采用Bonferroni法进行TT、AA和AT基因型携带者之间的两两比较,差异均有统计学意义(P<0.001)。其中AA基因型BMI平均水平均高于TA和AA基因型携带者。
2.3.23个年龄组rs9939609位点的遗传模式判定见图1。横坐标为md2=TT-AA,纵坐标为md1=AT-AA。少年组回归系数估计值β=0.656,95%CI(0.489~0.823),R2=0.911,置信区间包含0.5,λ=0.5,判断为加性遗传;成年组β=0.670,95%CI(0.562~0.778),R2=0.834,β值接近0.5,λ=0.5,判断为加性遗传;老年组β=0.523,95%CI(0.363~0.682),R2=0.934,λ=0.5,判断为加性遗传。
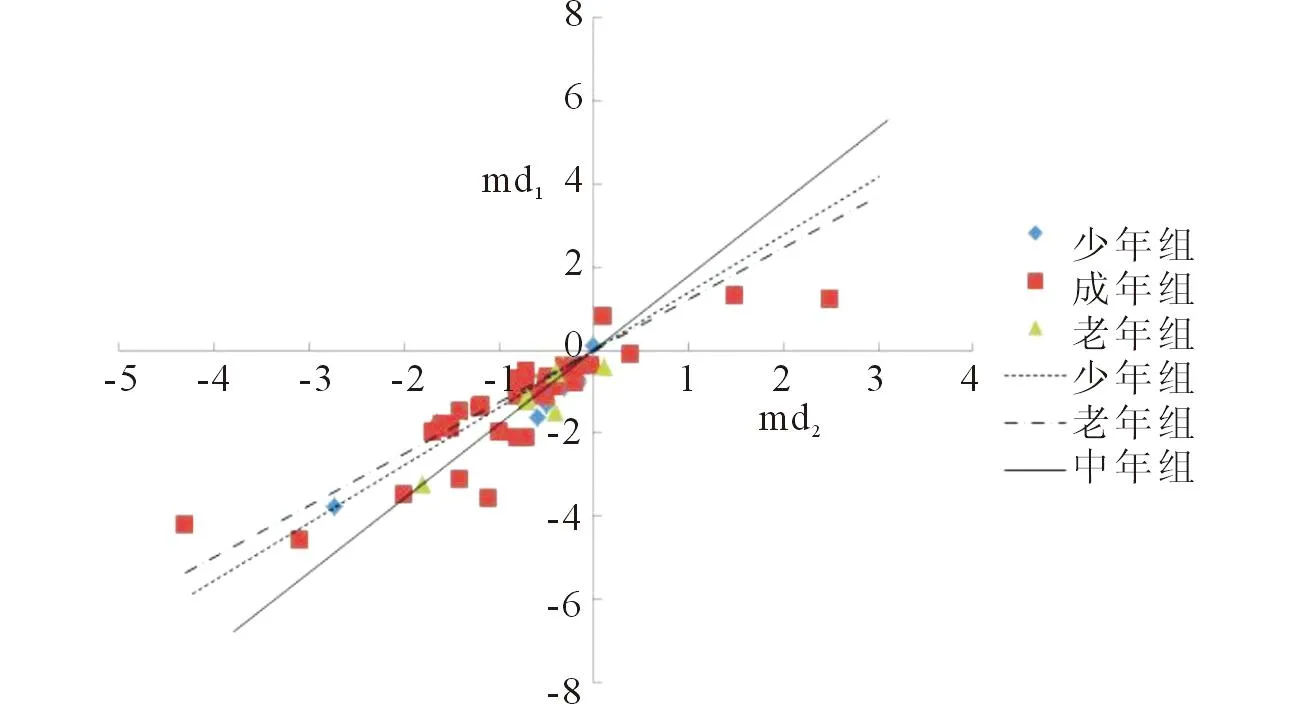
图1 3个年龄组rs9939609位点遗传模式分析
2.3.3遗传模式的验证结果见表2。对3个年龄组TT与AT,AT与AA分别进行meta分析,异质性检验结果显示各组纳入的研究间异质性均较高,采用随机效应模型合并效应值。3个年龄组TT与AT基因型间PZ值均<0.001,合并效应值具有统计学意义,说明TT基因型与AT基因型遗传作用不同,3个年龄组的rs9939609位点的遗传模式不符合显性遗传;AT与AA基因型间PZ值均<0.001,合并效应值具有统计学意义,说明AT基因型与AA基因型的遗传作用也不相同,3个年龄组该位点的遗传模式不符合隐性遗传。
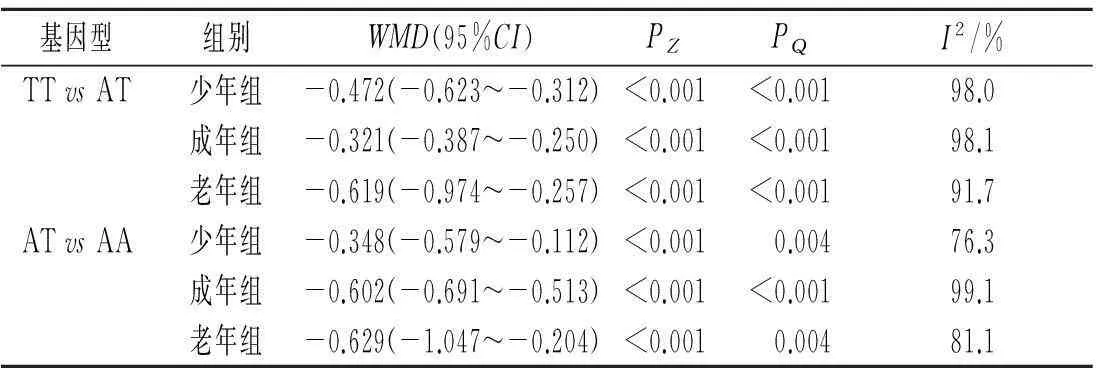
表2 3个年龄组rs9939609位点
依据参数λ判定3个年龄组该位点的遗传模式均为加性遗传,3个年龄组TT-AT和AT-AA两组95%CI均有重叠,说明TT-AT和AT-AA两组间差异无统计学意义,等位基因A和T的作用相同,验证rs9939609位点的遗传模式为加性遗传,结果见表3。
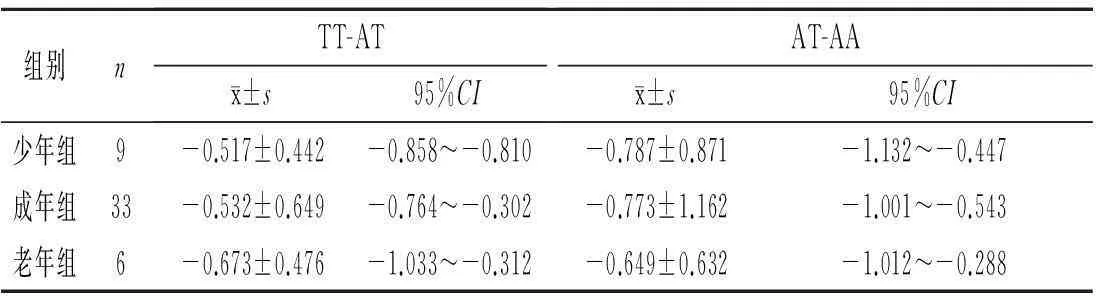
表3 3个年龄组rs9939609位点加性遗传模式效应
2.3.4等位基因遗传效应以BMI平均水平为因变量,按加性遗传模式,对基因型进行线性回归,结果显示A等位基因的β=1.998(P<0.001),即3种基因型BMI值大小依次为AA>AT>TT,其平均BMI依次相差1.998 kg/m2。
3讨论
虽然在一些关联性研究[6-19]中FTO基因rs9939609位点多态性被证实和肥胖的发生发展相关,但分析前提是假设在不同的遗传模式下该位点与疾病的关联强度,对其实际的作用方式和大小缺乏相关报道。该研究采用Meta-ANOVA方法,对纳入的国内外48篇文献进行综合定量分析,对于FTO基因rs9939609位点多态性与肥胖关联做出一个系统的评价,同时明确该位点的遗传模式。
Meta-ANOVA分析结果显示,3个年龄组FTO基因rs9939609位点AA、AT和TT 3种基因型携带者BMI平均水平之间差异有统计学意义,且AA基因型携带者BMI平均水平高于TA和AA基因型,提示FTO基因rs9939609位点多态性与肥胖有关,A等位基因携带者BMI较高。成年组回归系数估计值为0.670,95%CI不包含0.5,可能是由于该年龄段的人群生活压力较大,上班时会主动采取乘坐机动车、自驾车或电动车等代步工具,并且随着电视机、洗衣机、私家车、电脑网络等产品的普及率越来越高,日常非职业性体力活动正在大幅减少,导致环境因素对肥胖的影响较少年及老年人更加显著[21]。利用meta回归对该研究的异质性来源进行分析,发现研究类型为该研究的异质性来源(P=0.042,<0.05)。3个年龄组回归模型的决定系数R2分别为0.911、0.834和0.934,提示模型的拟合效果较好。由于成年组纳入的研究较多,不同研究间选择人群、研究方法等的不同,使得研究间的差异较大,因此R2较少年组和老年组低。由于每个研究的样本量大小不等,且相差较大,在进行回归分析时,对标准差进行WLS加权。加权前模型的赤池信息量准则评分远大于加权后,因此对标准差进行加权使模型更加优化,结果更精准。
综上所述,该研究通过meta-ANOVA 方法得出结论,FTO基因rs9939609位点多态性与肥胖有关联性,A等位基因有增加BMI的风险,该位点的遗传模式为加性遗传。由于该研究针对的只是基因型与BMI之间的关联分析,对于其他肥胖易感性状间的关联分析有待进一步的研究。同时,该研究仅考虑到单个基因位点的基因-疾病关联,对于多基因遗传的复杂疾病来说,meta-ANOVA模型能否用于多位点与疾病的关联分析尚需进一步探索。
参考文献
[1]MANOLIO TA.Genomewide association studies and assessment of the risk of disease[J].N Engl J Med,2010,363(2):166
[2]韩建文,张学军.全基因组关联研究现状[J].遗传,2011,33(1):25
[3]LITTLE J,HIGGINS JP,IOANNIDIS JP,et al.Strengthening the reporting of genetic association studies (STREGA): an extension of the STROBE statement[J].Eur J Epidemiol,2009,24(1):37
[4]严卫丽.第四讲:如何报告遗传学关联研究:国际报告规范STREGA解读[J].中国循证儿科杂志,2010,5(4):304
[5]GILLESPIE JH.Population genetics:a concise guide[M].[S.l.]: The Johns Hopkins University Press,1998.
[6]BAIK I,SHIN C.Interactions between the FTO rs9939609 polymorphism, body mass index, and lifestyle-related factors on metabolic syndrome risk[J].Nutr Res Pract,2012,6(1):78
[7]CORELLA D,CARRASCO P,SORL JV,et al.Education modulates the association of the FTO rs9939609 polymorphism with body mass index and obesity risk in the Mediterranean population[J].Nutr Metab Cardiovasc Dis,2012,22(8):651
[8]HUANG W,SUN Y,SUN J.Combined effects of FTO rs9939609 and MC4R rs17782313 on obesity and BMI in Chinese Han populations[J].Endocrine,2011,39(1):69
[9]LAPPALAINEN T,KOLEHMAINEN M,SCHWAB US,et al.Association of the FTO gene variant(rs9939609) with cardiovascular disease in men with abnormal glucose metabolism:the finnish diabetes prevention study[J].Nutr Metab Cardiovasc Dis,2011,21(9):691
[10]LAPPALAINEN T,LINDSTR MJ,PAANANEN J,et al.Association of the fat mass and obesity-associated(FTO) gene variant(rs9939609) with dietary intake in the finnish diabetes prevention study[J].Br J Nutr,2012,108(10):1859
[11]MAEKOV S,BERNASOVSK I,GABRIKOV D,et al.Association of the FTO rs9939609 polymorphism with obesity in Roma/Gypsy population[J].Am J Phys Anthropol,2012,147(1):30
[12]RAMOS AV,BASTOS-RODRIGUES L,RESENDE BA,et al.The contribution of FTO and UCP-1 SNPs to extreme obesity, diabetes and cardiovascular risk in Brazilian individuals[J].BMC Med Genet,2012,13:101
[13]THOMSEN M,DAHL M,TYBJRG-HANSEN A,et al.β2-adrenergic receptor Thr164lle polymorphism, obesity, and diabetes: comparison with FTO, MC4R, and TMEM18 polymorphisms in more than 64,000 individuals[J].J Clin Endocrinol Metab,2012,97(6):E1074
[14]RAUHIO A,UUSI-RASI K,NIKKARI ST,et al.Association of the FTO and ADRB2 genes with body composition and fat distribution in obese women[J].Maturitas,2013,76(2):165
[15]BINH TQ,PHUONG PT,NHUNG BT,et al.Association of the common FTO-rs9939609 polymorphism with type 2 diabetes,independent of obesity-related traits in a vietnamese population[J].Gene,2013,513(1):31
[16]陈家慧,何振娟,朱天闻.FTO基因rs9939609多态性与中国儿童肥胖及超重相关性的Meta分析[J].中华临床医师杂志:电子版,2013,7(17):7877
[17]万茜茜,周波,范晶,等.脂肪量和肥胖相关因子基因rs9939609多态性与2型糖尿病的关系研究[J].第三军医大学学报,2010,32(10):1091
[18]王芳,宓为峰,卢天兰,等.肥胖相关基因rs9939609多态性与利培酮4周治疗所致体质量增加的关联分析[J].中国心理卫生杂志,2013,27(2):157
[19]吴燕明,李卫国,盛秋明,等.FTO基因rs9939609位点多态性与儿童肥胖的相关性研究[J].临床儿科杂志,2014,32(6):547
[20]史晓薇,吕爱莉,任峰玲,等.15个短串联重复序列位点与大骨节病传递不平衡分析及与低硒暴露的交互作用[J].南方医科大学学报,2011,31(4):567
[21]李启富,梅玫.肥胖症与运动 营养治疗[J].中国实用内科杂志,2012,32(10):741
(2015-04-30收稿责任编辑赵秋民)
Application of Meta-ANOVA approach in defining genetic model of rs9939609 in FTO gene polymorphism
QIMinjie1),LIULi2),CHENYanzi1),ZHANFangfang1),PINGZhiguang1)
1)DepartmentofHealthStatistics,CollegeofPublicHealth,ZhengzhouUniversity,Zhengzhou450001
2)DepartmentofHistologyandEmbryology,CollegeofBasicMedicalSciences,ZhengzhouUniversity,Zhengzhou450001
Key wordsmeta-ANOVA;genetic model;association studies;gene polymorphism;FTO gene
中图分类号R181.2
通信作者#,男,1978年10月生,博士,副教授,研究方向:医学数据管理与挖掘,E-mail:pingzhg@163.com
基金项目*国家自然科学81001280,81202277;河南省高等学校重点科研资助项目16A330003
doi:10.13705/j.issn.1671-6825.2016.01.004
