维拉帕米对梗阻性黄疸大鼠肝损伤的保护作用及机制探讨
2016-02-16禹良国王崇高陆志斌蔡华忠徐三荣
禹良国,王崇高,陆志斌,蔡华忠,徐三荣
(1江苏建康职业学院,2南京市浦口区中心医院,江苏南京211800;3江苏大学附属医院,江苏镇江212001)
维拉帕米对梗阻性黄疸大鼠肝损伤的保护作用及机制探讨
禹良国1,王崇高2,陆志斌2,蔡华忠3,徐三荣3
(1江苏建康职业学院,2南京市浦口区中心医院,江苏南京211800;3江苏大学附属医院,江苏镇江212001)
目的:探讨梗阻性黄疸时大鼠肝组织细胞凋亡与NF-κB表达的变化,并研究维拉帕米对大鼠肝脏损伤的保护作用.方法:选取80只雄性SD大鼠随机分成假手术组(Sham组)、胆总管结扎组(BDL组)、胆总管结扎后不同剂量维拉帕米干预组(BDL+V1-3组),分别于术后第7天、14天将大鼠处死,比较各组大鼠肝组织中丙二醛(MDA)和超氧化物歧化酶(SOD)含量的变化、细胞凋亡及NF-κB P65蛋白的表达,以及血清丙氨酸氨基转移酶(ALT)、天冬氨酸氨基转移酶(AST)的变化.结果:各维拉帕米干预组MDA低于BDL组而SOD高于BDL组,维拉帕米可不同程度下调肝组织NF-κB的表达,并减轻细胞凋亡,且呈剂量依赖性.结论:钙通道阻滞剂维拉帕米可减轻梗阻性黄疸大鼠肝损害,NF-κB的活化可能是介导肝脏功能损害的重要因素.
维拉帕米;梗阻性黄疸;核因子-κB;细胞凋亡;肝损伤
0 引言
梗阻性黄疸(obstructive jaundice,OJ)是一种较为普遍的外科疾病,其会引起肝脏等机体各系统器官发生损害以及一系列的病理生理改变.有报道[1-3]表明,梗阻性黄疸患者有较高的死亡率和术后并发症发生率,这主要与其内促炎细胞因子的过度释放、毒素血症以及氧化应激等密切相关.肝组织核因子-κB(NF-κB)能高效参与诱导,可高效诱导参与TNF-α、IL-6、iNOS以及自由基等免疫和炎症反应的炎症介质[4],在多种免疫炎症相关基因的转录调控中起核心作用[5].本研究以自制梗阻性黄疸大鼠模型作为研究对象,探讨梗阻性黄疸时大鼠肝组织细胞凋亡与NF-κB表达的变化,并研究维拉帕米对大鼠肝脏损伤的保护作用,现报道如下.
1 材料和方法
1.1 实验动物及分组选取江苏大学实验动物中心80只体重为250~300 g的健康雄性SD大鼠作为研究对象,将其通过随机分组的方法分成5组:假手术组(Sham组),胆总管结扎组(BDL组),胆总管结扎后腹腔注射1 mg维拉帕米干预组(BDL+V1组),2 mg维拉帕米组(BDL+V2组),5 mg维拉帕米组(BDL+V3组),每组16只.
1.2 动物模型的建立大鼠在可自由饮水的条件下,禁食12 h后进行手术,麻醉方法为腹腔注射氯胺酮,剂量为100 mg/kg,在无菌环境中取上腹部正中纵切口进腹,用3-0号丝线在胆总管完全游离进行双重结扎,结间横断胆总管后逐层关腹.Sham组大鼠不进行结扎和切断,只游离胆总管.
1.3 处理方法BDL+V1-3组动物模型建立后第1天直至处死,分别给予维拉帕米(美国Sigma公司)1、2、5 mg/kg,腹腔注射.其余两组则同期给予等量生理盐水,腹腔注射.分别于给药后第7天、14天将动物处死(n=8),下腔静脉采血,留存血清备用;将大鼠右叶肝组织,部分置于4%多聚甲醛溶液固定,其余迅速置液氮再转存-70℃深低温冰箱.
1.4 检测指标
1.4.1 肝脏组织病理学 将固定好的肝脏组织常规石蜡包埋,HE染色制片后于光镜下观察.
1.4.2 肝功能测定 通过全自动生化分析仪(日本Olympus AU2700)检测大鼠血清各项肝功能指标包括总胆红素(TB)、丙氨酸氨基转移酶(ALT)以及天冬氨酸氨基转移酶(AST).
1.4.3 肝组织MDA和SOD的检测 取1.3方法下制备的大鼠肝组织200 mg,通过内切式匀浆机制备成10%肝组织匀浆(重量体积比加生理盐水),离心后取组织匀浆上清按说明书进行检测.MDA、SOD测定试剂盒购自南京建成生物工程研究所.
1.4.4 NF-κB P65蛋白的表达的检测 选择的方法为免疫组化Envision二步法,空白对照为以PBS代替一抗.兔抗大鼠NF-κB P65多克隆抗体(美国Cell Signaling Technology公司),Envision试剂盒(丹麦Dako公司).取1.3项下制备的肝组织(4%多聚甲醛固定),进行石蜡包埋后切片.根据光镜所见,阳性信号为细胞核和/或胞浆出现棕黄色颗粒.每张切片随机取5个高倍镜不重复视野,计算阳性细胞百分率.1.4.5 TUNEL法检测肝细胞凋亡 细胞凋亡检测试剂盒购于武汉博士德生物工程有限公司,以PBS代替一抗.凋亡细胞在光镜下细胞核中棕黄着色.每例切片计数5个400倍视野,凋亡指数(AI)为平均每100个细胞核中含凋亡细胞个数.
1.5 统计学处理采用SPSS17.0统计学软件进行单因素方差分析,计量资料用±s表示,组间比较用t检验,P<0.05表示差异有统计学意义.
2 结果
2.1 肝组织病理学改变根据肉眼观察,除Sham组外,其余各组大鼠第7天、14天处死后,肝脏均呈黄褐色,且明显肿大,胆总管近端出现显著扩张,且张力较大.根据光镜所见,BDL组大鼠第7天标本出现小胆管增生,汇管区改变明显,出现大量炎性细胞浸润,第14天标本小胆管增生明显,部分区域肝细胞出现变性、坏死;BDL+V1-3组大鼠肝脏病理改变较BDL组轻;Sham组大鼠则无显著肝脏病理改变.
2.2 各组大鼠肝功能指标变化情况比较Sham组的血清TB水平显著低于BDL+V1-3组和BDL组;BDL组的7 d、14 d血清ALT和AST水平均显著高于BDL+V1-3组,差异具有统计学意义(P<0.05,表1).
表1 各组大鼠血清生化指标的变化(n=16,±s)
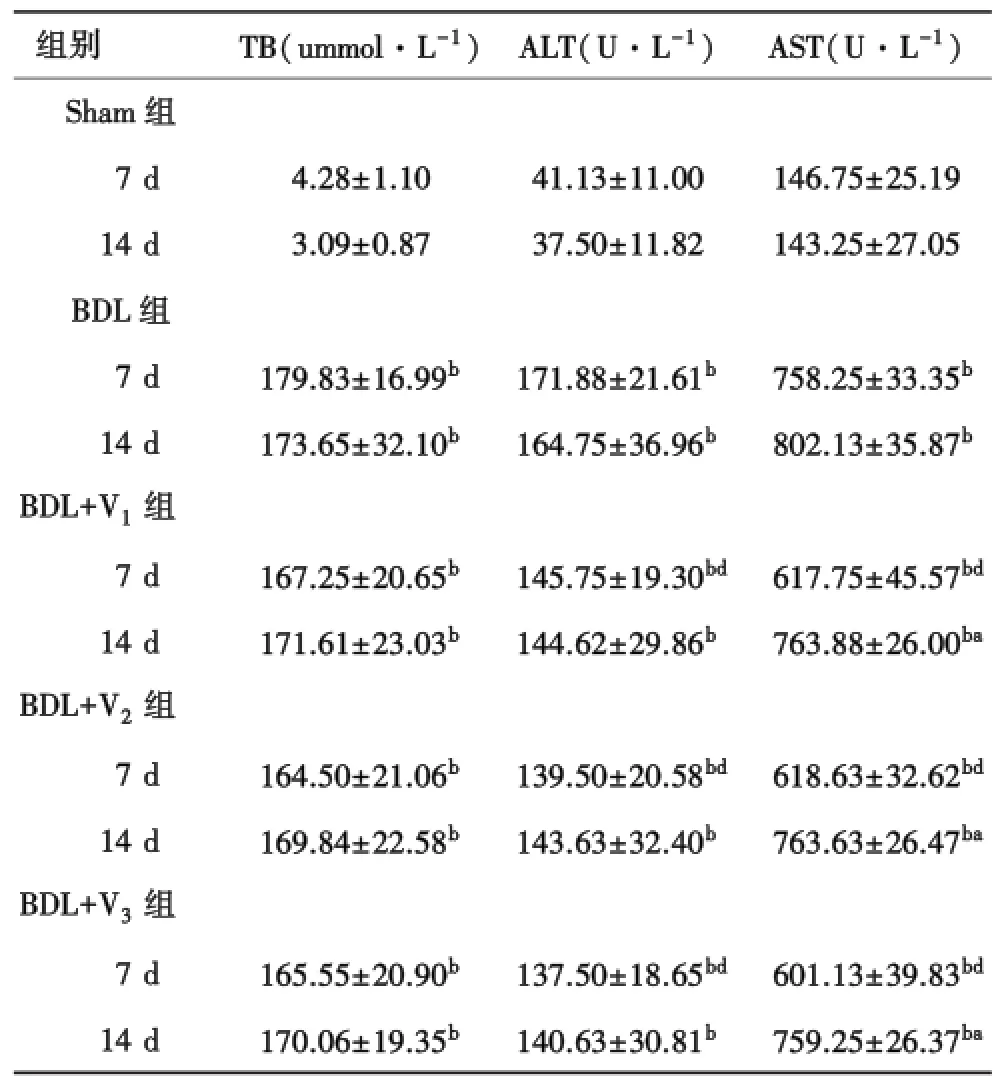
表1 各组大鼠血清生化指标的变化(n=16,±s)
bP<0.01 vs Sham组;aP<0.05 vs BDL组,dP<0.01 vs BDL组.
组别TB(ummol·L-1)ALT(U·L-1)AST(U·L-1)Sham组7 d4.28±1.1041.13±11.00146.75±25.19 14 d3.09±0.8737.50±11.82143.25±27.05 BDL组7 d179.83±16.99b171.88±21.61b758.25±33.35b14 d173.65±32.10b164.75±36.96b802.13±35.87bBDL+V1组7 d167.25±20.65b145.75±19.30bd617.75±45.57bd14 d171.61±23.03b144.62±29.86b763.88±26.00baBDL+V2组7 d164.50±21.06b139.50±20.58bd618.63±32.62bd14 d169.84±22.58b143.63±32.40b763.63±26.47baBDL+V3组7 d165.55±20.90b137.50±18.65bd601.13±39.83bd14 d170.06±19.35b140.63±30.81b759.25±26.37ba
2.3 各组大鼠肝组织MDA及SOD含量变化情况比较Sham组的血清MDA含量明显低于其它各组,但SOD含量明显高于其它各组;但在BDL+V1-3组7 d、BDL+V2-3组14 dMDA含量低于BDL组;而在BDL+V2-3组7 d、BDL+V1-3组14 dSOD含量高于BDL组,差异具有统计学意义(P<0.05,表2).
2.4 肝组织NF-κB P65蛋白表达及凋亡指数比较
Sham组肝组织仅出现少量淡黄色细胞胞浆,未发现胞核着色;BDL组胞浆染色加深,为棕黄色,且出现胞核着色;BDL组NF-κB P65蛋白在7 d和14 d的表达均显著高于BDL+V1-3组,差异具有统计学意义(P<0.05,表3).
表2 各组大鼠肝组织MDA及SOD含量变化情况比较(n=16,±s)
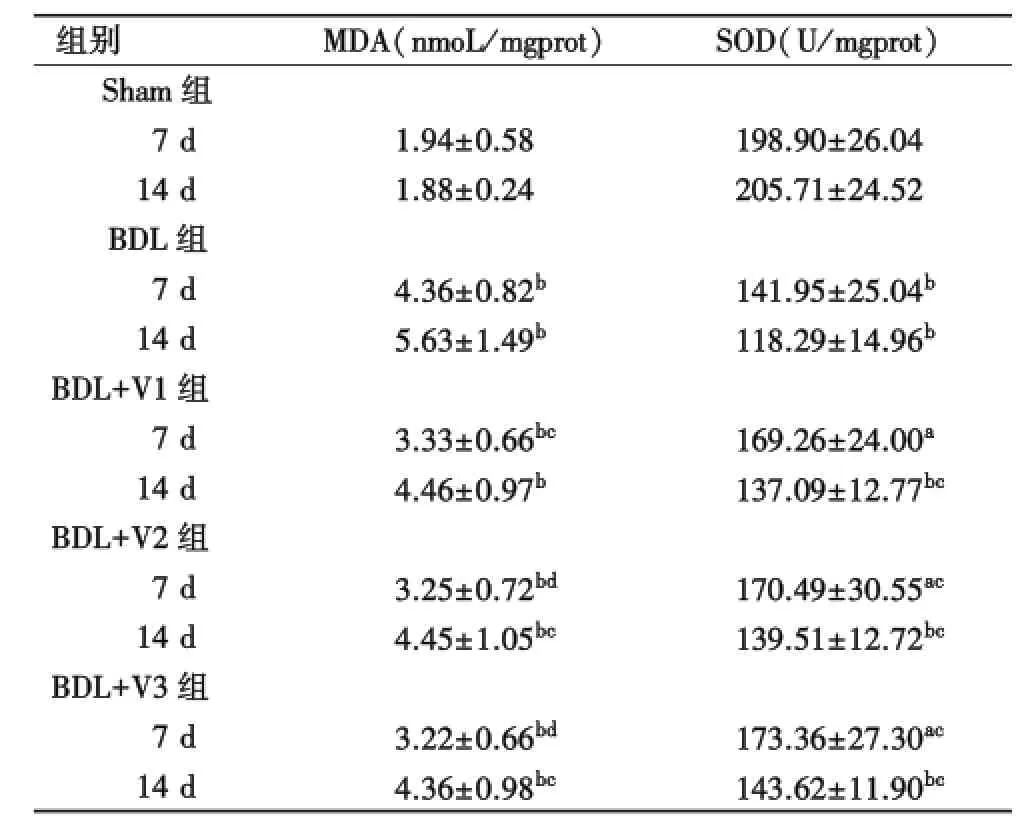
表2 各组大鼠肝组织MDA及SOD含量变化情况比较(n=16,±s)
aP<0.05 vs Sham组,bP<0.01 vs Sham组;cP<0.05 vs BDL组,dP<0.01 vs BDL组.
组别MDA(nmoL/mgprot)SOD(U/mgprot)Sham组7 d1.94±0.58198.90±26.04 14 d1.88±0.24205.71±24.52 BDL组7 d4.36±0.82b141.95±25.04b14 d5.63±1.49b118.29±14.96bBDL+V1组7 d3.33±0.66bc169.26±24.00a14 d4.46±0.97b137.09±12.77bcBDL+V2组7 d3.25±0.72bd170.49±30.55ac14 d4.45±1.05bc139.51±12.72bcBDL+V3组7 d3.22±0.66bd173.36±27.30ac14 d4.36±0.98bc143.62±11.90bc
表3 各组大鼠肝脏NF-κB P65蛋白表达及凋亡指数比较(n=16,±s)
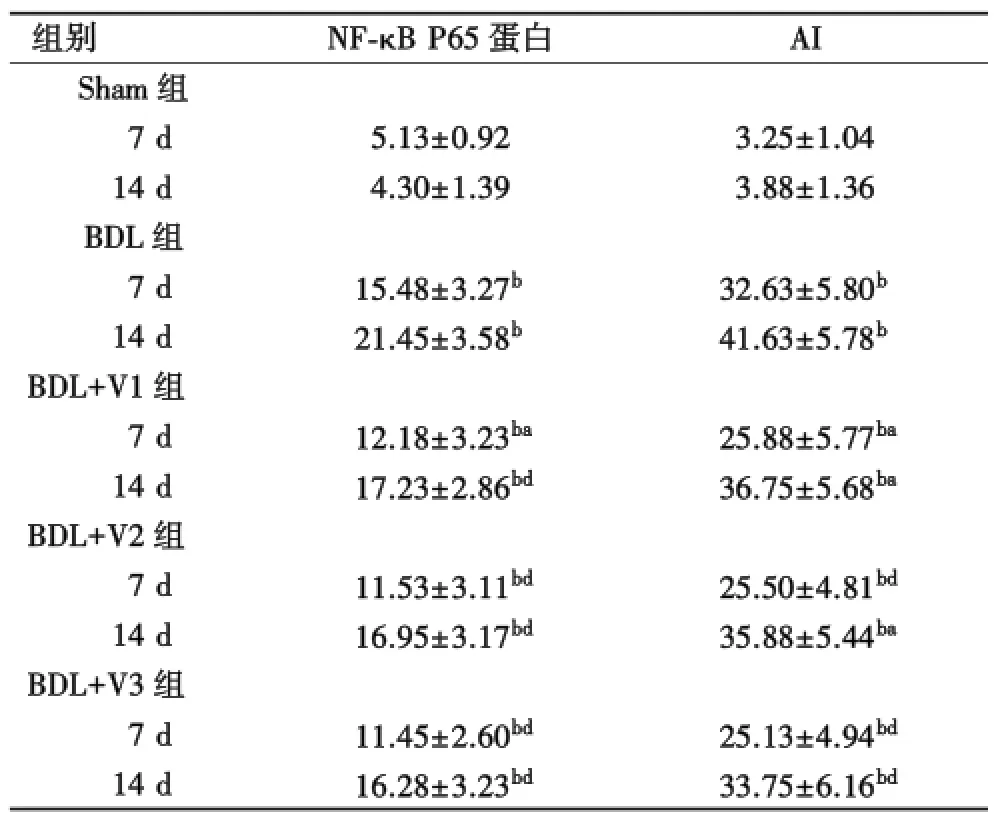
表3 各组大鼠肝脏NF-κB P65蛋白表达及凋亡指数比较(n=16,±s)
bP<0.01 vs Sham组;aP<0.05 vs BDL组,dP<0.01 vs BDL组.
组别NF-κB P65蛋白AI Sham组7 d5.13±0.923.25±1.04 14 d4.30±1.393.88±1.36 BDL组7 d15.48±3.27b32.63±5.80b14 d21.45±3.58b41.63±5.78bBDL+V1组7 d12.18±3.23ba25.88±5.77ba14 d17.23±2.86bd36.75±5.68baBDL+V2组7 d11.53±3.11bd25.50±4.81bd14 d16.95±3.17bd35.88±5.44baBDL+V3组7 d11.45±2.60bd25.13±4.94bd14 d16.28±3.23bd33.75±6.16bd
2.5 肝细胞凋亡的检测Sham组仅出现少量凋亡肝细胞,其余各组均出现大量凋亡肝细胞;但BDL组凋亡肝细胞显著高于BDL+V1-3组,差异具有统计学意义(表3).
2.6 NF-κB P65蛋白的表达与凋亡指数相关性分析
Spearman相关分析结果表明,梗阻性黄疸大鼠肝组织NF-κB p65蛋白的表达与细胞凋亡正相关(7 d:r=0.733,P<0.01;14 d:r=0.679,P<0.01).
3 讨论
NF-κB作为一种广泛存在于多种细胞中的转录因子,严重影响着机体的免疫和炎症反应.NF-κB在非激活状态下主要存在于胞浆中,其存在形式为与其抑制蛋白IκB结合成三聚体复合物.当其受到外界因素包括细胞因子、氧化应激以及细菌产物等刺激时被激活,然后进入细胞核,导致相关基因发生转录[4].正常情况下肝细胞中无活性NF-κB存在,但在肝枯否细胞中可以检测到NF-κB.相关研究[6-7]报道中指出,在肝枯否细胞中,NF-κB最初被激活,但是如果肝细胞受到白介素和肿瘤坏死因子等刺激,引起其NF-κB活性增强.相关研究[8-9]报道,梗阻性黄疸时肝脏的炎性损伤与NF-κB及其下游调控的炎症因子的高表达密切相关.
梗阻性黄疸时肝脏损害的重要特征为肝细胞的凋亡,而细胞凋亡的发生机制尚未充分阐明.目前的研究认为,梗阻性黄疸时细胞凋亡可能受到多种因素包括促炎细胞因子、氧自由基、线粒体功能障碍及胞内钙超载等的影响[5,10].目前临床上治疗梗阻性黄疸及其围手术期护理的主要内容为提高患者肝功能,避免肝细胞发生凋亡.Han等[11]报道表明,肝细胞凋亡在梗阻性黄疸早期开始出现,且其数量随着黄疸的加重而显著上升,但由于梗阻性黄疸后期患者的凋亡调控机制被激活,同时肝脏纤维组织出现增生,凋亡细胞数逐渐下降.细胞凋亡是梗阻性黄疸肝损害发生和发展变化的重要机制之一,同时其可能是梗阻性黄疸时肝脏损害的早期事件.
Hoesel等[4]报道表明,NF-κB参与细胞凋亡调控的具体机制尚未十分明确,但其能够调控多种凋亡相关基因的转录,能够起到抑制细胞凋亡和促进细胞凋亡的双重作用.Kucharczak等[12]报道因活化的NF-κB在不同时间、不同部位组成不同的二聚体,能够调控其相应靶基因以及转录相应蛋白质,所以能够在细胞凋亡的最终效应中起到双重作用,同时可能还受到同时激活的其他转录因子、细胞环境及外界刺激物种类等因素的影响.
正常机体内会有少量不同种类自由基产生,其中具有活性的氧自由基是作用最为广泛的一种.Aliomrani等[13]报道表明,氧自由基在患者发生胆道梗阻的早期就参与进来.Badger等[14]报道,胆道梗阻时细胞内、外活性氧量上升,其能够使细胞生物膜发生脂质过氧化反应,同时能够激活NF-κB,最终导致炎症蛋白基因以及促炎细胞因子的过度表达,这又能促进活性氧的生成形成正反馈环,进而使肝脏组织的炎性损伤加重.相关研究[15-16]报道表明,谷胱甘肽(GSH)、吡咯烷二硫代氨基甲酸酯(PDTC)以及超氧化物歧化酶(SOD)等能够通过抑制氧自由基的生成来实现抑制NF-κB活性的目的,同时还能抑制IL-1β和IL-6基因的表达.
生理情况下,钙离子在细胞内外存在巨大的浓度差,此为其信息传递的物质基础.如果细胞内Ca2+的释放增加或者细胞外Ca2+发生内流,则胞浆Ca2+浓度会上升,此时细胞即被激活.Collage等[17-18]报道细胞内钙稳态被打破是细胞发生炎性损伤的重要机制之一,Ca2+活动在各种炎症以及免疫性疾病的发生中起着非常重要的作用.研究[19-21]报道梗阻性黄疸引起的多种损伤因素如内毒素血症、缺血、缺氧以及氧化应激等均能导致肝细胞出现ATP缺乏,胞膜受损,Ca2+发生非正常跨膜内流,最终出现胞浆内钙超载现象.肝细胞、枯否细胞和肝窦内皮细胞均可出现钙超载现象.维拉帕米是一种钙通道阻滞剂,其作用的发生依赖于L型电压,其减轻细胞内钙超载的机制主要为与钙通道α亚单位两个不同的位点相结合,使通道蛋白构象发生改变,最终实现阻滞胞外Ca2+内流的目的.
本研究结果显示,梗阻性黄疸时,活性氧以及丙二醛的含量上升,但是抗氧化酶SOD含量下降;大量肝组织NF-κB被激活,同时凋亡肝细胞数量上升,两者呈正相关.腹腔注射不同剂量的维拉帕米后,ALT、AST、肝组织NF-κB P65蛋白及细胞凋亡较BDL组均显著下降,其下降程度与维拉帕米剂量相关.这提示维拉帕米能够通过抑制梗阻性黄疸时肝组织NF-κB的激活,降低肝脏损害程度.细胞内钙稳态及氧化/抗氧化等平衡状态被打破可能与NF-κB和细胞凋亡的变化密切相关.因钙通道阻滞剂能够调节细胞内钙稳态,所以能够避免活性氧的生成、调控NF-κB.同时,Steffan等[22]报道细胞内Ca2+浓度与IκB的降解呈正相关,钙通道阻滞剂能够通过避免IκB的降解,来实现抑制NF-κB活化转位的目的.
综上所述,NF-κB的激活在梗阻性黄疸时肝脏等器官损害的多种致病机制中起到纽带的作用[23],其持续、过度的激活能够增加肝脏损伤及各种并发症的发生率.将抑制NF-κB的表达与及早解除消除梗阻性黄疸始动环节结合起来,能够提高胆道梗阻患者的临床疗效,改善患者的预后.
[1]汤 地,吕明德,梁力建,等.阻塞性黄疸病人围手术期肝肾功能保护的临床研究[J].中华肝胆外科杂志,2002,8(10):614-616.
[2]Zhu L,Chen X.Change and significance of T-cell subsets and TNF-α in patients with advanced malignant obstructive jaundice treated by percutaneous transhepatic biliary external and internal drainage[J].Front Med China,2007,1(4):364-368.
[3]Martínez-Cecilia D,Reyes-Díaz M,Ruiz-Rabelo J,et al.Oxidative stress influence on renal dysfunction in patients with obstructive jaundice:A case and control prospective study[J].Redox Biol,2016(8):160-164.
[4]Hoesel B,Schmid JA.The complexity of NF-κB signaling in inflammation and cancer[J].Mol Cancer,2013,12:86.
[5]李达民.梗阻性黄疸致肝细胞凋亡的研究进展[J].中国普通外科杂志,2014,23(7):967-971.
[6]詹志林,卞建民,孔胜兵.PP2A在肝枯否细胞NF-κB活化中的调控作用及其效应机制[J].肝胆外科杂志,2011,19(6):467-470.
[7]Fox ES,Kim JC,Tracy TF.NF-kappaB activation and modulation in hepatic macrophages during cholestatic injury[J].J Surg Res,1997,72(2):129-134.
[8]贺 凯,苏 松,倪建斌,等.胆道梗阻肝损伤早期NF-κB活性变化的影响及意义[J].肝胆胰外科杂志,2013,25(6):477-479.
[9]Lin SY,Wang YY,Chen WY,et al.Beneficial effect of quercetin on cholestatic liver injury[J].J Nutr Biochem,2014,25(11):1183-1195.
[10]Kosar NM,Tosun M,Polat C,et al.Hepatocyte apoptotic index and p53 expression in obstructive jaundice rats[J].Bratisl Lek Listy,2014,115(6):352-356.
[11]Han JM,Kim HG,Choi MK,et al.Artemisia capillaris extract protects against bile duct ligation-induced liver fibrosis in rats[J].Exp Toxicol Pathol,2013,65(6):837-844.
[12]Kucharczak J,Simmons MJ,Fan Y,et al.To be,or not to be:NF-kappaB is the answer--role of Rel/NF-kappaB in the regulation of apoptosis[J].Oncogene,2003,22(56):8961-8982.
[13]Aliomrani M,Sepand MR,Mirzaei HR,et al.Effects of phloretin on oxidative and inflammatory reaction in rat model of cecal ligation and puncture induced sepsis[J].Daru,2016,24(1):15.
[14]Badger SA,Jones C,McCaigue M,et al.Cytokine response to portal endotoxaemia and neutrophil stimulation in obstructive jaundice[J].Eur J Gastroenterol Hepatol,2012,24(1):25-32.
[15]Gloire G,Legrand-Poels S,Piette J.NF-kappaB activation by reactive oxygen species:fifteen years later[J].Biochem Pharmacol,2006,72(11):1493-1505.
[16]Tokaç M,Aydin S,Taner G,et al.Hepatoprotective and antioxidant effects of lycopene in acute cholestasis[J].Turk J Med Sci,2015,45(4):857-864.
[17]Collage RD,Howell GM,Zhang X,et al.Calcium supplementation during sepsis exacerbates organ failure and mortality via calcium/calmodulin-dependent protein kinase kinase signaling[J].Crit Care Med,2013,41(11):e352-360.
[18]钱爱华,宋丹丹,李 勇,等.电压门控钙通道在三硝基苯磺酸诱导的炎症性内脏高敏中作用机制的研究[J].中华消化杂志,2011,31(6):381-386.
[19]戴 维,陈念平,陈赛红,等.柴胡皂苷d对阻塞性黄疸大鼠肝细胞游离钙及基质交联分子1的调控机制[J].中华实验外科杂志,2012,29(11):2122-2124.
[20]崔瑞冰,阎 明.肝细胞钙离子通道及其在乙醇诱导肝细胞损伤中作用研究进展[J].中国肝脏病杂志:电子版,2012,4(4):47-52.
[21]崔 宏,崔桂英,刘东举,等.维拉帕米对三磷酸肌醇引起的大鼠肝细胞钙释放激活的钙电流的影响[J].中国应用生理学杂志,2000,16(3):265-267.
[22]Steffan NM,Bren GD,Frantz B,et al.Regulation of IkB alpha phosphorylation by PKC-and Ca(2+)-dependent signal transduction pathways[J].J Immunol,1995,155(10):4685-4691.
[23]许朝龙,邬善敏.梗阻性黄疸对多器官系统损害及其机制的研究进展[J].腹部外科,2015,28(5):367-370.
Protective effect and mechanism of verapamil on liver injury of obstructive jaundice rats
YU Liang-Guo1,WANG Chong-Gao2,LU Zhi-Bin2,CAI Hua-Zhong3,XU San-Rong3
1Jiangsu Jiankang Vocational College,2Nanjing Pukou Central Hospital,Nanjing 211800,China;3Affiliated Hospital of Jiangsu University,Zhenjiang 212001,China
AIM:To investigate the role of NF-κB and apoptosis in liver injury of rats with obstructive jaundice and the protective effect of verapamil.METHODS:A total of 80 SD male rats were randomly divided into Sham group,BDL group and BDL+V1-3group,with 16 rats in each group.The rats were sacrificed at 7th and 14th day after operation,then the changes of MDA and SOD in hepatic tissue,hepatic NF-κB activities and cell apoptosis,ALT and AST of each group were compared.RESULTS:Compared with BDL group,lower MDA and higher SOD were found in different dose of verapamil group,verapamil can down-regulate the expression of NF-κB and reduce the apoptosis at different levels,presenting dose dependence.CONCLUSION:The activation of NF-κB may be one of the most important factors in liver injury.Verapamil can protect against the liver injury in rats with obstructive jaundice through reducing the expression of NF-κB and cell apoptosis.
verapamil;obstructive jaundice;NF-κB;apoptosis;liver injury
R96
A
2095-6894(2016)12-07-04
2016-10-22;接受日期:2016-11-10
南京市科技发展计划项目(201402061);南京医科大学科技发展基金项目(2012NJMU236)
禹良国.硕士,主治医师.研究方向:普通外科的基础与临床.E-mail:yu_lg@126.com
