复方苦参注射液联合化疗治疗晚期结直肠癌近期疗效及安全性的Meta分析
2016-02-10刘文波马建秀姚
刘文波马建秀姚 南
复方苦参注射液联合化疗治疗晚期结直肠癌近期疗效及安全性的Meta分析
刘文波1马建秀2姚 南3
大肠癌;结肠癌;直肠癌;复方苦参注射液;岩舒;Meta分析;系统评价;随机对照试验
结直肠癌(ACRC)是消化道常见恶性肿瘤之一,发病率居消化道恶性肿瘤第三位(仅次于胃癌及食管癌),死亡率居恶性肿瘤第五位[1]。近年来,我国结直肠癌的发病率有逐年上升的趋势,有报道称结直肠的发病率在我国沿海发达地区已经达到或接近高发国家的水平[2]。目前结直肠癌最主要的治疗仍然是外科手术治疗,但结直肠癌发病较隐匿,早期无明显临床症状,很多患者初诊时已至晚期,失去手术治疗机会。有报道称,结直肠癌患者在初诊时约30%已出现局部或远处转移[3]。化疗是这部分结直肠癌患者主要的治疗手段之一,目前临床上常采用以奥沙利铂、亚叶酸钙和氟尿嘧啶为基础的化疗方案,但化疗药物的不良反应较多且常较难耐受,因而有较多的患者中途被迫放弃化疗[4]。临床上常联合中医药治疗,在增加疗效、改善患者生存质量、减低毒副反应发生率和减轻患者痛苦等方面有很好的疗效,在延长患者生存期方面也发挥了一定的作用[5]。复方苦参注射液(商品名:岩舒)是一种复方中药制剂,从苦参、白茯苓等中草药中提取制成,其主要有效成分为苦参碱、脱氧苦参碱和氧化苦参碱。有研究[6]表明,复方苦参注射液能通过促进肿瘤细胞凋亡以及促进抑制转移因子表达抑制肿瘤转移等作用来发挥抗肿瘤活性。目前复方苦参注射液联合化疗治疗晚期结直肠癌患者的临床研究虽已很多,但缺乏系统评价。为客观评价复方苦参注射液联合化疗治疗晚期结直肠癌的近期疗效和安全性,我们开展此Meta分析,以期为临床治疗和相关研究提供更可靠的依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型 随机对照试验(RCT),无论是否采用分配隐藏及盲法,只要提及“随机分组”的均纳入研究。语种限于中文和英文。
1.1.2 研究对象 (1)>18岁,均经病理/细胞学检查确证为晚期结直肠癌(结肠癌或直肠癌);(2)预计生存期>3个月;(3)研究对象间具有可比性;(4)血液学、肝肾功能及心电图无明显异常,无明显化疗禁忌证;(5)无性别、种族及国籍限制;(6)受试者均签署知情同意书。
1.1.3 干预措施 对照组只给予单纯化疗;实验组给予复方苦参注射液联合化疗。两组所用化疗方案相同。
1.1.4 结局指标 (1)有效率:采用RECIST标准或WHO关于实体瘤近期疗效评价标准判定有效率:总有效率(RR)=CR(完全缓解)+PR(部分缓解);(2)生存质量:以卡氏(KPS)评分为标准:治疗前后评分增加或减少<10分者为稳定;减少>10分者为下降;增加>10分者为改善。(3)毒副反应:主要有骨髓抑制(白细胞减少和血小板降低)、恶心呕吐、周围神经毒性、脱发等(WHO或NCI标准,分为0~Ⅳ度)。
1.1.5 排除标准 (1)合并其他恶性肿瘤;(2)除复方苦参注射液(通用名:岩舒)以外还联合使用了其他中药;(3)结直肠癌术后化疗;(4)肝肾功、血液学或心电图有明显异常者;(5)局部或全身感染者;(6)没有明确的评价指标和统计所需基本数据的研究。
1.2 文献检索 计算机检索Cochrane图书馆、MEDLINE、PubMed、中国知网(CNKI)、维普(VIP)、万方数据库(WanFang Data)和中国生物医学文献数据库(CBM),全面查找有关复方苦参注射液联合化疗与单纯化疗比较治疗晚期结直肠癌的RCT,检索时限均从建库至2015年5月。并在Google Scholar、Medical Martix和百度学术等搜索引擎在互联网上查找相关文献,同时手工检索相关专业杂志并对纳入文献的参考文献进行检索。检索策略经过多次预检索后确定,所有检索均采用主题词与自由词相结合的方式。中文检索词包括大肠癌、结肠癌、直肠癌、复方苦参注射液、复方苦参注射剂、岩舒等;英文检索词包括 colorectalcancer、carcinomaofcolon、carcinoma of rectum、ku shen、kushen、ku-shen、matrine和yanshu等。
1.3 文献筛选和资料提取 所纳入的文献均严格按照纳入与排除标准由两位研究人员独立筛选,然后再使用事先设计好的资料提取表提取相关数据。提取内容包括:(1)纳入研究的一般资料(文题、作者姓名、发表时间以及文献来源);(2)纳入研究的特征(研究对象的一般情况、各组患者的基线可比性、干预措施、分配隐藏和盲法等);(3)结局指标(有效率、生存质量及毒副反应)。如遇分歧通过两位研究人员讨论解决或交由第三方裁定。资料不全或缺乏的通过电话或邮件联系作者予以补充。
1.4 纳入研究的方法学质量评价 按照Cochrane系统评价员手册5.1.0版[7]中的偏倚风险评价标准对纳入研究的方法学质量进行评价。评价内容包括:(1)随机序列产生的具体方式;(2)是否分采用配隐藏;(3)是否使用盲法;(4)结果数据是否完整性;(5)是否存在选择性报告结果;(6)是否有其他偏倚。针对上述6条,分别给予“是”、“否”或“不清楚”的评价,其中“是”表示低度偏倚,“否”表示高度偏倚,“不清楚”表示缺乏相关信息或偏倚情况不确定。
1.5 统计学方法 应用RevMan5.3软件进行Meta分析。近期疗效和安全性指标均采用比值比(OR)或相对危险度(RR)作为效应量,且均给出其95%可信区间(CI)。首先对纳入研究结果间的异质性运用χ2检验进行分析。若不存在异质性或者异质性较小(I2≤50%,P≥0.1),可认为纳入研究结果间同质性较好,则采用固定效应模型进行Meta分析;若存在异质性(I2>50%,P<0.1),首先则应对其异质性来源进行分析,若不存在临床异质性,则采用随机效应模型进行Meta分析,若存在临床异质性,可就其异质性来源进行亚组分析及或通过敏感性分析来判断其结果稳定性,或者仅进行描述性分析。
2 结果
2.1 文献检索结果 初检出文献372篇,经逐层筛选后,最终纳入20个RCT[8-27],共1614例晚期结直肠癌患者,其中实验组患者818例,对照组患者796例。
2.2 纳入研究的基本特征和纳入研究的方法学质量评价 纳入研究的基本特征和方法学质量评价分别见表1和表2。

表1 纳入研究的基本特征
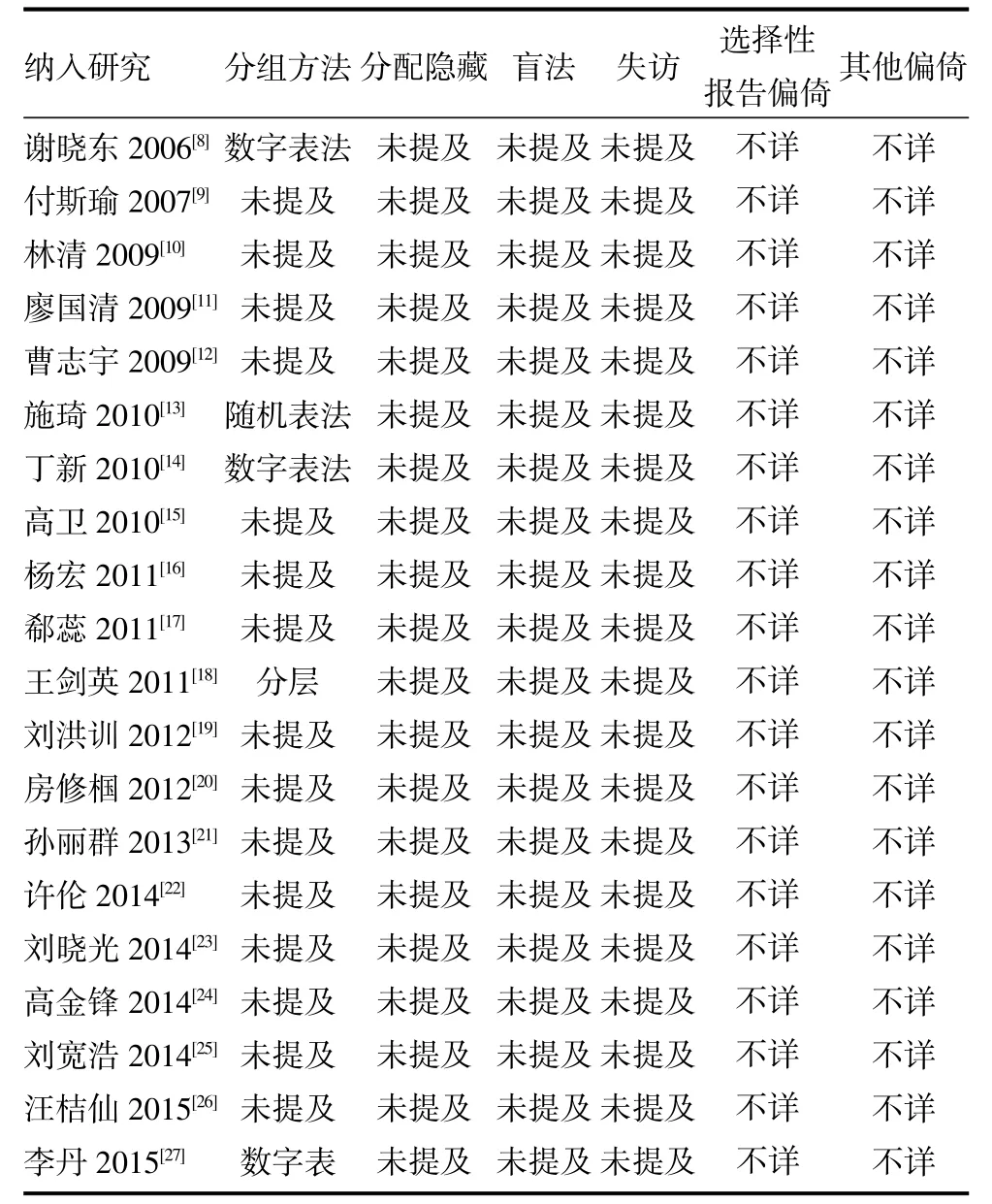
表2 纳入研究的方法学质量评价
2.3 Meta分析结果
2.3.1 有效率 共17项RCT[9-13,15-17,19-27]报道有效率指标。经异质性检验(P=0.56,I2=0%),结果表明各研究间无明显异质性,故采用固定效应模型进行分析,见图1。结果表明,两组有效率比较差异有统计学意义[0R=2.01,95%CI(1.58,2.55),P<0.00001]。
2.3.2 生存质量改善 共14项RCT[8,11-13,15-22,25-26]报道了生存质量改善情况。经异质性检验(P=0.39,I2= 0%),结果表明各研究间无明显异质性,故用固定效应模型进行分析,见图2。结果表明,两组生存质量改善比较差异有统计学意义 [0R=2.71,95%CI(2.11, 3.50),P<0.00001]。
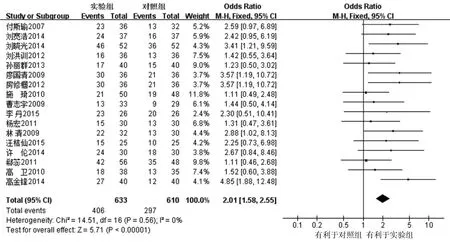
图1 两组患者疗效比较的Meta分析
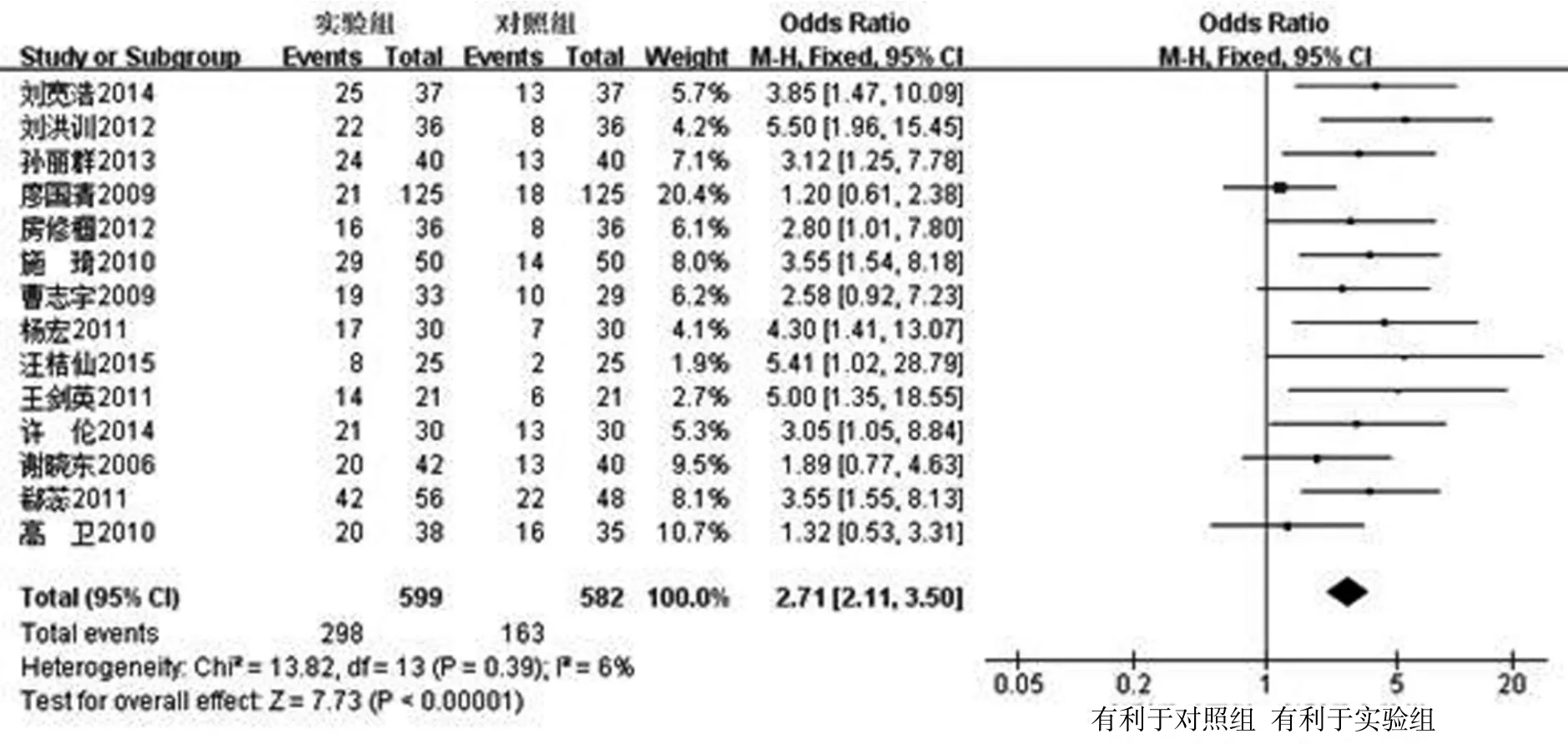
图2 两组患者生存质量改善比较的Meta分析
2.3.3 毒副反应 在临床试验中报告了多种不良反应,有骨髓抑制(主要包括白细胞减少和血小板减少)、恶心呕吐、腹泻、肝肾功能损害、脱发、周围神经毒性等,分别进行meta分析,见表3。结果表明,在白细胞减少[0R=0.23,95%CI(0.14,0.40),P<0.00001]、血小板减少[0R=0.46,95%CI(0.30,0.71),P=0.0004]、恶心呕吐[0R=0.33,95%CI(0.25,0.45),P<0.00001]、腹泻[0R=0.25,95%CI(0.15,0.39),P<0.00001]、肝功能[0R=0.19,95%CI(0.11,0.33),P<0.00001]、肾功能[0R=0.28,95%CI(0.11,0.72),P=0.008]、周围神经毒性[0R=0.33,95%CI(0.22,0.51), P<0.00001]和疼痛[0R=5.37,95%CI(1.92,15.04),P=0.001]等方面两组比较差异有统计学意义;而在减轻脱发 [0R= 0.94,95%CI(0.47,1.88),P=0.86]发生率方面两组比较差异无统计学意义(P>0.05)。

表3 两组患者患者毒副反应比较的Meta分析
2.3.4 发表偏倚分析 以比值比(OR)为横坐标,log [OR]为纵坐标绘制漏斗图,对纳入研究化疗期间疗效和生存质量进行发表偏倚分析(图3、图4),漏斗图显示大部分点都位于呈倒置漏斗的范围内,且基本对称于基线的两侧,提示不存在明显发表偏倚。
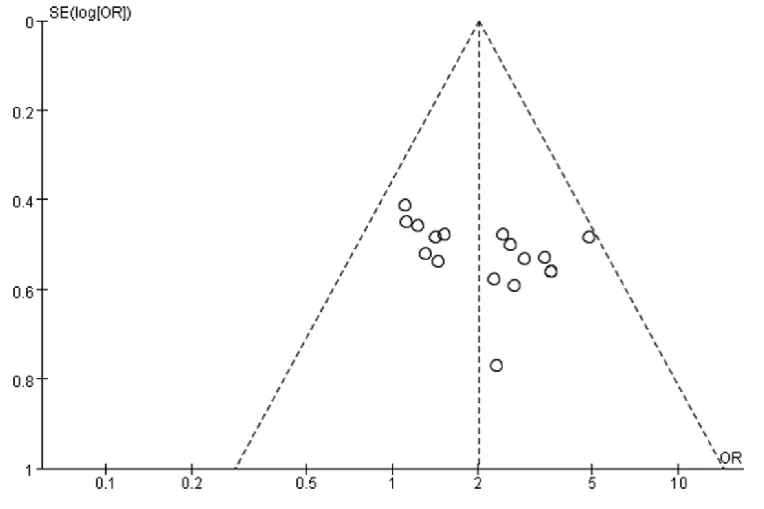
图3 化疗期间疗效发表偏倚漏斗图
3 讨论
目前用于转移性或复方性晚期结直肠癌的一线化疗方案有FOLFOX(奥沙利铂+亚叶酸钙+5-氟尿嘧啶)、FOLFIRI(伊立替康+5-氟尿嘧啶+四氢叶酸钙)、XELOXA(卡培他滨(希罗达)+奥沙利铂)或IROX(奥沙利铂+伊立替康)。随着对传统中药抗肿瘤机制研究的不断深入以及与化疗药物的联合应用的不断推广,传统抗肿瘤中药联合化疗在晚期结直肠癌的治疗中能在一定程度上增加化疗的疗效和可耐受性。有研究发现,复方苦参注射液在对恶性肿瘤有一定的疗效同时又能缓解化疗毒副反应[28]。
Meta分析结果显示,与单用化疗药物相比,复方苦参注射液联合化疗药物可提高近期疗效和改善生存质量,降低骨髓抑制、胃肠道反应、周围神经毒性、肝肾功能损害等并发症的发生率和缓解疼痛。
本系统评价局限性包括:(1)本研究仅以英文及中文作为检索语言,未对其他语种文献进行检索且最终纳入的文献全为中文文献,缺乏国外相关数据,可能存在一定的发表偏倚;(2)本研究纳入的20篇文献大部研究只报道随机分组未报告具体的随机序列产生方法、分配隐藏及盲法实施,可能会导致选择性偏倚、实施偏倚及测量偏倚,从而影响结果的可信度;(3)所有研究均缺乏长期随访的结果,所以尚不能评价复方苦参注射液联合化疗治疗晚期结直肠癌的远期疗效及生存率;(4)纳入的各研究的给药剂量、化疗方案和化疗周期不尽相同,可能对研究结果存在一定的影响。
综上所述,与单纯化疗相比,采用复方苦参注射液联合化疗药物可提高晚期结直肠癌的近期疗效和改善生存质量,降低骨髓抑制、胃肠道反应、肝肾功能损害、周围神经毒性等化疗毒副作用的发生率和缓解疼痛。但由于这些文献观察时间较短、缺乏长期随访跟踪试验,故复方苦参注射液联合化疗对晚期结直肠癌的远期疗效、生存率、改善患者的生存质量及减轻毒副反应的影响有待进一步探讨。因此更多高质量研究,特别是大样本、多中心的随机双盲对照试验需要开展,进一步评价其疗效和安全性。
[1]郑荣寿,张思维,吴良有,等.中国肿瘤登记地区2008年恶性肿瘤发病和死亡分析[J].中国肿瘤,2012,21(01):1-12.
[2]汪建平.重视结直肠癌流行病学研究[J].中国实用外科杂志,2013,33(08):622-624.
[3]Van Cutsem E,Costa F.Progress in the adjuvant treatment of colon Cancer:has it influenced clinical practice[J]. JAMA,2005,294(21):2758-2760.
[4]Kim JY,Kim YJ,Lee KW,et al.Practical outcome of adjuvant FOLFOX4 chemotherapy in elderly patients with stage III colon cancer:single-center study in Korea[J].Jpn J Clin Oncol,2013,43(2):132-138.
[5]李晓琳,马婧.中西医结合治疗结直肠癌的临床研究进展[J].现代中西医结合杂志,2013,22(3):323-325.
[6]李芮,杜健鹏,侯仰韶,等.复方苦参注射液对SGC-7901. HepG2和BEL-7402肿瘤细胞作用的实验研究[J].肿瘤研究与临床,2006,18(1):8-10.
[7]Higgins JPT,Green S.Cochrane Handbook for Systematic Reviews of Interventions Version 5.1.0[updated March 2011]. The Cochrane Collaboration,2011[OL].Available from:www. Cochrane-hand-book.org.
[8]谢晓冬,郑振东,刘大为,等.复方苦参注射液对晚期大肠癌患者生活质量影响的临床对照研究[C].第十届全国中西医结合肿瘤学术大会,2006.
[9]付斯瑜,李顺维.岩舒注射液联合化疗治疗晚期大肠癌的临床观察[J].中国医院用药评价与分析,2007,7(1):64-65.
[10]林清,吴华,谢忠,等.岩舒注射液联合FOLFOX方案治疗晚期大肠癌的临床观察[J].中国中药杂志,2009,34 (3):352-353.
[11]廖国清,曲怡梅,刘鹏辉,等.复方苦参注射液联合FOLFOX-4方案治疗晚期结直肠癌的临床研究[J].中国医院用药评价与分析,2009,9(3):207-208.
[12]曹志宇,蒲永东,何建苗,等.晚期结直肠癌应用复方苦参注射液联合FOLFOX-4方案化疗的临床观察[J].中国医院用药评价与分析,2009,9(12):940-941.
[13]施琦,王朝霞,赵庆洪.复方苦参注射液联合FOLFIRI方案治疗转移性或复发性晚期大肠癌50例[J].中国新药杂志,2010,19(17):1589-1592.
[14]丁新,肖秀英,杨晓燕,等.复方苦参注射液联合FOLFOX4方案治疗晚期结直肠癌的临床观察[J].中国癌症杂志,2010,20(11):860-863.
[15]高卫,李红宇,党琦.复方苦参注射液联合化疗治疗转移性结直肠癌疗效观察[J].山东医药,2010,50(41):85-86.
[16]杨宏,李慧,张英,等.复方苦参注射液联合化疗治疗结直肠癌30例[J].中国医药导报,2011,08(5):67-68.
[17]郗蕊.复方苦参注射液联合化疗治疗晚期大肠癌的临床效果[J].医药论坛杂志,2011,32(14):52-53.
[18]王剑英,崔晓梅,杜云英,等.复方苦参注射液配合化疗治疗晚期大肠癌的临床观察[J].中国现代药物应用,2011,05(6):146-147.
[19]刘洪训,华霞.复方苦参注射液联合化疗治疗晚期大肠癌36例[J].浙江中医杂志,2012,47(3):225.
[20]房修椢,张可帅.复方苦参注射液联合化疗治疗晚期结肠癌的临床疗效分析[J].肿瘤药学,2012,02(4):293-295.
[21]孙丽群.复方苦参注射液联合化疗治疗转移性结直肠癌临床研究[J].吉林中医药,2013,33(1):53-54.
[22]许伦.浅谈复方苦参注射液联合化疗治疗晚期结肠癌的临床疗效[J].当代医药论丛,2014,12(11):38-9.
[23]刘晓光.复方苦参注射液联合化疗治疗晚期结肠癌的可行性分析[J].中国现代药物应用,2014,8(19):150-151.
[24]高金锋,封革.复方苦参注射液联合化疗方案治疗晚期结肠癌40例[J].中国药业,2014,23(24):103-105.
[25]刘宽浩,王艺卓,苏滑.复方苦参注射液联合化疗治疗晚期大肠癌的疗效观察[J].河南外科学杂志,2014,20(4):39-40.
[26]汪桔仙,许金钗,郑霞辉.复方苦参注射液联合化疗治疗晚期大肠癌25例观察[J].浙江中医杂志,2015,50(3):230.
[27]李丹,张启洪,吴盛,等.复方苦参注射液联合化疗治疗晚期结肠癌临床研究[J].辽宁中医杂志,2015,42(05):1021-1022.
[28]付艳,王小京,肖文华,等.复方苦参注射液用于化疗的观察[J].中国医院用药评价与分析,2008,8(5):384-385.
(收稿:2015-08-22 修回:2016-01-24)
1兰州大学第一临床医学院(兰州 730000);2西北民族大学医学院(兰州 730000);3兰州大学第一医院普外科(兰州730000)
姚南,Email:Pro-YaoNan@163.com
