HPLC-MS/MS法同时测定人血浆中依那普利和依那普利拉的浓度
2016-01-31施振国
张 勇,施振国
HPLC-MS/MS法同时测定人血浆中依那普利和依那普利拉的浓度
张勇*,施振国
[摘要]目的建立人血浆中依那普利和依那普利拉含量测定的高效液相色谱-串联质谱(HPLC-MS/MS)方法。方法血浆样品加入内标(贝那普利拉),以含0.1%甲酸的甲醇沉淀蛋白后,进行HPLC-MS/MS分析。色谱柱为Hedera ODS-2 C18(150 mm×2.1 mm,5 μm),流动相为甲醇-0.5%甲酸水溶液梯度洗脱,流速为0.4 mL/min,柱温为30 ℃,采用多反应监测(MRM)方式进行定量分析,用于监测的离子质荷比分别为m/z 377.2 → m/z 234.3(依那普利)、m/z 349.3 → m/z 206.2(依那普利拉)和m/z 397.4 → m/z 351.4(内标,贝那普利拉)。结果人血浆中依那普利和依那普利拉的线性范围分别为0.2~200 ng/mL(r=0.999 9)、0.5~120 ng/mL(r=0.999 3);批内、批间精密度均<11.3%。结论该方法快速、灵敏、专属性强,可用于人血浆中依那普利和依那普利拉浓度的测定。
[关键词]依那普利;依那普利拉;高效液相色谱-串联质谱法;人血浆
[Abstract]ObjectiveTo establish a method for determination of enalapril and enalaprilat in human plasma by high-performance liquid chromatography tandem mass spectrometry.MethodsAfter being mixed with the internal standard benazeprilat,plasma samples were deproteinized with methanol (0.1% formic acid) and separated by HPLC-MS/MS on a 30 ℃ Hedera ODS-2 C18(150 mm×2.1 mm,5 μm)column with a gradient elution by the mobile phase of methanol (A) and 0.1 % formic acid water solution (B) at a flow rate of 0.4 mL/min.Quantification was performed using multiple reaction monitoring (MRM) of the transitions of m/z 377.2 → m/z 234.3 for enalapril,m/z 349.3 → m/z 206.2 for enalaprilat and m/z 397.4 → m/z 351.4 for IS (benazeprilat),respectively.ResultsCalibration curves for enalapril and enalaprilat were linear over the range of 0.2~200 ng/mL (r=0.999 9),0.5 ~ 120 ng/mL(r=0.999 3),respectively.The intra-/inter-batch RSD was less than 11.3%.ConclusionThe established method is rapid, specific and sensitive,it could be used for the quality control for the quantification of enalapril and enalaprilat in human plasma.
收稿日期:2015-04-17
通信作者*
DOI:10.14053/j.cnki.ppcr.201512020
Simultaneous determination of enalapril and enalaprilat in human plasma by high-performance liquid chromatography tandem mass spectrometryZHANG Yong*,SHI Zhen-guo(Department of Pharmacy,Chinese PLA General Hospital,Beijing 100853,China)
Key words:Enalapril;Enalaprilat;HPLC-MS/MS;Human plasma
0内容
依那普利是临床上常用的一线血管紧张素转换酶抑制剂(ACEI)类降压药,口服后在人体内经肝脏代谢为活性代谢产物依那普利拉,通过抑制血管紧张素转化酶,降低体内血管紧张素Ⅱ的含量,使全身血管舒张而实现降压的功效[1-2]。目前用于同时定量测定人体内依那普利及依那普利拉的方法主要有高效液相色谱-质谱法(HPLC-MS)[3-4]、高效液相色谱-串联质谱法(HPLC-MS/MS)[5-7],但均存在样品前处理繁琐、样品用量大、灵敏度不高等不足,本研究采用直接蛋白沉淀的样品前处理方法,建立了一种高效、准确、灵敏的HPLC-MS/MS方法,进行人体内依那普利及依那普利拉血药浓度的定量分析。
1材料
1.1药物与试剂马来酸依那普利对照品(批号:100705-201203)、依那普利拉对照品(批号:100707-200401)、贝那普利拉对照品(批号:100771-201001)均购自中国食品药品检定研究院;甲醇(色谱纯,德国Merck公司);甲酸(分析纯,国药集团化学试剂有限公司);水为去离子水。
1.2仪器Agilent 6410B高效液相色谱-串联质谱联用仪,含:双高压泵、自动进样器、柱温箱、电喷雾离子化接口、三重四极杆质谱检测器。色谱工作站:MassHunter Workstation Software。
2方法与结果
2.1色谱条件色谱柱:Hedera ODS-2 C18(150 mm×2.1 mm,5 μm,江苏汉邦科技有限公司);预柱:C18保护柱(4.0 mm × 2.0 mm,5 μm,美国Phenomenex公司)。流动相:甲醇(A)- 0.5%甲酸水溶液(B)梯度洗脱:0~0.5 min,B 为 70%;0.5~0.75 min,B 由70%降为 30%;0.75~4 min,B 为 30%;4~4.25 min,B由30%升为 70%。4.25~7 min,B 为 70%。流速:0.4 mL/min;柱温:30 ℃;进样量:5 μL。
2.2质谱条件离子检测方式为多反应监测(MRM);离子化方式为气动辅助电喷雾离子化(ESI);传输区电压:120 V;干燥气流速:10 L/min;雾化室压力:40 psig;干燥气温度:350 ℃。用于定量分析监测离子对:依那普利,[M+H]+,m/z377.2 →m/z234.3(碰撞能量:18 eV);依那普利拉,[M+H]+,m/z349.3 →m/z206.2(碰撞能量:15 eV);内标(贝那普利拉),[M+H]+,m/z397.4 →m/z351.4(碰撞能量:20 eV)。
2.3溶液的制备分别精密称取盐酸依那普利对照品、依那普利拉对照品、内标(贝那普利拉)对照品适量,置于10 mL容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得浓度为1 mg/mL的各储备液。所有储备液置于4 ℃冰箱中保存待用。
2.4血浆样品的处理精密吸取血浆样品200 μL,置于1.5 mL离心管中,加入内标(2 μg/mL)对照品溶液10 μL,旋涡混匀,加入甲醇(含0.1%甲酸)600 μL,旋涡3 min,静置10 min后于15 600 r/min离心10 min,吸取上清液转移至自动进样器样品瓶中,进行HPLC-MS/MS分析,进样量为5 μL。
2.5方法学验证
2.5.1专属性分别取6个不同来源的空白血浆200 μL,除不加内标外,其余按“2.4”项下操作,进行HPLC-MS/MS分析,得空白血浆样品色谱图;将依那普利、依那普利拉和内标对照品加入空白血浆后,同法操作,得血浆样品色谱图;取健康受试者给药后的血浆样品,同法操作,得健康受试者血浆样品色谱图。典型色谱图见图 1。由图1可见,依那普利、依那普利拉和内标的保留时间分别约为3.9 min、3.6 min和3.9 min,各成分峰形良好,无杂峰干扰测定。本方法具有较高的特异性,能准确测定血浆中依那普利的浓度,灵敏度较高。

图1 人血浆中依那普利、依那普利拉和内标(贝那普利拉)的色谱图
2.5.2线性范围与定量下限取1.5 mL离心管数支,分别加入不同量的依那普利对照品溶液后以氮气流吹干,加入空白血浆0.2 mL,旋涡混匀,配成含依那普利浓度分别为0.2、1、3、10、30、100、200 ng/mL及依那普利拉0.5、2、5、15、40、80、120 ng/mL的标准含药血浆,按“2.4”项下操作,记录色谱图,分别计算依那普利以及依那普利拉峰面积As和内标峰面积Ai的比值f。以平均比值f(f=As/Ai)对血药浓度C作权重回归计算,用加权最小二乘法(W=1/χ2)进行回归运算,得出血浆样品中依那普利和依那普利拉标准曲线的典型权重回归方程,依那普利:f=0.005 732+0.065 80×C(r=0.999 9),依那普利拉:f=0.014 00+0.005 874×C(r=0.999 3)。依那普利在血浆中的定量下限为0.2 ng/mL,依那普利拉在血浆中的定量下限为0.5 ng/mL。
2.5.3精密度和准确度制备含依那普利浓度分别为0.5、20、180 ng/mL及依那普利浓度分别为1、10、100 ng/mL的标准含药血浆样品,每个浓度配制5份,并配制1条标准曲线,按“2.4”项下操作,共配制3个分析批,记录色谱图,计算样品和内标峰面积的比值f,代入当批的标准曲线,求得实测浓度及其准确度,计算批内和批间精密度。结果表明,本方法的准确度与精密度RSD均<15%,符合生物样品分析要求(表1)。
2.5.4基质效应和提取回收率按“2.4”项下操作,分别制备6种不同来源的空白血浆上清液适量,加入适量依那普利和依那普利拉对照品溶液及内标溶液,配制依那普利浓度分别为0.5、20、180 ng/mL及依那普利浓度分别为1、10、100 ng/mL的含药血浆样品,每个浓度6份,进行LC-MS/MS分析,记录依那普利、依那普利拉和内标峰面积(A),并分别计算依那普利、依那普利拉峰面积和内标峰面积的平均值(B);以水代替空白血浆,其余操作同上,每个浓度3份进行LC-MS/MS分析,记录依那普利、依那普利拉和内标的峰面积,并分别计算依那普利、依那普利拉峰面积和内标峰面积的平均值(C);按“2.5.3”项下操作,配制依那普利浓度分别为0.5、20、180 ng/mL,依那普利浓度分别为1、10、100 ng/mL的标准含药血浆样品,每种浓度配制5份,进行LC-MS/MS分析,记录依那普利、依那普利拉和内标峰面积(D)。依那普利、依那普利拉和内标的介质效应的计算公式:ME(%)=A/C×100%;依那普利、依那普利拉和内标的提取回收率的计算公式:R(%)=D/B×100%。结果表明,人血浆样品中依那普利、依那普利拉和内标的介质效应均为85%~115%,可认为没有介质效应。不同浓度待测物的提取回收率恒定。见表1。
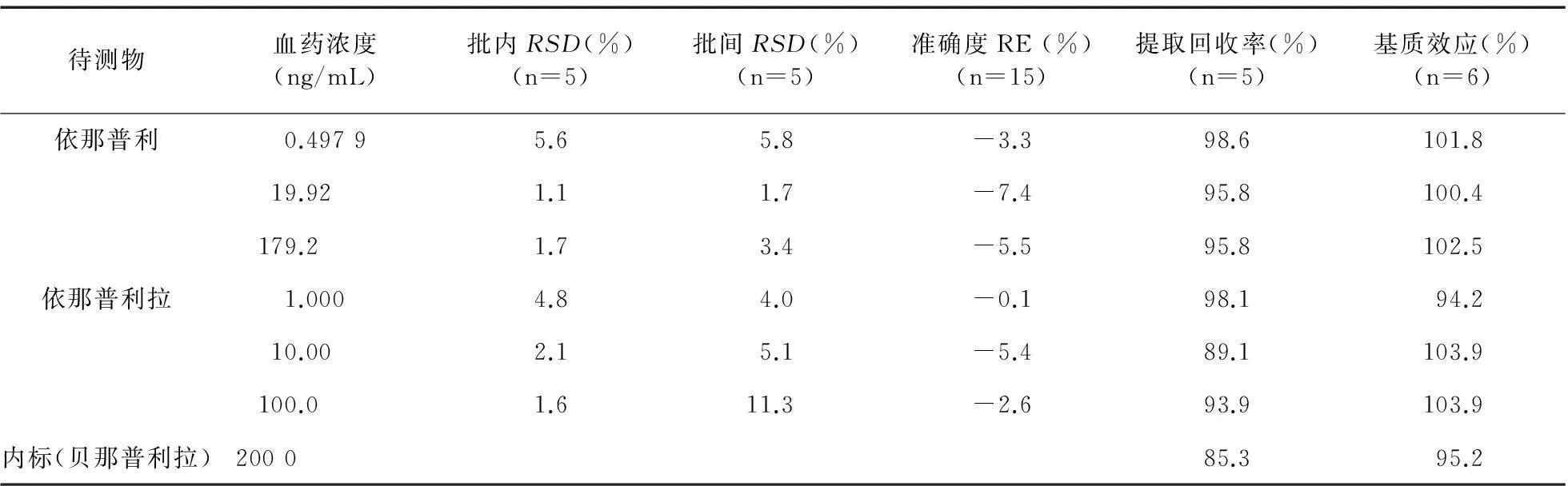
表1 人血浆中依那普利和依那普利拉的精密度、准确度、提取回收率和基质效应结果
注:RSD:相对标准偏差;RE:相对误差
2.5.5稳定性配制含依那普利浓度分别为0.5、20、180 ng/mL及含依那普利拉浓度分别为1、10、100 ng/mL的含药血浆适量,每种浓度分取12份,每份0.2 mL。3份于配制好后按“2.4”项下操作,并立即分析,并在测定完成后,在进样器样品盘中放置11.5 h后再次进样分析;3份于室温放置10 h后按“2.4”项下操作分析;3份于配制好后反复冻融3次,按“2.4”项下操作分析;3份于配制好后放入-20 ℃冰箱中冷冻保存8周后,取出化冻,按“2.4”项下操作分析。由相应的标准曲线方程求出各样品的浓度,计算测得浓度平均值。结果表明,依那普利及依那普利拉血浆样品在室温下放置10 h、进样器中放置11.5 h、反复冻融3次及冰冻放置8周条件下的稳定性良好。
3讨论
本研究采用蛋白沉淀法对血浆样品进行前处理,分别考察了样品经不同蛋白沉淀剂(甲醇、乙腈)处理后,待测物的提取回收率,结果表明,血浆样品经甲醇处理后,提取回收率稳定且高于乙腈处理的样品。
当采用质谱法对生物样品进行定量分析时,如何解决基质效应,保证样品测定的准确度至关重要。本研究在选择甲醇作为样品前处理的蛋白沉淀剂的基础上,通过加入甲酸调节血浆样品的pH值,最大程度地将血浆样品中的内源性杂质随血浆蛋白沉淀除去,同时采用梯度洗脱的方式避免了基质效应的产生,保证了样品测定的准确。通过优化甲酸的浓度(0、0.1%、0.3%、0.5%、1.0%),最终选择加入3倍血浆样品体积的甲醇(含0.1%甲酸)作为样品的前处理方法。为改善依那普利和依那普利拉的色谱保留,改善色谱峰形,提高待测物的检测灵敏度,本研究选择0.5%的甲酸水溶液作为水相,从而保证了样品测定的高效、灵敏。
参考文献:
[1]张洪波.吲达帕胺与依那普利联合应用治疗中、重度高血压疗效观察[J].实用药物与临床,2005,8(3):35-36.
[2]李鹏,赵焕军,郝兵.缬沙坦和依那普利治疗原发性高血压的对比研究[J].实用药物与临床,2006,9(3):143-144.
[3]刘灿,杨龙华,丁黎,等.人血浆中依那普利及依那普利拉的测定及其在人体内的药动学[J].中国临床药学杂志,2006,15(1):34-37.
[4]肖遐,袁洪,谭鸿毅,等.HPLC-MS法同时测定人血浆中依那普利及其代谢物依那普利拉的浓度[J].中南药学,2008,6(1):33-35.
[5 ]张梦琪,刘罡一,贾晶莹,等.液相色谱-串联质谱法测定人血清中依那普利及依那普利拉的浓度[J].中国新药与临床杂志,2009,28(10):761-765.
[6]Lu S,Jiang K,Qin F,et al.Simultaneous quantification of enalapril and enalaprilat in human plasma by high-performance liquid chromatography-tandem mass spectrometry and its application in a pharmacokinetic study[J].J Pharm Biomed Anal,2009,49(1):163-167.
[7]Gu Q,Chen X,Zhong D,et al.Simultaneous determination of enalapril and enalaprilat in human plasma by liquid chromatography-tandem mass spectrometry[J].J Chromatography B,2004,813(1-2):337-342.
作者单位:1.嘉兴市食品药品检验检测院,浙江 嘉兴 314000;2.浙江嘉兴学院,浙江 嘉兴 314000
