HPLC法同时测定氨咖黄敏胶囊中二组分的含量
2016-01-31程爱平
邹 燕,程爱平,林 灿
HPLC法同时测定氨咖黄敏胶囊中二组分的含量
邹燕1*,程爱平1,林灿2
[摘要]目的建立高效液相色谱法同时测定氨咖黄敏胶囊中对乙酰氨基酚、咖啡因2种成分的含量。方法采用Agilent extend-C18(150 mm×4.6 mm,5 μm)色谱柱,流动相为乙腈(A)-三乙胺溶液(1 mL三乙胺加79 mL水,调pH至3.1,B)(17∶83),流速1.0 mL/min,检测波长217 nm;柱温25 ℃,进样量15 μL。结果对乙酰氨基酚、咖啡因的线性浓度范围分别为831.33~2 078.33 μg/mL (r=0.999 6)和50.27~125.67 μg/mL (r=0.999 4),两组分平均回收率分别为99.99% (RSD=0.02%)和100.14% (RSD=0.52%)。结论该方法灵敏度、准确度高,重复性好,适用于氨咖黄敏胶囊中对乙酰氨基酚和咖啡因2种有效成分的测定。
[关键词]氨咖黄敏胶囊;对乙酰氨基酚;咖啡因;高效液相色谱;含量测定
[Abstract]ObjectiveTo establish a method for simultaneous determination of paracetamol and caffeine in paracetamol,caffeine,artificial cow-bezoar and chlorphenamine maleate capsules by HPLC.MethodsThe HPLC system consisted of Agilent extend-C18column (150 mm×4.6 mm,5 μm) with a mobile phase of acetonitrile (A)-triethylamine solution (1 mL triethylamine+ 79 mL water,pH 3.1,B) (17∶83),the flow rate was 1.0 mL/min and the detection wavelength was at 217 nm.The column temperature was 25 ℃,and the sample quantity was 15 μL.ResultsThe linear ranges of paracetamol and caffeine were 831.33~2 078.33 μg/mL (r=0.999 6) and 50.27~125.67 μg/mL (r=0.999 4),and the average recovery rates were 99.99% (RSD=0.02%) and 100.14% (RSD=0.52%).ConclusionThe method is of high sensitivity,accuracy and repeatability,it can be used for the determination of paracetamol and caffeine in paracetamol,caffeine,artificial cow-bezoar and chlorphenamine maleate capsules.
收稿日期:2015-03-28
通信作者*
DOI:10.14053/j.cnki.ppcr.201512021
Content determination of two components in paracetamol,caffeine,artificial cow-bezoar and chlorphenamine maleate capsules by HPLCZOU Yan1*,CHENG Ai-ping1,LIN Can2(1.Jiaxing Institiute for Food and Drug Control,Jiaxing 314000,China;2.Jiaxing University,Jiaxing 314000,China)
Key words:Paracetamol,caffeine,artificial cow-bezoar and chlorphenamine maleate capsules;Paracetamol;Caffeine;HPLC;Content determination
0引言
氨咖黄敏胶囊是感冒用药类非处方药,适用于缓解普通感冒及流行性感冒所引起的发热、头痛、打喷嚏、咽喉疼痛、鼻塞等症状。本品为复方制剂,主要有效成分为对乙酰氨基酚、咖啡因、马来酸氯苯那敏和人工牛黄。该药物的质量标准收录在《中国药品标准》的化学药品第三册中[1]。在国家药品标准中,对乙酰氨基酚的含量测定采用回流后外标指示剂法,咖啡因则采用氯仿萃取后滴定法测定,这两种方法操作较繁琐、存在的不确定因素较多。本文主要通过高效液相色谱法同时测定对乙酰氨基酚、咖啡因两种成分的含量,结果表明方法可行,现报道如下。
1仪器与试药
1.1仪器Agilent1200高效液相色谱仪(安捷伦公司);UV-2501PC紫外分光光度计(日本岛津公司);XS105DU电子天平(梅特勒-托利多有限公司);Delta320H酸度计(梅特勒-托利多有限公司);超声波清洗仪(USC502,上海波龙电子设备有限公司)。
1.2药品与试剂氨咖黄敏胶囊(标示量为对乙酰氨基酚250 mg/粒、咖啡因15 mg/粒,浙江康恩贝股份有限公司,批号:20140313、20140827、20141001),对乙酰氨基酚对照品(含量100%,中国药品生物制品检定所,批号:100018-200408),咖啡因对照品(含量100%,中国药品生物制品检定所,批号:171215-201211)。磷酸(杭州化学试剂有限公司)分析纯,乙腈(德国德姆施塔市墨客股份有限公司)色谱纯,三乙胺[赛默飞世尔科技(中国)有限公司]色谱纯。
2方法与结果
2.1分析方法验证
2.1.1色谱条件色谱柱:Agilent extend-C18(150 mm×4.6 mm,5 μm);流动相:A相为乙腈,B相为三乙胺-水(1∶79),A∶B为17∶83;流速:1.0 mL/min;检测波长:217 nm;柱温:25 ℃;进样量:15 μL。在该色谱条件下对照品中两种成分的色谱峰分离度>1.5,理论塔板数均>2 000,符合使用条件。
2.1.2储备溶液的配制精密称取咖啡因对照品7.54 mg置10 mL容量瓶中,加流动相超声5 min溶解后定量稀释至刻度,摇匀,即得储备液;放入4 ℃冰箱保存备用。精密称取对乙酰氨基酚对照品12.47 mg置于10 mL容量瓶中,精密加入上述咖啡因对照品的储备溶液1 mL,超声3 min溶解后用流动相定容得混合对照品溶液。
2.1.3供试品溶液的配制取氨咖黄敏胶囊30粒,取内容物精密称定,研细,精密称取适量(约相当于对乙酰氨基酚250 mg),置于20 mL容量瓶中,加入少量流动相超声溶解10 min,冷却后定容。用滤纸过滤后,精密量取1 mL续滤液至10 mL容量瓶稀释至刻度,即得供试品溶液。
2.1.4线性范围取混合对照品溶液,依次精密吸取10、12、15、17、20、22、25 μL混合对照溶液注入高效液相色谱仪,记录色谱图。见图1。以峰面积(Y)为纵坐标、对照品浓度(X,μg/mL)为横坐标,分别绘制标准曲线,计算回归方程。得对乙酰氨基酚方程Y=3.718 1 X+7 606.1 (r=0.999 6),线性范围831.33~2 078.33 μg/mL;咖啡因方程Y=40.252 X+1 186.2 (r=0.999 4),线性范围50.27~125.67 μg/mL。

图1 HPLC色谱图
2.1.5精密度试验取“2.1.2”项下混合对照品溶液,按“2.1.1”项条件,连续平行进样5次。结果显示,对乙酰氨基酚峰面积的RSD为0.21%,咖啡因峰面积的RSD为0.15%。
2.1.6稳定性试验为了考察溶液的稳定性,取“2.1.3”项下供试品溶液,分别于0、2、4、24 h,按“2.1.1”项下色谱分析条件进行测定,记录下2种成分的相应峰面积。结果对乙酰氨基酚RSD为0.56%,咖啡因RSD为1.22%,表明该样品溶液在24 h内稳定性良好。
2.1.7重复性取“2.1.3”项下供试品溶液,按照 “2.1.1”条件连续进样5次,记录两组分相应峰面积,得对乙酰氨基酚的RSD为0.3%,咖啡因为1.8%,表明两组分的重复性良好。
2.1.8加样回收率精密称取对乙酰氨基酚对照品1 260.00 mg、咖啡因对照品75.04 mg置50 mL量瓶中,加流动相溶解并稀释至刻度,摇匀;精密称取已知含量的供试品适量(约相当于对乙酰氨基酚250 mg) 3份,分别置于20 mL容量瓶中,各加入上述对照品混合溶液8、10、12 mL,加入少量流动相超声溶解10 min,冷却后定容。用滤纸过滤后,精密量取1 mL续滤液置20 mL容量瓶加流动相稀释至刻度,得加样回收率溶液。按“2.1.1”项色谱条件进行分析,计算含量,结果见表1。
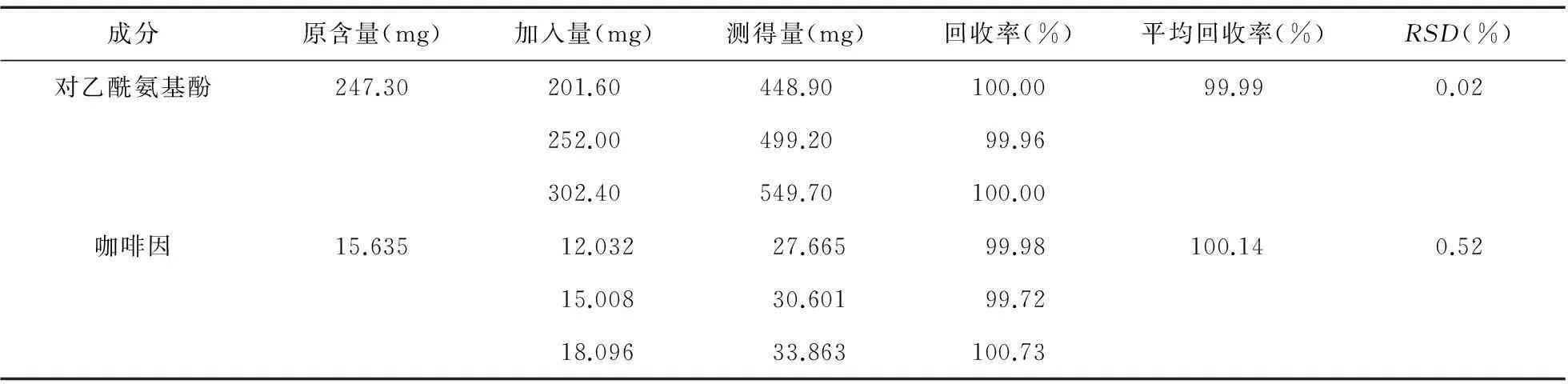
表1 回收率试验结果
2.2样品测定取康恩贝公司生产的3批不同的氨咖黄敏胶囊内容物按“2.1.3”项方法制成3份供试品溶液,注入高效液相色谱仪,按“2.1.1”项下色谱条件对3个供试品进行色谱分析,得到实验数据,计算得到3批样品中2种成分的百分含量。同时,按照国家药品标准对含量进行测定,并与色谱法所得的结果进行比较,见表2。两种方法实验结果较为接近,相比较而言色谱法耗时少,操作简便。

表2 样品含量测定结果(n=3)
3讨论
3.1波长的选择根据相关文献资料[2-5],选用常用的十八烷基键和硅胶色谱柱;另选定乙腈-三乙胺溶液(1 mL三乙胺加79 mL水,用磷酸调pH至3.1)(17∶83)为初始流动相,对2种成分的对照品进行溶解,然后用于紫外扫描。因每粒胶囊中含有对乙酰氨基酚250 mg、咖啡因15 mg,含量相差较大,为了避免在含量测定时对乙酰氨基酚浓度过高出现平峰或者咖啡因浓度过低不易出峰,选择的波长应以Abs值咖啡因>对乙酰氨基酚为宜,且两者的Abs差值尽量大。
取对乙酰氨基酚对照品、咖啡因对照品,用流动相制得含对乙酰氨基酚对照品8 μg/mL的溶液和含咖啡因对照品10 μg/mL的溶液。用 UV-2501PC紫外分光光度计在200~300 nm波长处对两种溶液进行波长扫描,见图2。由图2可见,在约200~230 nm波长处,对乙酰氨基酚的Abs先于217.38处达到最小值,然后逐渐变大,且与咖啡因的Abs差值较大,故选择217 nm作为测定波长。
3.2流动相比例的调整选择乙腈为A相、三乙胺溶液(三乙胺∶水为1∶79,溶液用磷酸调pH至3.1抽滤)为B相,通过工作站调整有机相与水相的比例并保持其他条件不变。结果显示,不同流动相比例下,各峰的分离度均>1.5,最终选定分离度>3且保留时间相对较短的流动相比例,即A∶B为17∶83。
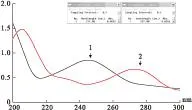
图2 UV图谱
3.3柱温的选择笔者分别对日常实验中最为常用的25、30、35 ℃进行了试验,结果显示,温度对该样品中所测2种成分含量没有显著影响,所以选择药品检验中较为常用的柱温(25 ℃)作为该项实验柱温。
3.4流速的选择为了选定适宜的流速,分别选用常用流速0.5、1、1.5 mL/min进行试验,结果显示,当流速为1.5 mL/min时,各峰的理论板数明显降低,该流速舍去不考虑。流速为0.5、1 mL/min时,各参数均符合要求,此次选择较为常用的1.0 mL/min。
本法选定的色谱条件效率高,分离度好,柱效理想;样品的前处理较国家标准更简单、快速;实验结果与传统方法所得实验结果相近。因此,采用HPLC法同时测定氨咖黄敏胶囊中的对乙酰氨基酚和咖啡因的含量是可行的,为该药品标准的修订提供了参考。
参考文献:
[1]国家药典委员会.国家药品标准化学药品地方标准上升国家标准[S].2002:263.
[2]孙超,崔潇,成秉辰,等.HPLC法同时测定氨咖黄敏胶囊中三种成分[J].哈尔滨商业大学学报(自然科学版),2013,29(2):145-147,175.
[3]吴俊芳,张涛,李丽萍.高效液相色谱法测定氨咖黄敏胶囊的含量[J].中国药业,2011,20(4):33-34.
[4]张英芳,李明霞,韩春英.HPLC法同时测定氨咖黄敏胶囊中三组分的含量[J].齐鲁药事,2012,21(8):462-463.
[5]陈玉璞,张毅,董智攀.高效液相色谱法同时测定氨咖黄敏胶囊中对乙酰氨基酚和马来酸氯苯那敏的含量[J].中国医药导报,2010,7(4):38-39.
作者单位:1.中国医科大学药学院,沈阳 110001;2.辽宁省建平县医院药局,朝阳 122400;3.辽宁省中药研究所,沈阳 110041
