毛细管电泳法检测糖化血红蛋白的分析性能评估
2016-01-20刘文彬金中淦唐丽萍王美娟欧元祝虞啸炫
李 卿, 刘文彬, 金中淦, 唐丽萍, 王美娟, 欧元祝, 虞啸炫, 居 漪
(上海市临床检验中心生化室,上海 200126)
毛细管电泳法检测糖化血红蛋白的分析性能评估
李卿,刘文彬,金中淦,唐丽萍,王美娟,欧元祝,虞啸炫,居漪
(上海市临床检验中心生化室,上海 200126)
摘要:目的评估毛细管电泳(CE)法检测糖化血红蛋白(HbA1c)的精密度、正确度、线性和抗干扰性,并与高效液相色谱法(HPLC)进行比对。方法根据不同的评估内容,收集相应样本,分别使用SEBIA CAPILLARYSTM2 Flex Piercing毛细管电泳仪(毛细管电泳法)、ARKRAY HA-8160全自动HbA1c分析仪(HPLC)和IFCC参考方法检测HbA1c。采用SPSS 19.0 软件进行统计描述及线性回归模型分析。结果毛细管电泳法检测HbA1c在常见浓度(4.91%~9.67%)下的不精密度均<2%;与IFCC参考方法,相关程度较好(R2=0.993);当HbA1c浓度为5.0%~17.6%时,毛细管电泳法具有良好的线性(R2= 0.995),对氨甲酰化血红蛋白、不稳定HbA1c、胆红素、乳糜微粒等具有较好的抗干扰能力(绝对偏倚≤0.5%)。毛细管电泳法HbA1c的测定值与HPLC具有较好的相关性(R2=0.993)。 结论毛细管电泳法的精密度、正确度、线性和抗干扰性等分析性能均符合临床实验室常规检测HbA1c的要求。
关键词:糖化血红蛋白;毛细管电泳法;高效液相色谱
中图分类号:
文章编号:1673-8640(2015)02-0181-04R446.1
文献标志码:码:A
DOI:10.3969/j.issn.1673-8640.2015.02.019
Abstract:ObjectiveTo evaluate the precision, accuracy, linearity and anti-interference ability of capillary electrophoresis (CE) for the determination of hemoglobin A1c(HbA1c),and compare it with high performance liquid chromatography (HPLC). MethodsSamples were collected according to each evaluation protocol. Samples were determined by SEBIA CAPILLARYSTM2 Flex Piercing HbA1canalyzer (CE method), ARKRAY HA-8160 automatic HbA1canalyzer (HPLC) and IFCC reference method. Statistical analysis and linear regression analysis were performed by SPSS 19.0. ResultsThe impression at common HbA1clevels (4.91%-9.67%) was <2%. The CE method and IFCC reference method showed good correlation (R2=0.993). The linearity was good (R2= 0.995) from HbA1c5.0% to 17.6%. The results were not significantly influenced by carbamylated hemoglobin, labile HbA1c, bilirubin, chylomicron and so on (absolute bias ≤0.5%). SEBIA and HA-8160 showed good correlation (R2=0.993). ConclusionsThe precision, accuracy, linearity and anti-interference ability of SEBIA can meet the requirement of routine HbA1cdetermination in clinical laboratories.
作者简介:李卿,男,1981年生,硕士,主管技师,主要从事临床生化检验标准化工作。
通讯作者:居漪,联系电话:021-68316300-1204。
收稿日期:(2014-05-29)
Evaluation on the analytical performance of capillary electrophoresis for the determination of HbA1cLIQing,LIUWenbin,JINZhonggan,TANGLiping,WANGMeijuan,OUYuanzhu,YUXiaoxuan,JUYi.(DepartmentofClinicalChemistry,ShanghaiCenterforClinicalLaboratory,Shanghai200126,China)
Key words: Hemoglobin A1c; Capillary electrophoresis; High performance liquid chromatography

糖化血红蛋白(hemoglobin A1c, HbA1c)可以反映血糖的长期控制情况,与1型和2型糖尿病并发症风险高度相关。因此,多个国家和国际组织建议用于糖尿病的诊断和监测[1-3]。HbA1c的临床价值依赖于其检测结果的可靠性,其中常规检测方法的分析性能是临床实验室需要重点关注的。近期,一种新型的、面向常规检测的毛细管电泳(capillary electrophoresis, CE)法问世,其检测原理是利用不同血红蛋白组分在碱性缓冲液及高电压环境中,在电渗流和电场力的作用下的泳动速率不同而完成分离,其分辨率高于传统的离子交换色谱法和琼脂糖电泳。国内的临床实验室已开始应用,但缺少对其分析性能的评估。为此,我们对CE法的分析性能进行了评估。
材料和方法
一、材料
1.对象样本为用EDTA真空管采集的全血。采样后4 ℃保存(≤5 d)。如果需要保存更久,则将样本分装保存于-80 ℃,可在4 ℃条件下冻融,24 h内完成检测。
2.仪器和试剂AEBIA CAPILLARYSTM2 Flex Piercing毛细管电泳仪(CE法)及配套试剂[溶血清(批号28083/01)、缓冲液(批号21112/01)]、CAPILLARYS HbA1c标准品、CAPILLARYS HbA1c质控品均由法国赛比亚公司提供。ARKRAY HA-8160全自动HbA1c分析仪[高效液相色谱法(high performance liquid chromatography, HPLC);日本爱科来株式会社]。安捷伦1200型HPLC仪(美国安捷伦公司)。P/ACE MDQ毛细管电泳仪(美国贝克曼库尔特公司)。
二、性能分析
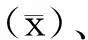
2.比对试验随机收集208份全血样本,分别使用评价方法(CE)和对照方法(HPLC)检测HbA1c。共检测13批,每批检测2次,每次检测16个样本。计算相关系数(r)、斜率(b)、截距。评价标准:决定系数(R2)≥0.95,b为0.95~1.05。
3.线性范围收集高(H)、低(L)浓度HbA1c全血样本,按一定比例进行混合。将检测结果与理论值进行比较,计算各稀释度的相对偏倚和相关性。评价标准:相对偏倚≤8%,R2≥0.95。
4.干扰试验收集高、中、低3个HbA1c浓度(L1~L3)的全血样本,进行如下预处理。(1)氨甲酰化血红蛋白干扰:配置氰酸钾溶液浓度为0、0.15、0.5和1.0 mmol/L,将样本与氰酸钾溶液混合后37 ℃孵育3 h;(2)不稳定HbA1c干扰:配置浓度为 0、1、5、10和50 g/L的葡萄糖溶液,将样本与不同浓度葡萄糖溶液混合后37 ℃孵育1 h;(3)胆红素干扰:将不同浓度(0.0、32.8、65.6、98.4、131.2、164.0、196.8、229.6、262.4、295.2、328.0 μmol/L)胆红素干扰物质按一定比例与样本混合;(4)乳糜微粒干扰:将不同浓度(0、150、300、450、600、750、900、1 050、1 200、1 350 、1 500 FTU)乳糜微粒按一定比例与样本混合;(5)总血红蛋白干扰:收集高、中、低3个HbA1c浓度(L1~L3)且血红蛋白浓度为120 g/L的全血样本,将样本血红蛋白浓度分别稀释/浓缩为40、80、120和180 g/L;(6)血红蛋白F(HbF)干扰:使用新鲜脐带血与样本按一定比例混合,配制成HbF浓度大约为5%、10%、15%的样本。预处理完成后,分别采用CE法检测,每个处理组检测2次。统计处理前样本的检测结果均值与处理后样本的检测结果均值,计算两者之间的绝对偏倚(绝对偏倚=处理后结果均值-处理前结果均值)。评价标准:|绝对偏倚|≤0.5%。
5.与国际临床化学与检验医学联合会(Internation Federation of Clinical Chemistry and Laboratong medicine, IFCC)参考方法[4]的相关性分析收集15个临床样本,浓度范围为5.2%~11.3%。使用生理盐水洗涤红细胞3次,向红细胞浓缩液中加入蛋白内切酶酶解,酶解产物经HPLC收集HbA1c和HbA0的混合物。使用P/ACE MDQ毛细管电泳仪对HbA1c/HbA0进行分离并积分定量计算。取重复测定结果的平均值。
三、统计学方法
采用SPSS 19.0软件进行统计分析。采用Pearson法分析两种方法的相关性,以Bland-Altman评价两种方法的一致性。P<0.05为差异有统计学意义。
结果
一、总精密度
4个样本的HbA1c浓度范围为4.91%~9.67%,CV均<2%。见表1。
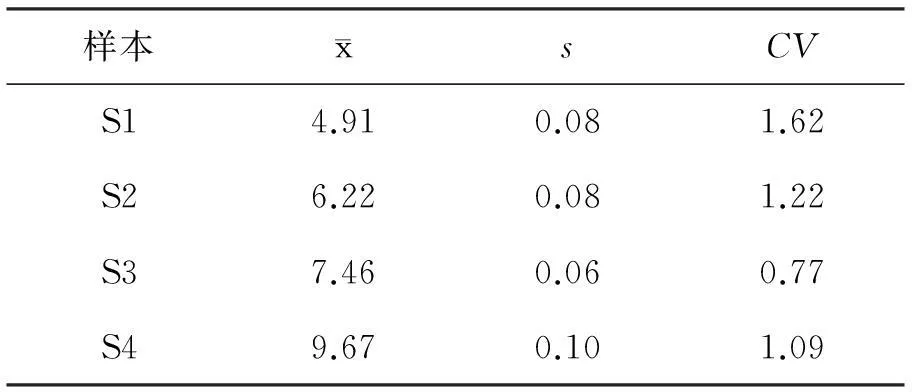
表1 总精密度 (%)
二、比对试验
CE法与HPLC具有较好的相关性(R2=0.993),见图1(a)。以两种方法的差值为纵坐标、均值为横坐标绘制Bland-Altman图,差值的95%可信区间为(-0.38%,0.27%)。CE法检测值与HPLC检测值的差值表现出一定程度的浓度依赖现象,即随着HbA1c浓度的升高,CE法检测值逐渐低于HPLC,见图1(b)。
三、线性范围
在HbA1c为5.0%~17.6%的范围内,直线回归分析的拟合度很好(R2=0.995,高于R2=0.95的判定限)。见图2。直线回归方程为Y=0.972X+0.167,其中Y是同一样本多次检测均值,X是预测值。实测值与理论值相对偏倚的范围为0.16%~5.71%,低于预定值(8%)。
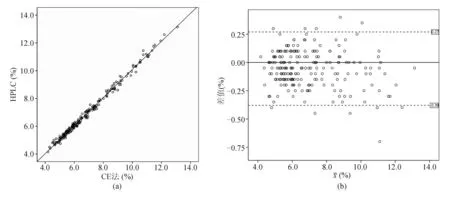

图1CE法与HPLC的比对结果
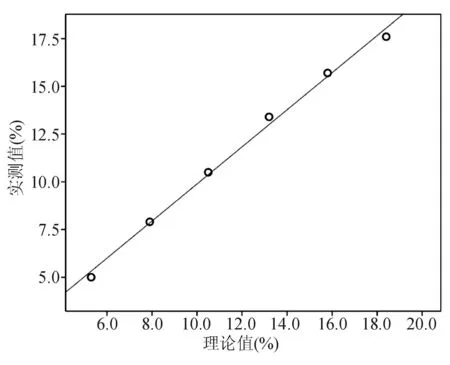
图2 HbA1c理论值和实测值的散点图
四、干扰因素
在整个HbA1c浓度范围(4.6%~8.7%)内,氨甲酰化血红蛋白、不稳定HbA1c、胆红素、乳糜微粒、不同浓度的总血红蛋白和HbF对CE法检测HbA1c有一定影响,但未观察到浓度依赖现象,见表2。所有干扰因素均造成检测结果出现一定程度的升高(0.05%~0.32%)。干扰最强的是HbF (α2γ2),最弱的是乳糜微粒。
五、CE法与IFCC参考方法的相关性分析
CE法与IFCC参考方法的相关性较好(R2=0.993)。

表2 不同干扰因素引起HbA1c检测结果的绝对偏倚 (%)
注:括号内数字为绝对偏倚的范围
讨论
HbA1c作为重要的糖尿病标志物之一,已用于调整糖尿病治疗方案及预测并发症的情况。HbA1c的常规检测方法有两大类:一类是基于其结构特点,如亲和层析法、免疫法、酶法等等;另一类是基于其电荷特点,如离子交换法、电泳法。临床实验室中最常见的是HPLC(包括亲和层析法和离子交换法)和免疫法。CE法根据糖化血红蛋白与非糖化血红蛋白所带电荷的不同进行分离,一直作为IFCC发布的一级参考方法,从未在临床实验室中应用。最近法国赛比亚公司研发了SEBIA CAPILLARYSTM2 Flex Piercing CE检测仪,使常规实验室能使用CE法检测HbA1c。本研究结果显示其总精密度较好,CV为0.77%~1.62%。
HPLC是目前临床使用最广泛的检测HbA1c的方法,其测定结果直接用于临床医生评估患者血糖的长期控制情况。临床研究如美国糖尿病控制与并发症研究(Diabetes Control and Complications Trial, DCCT)和英国糖尿病前瞻性研究(The UK Prospective Diabetes Study, UKPDS)明确了HPLC法与糖尿病并发症的关系。本研究结果显示CE法与HPLC具有较好的相关性[R2=0.993,差值的95%可信区间为(-0.38%,0.27%)],说明对其检测结果的临床判断可以参照基于HPLC建立的临床观察结果。但是随着HbA1c浓度的升高,CE法检测值逐渐低于HPLC。在HbA1c浓度为4.6%~8.7%的范围内,被调查的干扰因素会造成检测结果出现一定程度的升高,这与WEYKAMP等[5]的评估结果一致。其中干扰最为明显的是HbF (α2γ2),主要原因是其电荷及结构类似于HbA1c;最弱的是乳糜微粒,主要原因是其不带电。CE法与IFCC参考方法具有较好的相关性(R2=0.993)。
综上所述,CE法显示出了较好的精密度和抗干扰能力,与HPLC和IFCC参考方法的相关性和一致性较好,适合于临床实验室检测HbA1c。
参考文献
[1]SACKS DB, ARNOLD M, BAKRIS GL, et al. Guidelines and recommendations for laboratory analysis in the diagnosis and management of diabetes mellitus[J]. Diabetes Care,2011, 34 (6): e61-e99.
[2]JOHN WG, UK Department of Health Advisory Committee or Diabetes. Use of HbA1c in the diagnosis of diabetes mellitus in the UK. The implementation of World Health Organization guidance 2011[J]. Diabet Med,2012, 29 (11): 1350-1357.
[3]American Diabetes Association. Standards of medical care in diabetes--2014[J]. Diabetes Care,2014, 37 (Suppl 1): S14-S80.
[4]JEPPSSON JO, KOBOLD U, BARR J, et al. Approved IFCC reference method for the measurement of HbA1c in human blood[J]. Clin Chem Lab Med, 2002, 40 (1): 78-89.
[5]WEYKAMP C, WAENINK-WIEGGERS HW, KEMNA E, et al. HbA1c: performance of the Sebia Capillarys 2 Flex Piercing[J]. Clin Chem Lab Med,2013, 51 (6): e129-e131.
(本文编辑:龚晓霖)