碘化钾催化CO2与氧化苯乙烯合成苯乙烯环状碳酸酯条件的优化
2015-12-31杨海健,宋念念,黄海丽等
碘化钾催化CO2与氧化苯乙烯合成苯乙烯环状碳酸酯条件的优化
杨海健,宋念念,黄海丽,金亚美,彭静,杨洪委
(中南民族大学 化学与材料科学学院,武汉 430074)
摘要用碘化钾催化CO2与氧化苯乙烯(SO)合成苯乙烯环状碳酸酯,分别从溶剂、催化剂用量、温度、CO2压力和反应时间进行探讨,得出了最佳条件.结果表明:以无水乙醇为溶剂,催化剂用量r(KI∶SO)=1∶250,在170℃,CO2压力5 MPa,反应时间5 h,苯乙烯环状碳酸酯的产率和选择性均达到100%.
关键词碘化钾;二氧化碳;氧化苯乙烯;苯乙烯环状碳酸酯;优化条件
收稿日期2014-02-21
作者简介杨海健(1974-),男,教授,博士,研究方向:超临界二氧化碳,E-mail: yanghaijian@vip.sina.com
基金项目国家自然科学基金资助项目(51073175)
中图分类号O643.32+1文献标识码A
Optimal Condition for Styrene Carbonate from Carbon Dioxide and
Styrene Oxide Coupling Reaction Catalyzed by Potassium Iodide
YangHaijian,SongNiannian,HuangHaili,JinYamei,PengJing,YangHongwei
(College of Chemistry and Materials Science,South-Central University for Nationalities,Wuhan 430074,China )
AbstractPotassium iodide was used to catalyze the coupling reaction of carbon dioxide and styrene oxide for the production of styrene carbonate. The effects of solvent, catalyst amounts,temperature, CO2 pressure and reaction time were assessed to obtain the optimal condition. The results showed that both the yield and selectivity of styrene carbonate could reach to 100%,using anhydrous ethanol as solvent, with the mole ratio of potassium iodide and styrene oxide of 1∶250, under 170℃ and 5 MPa of CO2 pressure for 5 h.
Keywordspotassium iodide; carbon dioxide; styrene oxide; styrene carbonate; optimal conditions
环状碳酸酯应用广泛,可用作非质子极性溶剂和高能密度电池和电容的电解液,还可用于混合物萃取分离,合成聚碳酸酯、热硬化性树脂和热记录材料等[1].1956年,Lichtenwalter和Cooper等[2]首先报道利用CO2和环氧烷烃直接合成相应的环状碳酸酯,引起了学界关注并展开了相关研究.关于催化CO2与环氧烷烃环加成反应合成环状碳酸酯的催化剂主要有碱金属盐、季胺盐、季膦盐、金属氧化物、过渡金属配合物、离子交换树脂和离子液体等[3-9]. CO2是一种储量丰富、可再生的廉价碳源,同时又是主要的温室气体,从环境和经济上CO2和环氧烷烃的环加成反应都是最具应用价值和前景的化学反应之一.
1993年,Kihara等[10]考察了不同碱金属卤化物对CO2与2,3-环氧丙基苯基醚之间环加成反应的催化性能,其中LiBr显示了最高的催化活性.碱金属卤化物可单独作为环加成催化剂,也可与其它助剂组成环加成催化剂体系.目前应用广泛的工业生产碳酸丙烯酯(PC)的催化剂KI, 在冠醚、聚乙二醇等助剂存在时, 能高收率地合成PC[11].Sun等[12]在含水体系中, 不添加任何有机助剂, 碱金属卤化物表现出很高的催化活性,由于大量水的存在, 反应生成了较多的1,2-丙二醇,导致PC选择性较低.
CO2作为一种廉价而丰富的碳资源,具有独特的物理和化学特性,前期已研究了超临界CO2的溶解和萃取[13-15].随着原子经济性和绿色化学的发展,更多化学反应以CO2为原料,CO2和环氧烷烃的环加成反应成为最具应用价值和前景的反应之一.本文选择单一的碘化钾作为CO2与氧化苯乙烯开环加成反应的催化剂.作为碱金属卤化物的代表,碘化钾具有高效的催化活性,来源丰富,安全无毒,成分简单,价廉易得.通过对反应条件如催化剂用量、反应温度、CO2压力、反应时间等一系列变换,在一定程序下进行CO2与氧化苯乙烯的环加成反应,对产物进行核磁共振氢谱(1HNMR)表征,得出各个条件变化的优劣,获得该反应的最佳条件,为可控合成和催化应用提供理论依据.
1实验部分
1.1试剂和仪器
碘化钾、丙酮、二氯甲烷、无水乙醇均为市售分析纯,CO2纯度99.99%,氧化苯乙烯经NaH回流纯化.核磁共振仪(NMR, AVANCE III 400,瑞士布鲁克公司).
1.2苯乙烯环状碳酸酯的合成
苯乙烯环状碳酸酯的合成如图1所示.将一定量的碘化钾、10 mL氧化苯乙烯和10 mL合适的溶剂加入反应釜中.反应釜中CO2加至一定压力,预热20 min.预热完毕,将釜内压力升至所需压力反应一段时间.反应完毕后,放出釜内余气,取出釜中混合物并旋蒸去除溶剂,所得产物用氘代氯仿作溶剂经核磁共振氢谱测试得出产率.
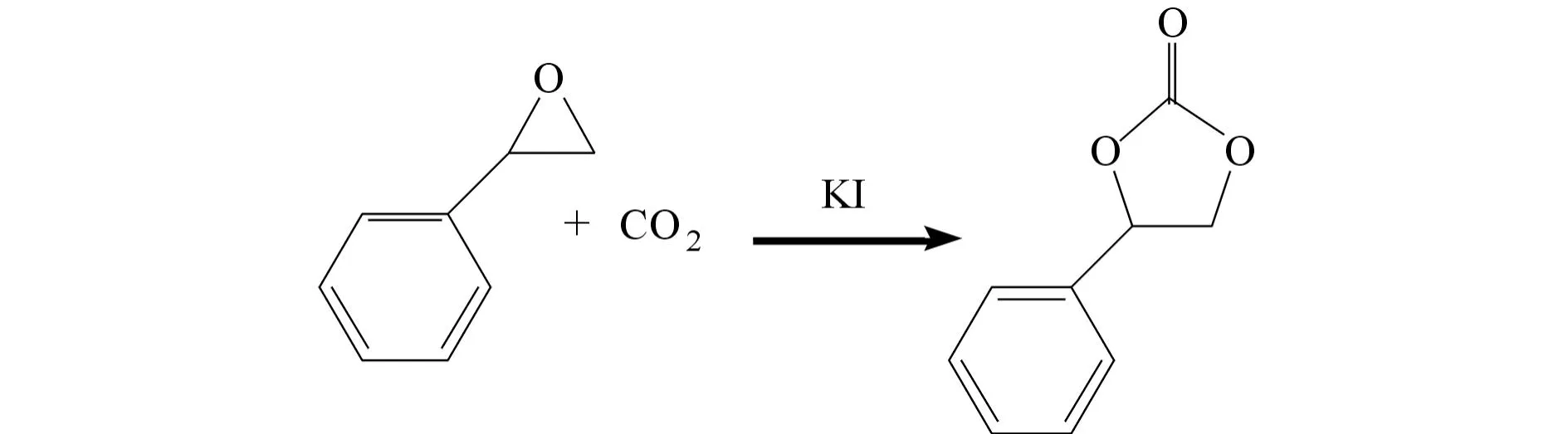
图1 苯乙烯环状碳酸酯的合成 Fig.1 The synthesis of styrene cyclic carbonate
2结果与讨论
2.1产物表征
合成的苯乙烯环状碳酸酯的1HNMR图结果见
图2,7.2~7.5处的多重峰归属于苯乙烯环状碳酸酯苯环上的氢,5.7处的三重峰归属于苯乙烯环状碳酸酯上a位置处次甲基上的氢,4.7和4.3处的两个三重峰分别归属于苯乙烯环状碳酸酯上b,c位置处亚甲基上的两个氢.上述1H NMR图数据证实了苯乙烯环状碳酸酯的合成.
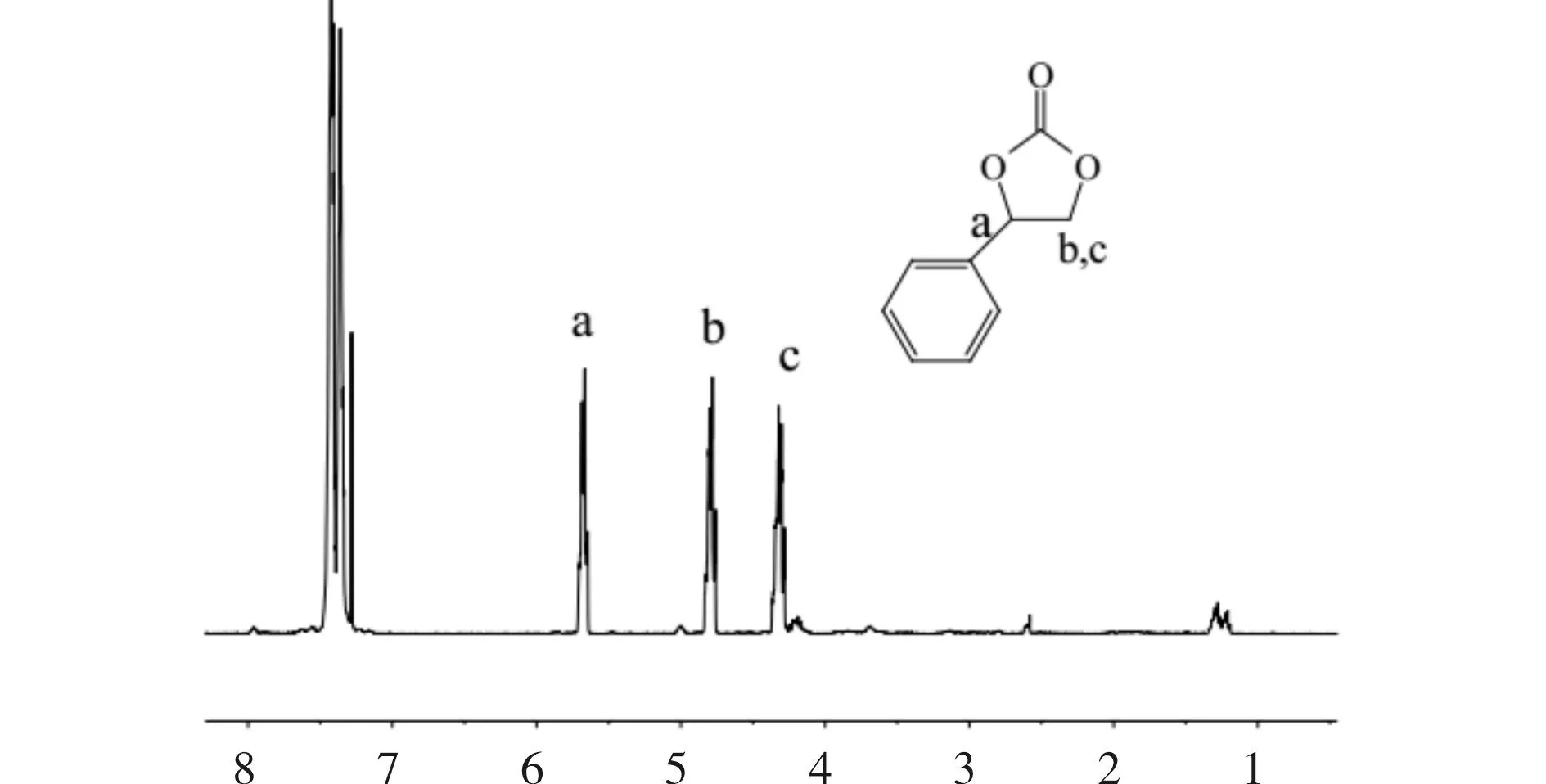
δ 图2 苯乙烯环状碳酸酯的 1H NMR图 Fig.2 1H NMR spectra (CDCl 3) of styrene carbonate
2.2反应条件对KI催化SO和CO2耦合反应活性的影响
2.2.1溶剂对产率的影响
溶剂对催化活性的影响结果见表1.由表1可知,添加4种溶剂时苯乙烯环状碳酸酯的产率由小至大分别为:去离子水<二氯甲烷<丙酮<无水乙醇,用无水乙醇为溶剂,产率可达100%.
由该类反应的可能机理推测,苯乙烯环状碳酸酯的产率与以下3个因素有关:(1)游离I-的数量;(2)环氧烷烃的开环能力;(3)CO2的插入情况.在上述4种溶剂中,丙酮、无水乙醇、二氯甲烷、去离子水这4种溶剂的极性大小顺序为:去离子水>丙酮>乙醇>二氯甲烷,催化剂KI极性很大,溶剂效应使KI在这4种溶剂中的催化效率本应随溶剂极性的增大而增大,但由于乙醇是质子型溶剂,与底物氧化苯乙烯易形成氢键,活化环氧烷,使催化活性比在丙酮中高.去离子水是一种极性的无机溶剂,由于其易与游离的I-相结合形成氢键,使部分催化剂起不到催化作用,导致苯乙烯环状碳酸酯的产率很低.
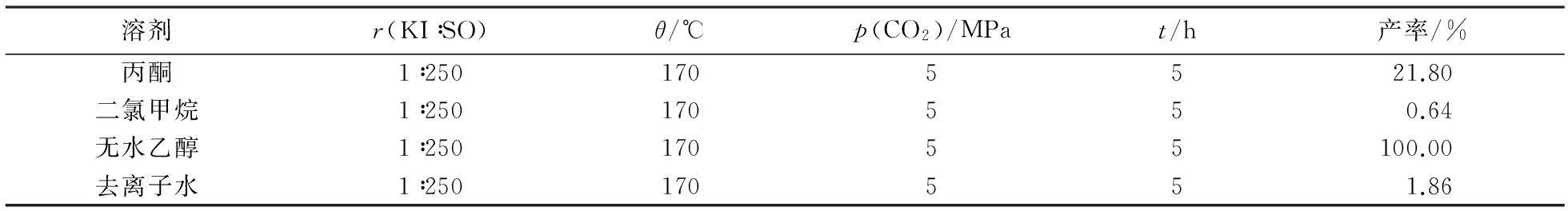
表1 溶剂对催化活性的影响
2.2.2催化剂用量对产率的影响
无水乙醇10 mL, SO=0.0874 mol (10 mL),在170℃,5 MPa CO2压力条件下反应5 h,催化剂用量对产率的影响结果见图3.由图3可知,当KI与反应物SO的摩尔比超过1∶250时,苯乙烯环状碳酸酯的产率高达100%,当其摩尔比小于1∶250时,随着催化剂量的减少,产物苯乙烯环状碳酸酯的产率显著下降.因催化剂用量较多时,可提供更多的活性中心,使反应更好地进行,催化效果更好.当催化剂用量较少时则因活性中心较少而起不到很好的催化效果.故催化剂KI与SO的摩尔比为1∶250为最佳用量.
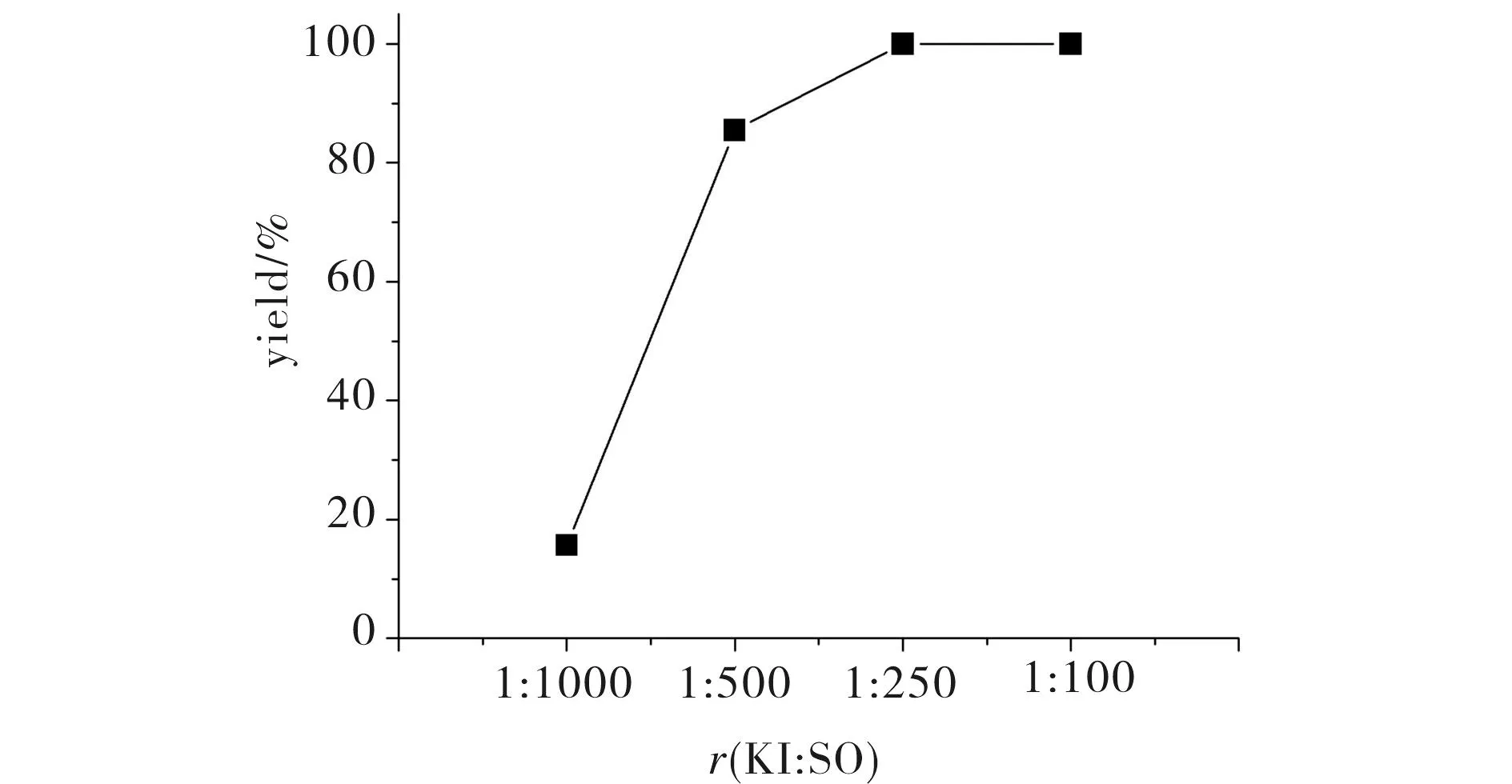
图3 KI和SO摩尔比对苯乙烯环状碳酸酯产率的影响 Fig.3 The effect of the molar ratio of KI and SO on the yield of styrene carbonate
2.2.3温度对产率的影响
在无水乙醇10 mL, SO=0.0874 mol(10 mL),KI=0.058 g,在5 MPa CO2压力条件下反应5 h,不同温度对产率的影响结果见图4.由图4可知,低于100℃时苯乙烯环状碳酸酯的产率很低,此时反应基本上没有发生.反应温度高于100℃时,随着温度的升高,产率显著升高.当反应温度达到170℃时,产率便可达到100%.因为当反应温度较低时系统得到的能量不足以克服该反应发生所需的能垒,而当反应温度较高时系统得到的能量也增大,克服发生反应的能垒使反应进行,生成一定量的产物.故选择170℃为最佳温度.
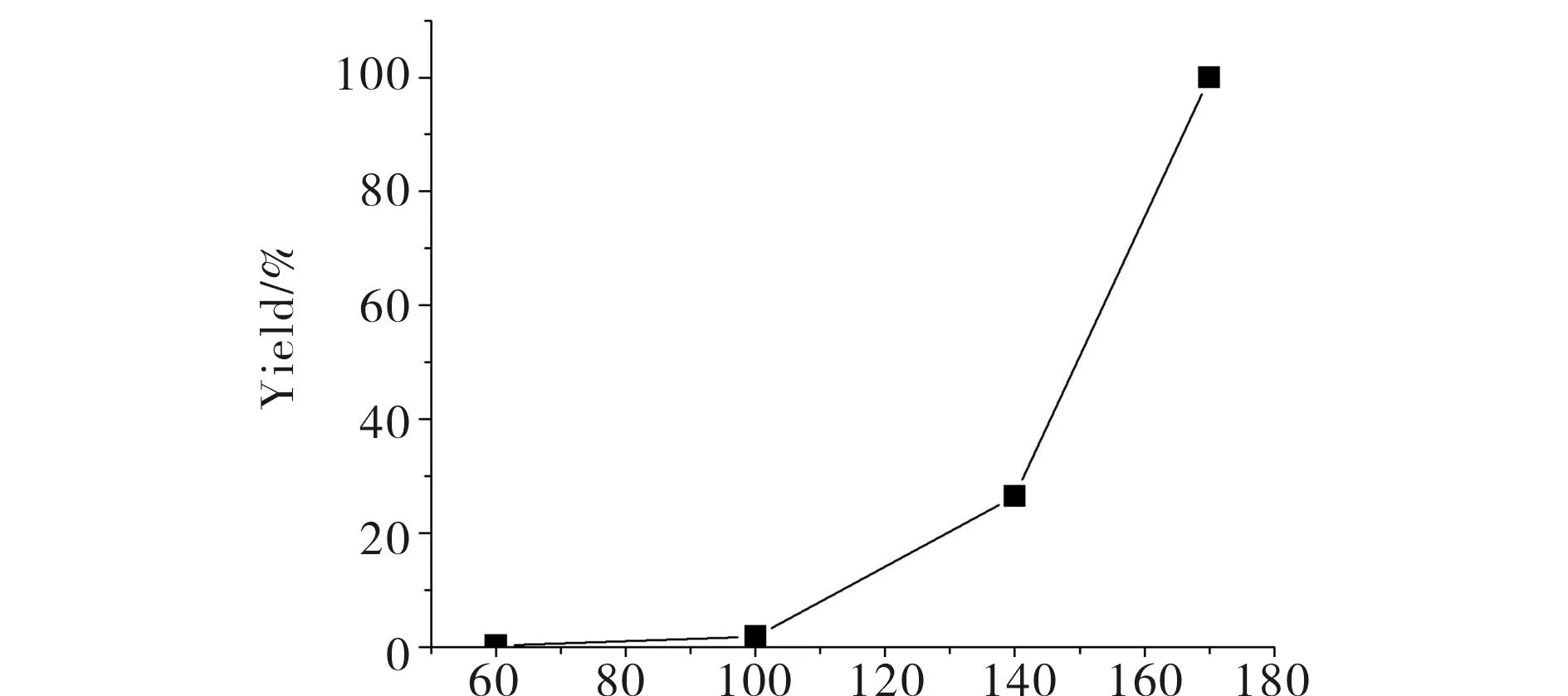
θ/℃ 图4 反应温度对苯乙烯环状碳酸酯产率的影响 Fig.4 The effect of reaction temperature on the yield of styrene carbonate
2.2.4CO2压力对产率的影响
无水乙醇10 mL, SO=0.0874 mol (10 mL), KI=0.058 g,在170℃条件下反应5 h,CO2压力对产率的影响结果见图5.由图5可知,CO2压力在1~7 MPa产率均较高,且先增后减,而在5 MPa时产率达到100%.由于体系存在两相,上层是富含CO2的气相,下层是富含氧化苯乙烯的液相,CO2在液相中的浓度随压力的增加而增加,有利于反应进行;而氧化苯乙烯在液相中的浓度随压力增加而下降,不利于反应进行[16].这些相反因素的竞争,导致压力对产率影响曲线中有个最大值,即最佳压力选择5 MPa.
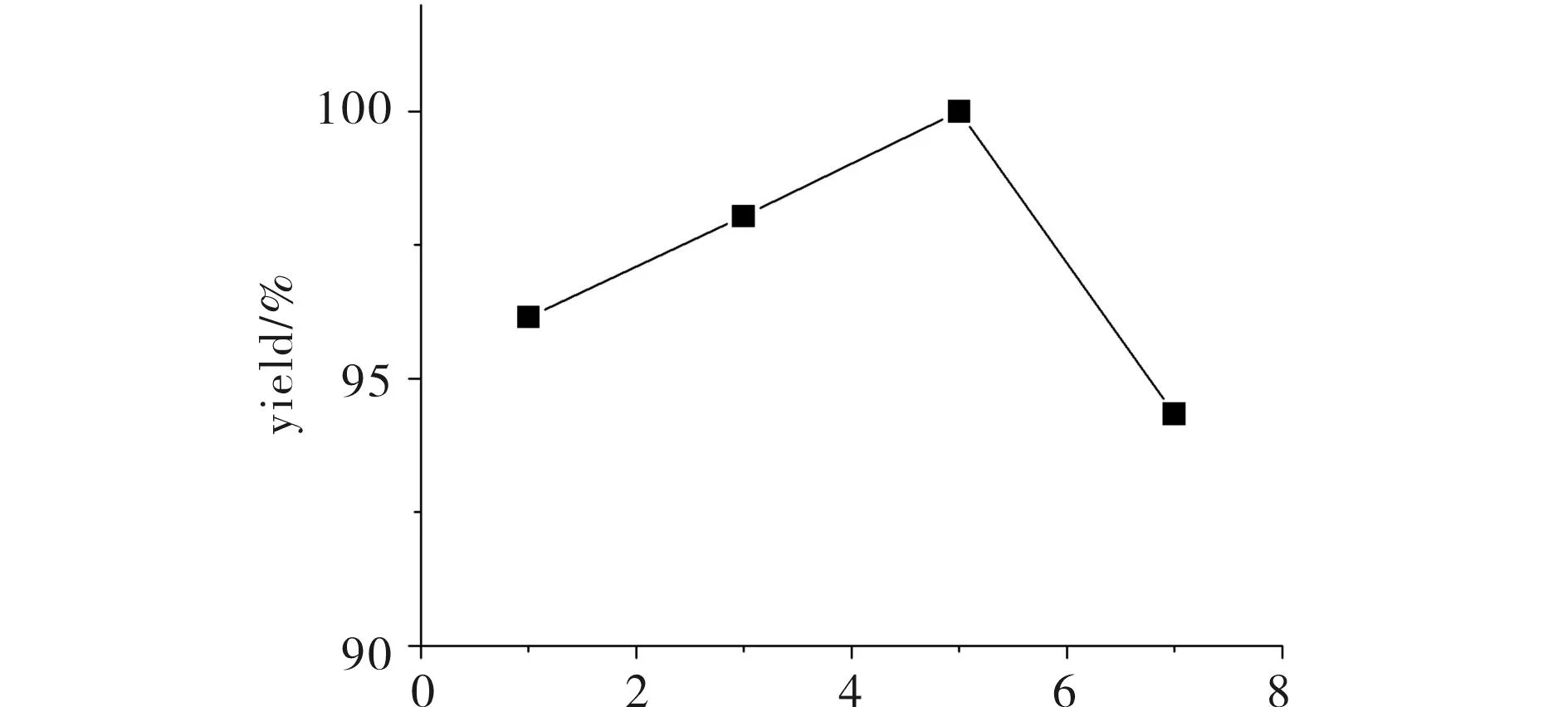
p(CO 2)/MPa 图5 CO 2压力对苯乙烯环状碳酸酯产率的影响. Fig.5 The effect of CO 2 pressure on the yield of styrene carbonate
2.2.5反应时间对产率的影响
在无水乙醇10 mL,SO=0.0874 mol(10 mL),KI=0.058 g,170℃,5 MPa CO2压力下,反应时间对产率的影响结果见图6.由图6可知,在1~5 h内,苯乙烯环状碳酸酯的产率随时间的延长显著升高,5 h即达100%.因为当反应时间较短时,反应物与催化剂尚不能充分接触使反应充分进行,随着时间的延长,反应物与催化剂的接触越来越充分从而催化效果加强,产物产率显著提高.
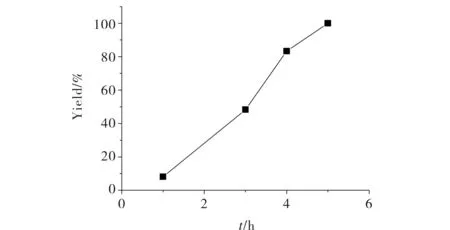
图6 反应时间对苯乙烯环状碳酸酯产率的影响 Fig.6 The effect of reaction time on the yield of styrene carbonate
3结语
碘化钾催化CO2与氧化苯乙烯(SO)合成苯乙烯环状碳酸酯的最佳反应条件为:溶剂为无水乙醇,r(KI∶SO)=1∶250,反应温度170℃,CO2压力5 MPa,反应时间5 h,在该条件下苯乙烯环状碳酸酯的产率可达100%.对该条件下的产物进行核磁共振氢谱(1H NMR)表征,得出苯乙烯环状碳酸酯的选择性也达到了100%.由于催化剂碘化钾来源丰富、安全无毒、廉价易得,具有很高的催化活性,故碘化钾催化CO2与氧化苯乙烯合成苯乙烯环状碳酸酯的反应能很好地应用于工业生产中.
参考文献
[1]Clements J H. Reactive applications of cyclic alkylene carbonates [J]. Ind Eng Chem Res, 2003, 42(4): 663-674.
[2]North M, Pasquale R, Young C. Synthesis of cyclic carbonates from epoxides and CO2[J]. Green Chem, 2010, 12(9): 1514-1539.
[3]Sun J, Wang L, Zhang S, et al. ZnCl2phosphonium halide: An efficient Lewis acid/base catalyst for the synthesis of cyclic carbonate[J]. J Mol Catal A: Chem, 2006, 256(1): 295-300.
[4]Yamaguchi K, Ebitani K, Yoshida T, et al. Mg-Al mixed oxides as highly active acid-base catalysts for cycloaddition of carbon dioxide to epoxides[J]. J Am Chem Soc, 1999, 121(18): 4526-4527.
[5]Ion A, Parvulescu V, Jacobs P, et al. Sc and Zn-catalyzed synthesis of cyclic carbonates from CO2and epoxides[J]. Appl Catal A: Gen, 2009, 363(1): 40-44.
[6]Song J, Zhang Z, Hu S, et al. MOF-5/n-Bu4NBr: an efficient catalyst system for the synthesis of cyclic carbonates from epoxides and CO2under mild conditions[J]. Green Chem, 2009, 11(7): 1031-1036.
[7]Ji D, Lu X, He R. Syntheses of cyclic carbonates from carbon dioxide and epoxides with metal phthalocyanines as catalyst[J]. Appl Catal A: Gen, 2000, 203(2): 329-333.
[8]杨海健,黄海丽,彭静,等.卤化锌pph3/n-Bu4NBr催化体系催化二氧化碳的化学固定[J].中南民族大学学报:自然科学版,2014,33(4):1-5.
[9]Bhanage B M, Fujita S, Ikushima Y, et al. Synthesis of dimethyl carbonate and glycols from carbon dioxide, epoxides, and methanol using heterogeneous basic metal oxide catalysts with high activity and selectivity[J]. Appl Catal A: Gen, 2001, 219(1): 259-266.
[10]Kihara N, Hara N, Endo T. Catalytic activity of various salts in the reaction of 2, 3-epoxypropyl phenyl ether and carbon dioxide under atmospheric pressure[J]. J Org Chem, 1993, 58(23): 6198-6202.
[11]Huang J W, Shi M. Chemical fixation of carbon dioxide by NaI/PPh3/PhOH[J]. J Org Chem, 2003, 68(17): 6705-6709.
[12]Sun J, Ren J, Zhang S, et al. Water as an efficient medium for the synthesis of cyclic carbonate[J]. Tetrahedron Lett, 2009, 50(4): 423-426.
[13]杨海健,赵璐,向力,等.甲氧羰基乙酸己酯在超临界二氧化碳中溶解行为[J].中南民族大学学报:自然科学版,2014,33(3):1-5.
[14]杨海健,彭静,洪洪委.8-羟基喹啉在超临界CO2中萃取金属离子研究[J].中南民族大学学报:自然科学版,2014,33(1):1-6.
[15]Zhao L,Yang H J,Cai Z F.Solubility comparison and partial molar volumes of 1,2-hexanediol before and after end-group modification by methyl oxalyl chloride and ethyl oxalyl monochloride in supercritical CO2[J].J Chem Thermodyn,2013,57:46-53.
[16]Shi T Y, Wang J Q, Sun J, et al. Efficient fixation of CO2into cyclic carbonates catalyzed by hydroxyl-functionalized poly (ionic liquids)[J]. RSC Adv, 2013, 3(11): 3726-3732.
