Triton X-100六角液晶相中制备镁铝层状双金属氢氧化物纳米片及其药物载体应用
2015-12-29赵继宽谢艳芳侯万国
赵继宽 谢艳芳 徐 洁 侯万国
(1青岛科技大学化学与分子工程学院,生态化工国家重点实验室培育基地,山东青岛266042;2山东大学胶体与界面化学教育部重点实验室,济南250100)
Triton X-100六角液晶相中制备镁铝层状双金属氢氧化物纳米片及其药物载体应用
赵继宽1谢艳芳1徐 洁1侯万国2,*
(1青岛科技大学化学与分子工程学院,生态化工国家重点实验室培育基地,山东青岛266042;2山东大学胶体与界面化学教育部重点实验室,济南250100)
以Triton X-100六角相溶致液晶作微反应器,采用共沉淀法制备了镁铝层状双金属氢氧化物(LDHs)纳米薄片(L-LDHs).以双氯芬酸钠(DS)为药物模型分子,采用离子交换法制备了DS插层LDHs(DS/L-LDHs)纳米杂化物,在37.0°C、pH=7.2的缓冲溶液中,考察了纳米杂化物的药物释放性能,并与传统溶液共沉淀法制备的镁铝LDHs(S-LDHs)纳米片状颗粒进行了对比.采用粉末X射线衍射(XRD)、傅里叶变换红外(FT-IR)光谱、场发射扫描电镜(FE-SEM)、透射电镜(TEM)和N2吸附-脱附等技术对所制备的LDHs和DS/LDHs样品的晶体结构、比表面积、形貌特征等进行了表征.结果表明,L-LDHs比S-LDHs具有更低的片厚度,更高的比表面积和药物负载量,所形成的DS/L-LDHs纳米杂化物药物释放速率也明显低于DS/S-LSHs,即L-LDHs更适于作药物载体.DS/L-LDHs纳米杂化物的药物释放过程符合准二级动力学方程,受颗粒内部扩散过程控制.溶致液晶模板法可实现LDHs的形貌可控制备,为LDHs基功能材料的研发提供了新途径.
层状双金属氢氧化物;溶致液晶;Triton X-100;纳米杂化物;药物释放
1 引言
层状双金属氢氧化物(LDHs)又称类水滑石,是由两种或两种以上金属元素形成的具有水滑石层状结构的氢氧化物.1,2LDHs主体层板带结构正电荷,层间存在可交换的阴离子.含阴离子基团的功能分子如药物3-6和农用化学品7,8等分子可通过离子交换法、共沉淀法或结构重建法等插入LDHs层板之间,制备有机/无机纳米杂化物.9对于电中性或疏水性功能分子,因缺乏插层驱动力(静电吸引力),常先将磷酯、10十二烷基硫酸钠、11,12β-环糊精13等分子引入LDHs层间通道,构筑疏水空间,进而实现功能分子插层(“溶解”).前期研究表明,药物/LDHs纳米杂化物不仅可明显提高药物分子的溶解性、14稳定性及输送效率,15,16还可有效控制其药物释放速率,17-19受到人们关注.实际上,LDHs已成为一类极具应用前景的无机层状药物载体.20
近期,LDHs纳米薄片(nanosheets)的制备受到关注,因其可用作自组装法制备功能材料的构建基元.1,2,21-24我们前期研究表明,23用LDHs纳米薄片与药物共组装制备药物插层LDHs(药物/LDHs)纳米杂化物,与常规LDHs颗粒相比,可降低(或消除)插层阻力,充分利用LDHs的通道内部空间,提高载药量,改善药物缓释效果等.LDHs纳米薄片的制备途径有两种:其一为“自上而下”(top-down),1,2将LDHs颗粒在溶剂中剥离成纳米单片;其二为“自下而上”(bottom-up),2如Hu等24以反相微乳液作为纳米反应器,利用其限域效应调控LDHs厚度,采用共沉淀反应制备了LDHs单层片(monolayer).表面活性剂溶致液晶具有有序微空间,能否用作模板“自下而上”制备LDHs纳米薄片,是一个值得研究的课题.
所谓溶致液晶(LLC),是由表面活性剂在溶剂中形成的长程有序聚集结构,25属热力学稳定体系,兼有液体可流动性和晶体各向异性的特点.常见的LLC相结构包括层状相、六角相、反六角相和立方相.液晶中亲水区和亲油区相互间隔,重复间距处于纳米尺度范围.采用LLC作模板或微反应器已广泛用于不同组成和形貌的纳米材料制备,26而用于制备LDHs纳米材料鲜有报道.本课题组27前期采用非离子表面活性剂辛基酚聚氧乙烯(9-10)醚(Triton X-100)构建的六角相溶致液晶作微反应器,制备钴铁LDHs,获得由纳米片构筑的绳状多级结构体,具有典型的类过氧化酶催化活性,表明溶致液晶具有形貌调控作用,但其规律还需探索研究.
本文采用Triton X-100在镁/铝混合盐溶液构建的六角相溶致液晶作微反应器,制备了Mg2A l LDHs(L-LDHs)纳米薄片;通过离子交换法,制备了双氯芬酸钠(DS)插层L-LDHs(DS/L-LDHs)纳米杂化物,考察了其在模拟肠液(37.0°C,pH=7.2)环境中的药物释放行为,并与传统溶液共沉淀法制备的Mg2A l LDHs(S-LDHs)样品进行了对比.以期探索溶致液晶模板法的特点,为LDHs基药物输送-控释体系的研发提供依据.
2 实验部分
2.1 试剂与仪器
Triton X-100(Sigma-Aldrich,Laboratory grade);双氯芬酸钠(郑州兴人化工产品有限公司,分析纯);氯化铝、氨水(国药集团化学试剂有限公司),分析纯;氯化镁、磷酸氢二钠(天津市广成化学试剂有限公司),分析纯;氯化钠(天津博迪化工股份有限公司,质量分数≥99.5%);碳酸钠(上海润捷化学试剂有限公司,分析纯);去离子水.
日本Rigaku D/max-2500/PC型X射线衍射仪(Cu Kα,2θ范围1.5°-70°,扫描速率5(°)·m in-1);德国Bruker公司Vertex 70型傅里叶红外光谱仪(4000-400 cm-1,分辨率1 cm-1);厦门麦克奥迪Motic B2-223型偏光显微镜(带图像控制器);奥地利HMBGSAX型小角X射线散射仪(50 kV,40mA);日本JE-OL公司JSM-6700F型场发射扫描电子显微镜(FESEM,3.0 kV);日本JEOL公司JEM-2100型透射电子显微镜(TEM,200 kV);北京普析通用仪器有限责任公司TU-1901型紫外-可见分光光度计;北京金埃谱科技有限公司V-Sorb 2800P比表面积及孔径分析仪(样品在120°C抽真空预处理3 h);美国Leeman Prodigy XP电感耦合等离子体(ICP)原子发射光谱仪.
2.2 六角相溶致液晶构建及LDHs制备
用Triton X-100在MgCl2/A lCl3混合盐溶液中构建溶致液晶,28其中Triton X-100的浓度为48%(w,质量分数),nMg2+/nAl3+=2,金属阳离子总浓度(Csalt)为360mmol·L-1.在塑料离心管中,按设计量加入各试剂及水,用涡旋混匀器混匀,经离心排除气泡后室温静置24 h,即得溶致液晶样品.
按nNH3·H2O/2(nMg2++nAl3+)=4的比例向溶致液晶样品中加入稀氨水(4mol·L-1)作沉淀剂,室温静置反应48 h,倾去上层液体(未反应的稀氨水),先后用水和无水乙醇反复洗涤,以除去表面活性剂和电解质,离心得到LDHs样品,记为L-LDHs.
作为对比,采用传统共沉淀法制备了Mg2A l LDHs样品.配制MgCl2/A lCl3混合盐溶液,其为360mmol·L-1,按1.2的比例向混合盐溶液添加共沉淀剂稀氨水(4 mol·L-1),静置45m in,经过抽滤和洗涤,沉淀物在80°C下胶溶24 h,得LDHs样品,记为S-LDHs.
2.3 双氯芬酸钠/LDHs纳米杂化物制备
采用离子交换法制备DS/LDHs纳米杂化物.用乙醇/水(体积比1:1)混合溶剂配制浓度为0.1mol· L-1的DS溶液,在60°C、N2保护和磁力搅拌下按比例加入L-LDHs(或S-LDHs),搅拌反应3 d,用乙醇/水混合溶剂离心洗涤,所得沉淀于60°C干燥得DS/L-LDHs(或DS/S-LDHs)纳米杂化物.
2.4 载药量测定
采用紫外-可见分光光度计法测定DS/LDHs纳米杂化物的载药量(Ain,质量分数).称取0.034 g杂化物,加入1m LHCl溶液(2mol·L-1)溶解LDHs无机层板,移至100m L容量瓶中并用氯化钠-磷酸氢二钠-碳酸钠缓冲溶液(pH=7.2)定容.用TU-1901型紫外分光光度计于波长276 nm处测定溶液的吸光度,依据标准曲线得出溶液中DS的浓度,进而得出纳米杂化物载药量.
2.5 药物释放实验
称取0.030 g纳米杂化物,加入到500m L氯化钠-磷酸氢二钠-碳酸钠缓冲溶液(pH=7.2)中,恒温(37.0±0.2)°C下搅拌,每隔一定时间(t)取4m L悬浮液并补充相同体积的溶剂,用孔径为0.45μm滤膜立即过滤悬浮液,测定滤液吸光度,得出DS浓度.根据下式计算t时刻药物释放量qt(质量百分数)及药物释放率Xt.

其中,C与V分别为缓冲溶液中药物浓度以及缓冲溶液体积,m为杂化物质量.每组实验平行做三次,结果取其平均值.
3 结果与讨论
3.1 偏光织构观测和SAXS表征
用Triton X-100在纯水和MgCl2/A lCl3混合盐溶液中分别构建了液晶相,其中Triton X-100浓度为48%(w),nMg2+/nAl3+=2,考察了Csalt的影响.在纯水和Csalt=360mmol·L-1的混合盐溶液中,其液晶相的偏光织构图均呈现典型的扇形织构(见图1),表明Triton X-100在纯水和混合盐溶液中具有类似的聚集行为,均可形成六角相液晶结构.图2给出了小角度X射线散射(SAXS)结果.在纯水和Csalt=360 mmol·L-1混合盐溶液中的液晶相均出现明显的三级散射峰(图2(A,B)),且第一、二、三级散射峰对应的散射因子(S)的比值为表明所形成的六角相溶致液晶都具有较好的长程有序结构.29当Csalt增大至500mmol·L-1时,其液晶相的SAXS图上只显示了第一和第二级散射峰(图2C),表明液晶相结构的长程有序性下降.为保证液晶相在共沉淀反应过程中具有完整的相结构,故选取Csalt=360mmol·L-1用于制备LDHs.

图1 Triton X-100分别与(A)纯水、(B)氯化镁/氯化铝混合盐溶液构建的六角相溶致液晶偏光织构图Fig.1 Polarized opticalm icrographsof lyotropic liquid crystals composed of Triton X-100w ith(A)water and(B) M gCl2/AlCl3m ixed salt solutions

图2 Triton X-100在(A)水和(B,C)氯化镁/氯化铝混合盐溶液中构建的六角相溶致液晶小角度X射线散射(SAXS)图Fig.2 Smallangle X-ray scattering(SAXS)patternsof lyotropic liquid crystals composed of Triton X-100w ith(A) water and(B,C)M gCl2/AlCl3m ixed salt solutions
3.2 XRD和FT-IR表征
图3为LDHs和DS/LDHs纳米杂化物的粉末X射线衍射谱图.可以看出,L-LDHs和S-LDHs均具有典型的类水滑石衍射峰(图3(A,B)),(003)、(006)、(009)和(110)晶面衍射峰清晰、尖锐,表明两样品均具有良好类水滑石相层状结构;其层间距d(003)分别为0.79和0.78 nm,LDHs的层板厚度约0.48 nm,8据此可知L-LDHs和S-LDHs对应的通道高度(gallery height)分别为0.31和0.30 nm,与文献30,31报道一致.采用Gauss98程序B3LYP/6-31G密度泛函优化法32计算的Triton X-100分子的长、宽、厚分别为4.57、0.52和0.43 nm,三维尺寸均大于L-LDHs的通道高度,表明Triton X-100分子未插入(或未保留在)LLDHs样品中.DS/L-LDHs和DS/S-LDHs也呈现出清晰的(003)、(006)、(009)和(110)晶面特征衍射峰(图3(C,D)),但其(003)峰位置与其前体LDHs相比明显前移,表明DS插入LDHs层间,且形成的纳米杂化物仍保持了较完整的类水滑石相层状结构. DS/L-LDHs和DS/S-LDHs的d(003)值分别为2.47和2.34 nm,则其通道高度分别约为1.99和1.86 nm.采用Gauss程序计算DS分子(结构式见图4)的长、宽、厚分别为1.31、0.61和0.49 nm,由于杂化物通道高度大于DS分子长度而小于其两倍长度,故而推测DS阴离子在LDHs层间可能以交错反平行状态排列,其―COO-基键合在层板上.DS/L-LDHs的d(003)值比DS/S-LDHs的略大,原因不很清楚,可能是前者DS插入量大所致(见3.4节).
另外,金属元素含量测定结果表明,所合成的L-LDHs、S-LDHs以及DS/L-LDHs和DS/S-LDHs样品具有相近的Mg/Al摩尔比(2.06-2.09),且与原料配比(nMg2+/nA l3+=2)基本一致.

图3 LDHs和DS/LDHs纳米杂化物的粉末X射线衍射(XRD)图Fig.3 Powder X-ray diffraction(XRD)patternsof LDHs and DS/LDHsnanohybrids

图4 双氯芬酸钠结构式Fig.4 Structureof diclofenac sodium
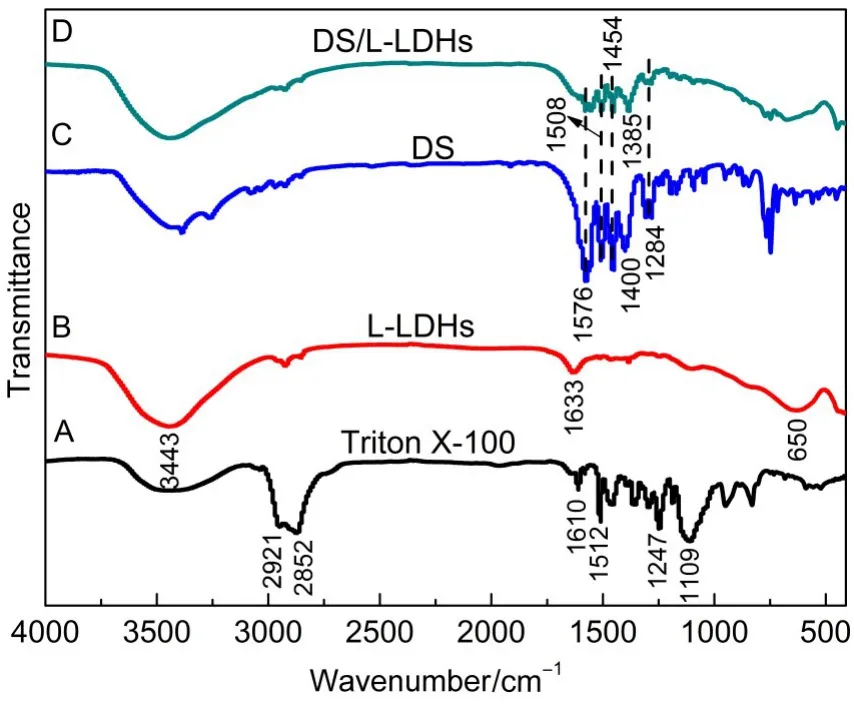
图5 (A)Triton X-100、(B)L-LDHs、(C)DS和(D)DS/LLDHs的傅里叶变换红外(FT-IR)光谱图Fig.5 Fourier transform infrared(FT-IR)spectra of(A) Triton X-100,(B)L-LDHs,(C)DS,and(D)DS/L-LDHs
图5为Triton X-100、DS、LDHs和DS/L-LDHs样品的FT-IR谱图.在Triton X-100的谱图上(图5A),2921和2852 cm-1处的吸收峰分别归属于C―H的不对称和对称伸缩振动,331400~1600 cm-1间的吸收峰是苯环骨架C=C的伸缩振动特征吸收峰,34在1109 cm-1出现的是C―O―C醚氧键伸缩振动峰.12L-LDHs呈现出类水滑石相的特征吸收峰(图5B), 3443 cm-1处的峰为层板O―H的伸缩振动吸收峰,351633 cm-1处出现的是层间水分子中O―H弯曲振动吸收峰,650 cm-1处的吸收峰归属于层板金属-氧键振动吸收;27另外,在2921和2852 cm-1处出现了较弱的C―H伸缩振动吸收峰,表明L-LDHs中含有少量的Triton X-100,可能吸附在颗粒表面上.在DS的FT-IR谱图上(图5C),1576和1400 cm-1处的峰分别是―COO-的不对称和对称伸缩振动吸收峰,301508 和1454 cm-1处的吸收峰归属为苯环上C=C伸缩振动,341284 cm-1处的吸收峰对应仲芳胺C―N伸缩振动.36在DS/L-LDHs谱图(图5D)中,观察到LDHs 和DS的特征吸收峰,但对应的―COO-对称伸缩振动吸收峰(1400 cm-1)向低波数移动至1385 cm-1,与文献30,37报道一致,可能是―COO-基团与LDHs层板间的静电作用和氢键作用所致.另外,在LDHs和DS/L-LDHs的FT-IR谱图中均未出现CO32-在1368 cm-1处的v3振动特征吸收峰,35表明所制备的样品基本不含CO32-离子.

图6 LDHs和DS/LDHs纳米杂化物的(A-D)TEM和(E-H)SEM照片Fig.6(A-D)TEM and(E-H)SEM imagesof LDHsand DS/LDHsnanohybrids
3.3 TEM和SEM表征
图6给出了LDHs和DS/LDHs纳米杂化物的TEM和SEM照片.由图可以看出,L-LDHs为不规则的卷曲薄片(图6(A,E)),具有纳米单层片特征,1,2而S-LDHs为典型的六角片状颗粒(图6(C,G)),二者的横向尺寸无明显差异,均为100-250 nm;L-LDHs片厚度显著低于S-LDHs,即使干燥聚集(SEM样品制备所致)后,L-LDHs样品的片厚度(~14 nm)也仅为S-LDHs样品(~30 nm)的一半.这些结果表明,六角液晶相对LDHs的生长起到调控作用.LDHs的晶胞单元为八面体结构,它们共用棱边二维延伸成片层结构.在六角液晶相中发生共沉淀反应生成LDHs时,其沿液晶相微水区的横向生长不受限制,而其纵向生长受微水区厚度限制,故而形成纳米薄片.27六角液晶相对LDHs生长的调控作用示意图见图7.N2吸附-脱附结果(图8)表明,L-LDHs与SLDHs样品的BET比表面积分别为138和60m2·g-1,其相对大小与形貌观察结果一致.
与前体LDHs相比,药物插层后发生明显聚集(图6(B,D)),可能是由DS与LDHs间的静电吸引作用以及DS分子间的π-π和疏水作用所致.另外,所形成的DS/L-LDH颗粒厚度似乎也比DS/S-LDHs的小(图6(F,H)).
3.4 DS/LDHs纳米杂化物的载药量及药物释放动力学
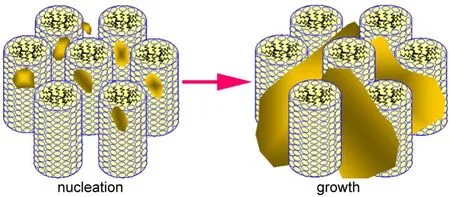
图7 六角液晶相中L-LDHs纳米片成核与生长过程示意图Fig.7 Schem atic diagram of nucleation and grow th of L-LDH nanosheets in the hexagonal liquid crystalmedia

图8 S-LDHs与L-LDHs样品N2吸附-脱附等温线Fig.8 N2adsorption-desorption isotherm sof S-LDHsand L-LDHs sam p les

图9 DS/LDHs纳米杂化物及物理混合物的药物释放动力学曲线Fig.9 Drug releasing kinetics curvesof DS/LDHsand their physicalm ixture

图10 DS/LDHs纳米杂化物药物释放数据的准二级动力学方程拟合直线Fig.10 Fitted linesof drug releasing data for DS/LDHsnanohybridsaccording to pseudo-second order kineticsequation
对DS/L-LDHs和DS/S-LDHs的载药量检测结果表明,前者的载药量大于后者,分别为51.9%和43.2%(w).这是因为在纳米杂化物制备过程中,LLDHs体系除发生常规的离子交换外,还会发生纳米薄片与DS间的共组装,LDHs内部空间可得到更充分利用,因而其载药量相对较高,这与前期研究结果一致.23
图9为DS/L-LDHs和DS/S-LDHs在(37.0± 0.2)°C、pH=7.2的磷酸缓冲溶液中的药物释放动力学曲线,为对比也绘入了DS与L-LDHs物理混合物(与杂化物同组成,研磨而成)的药物释放(或溶解)结果.可以看出,物理混合物的药物释放速度很快,5 min时释放率即超过90%,随后趋于平衡.与之相比,DS/L-LDHs和DS/S-LDHs纳米杂化物的药物释放速率要缓慢得多,100m in时的药物释放率分别为53.4%和61.8%,达释放平衡时的时间分别为550和280m in,平衡释放率均约为73%.另外,相对而言, DS/L-LDHs的药物释放速率低于DS/S-LDHs,表明L-LDHs更适合作药物载体.原因不很清楚,可能是在DS/L-LDHs纳米杂化物形成时,所伴随的LDHs纳米薄片与DS间的共组装过程,使药物分子更多地进入LDHs的内部空间,药物扩散路径增长,因而其药物释放速率相对较低.
采用动力学方程22,23,32,38对药物释放数据进行了拟合,结果表明符合准二级动力学方程.准二级动力学方程可表示为:

其中,qe为平衡药物释放量,Xt为t时刻药物释放率, k2为准二级动力学方程速率常数.DS/L-LDHs和DS/S-LDHs的t/Xt-t拟合线见图10,其线性相关系数(R2)分别为0.997和0.999,据其截距得出的k2值分别为1.85和4.07m in-1,也表明DS/L-LDHs的药物释放速率低于DS/S-LDHs.
药物扩散过程包括LDHs颗粒内部的扩散和颗粒外部溶剂化层中的扩散,其中速率慢的步骤为释放过程速率控制步骤.Bhaskar等39提出了一个确定颗粒内部扩散是否为速率控制步骤的简单方法.对颗粒内部扩散控制的释放过程,其药物释放率Xt与时间t的关系为:

其中,dp为颗粒直径,D为扩散系数.如果颗粒内部扩散是释放速率控制步骤,则-ln(1-Xt)与t0.65呈线性关系.图11是DS/L-LDHs药物释放数据拟合结果,可见-ln(1-Xt)与t0.65间呈良好的线性关系,R2为0.984,表明颗粒内部扩散是药物释放过程的速率控制步骤.

图11 DS/L-LDHs纳米杂化物药物释放数据的-ln(1-Xt)-t0.65拟合直线Fig.11 Fitted-ln(1-Xt)-t0.65line of drug releasing data for DS/L-LDHsnanohybrid
4 结论
采用Triton X-100构建的六角相溶致液晶作微反应器,成功制备了LDHs纳米薄片,表明液晶相对LDHs形貌有重要的调控作用.与传统共沉淀法制备的LDHs片状颗粒相比,L-LDHs纳米薄片具有更高的DS负载量,且所形成的DS/L-LDHs纳米杂化物药物释放速率也明显低于DS/S-LDHs,表明LLDHs纳米薄片更适于作药物载体.DS/L-LDHs纳米杂化物的药物释放过程符合准二级动力学方程,药物在颗粒内部的扩散为其速率控制步骤.溶致液晶有序分子组合体作模板,可实现纳米颗粒的形貌可控制备,具有重要应用前景.
(1)Nie,H.Q.;Hou,W.G.Acta Phys.-Chim.Sin.2011,27,1783.[聂宏骞,侯万国.物理化学学报,2011,27,1783.]doi:10.3866/ PKU.WHXB20110826
(2)Wang,Q.;O'Hare,D.Chem.Rev.2012,112,4124.doi:10.1021/ cr200434v
(3)Costantino,U.;Ambrogi,V.;Nocchetti,M.;Perioli,L. M icroporousMesoporousMat.2008,107,149.doi:10.1016/j. m icromeso.2007.02.005
(4)Khan,A.I.;Lei,L.;Norquist,A.J.;O'Hare D.Chem.Commun. 2001,No.22,2342.
(5)Wei,M.;Yuan,Q.;Evans,D.G.;Wang,Z.;Duan,X.J.Mater. Chem.2005,15,1197.doi:10.1039/b416068a
(6)Ni,Z.M.;Xia,S.J.;Wang,L.G.;Xing,F.F.;Pan,G.X.;Hu,J. Chem.J.Chin.Univ.2007,28,1214.[倪哲明,夏胜杰,王力耕,邢方方,潘国祥,胡 军.高等学校化学学报,2007,28, 1214.]
(7)Cardoso,L.P.;Celis,R.;Cornejo,J.;Valim,J.B.J.Agric.Food Chem.2006,54,5968.doi:10.1021/jf061026y
(8)Khan,A.I.;Ragavan,A.;Fong,B.;Markland,C.;O'Brien,M.; Dunbar,T.G.;Williams,G.R.;O'Hare,D.Ind.Eng.Chem.Res. 2009,48,10196.doi:10.1021/ie9012612
(9)Newman,S.P.;Jones,W.New J.Chem.1998,22,105.doi: 10.1039/a708319j
(10)Begu,S.;Aubert-Pouessel,A.;Polexe,R.;Leitmanova,E.; Lerner,D.A.;Devoisselle,J.M.;Tichit,D.Chem.Mater.2009, 21,2679.doi:10.1021/cm803426j
(11)Wang,B.;Zhang,H.;Evans,D.G.;Duan,X.Mater.Chem. Phys.2005,92,190.doi:10.1016/j.matchemphys.2005.01.013
(12)Zhao,J.K.;Fu,X.M.;Zhang,S.Z.;Hou,W.G.Appl.Clay Sci. 2011,51,460.doi:10.1016/j.clay.2011.01.009
(13)Liu,X.L.;Wei,M.;Wang,Z.L.;Evans,D.G.;Duan,X. J.Phys.Chem.C 2008,112,17517.
(14)Ambrogi,V.;Fardella,G.;Grandolini,G.;Nocchetti,M.; Perioli,L.J.Pharm.Sci.2003,92,1407.
(15)Choy,J.H.;Kwak,S.Y.;Jeong,Y.J.;Park,J.S.Angew.Chem. Int.Edit.2000,39,4042.
(16)Choy,J.H.;Jung,J.S.;Oh,J.M.;Park,M.;Jeong,J.;Kang,Y. K.;Han,O.J.Biomaterials2004,25,3059.doi:10.1016/j. biomaterials.2003.09.083
(17)Gu,Z.;Thomas,A.C.;Xu,Z.P.;Campbell,J.H.;Lu,G.Q. Chem.Mater.2008,20,3715.
(18)Li,F.;Jin,L.;Han,J.;Wei,M.;Li,C.Ind.Eng.Chem.Res. 2009,48,5590.
(19)Li,Y.;Du,N.;Hou,W.;Liu,S.Chem.Res.Chin.Univ.2014, 30,137.
(20)Qin,Z.G.;Cao,F.;Ping,Q.N.;Zhang,C.Prog.Pharm.Sci. 2013,37,615.[秦志国,操 锋,平其能,张 灿.药学进展, 2013,37,615.]
(21)Lee,J.H.;Jung,D.Y.Chem.Commun.2012,48,5641.doi: 10.1039/c2cc30449j
(22)Wu,X.W.;Du,N.;Li,H.P.;Zhang,R.J.;Hou,W.G.Acta Chim.Sin.2014,72,963.[兀晓文,杜 娜,李海平,张人杰,侯万国.化学学报,2014,72,963.]doi:10.6023/A 14030146
(23)Wang,S.;Wu,X.W.;Li,H.P.;Zhang,R.J.;Hou,W.G.Chem. J.Chin.Univ.2014,35,1982.[王 爽,兀晓文,李海平,张人杰,侯万国.高等学校化学学报,2014,35,1982.]
(24)Hu,G.;Wang,N.;O'Hare,D.;Davis,J.Chem.Commun.2006, No.3,287.
(25)Zhao,J.K.;Chen,X.;Sui,Z.M.;Zhu,B.L.;Xu,L.M.;Yang, C.J.Prog.Chem.2003,15,451.[赵继宽,陈 晓,隋震鸣,朱宝林,许丽梅,杨春杰.化学进展,2003,15,451.]
(26)Zhao,J.K.;Ji,S.M.China SurfactantDeterg.Cosmetics2006, 36,308. [赵继宽,吉淑梅.日用化学工业,2006,36,308.]
(27)Zhao,J.K.;Xie,Y.F.;Yuan,W.J.;Li,D.X.;Liu,S.F.;Zheng, B.;Hou,W.G.J.Mater.Chem.B 2013,1,1263.doi:10.1039/ c2tb00389a
(28)K laus,B.J.Colloid Interface Sci.1982,86,73.doi:10.1016/ 0021-9797(82)90042-X
(29)Quilliet,C.;Ponsinet,V.;Cabuil,V.J.Phys.Chem.1994,98, 3566.doi:10.1021/j100065a004
(30)Ambrogi,V.;Fardella,G.;Grandolini,G.;Perioli,L.;Tiralti,M. C.AAPSPharmSciTech 2002,3,1.
(31)Xia,S.J.;Ni,Z.M.;Xu,Q.;Hu,B.X.;Hu,J.J.Solid State Chem.2008,181,2610.doi:10.1016/j.jssc.2008.06.009
(32)Mora,M.;Lopez,M.I.;Jimenez-Sanchidrian,C.;Ruiz,J.R. Spectrochim.Acta PartA 2011,78,989.doi:10.1016/j. saa.2010.12.013
(33)Wei,M.;Shi,S.X.;Wang,J.;Li,Y.;Duan,X.J.Solid State Chem.2004,177,2534.doi:10.1016/j.jssc.2004.03.041
(34)Iyi,N.;Matsumoto,T.;Kaneko,Y.;Kitamura,K.Chem.Mater. 2004,16,2926.doi:10.1021/cm049579g
(35)Xu,S.C.Organic Chemistry,2nd ed.;Higher Education Press: Beijing,1993;pp 373-374.[徐寿昌.有机化学.第二版;北京:高等教育出版社,1993:373-374.]
(36)Panda,H.S.;Srivastava,R.;Bahadur,D.J.Phys.Chem.B 2009,113,15090.doi:10.1021/jp905440e
(37)Zhang,H.;Zou,K.;Guo,S.H.;Duan,X.J.Solid State Chem. 2006,179,1792.doi:10.1016/j.jssc.2006.03.019
(38)Zhao,M.;Xu,J.;Hou,W.G.Chem.J.Chin.Univ.2012,33, 1572.[赵 满,徐 洁,侯万国.高等学校化学学报,2012, 33,1572.]
(39)Bhaskar,R.;Murthy,R.S.R.;M iglani,B.D.;Viswanathan,K. Int.J.Pharm.1986,28,59.doi:10.1016/0378-5173(86)90147-X
Preparation o fMg2Al Layered Doub le Hyd roxide Nanosheets from Triton X-100 Hexagonal Lyo trop ic Liquid Crystaland Their App lication as Drug Carriers
ZHAO Ji-Kuan1XIE Yan-Fang1XU Jie1HOUWan-Guo2,*
(1State Key Laboratory Base ofEco-chemical Engineering,College ofChemistry and Molecular Engineering, Qingdao University ofScience and Technology,Qingdao 266042,Shandong Province,P.R.China;2Key Laboratory ofColloid and Interface Chemistry(M inistry ofEducation),Shandong University,Jinan 250100,P.R.China)
A hexagonal lyotropic liquid crystal(LLC)was constructed w ith nonionic surfactant Triton X-100 and m ixed magnesium chloride/alum inum chloride aqueous solutions.Layered double hydroxide(LDH) nanosheets(L-LDHs)were prepared using the LLC as a m icroreactor.A nanohybrid material of L-LDHs intercalated w ith a m odelanionic drug,diclofenac sodium(DS;DS/L-LDHs)was synthesized using an ionexchangemethod.The drug-release profile of DS/L-LDH was investigated undermoderate conditions,i.e., 37.0°C and pH 7.2.The resu lts were com pared w ith those for common LDH flaky partic les(S-LDHs) synthesized using a traditionalsolution coprecipitationmethod.The crystalline structures,specific surface areas, andmorphologies of these LDHs and DS/LDHs nanohybrids were characterized using powder X-ray diffraction (XRD),Fourier-transform infrared(FT-IR)spectroscopy,field-em ission scanning electronm icroscopy(FE-SEM), transm ission electron m icroscopy(TEM),and N2adsorption-desorption.The results show that the L-LDHparticles are less thick,and have largerspecific surface areas and higherDS-loading capacities than the S-LDH particles.Drug release by the DS/L-LDH nanohybrid was clearly lower than thatby the DS/S-LDH nanohybrid. This indicates that the L-LDH nanosheets aremore suitable for use as drug carriers than the S-LDHs.Drug release by the DS/L-LDH nanohybrid can be described using a pesudo-second-order kineticmodel,and drug diffusion through the LDH particles is the rate-lim iting step.LLC can be used as a tem plate formorphologycontrolled synthesis of LDHs.
Layered double hydroxide;Lyotropic liquid crystal;Triton X-100;Nanohybrid; Drug release
O648.1
icle]
10.3866/PKU.WHXB201504021 www.whxb.pku.edu.cn
Received:January 19,2015;Revised:April2,2015;Published onWeb:April2,2015.
∗Corresponding author.Email:wghou@sdu.edu.cn;Tel:+86-532-84023654.
The projectwas supported by the National Natural Science Foundation of China(20903059,21173135,21403121)and Natural Science Foundation of Shandong Province,China(ZR2009BM 043,ZR2013BQ013).
国家自然科学基金(20903059,21173135,21403121)及山东省自然科学基金(ZR2009BM 043,ZR2013BQ013)资助项目
©Editorialofficeof Acta Physico-Chim ica Sinica