Cu/SiO2催化剂结构对乙酸甲酯加氢性能的影响
2015-12-29邱坤赞郭文文王海霞朱玲君王树荣
邱坤赞 郭文文 王海霞 朱玲君 王树荣
(浙江大学能源清洁利用国家重点实验室,杭州310027)
Cu/SiO2催化剂结构对乙酸甲酯加氢性能的影响
邱坤赞 郭文文 王海霞 朱玲君 王树荣*
(浙江大学能源清洁利用国家重点实验室,杭州310027)
采用尿素水解法制备了Cu/SiO2催化剂,探究其用于乙酸甲酯(MA)加氢制取乙醇的催化性能,并通过N2物理吸附、X射线衍射(XRD)、程序升温还原(TPR)、透射电子显微镜(TEM)和X射线光电子能谱(XPS)等表征方法分析了催化剂的物理化学特性,探究了铜负载量和还原温度等对催化剂结构的影响,以及与催化活性之间的关系.发现在铜负载量分别为10%、20%和30%(质量分数,w)的催化剂中,铜负载量为20%的催化剂因具有较多且分散均匀的活性组分而表现出最佳的加氢效果.接着在铜负载量为20%的催化剂上研究了还原温度(270,350,450°C)对催化性能的影响,发现在350°C下还原的催化剂活性最高,在最佳的反应条件下,乙酸甲酯转化率达到97.8%,乙醇选择性达到64.9%(理论最大值为66.6%),主要归属于它具有较高的铜物种分散度,最合适的Cu0/(Cu0+Cu+)摩尔比例,同时实现了解离氢气和活化乙酸甲酯的功能.
乙酸甲酯;乙醇;加氢;Cu/SiO2;尿素水解法;Cu0/(Cu0+Cu+)摩尔比
1 引言
乙醇是一种重要的工业原料,被广泛应用于能源、化工、食品等领域,其作为车用燃料添加剂或替代品更是得到大力发展.目前,乙烯水合法生产乙醇技术因成本较高已逐渐被淘汰;而采用粮食发酵法存在与人争粮、与粮争地的弊端,纤维素发酵法存在预处理较困难且易造成污染的问题.合成气来源广泛,可以经过煤、生物质气化或天然气重整获得,以合成气合成乙醇近年来成为研究的热点.1-3
直接法以价格昂贵的铑基催化剂为主,面临着CO转化率低、乙醇选择性低等问题.4,5间接法有多种路径,研究者在该领域开展了相关的工作.6-8Wang等7以合成气和二甲醚(DME)为原料,利用氢型丝光沸石(H-MOR)和Cux-Zny-O为催化剂,经二甲醚羰基化和乙酸甲酯(MA)加氢过程合成乙醇.Liu等8集成了甲醇脱水、二甲醚羰基化和乙酸甲酯(MA)加氢三个过程合成乙醇.上述反应流程如下:

其中乙酸甲酯加氢是间接法制取乙醇的关键步骤之一,其效果将影响整个合成乙醇路线的经济性.
Cu基催化剂是有效的酯加氢催化剂,其作为催化剂常用的载体有SiO2、9ZnO、10,11碳纳米管(CNTs)12及六方介孔分子筛(HMS)、13SBA-1514等.Wang等12研究了Cu/CNTs上的乙酸甲酯加氢实验,发现活性组分在碳纳米管孔道的分布,以及碳纳米管的内径大小都会影响加氢效果.在最佳的催化剂Cu-S-973上,当反应流速为时,乙酸甲酯转化率为22.5%,乙醇选择性为27.6%.Brands等15研究了Cu/SiO2上不同助剂的添加对酯加氢影响的研究,发现以Co为助剂的Cu/ SiO2上乙酸甲酯加氢的转化率最高达70%,乙醇的选择性为47%.SiO2同时具有弱的酸中心和弱的碱中心,有利于酯加氢反应的进行.16而且Zhu等9研究发现,与浸渍法相比,均匀沉积沉淀法制备的Cu/ SiO2催化剂的铜颗粒分布更均匀,催化活性更高.另外沉淀法中以尿素作为沉淀剂,尿素溶解后为均匀体系,在一定温度下尿素水解缓慢释放氢氧根离子,这样沉淀更均匀.而且负载量不同,还原温度不同都会影响催化剂结构,进而影响到加氢性能.17,18本文利用均匀沉积沉淀法,以尿素为沉淀剂,制备了Cu/SiO2催化剂,以探究其对乙酸甲酯加氢制备乙醇反应的催化活性,同时探讨了铜负载量和还原温度等对催化剂结构的影响,以及与催化活性之间的关系.
2 实验
2.1 催化剂制备
采用尿素水解法制备Cu/SiO2催化剂,所用到的原料Cu(NO3)2∙3H2O和尿素为国药试剂,硅溶胶购于浙江宁波宇达化工有限公司.首先根据铜的负载量,称取一定量的尿素和Cu(NO3)2∙3H2O(尿素/铜摩尔比为4:1)溶解于去离子水中,待完全溶解后,缓慢加入一定量的硅溶胶,搅拌4h.接着将该混合溶液移至90°C油浴中进行水解,至溶液pH=6.5时将其过滤洗涤至中性.得到的沉淀物在120°C下干燥过夜,然后在450°C下焙烧4h,制得铜负载量为10%、20%和30%(w)的催化剂,表示为10U、20U和30U.
2.2 催化剂表征
催化剂中金属的实际负载量采用电感耦合等离子体原子发射光谱(ICP-AES,ThermoiCAP 6000)测量.首先将该催化剂加入逆王水(HNO3: HCl,体积比为3:1)中,然后在微波下完全消解,接着测定其元素含量.
催化剂的比表面积、孔径分布和孔容的分析在QuadrasorbSI上进行,在77K温度下记录催化剂的吸附脱附曲线.在测试之前,首先将样品在573K下脱气3h.对其比表面积的分析采用Bruuauer-Emmett-Teller(BET)方法,孔径分布采用Barrett-Joyner-Halenda(BJH)模型.
X射线衍射(XRD)在PANalyticalX'PertPROX射线衍射仪上记录,操作条件为40kV,30mA,衍射角2θ的范围为10°-90°,各个晶面的晶粒大小根据Scherrer公式计算.
颗粒分布和颗粒大小通过透射电镜(TEM, Philips-FEI,TecnaiG2F30)进行分析.
程序升温还原(TPR)测试在MicromeriticsAuto-ChemII2920上进行,首先装入一定量的样品,然后在氦气条件下250°C预处理1h,接着降温至50°C,通入还原气体10%H2/He气体,以10°C∙min-1的升温速率升至800°C,氢气的浓度用热导检测器来检测.
采用X射线光电子能谱(XPS)分析样品表面的各元素.仪器为美国PHI公司的5000CESCASystem;采用条件为镁靶(hν=1253.6eV),以C1s(结合能为284.6eV)为基准进行结合能校正,误差±0.2eV.
2.3 催化剂活性测试
催化剂的活性测试实验在固定床反应器上进行.催化剂的装填量为2g,下层装填石英砂.反应开始前,在常压、氢气气氛下对催化剂(10U、20U和30U)原位还原3h,还原温度350°C,升温速率为5°C·min-1,H2流量为50mL·min-1.此外,对20U催化剂的还分别在270、350和450°C下进行还原,还原后的催化剂表示为270R-20U、350R-20U和450R-20U.还原结束后,将温度降至反应温度,压力升至反应压力,然后开始进行测试实验.实验中,乙酸甲酯和H2分别经微量泵和质量流量计进入反应预热区,随后进入反应器进行反应.气体产物通过在线的气相色谱进行检测,液体产物经过冷凝器收集后在色谱Agilent7890A上进行分析.
主要发生的反应为:
(1)乙酸甲酯加氢生成乙醇反应

(2)乙醇与乙酸甲酯酯交换反应

(3)乙酸乙酯的加氢反应

乙酸甲酯转化率的计算公式为:

产物选择性的计算公式为:

式中nMAin和nMAout分别指给料和产物中乙酸甲酯的摩尔量;nCm指产物Cm的摩尔量,m指产物Cm所含的碳数.由于1mol乙酸甲酯加氢生成1mol甲醇和1 mol乙醇,因此根据上面的计算公式,乙醇的理论最大选择性为66.6%.

表1 Cu/SiO2催化剂的物理结构特性Table1 Texturalpropertiesof the Cu/SiO2catalysts
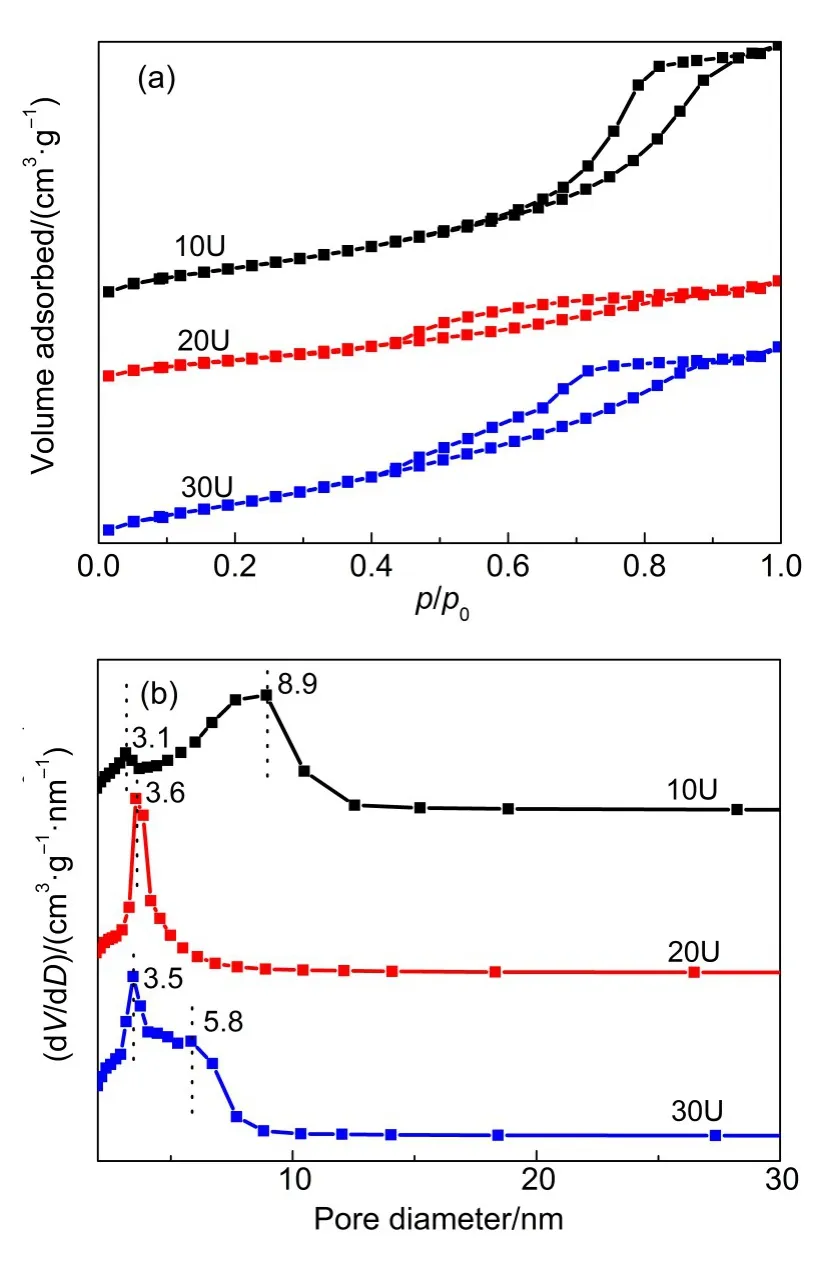
图1 催化剂的(a)N2吸附-脱附等温曲线和(b)孔径分布图Fig.1 (a)N2adsorption-desorption isotherm sand(b)pore size distribution curvesof the catalysts
3 结果与讨论
3.1 不同铜负载量对加氢性能的影响
3.1.1 不同铜负载量催化剂的结构特性
不同铜负载量催化剂的物理结构特性如表1所示.10U、20U和30U催化剂的实际铜负载量分别为9.7%、18.4%和25.2%.其中10U和20U催化剂实际铜负载量接近理论值,而30U的偏小些.从表中可以看出,10U催化剂的比表面积为281m2·g-1,平均孔径为6.4nm.当负载量增加接近到20%时,催化剂的比表面积减少到204m2·g-1,可能是由于一定程度的铜物种的积聚和二氧化硅结构的破坏及重组;17平均孔径也减小到4.3nm.当负载量继续增加时,比表面积增加到30U的333m2·g-1,这可能归因于铜硅酸盐的形成.19,20图1(a)显示了三个催化剂的N2吸附-脱附曲线,三条曲线都属于LangmuirIV型,迟滞环形状都属于H2型.此结果表明,三个催化剂均具有较好的介孔结构.图1(b)为催化剂的孔径分布曲线图,10U和30U催化剂为双孔分布结构,其中10U催化剂的孔径分布集中3.1和8.9nm,30U催化剂的孔径分布集中在3.5和5.8nm,而20U催化剂的孔径分布相对集中,在3.6nm左右,一方面是由于新孔道的形成,另一方面是由于在均匀沉积沉淀法制备催化剂过程中,铜物种进入到孔道中.
焙烧后的10U、20U、30U催化剂的XRD衍射图如图2(a)所示,在22.5°处均有对应SiO2的特征衍射峰.在三个催化剂上都没有观察到CuO的衍射峰,这可能是由于CuO高度分散且颗粒粒径较小的原因.催化剂的XRD衍射图上在31.2°和35.8°出现了一个较宽的衍射峰,这主要归属于铜硅酸盐.21在10U和20U的催化剂上衍射峰强度较弱,这可能是由于铜硅酸盐含量较低.还原后的10U、20U、30U催化剂的XRD衍射图如图2(b)所示.三个催化剂还原后,在22.5°处均有对应SiO2的特征衍射峰.另外,三个催化剂还出现了另外四个衍射峰,对应于Cu2O (2θ=36.4°,42.3°,61.4°,73.6°),且随着铜负载量的增加,四个衍射峰的强度逐渐增强,这可能是因为铜含量的增多,以及颗粒粒径略微增大的原因.由Scherrer公式计算得到,三个催化剂上Cu2O物种的颗粒粒径在4-5nm范围内.各个催化剂的XRD谱图中观察不到有关金属Cu的结晶相,这可能是由于金属铜颗粒分散较均匀,而且颗粒较小,因此没有检测出来.

图2 (a)焙烧后和(b)还原后10U、20U和30U催化剂的X射线衍射(XRD)图Fig.2 X-ray diffraction(XRD)patternsof the 10U, 20U,and 30U catalysts(a)after calcination and (b)after reduction

图3 10U、20U和30U催化剂的程序升温还原(TPR)图Fig.3 Tem perature programm ed reduction(TPR) patternsof the 10U,20U,and 30U catalysts

图4 不同铜负载量的Cu/SiO2催化剂的乙酸甲酯(MA)加氢活性Fig.4 M ethylacetate(MA)hydrogenation over Cu/SiO2catalystsw ith different copper loading amounts
10U、20U、30U催化剂的TPR曲线如图3所示,三个催化剂在~209°C都呈现出一个较窄较尖的还原峰,且峰面积随着负载量的增加而增大.分散均匀的CuO颗粒的还原温度一般较低(~250°C),低于体相CuO的还原温度.22而对于铜硅酸盐,由于铜离子和SiO2之间强烈的相互作用,其还原到Cu+的温度与高度分散的CuO的还原温度相重合,23而将其进一步还原为Cu0的还原温度较高,通常大于600°C.因此,由此推断,209°C的还原峰主要归属于分散均匀的CuO到Cu+和Cu0的还原,以及铜硅酸盐到Cu+的还原.
3.1.2 不同铜负载量催化剂的加氢性能
图4显示了不同铜负载量的Cu/SiO2催化剂在乙酸甲酯加氢制备乙醇反应中的活性.反应条件为T=240°C,p=2.0MPa,n(H2)/n(MA)=5,液体空速(LHSV)=0.6h-1.在10U催化剂上,乙酸甲酯的转化率仅为33.3%,乙醇的选择性为33.5%,主要副产物为乙酸乙酯,选择性为41.7%.乙酸乙酯为反应生成的乙醇和乙酸甲酯进一步经过酯交换反应生成.当铜的负载量增加时,20U和30U催化剂的乙酸甲酯转化率和乙醇选择性都明显的提高.这可能是因为10U催化剂上活性中心较少,加氢能力不足,而20U和30U催化剂上铜物种的活性中心数量显著增多的原因.20U催化剂呈现了最好的加氢效果,乙酸甲酯转化率和乙醇选择性分别达到93.2%和60.9%,主要副产物乙酸乙酯的选择性为6.3%.与20U催化剂相比,30U催化剂的乙酸甲酯转化率(90.1%)略有下降,乙醇选择性(59.7%)基本不变,乙酸乙酯选择性(8.7%)略有上升.由催化剂的结构可知,这可能是因为与30U催化剂相比,铜物种颗粒粒径更小的原因.合适的铜负载量不仅决定了催化剂活性位数量,而且决定了催化剂特殊的孔道结构.Cu/SiO2催化剂最佳铜的负载量为20%(w).

图5 不同温度还原后20U催化剂的透射电子显微镜(TEM)图Fig.5 Transm ission electronm icroscopy(TEM)imagesof 20U catalyst reduced at different temperatures
3.2 不同还原温度影响
3.2.1 TEM
不同还原温度对催化剂的加氢效果也有较大的影响,因此我们接着考察了最佳Cu负载量的20U催化剂在不同还原温度下的加氢效果.不同温度还原后的20U催化剂的TEM图如图5所示.图5(a1)为20U催化剂270°C还原后的TEM图,从图中可以看出活性组分分布均匀.从高倍率的透射电镜图(图5 (a2,b2,c2))中观察到一些晶格条纹,对应于Cu和Cu2O晶体,表明还原后两种晶体的存在,与XRD的结果相吻合.而对于450°C还原后的催化剂,颗粒粒径大于5nm的增多(图5(c1)),这可能是因为还原温度较高,活性颗粒发生部分团聚的原因.颗粒的平均粒径公式通过公式计算,24wi为粒径为di的颗粒的个数.可见在270、350、450°C三个温度下还原的催化剂均具有高分散的纳米级铜颗粒,平均粒径分别为4.4、4.5、4.8nm.
3.2.2 XPS
图6为不同温度还原后的20U催化剂的XPS和X射线诱导俄歇电子能谱(XAES)谱图.图6(a)中三种催化剂的Cu2p3/2的结合能在932.4eV左右,由文献可知,25CuO中的Cu2p3/2的结合能大约为933.5 eV,当其与载体有强烈相互作用时,结合能将大于934.9eV,说明三种催化剂中的铜物种非CuO,Cu2+被还原为Cu+或Cu0.而通常Cu+和Cu0的结合能非常接近,不能通过它们的Cu2p3/2结合能来区分,要依靠XAES能谱来区分.图6(b)为不同还原温度的20U催化剂的CuLMMXAES俄歇谱图,从图中可以看出,三种催化剂的俄歇谱图均呈现不对称、较宽的峰型,说明三种催化剂中Cu+和Cu0共同存在. 914.1和917.0eV分别归属于Cu+和Cu0.经过去卷积计算,270R-20U、350R-20U、450R-20U催化剂的Cu0/(Cu0+Cu+)摩尔比值分别为0.398、0.492、0.425,其中经350°C还原的催化剂具有最高的Cu0/(Cu0+ Cu+)摩尔比.这可能是由于还原温度为270°C较低,还原不彻底,因此270R-20U催化剂中Cu+比例较高;而当还原温度为450°C时,温度较高,还原过程中部分颗粒发生团聚,Cu物种颗粒较大,使得还原较难进行,因此Cu0的比例相比于350R-20U较低些.

图6 不同温度还原后Cu/SiO2催化剂的(a)Cu 2p XPS谱图和(b)Cu LMM俄歇谱图Fig.6 (a)Cu 2p XPSspectra and(b)Cu LMM Auger spectra of the Cu/SiO2catalysts reduced at different tem peratures
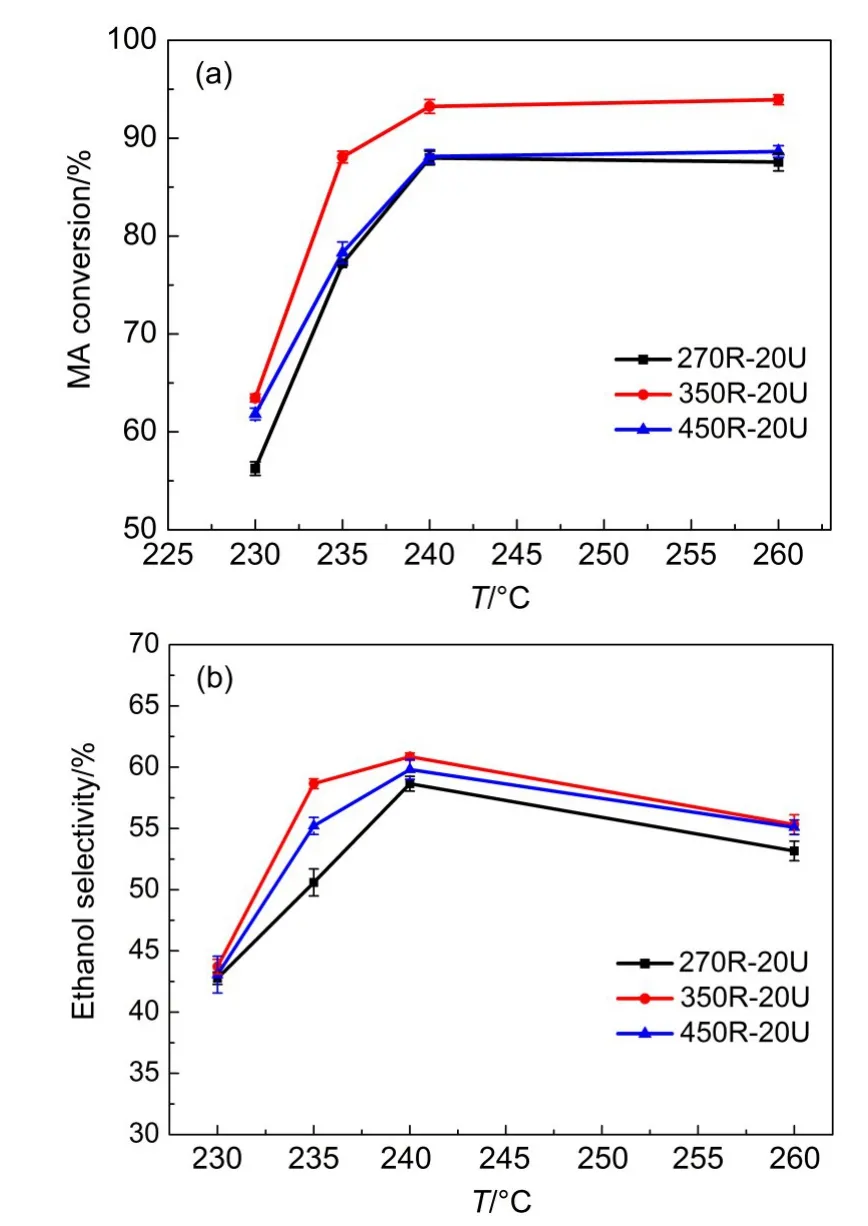
图7 20U催化剂上还原温度对(a)乙酸甲酯转化率和(b)乙醇选择性的影响Fig.7 Influenceof reduction temperatureon(a)MA conversion and(b)ethanolselectivity over 20U catalyst
3.2.3 还原温度对加氢性能的影响
图7给出了不同还原温度下20U催化剂上的加氢活性.从图中可以看出,随着反应温度的增加,三个催化剂上乙酸甲酯的转化率均增加,在240°C时分别达到最大值88.0%、93.2%和88.1%,之后均趋于稳定;乙醇的选择性随反应温度的增加均呈现先增加后减少的趋势,温度较高时,副产物的含量增多.乙醇的选择性均在240°C时达到最大,分别为58.7%、60.9%和59.8%.同一反应温度下,三个催化剂的加氢活性从高到低为:350R-20U>450R-20U>270R-20U.
还原温度主要影响了Cu/SiO2催化剂上Cu0/ (Cu0+Cu+)的摩尔比.研究发现,在酯加氢过程中, Cu0起到解离吸附H2的作用,而Cu+能够稳定甲基和乙酰基.而且Cu+可提供亲电子位或Lewis酸位使得C=O键极化,从而使得酯基的活性增加.17而且研究表明,20,26当Cu+/Cu0的摩尔比为1时是最佳的.因此,我们认为经350°C还原的催化剂的加氢效果归属于适量的Cu0和Cu+的协同作用,同时实现解离氢气和活化乙酸甲酯的功能,获得了最佳的乙酸甲酯加氢效果.350R-20U催化剂上乙酸甲酯加氢的反应示意图如图8所示.由此得出,350R-20U催化剂优良的加氢效果归属于其具有活性组分分散均匀,且最合适Cu0/(Cu0+Cu+)摩尔比等特点的原因.
图9显示了氢酯比对乙酸甲酯转化率和乙醇选择性的影响.从图中看出随着氢酯比的增加,乙酸甲酯转化率和乙醇选择性均呈逐渐增加的趋势,而副产物乙酸乙酯选择性逐渐降低.这可能是因为在高氢酯比条件下,副产物乙酸乙酯被进一步加氢生成了乙醇.当n(H2)/n(MA)=30时,乙酸甲酯转化率达到97.8%,乙醇选择性达到64.9%,接近理论最大值66.6%,乙酸乙酯选择性仅为1.1%.

图8 350R-20U催化剂上乙酸甲酯加氢的反应示意图Fig.8 Reaction diagram ofM A hydrogenation over 350R-20U catalyst

图9 350R-20U催化剂上氢酯摩尔比对乙酸甲酯转化率和产物选择性的影响Fig.9 Influenceof n(H2)/n(MA)on MA conversion and product selectivity over 350R-20U catalyst
4 结论
采用尿素水解法制备了不同铜负载量(10U、20U、30U)和不同还原温度(270R-20U、350R-20U、450R-20U)的Cu/SiO2催化剂,发现Cu/SiO2催化剂上乙酸甲酯的加氢性能与催化剂的结构密切相关. 350R-20U催化剂呈现出最优良的加氢效果,由表征发现这不仅归属于其具有较高的铜物种分散度和较小的颗粒粒径(~4.5nm),而且由于其最合适Cu0/ (Cu0+Cu+)摩尔比(0.492),同时实现了氢气的解离和乙酸甲酯的活化.在p=2.0MPa,T=240°C,n(H2)/n(MA)=30时,乙酸甲酯转化率达到97.8%,乙醇选择性达到64.9%,接近理论最大值(66.6%).
(1)Subramani,V.;Gangwal,S.K.Energy Fuels2008,22(2), 814.doi:10.1021/ef700411x
(2)Chen,W.M.;Ding,Y.J.;Xue,F.;Song,X.G.Acta Phys.-Chim.Sin.2015,31(1),1.[陈维苗,丁云杰,薛 飞,宋宪根.物理化学学报,2015,31(1),1.]doi:10.3866/PKU. WHXB201411054
(3)He,J.;Zhang,W.Appl.Energy 2011,88(4),1224.doi:10.1016/ j.apenergy.2010.10.022
(4)Choi,Y.M.;Liu,P.J.Am.Chem.Soc.2009,131(36), 13054.doi:10.1021/ja903013x
(5)Hu,J.L.;Wang,Y.;Cao,C.S.;Elliott,D.C.;Stevens,D.J.; White,J.F.Catal.Today 2007,120(1),90.doi:10.1016/j. cattod.2006.07.006
(6)Gong,J.L.;Yue,H.R.;Zhao,Y.J.;Zhao,S.;Zhao,L.;Lv,J.; Wang,S.P.;Ma,X.B.J.Am.Chem.Soc.2012,134(34), 13922.doi:10.1021/ja3034153
(7)Wang,D.;Yang,G.H.;Ma,Q.X.;Yoneyama,Y.;Tan,Y.S.; Han,Y.Z.;Tsubaki,N.Fuel2013,109,54.doi:10.1016/j. fuel.2012.08.059
(8)Liu,Y.Y.;Murata,K.;Inaba,M.;Takahara,I.Fuel Process. Technol.2013,110,206.doi:10.1016/j.fuproc.2012.12.016
(9)Zhu,Y.Y.;Wang,S.R.;Zhu,L.J.;Ge,X.L.;Li,X.B.;Luo,Z. Y.Catal.Lett.2010,135(3),275.
(10)Hao,A.X.;Yu,Y.;Chen,H.B.;Mao,C.P.;Wei,S.X.;Yin,Y. S.Acta Phys.-Chim.Sin.2013,29(9),2047.[郝爱香,于杨,陈海波,毛春鹏,魏士新,殷玉圣.物理化学学报,2013,29(9),2047.]doi:10.3866/PKU.WHXB201306211
(11)Zhu,Y.M.;Shi.L.J.Ind.Eng.Chem.2014,20(4),2341.doi: 10.1016/j.jiec.2013.10.010
(12)Wang,D.;Yang,G.H.;Ma,Q.X.;Wu,M.B.;Tan,Y.S.; Yoneyama,Y.;Tsubaki,N.ACSCatal.2012,2(9),1958.doi: 10.1021/cs300234e
(13)Yin,A.Y.;Guo,X.Y.;Dai,W.L.;Li.H.X.;Fan,K.N.Appl. Catal.A-Gen.2008,349,91.doi:10.1016/j.apcata.2008.07.020
(14)Wang,S.R.;Guo,W.W.;Wang,H.X.;Zhu,L.J.;Yin,S.;Qiu, K.Z.New J.Chem.2014,38(7),2792.
(15)Brands,D.S.;Poels,E.K.;Bliek,A.Appl.Catal.A 1999,184, 279.doi:10.1016/S0926-860X(99)00106-4
(16)Fu,J.P.;Zhao,Y.;Zhou,Q.;Wang,S.H.;Wu,Z.A.;Xie,G.Q.; Luo,M.F.IndustrialCatalysis2014,22(10),736.[付金萍,赵 洋,周 强,王树华,吴周安,谢冠群,罗孟飞.工业催化, 2014,22(10),736.]
(17)Yin,A.Y.;Guo,X.Y.;Dai,W.L.;Fan,K.N.J.Phys.Chem.C 2009,113(25),11003.doi:10.1021/jp902688b
(18)Huang,W.;Wang,J.G.;Sun,Z.Q.;Liu,J.Y.;Hou,Y.B.;Jia, L.T.;Li,D.B.JournalofFuelChemistry and Technology 2014,42(1),253.[黄 巍,王俊刚,孙志强,刘俊义,侯摇博,贾丽涛,李德宝.燃料化学学报,2014,42(1),253.]
(19)van derGrift,C.J.G.;Elberse,P.A.;Mulder,A.;Geus,J.W. Appl.Catal.1990,59(1),275.doi:10.1016/S0166-9834(00) 82204-6
(20)Chen,L.F.;Guo,P.J.;Qiao,M.H.;Yan,S.R.;Li,H.X.;Shen, W.;Long,H.J.Catal.2008,257(1),172.doi:10.1016/j. jcat.2008.04.021
(21)Toupance,T.;Kermmarec,M.;Lambert,J.F.;Louis,C.J.Phys. Chem.B 2002,106,2277.doi:10.1021/jp013153x
(22)Marchi,A.J.;Fierro,J.L.G.;Santamaría,J.;Mozón,A.Appl. Catal.A 1996,142,375.doi:10.1016/0926-860X(96)00087-7
(23)van derGrift,C.J.G.;Mulder,A.;Geus,J.W.Appl.Catal. 1990,60,181.doi:10.1016/S0166-9834(00)82181-8
(24)Hou,Z.Y.;Gao,J.;Guo,J.Z.Liang,D.;Lou,H.;Zheng,X.M. J.Catal.2007,250(2),331.doi:10.1016/j.jcat.2007.06.023
(25)Wagner,C.D.;Riggs,W.M.;Davis,L.E.;Moulder,J.F.; Muilenberg,G.E.Handbook ofX-ray Photoelectron Spectroscopy;Perkin-Elmer Corporation,Physical Electronics Division:M innesota,1979.
(26)Lin,H.Q.;Zheng,X.L.;He,Z.;Zheng,J.W.;Duan,X.P.; Yuan,Y.Z.Appl.Catal.A 2012,28,445.
In fluence o f Catalyst Struc tu re on Perfo rm ance o f Cu/SiO2in Hyd rogenation o fMethylAcetate
QIU Kun-Zan GUOWen-Wen WANG Hai-Xia ZHU Ling-Jun WANG Shu-Rong*
(State Key Laboratory ofClean Energy Utilization,Zhejiang University,Hangzhou 310027,P.R.China)
Cu/SiO2catalysts for the hydrogenation ofmethylacetate(MA)to ethanolwere prepared using the urea hydrolysismethod.The catalysts were characterized using N2-physisorption,X-ray diffraction(XRD), temperature-programmed reduction(TPR),transm ission electronm icroscopy(TEM),and X-ray photoelectron spectroscopy(XPS).The effects of the copper loading and reduction tem perature on the catalyststructure and catalytic performance were investigated.Experimentalstudies of the influence of the copper loading showed thata 20%(mass fraction,w)Cu/SiO2catalysthad uniform ly dispersed copper particles and a large number ofactive centers,and therefore gave the besthydrogenation performances among the three catalystswith the copper loadings of 10%,20%,and 30%,respectively.Then 20%(w)Cu/SiO2was reduced at different tem peratures(270,350,and 450°C).The results showed that20%(w)Cu/SiO2reduced at350°C had the best catalytic activity.This was attributed to the homogeneous distribution of coppernanoparticles,and appropriate Cu0/(Cu0+Cu+)molar ratio,which achieved simultaneous dissociation ofhydrogen and MAactivation.Under the optimum reaction conditions,the MA conversion and ethanolselectivity reached 97.8%and 64.9%(theoretical m aximum value:66.6%),respectively.
Methylacetate;Ethanol;Hydrogenation;Cu/SiO2;Urea hydrolysismethod; Cu0/(Cu0+Cu+)molar ratio
O643
icle]
10.3866/PKU.WHXB201503272 www.whxb.pku.edu.cn
Received:January 19,2015;Revised:March 27,2015;Published onWeb:March 27,2015.
∗Corresponding author.Email:srwang@zju.edu.cn;Tel:+86-571-87952801.
The projectwassupported by the NationalNatural Science Foundation of China(51276166),NationalScienceand Technology Supporting Plan through Contract,China(2015BAD15B06),and Program of Introducing Talentsof Discipline to University,China(B08026).
国家自然科学基金(51276166),“十二五”国家科技支撑计划课题(2015BAD15B06)和“高等学校学科创新引智计划”(B08026)资助
©Editorialofficeof Acta Physico-Chim ica Sinica