Co-B/γ-Al2O3非晶态催化剂的制备及其催化乳酸乙酯液相加氢性能
2015-12-29赵凤伟沈美玉杜长海长春工业大学化学工程学院长春130012
赵凤伟 沈美玉 王 琳 杜长海(长春工业大学化学工程学院,长春130012)
Co-B/γ-Al2O3非晶态催化剂的制备及其催化乳酸乙酯液相加氢性能
赵凤伟 沈美玉 王 琳 杜长海*
(长春工业大学化学工程学院,长春130012)
采用浸渍-还原法制备了负载型Co-B/γ-Al2O3非晶态合金催化剂,并将其应用于乳酸乙酯液相加氢制备1,2-丙二醇(1,2-PDO)反应中,研究了其催化加氢性能.采用电感耦合等离子体(ICP)发射光谱仪、X射线衍射(XRD)仪、透射电子显微镜(TEM)、差示扫描量热(DSC)、X射线光电子能谱(XPS)等手段对催化剂的性能进行了表征,考察了制备条件对催化剂性能的影响.结果表明,新鲜的Co-B/γ-Al2O3催化剂具有非晶态结构,Co-B均匀地分散在载体γ-Al2O3上.随着Co负载量的增加,催化剂的热稳定性提高,催化剂表面Co/B原子比增加.当金属Co理论负载量为30%(质量分数,w)时,Co-B/γ-Al2O3催化剂表现出最高的加氢催化性能,在160°C,氢气压力为6.0 MPa条件下反应9 h,乳酸乙酯的转化频率(TOF)为1.41 h-1,转化率达到93.63%,1,2-丙二醇的选择性达到96.10%.催化剂的加氢性能取决于其分散均匀的Co-B纳米粒子、较高的表面Co/B原子比及Co和B之间的电子转移效应.
非晶态催化剂;Co-B/γ-Al2O3;乳酸乙酯;1,2-丙二醇;催化加氢
©Editorial office ofActa Physico-Chimica Sinica
1 引言
1,2-丙二醇(1,2-PDO)是一种重要的有机化工原料,主要用做生产不饱和聚酯的中间体,并广泛应用在食品、药品、化妆品等重要领域.1工业上主要采用环氧丙烷水合法生产1,2-PDO.2它依赖石油基产品环氧丙烷做原料,环境污染严重.利用可再生的生物质资源生产高附加值化工产品替代化石原料的生产,是一条绿色环保路线并成为研究热点.乳酸作为一种重要的生物质平台化合物,其加氢制备1,2-PDO已得到广泛的研究.3,4
乳酸及其衍生物加氢反应主要采用负载型Ru基催化剂.5-8由于贵金属资源稀少且价格较高,Ru基催化剂的应用受到限制.近来,研究者将焦点转向非贵金属Cu基9,10和Co基11,12催化剂.Kasinathan等10制备的Cu/SiO2催化剂用于该反应需要较高的Cu负载量(80%(w))和很长的反应时间(30 h)才能获得较高的1,2-PDO收率.此外,Cu基催化剂往往需要辅助加入Zn、Cr等助剂提高催化性能.13Huang等12研究表明,Co/SiO2在乳酸乙酯加氢制备1,2-PDO反应中展现的催化性能略高于Cu/SiO2.Xue等11采用沉淀-凝胶(PG)法制备Co/SiO2催化剂,用于乳酸乙酯液相加氢反应中,乳酸乙酯转化率达到90.4%,1,2-PDO选择性为95.8%.可见,Co基催化剂有利于乳酸乙酯加氢反应.
非晶态合金催化剂作为一种新型高效绿色催化材料已用于多种加氢反应中.14-16Luo等6用助剂Sn改性的Ru-B/γ-Al2O3非晶态催化剂显著促进了乳酸乙酯加氢反应,乳酸乙酯转化率达到90.7%时, 1,2-PDO选择性为91.5%.Fan等8制备的Ru-B/TiO2非晶态催化剂,以水做溶剂,催化乳酸乙酯加氢制1, 2-PDO,产率为93%.Co-B非晶态催化剂在肉桂醛、柠檬醛等多种加氢反应中表现出较好的活性和选择性,17,18且更具竞争优势,但该类催化剂用于乳酸及其衍生物加氢制备1,2-PDO尚未有报道.在前期研究19的基础上,本文采用浸渍-还原法制备了负载型Co-B/γ-Al2O3非晶态合金催化剂,并用于乳酸乙酯液相加氢制备1,2-PDO反应,并研究其催化性能.
2 实验部分
2.1 实验药品
四水合乙酸钴(Co(COOH)2·4H2O,AR),硼氢化钠(NaBH4,≥96%),国药集团化学试剂有限公司;乳酸乙酯(C5H10O3,AR),邻二甲苯(C8H10,AR),天津光复精细化工有限公司;无水乙醇(AR),氢氧化钠(AR),正庚烷(C7H16,AR),北京化工厂;γ-Al2O3(工业级),抚顺石化公司催化剂厂;氮气(≥99.99%),氢气(≥99.99%),长春巨洋气体有限责任公司.
2.2 催化剂制备
0.5 g γ-Al2O3(60-80目)加入适量蒸馏水中,搅拌2 h.然后加入适量Co(COOH)2·4H2O,保持Co2+浓度为0.2 mol·L-1,继续剧烈搅拌4 h.氮气保护下,逐滴滴加2 mol·L-1的NaBH4溶液(溶解在0.2 mol·L-1的NaOH溶液中),其中NaBH4与Co2+的摩尔比为3:1.滴加完毕继续搅拌30 min,静置30 min.所得黑色固体颗粒经去氧离子水反复洗涤至中性,然后用无水乙醇洗涤3次,除去其中的水溶性离子,即得X%(w)Co-B/γ-Al2O3催化剂,其中X%表示金属Co的理论负载量(w),即为m(Co)/(m(Co)+m(γ-Al2O3))× 100%.样品保存在正庚烷中备用.非负载型Co-B催化剂样品的制备过程、参数及保存方法同Co-B/γ-Al2O3催化剂的制备.
2.3 催化剂的表征
催化剂体相组成采用电感耦合等离子体发射光谱仪(ICP-OES,美国ThermoScientific iCAP6300型)测定.X射线粉末衍射谱(XRD)在Rigaku RINT-2000衍射仪上进行.采用Cu Kα(λ=0.15405 nm)为辐射源,工作电压40 kV,工作电流30 mA,扫描范围10°-80°,扫描速率5(°)·min-1.非晶态合金催化剂的热稳定性采用差示扫描量热仪(DSC)测定.DSC在NETZSCH STA 409 PC/PG上进行,使用氩气为保护气,测试温度50-550°C,升温速率10°C·min-1. TEM图像用JEOL JEM-2000EX透射电子显微镜获得,观察样品形貌,颗粒大小及分散度.选区电子衍射(SAED)图在JEOL JEM-2000EX上测定,用于确定相状态,点分辨率0.23 nm,晶格分辨率0.14 nm. X射线光电子能谱(XPS)在VG Microtech 3000 Multilab型光电子能谱上测定,采用Al Kα作激发光源(hν=1486.6 eV),电子结合能用碳C 1s(284.6 eV)进行校正.
2.4 催化剂活性评价
乳酸乙酯加氢反应在50 mL高压反应釜中进行.将0.25 g催化剂,2 mL乳酸乙酯和7 mL正庚烷加入反应釜中,密封后通高纯氢气3次以排尽釜内的空气.待釜内空气排净,充入6 MPa氢气后将高压釜放入160°C油浴中,待温度再次稳定后开启搅拌并计时,设定搅拌速度为1000 r·min-1,以消除内扩散效应的影响.产物采用气相色谱(SP-2100)进行分析,氢火焰离子检测器(FID)检测,色谱柱为Rtx-Wax(30 m×0.32 mm×0.25 μm)毛细管柱,使用邻二甲苯为内标物进行定量分析.
3 结果与讨论
3.1 XRD表征分析
图1为催化剂样品的XRD谱图.可以看出,新鲜Co-B样品(图1(a))在2θ=45°,23°附近均有一宽弥散峰,对应非晶态合金的特征衍射峰和无定形氧化硼的特征峰.14,20Co-B样品在200°C处理2 h的谱图(图1(b))中只有非晶态的特征峰,说明Co-B在200°C仍保持非晶态结构.继续升高热处理温度到350°C,此时Co-B样品(图1(c))在2θ=45°,76°出现金属Co衍射峰,在2θ=42°,48°出现晶态Co2B的衍射峰,表明Co-B发生了晶化.21比较图1(d)与图1(e)的XRD谱图发现,负载后的新鲜30%(w)Co-B/γ-Al2O3催化剂XRD谱图与载体γ-Al2O3谱图基本相同,但是衍射峰强度明显减弱,表明Co-B非晶态合金均匀分散在γ-Al2O3载体表面上.30%(w)Co-B/γ-Al2O3样品在200°C处理后(图1(f)),没有出现新的衍射峰, 350°C下处理2 h(图1(g))出现Co3O4的衍射峰,22600°C焙烧后(图1(h))衍射峰强度显著增加,Co-B/ γ-Al2O3样品逐渐由非晶态结构向晶态结构转化.

图1 催化剂样品的XRD谱图Fig.1 XRD patterns of the catalyst samples
3.2 TEM表征分析
图2为非晶态催化剂的TEM和SAED图.从图2(b)可见,非负载型Co-B催化剂中的Co-B纳米粒子严重团聚,分散度较差,平均粒径约为60 nm.在图2(a)中,30%(w)Co-B/γ-Al2O3催化剂的Co-B纳米粒子均匀分散在γ-Al2O3载体表面且粒径在10-20 nm之间.这种显著的差异,归因于γ-Al2O3载体的引入以及Co-B非晶态合金纳米粒子与γ-Al2O3载体之间的相互作用力有效地阻碍和抑制表面高能纳米粒子的迁移和团聚,使得负载后的催化剂具有更高的分散度和更小的粒径.23图2(c)为40%(w)Co-B/γ-Al2O3的TEM图,出现催化剂颗粒之间的覆盖和聚集现象,较30%(w)Co-B/γ-Al2O3样品分散度严重下降.此外,两个催化剂的SAED图中均只有非晶态合金特有的衍射环,表明催化剂具有非晶态结构,与XRD表征结果一致.6,17

图2 催化剂样品的TEM图Fig.2 TEM images of the catalyst samples
3.3 DSC表征分析
图3是制备的Co-B和Co-B/γ-Al2O3催化剂的DSC曲线.由图3可见,Co-B和Co-B/γ-Al2O3的DSC曲线相似,说明样品的晶化过程类似.催化剂的DSC曲线均在200-400°C之间出现强度较弱的较宽放热峰,对应于催化剂升温过程中,非晶态合金表面不稳定化合物的结晶放热峰,是催化剂完全晶化之前的中间态.24随着温度升高,DSC曲线在450-520°C之间出现强度较大的结晶放热峰,由非晶态合金主体发生晶化产生.图3(a)显示,非负载型Co-B合金的晶化温度在470°C左右,20%(w)Co-B/γ-Al2O3(图3(b))在450-550°C测试温度范围内没有出现较强的放热峰,说明该样品在550°C时还未发生非晶态主体的晶化过程,其热稳定性较高.随着Co负载量的增加,30%(w)Co-B/γ-Al2O3(图3(c))和40%(w)Co-B/γ-Al2O3样品(图3(d))在490°C附近出现较强的放热峰,较非负载Co-B样品提高了20°C,说明负载型非晶态Co-B合金具有更高的热稳定性.25非晶态纳米粒子的团聚是晶化的前提条件,14由TEM表征结果也可推断出非负载Co-B合金的热稳定性较差,这与DSC表征结果吻合.非晶态合金的负载化提高了非晶态合金催化剂的热稳定性,这与文献报道21,23,25一致.

图3 催化剂样品的差示扫描量热(DSC)曲线Fig.3 Differential scanning calorimetry(DSC) curves of the catalyst samples
3.4 XPS表征分析
催化剂的XPS谱图如图4所示.催化剂的体相和表面组成见表1.根据表1数据,催化剂体相组成接近,表面组成却相差较大.随着负载量增加,负载型Co-B/γ-Al2O3催化剂的表面Co/B原子比先增大后减小.30%(w)Co-B/γ-Al2O3样品拥有最大表面Co/B原子比,且显著高于非负载型Co-B催化剂.我们推测Co/B表面原子比可能与分散度密切相关:载体γ-Al2O3的引入,提高了非晶态合金纳米粒子的分散度,有助于Co在表面富集从而使更多的活性中心暴露在表面.26由TEM表征图可知,负载量增加,载体表面Co-B纳米粒子覆盖和聚集严重,21分散度下降导致表面Co/B原子比大大降低,因此40%(w)Co-B/ γ-Al2O3样品的Co/B表面原子比最小.图4为B 1s及Co 2p谱带分峰拟合的结果.从图4(a)可见,B元素以元素态B0及氧化态B2O3两种形式存在,且对于所有催化剂样品,B的结合能没有明显的变化,表明氧化态B2O3的出现可归因于BH4-的水解,而非表面元素态B0的氧化.27元素态B0的结合能(187.7-188.0eV)均比标准B0结合能(187.1 eV)高,这表明非晶态合金中,B与Co之间存在相互作用,B作为电子供体将部分电子转移给Co,表现为缺电子态,这与文献报道一致.17,18,21在图4(b)Co 2p谱带中,Co元素有两种形式,且主要以氧化态Co2+存在.元素态Co0结合能位于777.5 eV附近,较Co0的标准结合能(778.3 eV)低0.8 eV.这意味着在非晶态Co-B合金中,Co和B之间的电子转移效应使Co接受B转移的电子,成为富电子体.20在所有样品中,元素态Co0结合能基本不变,其原因可能是Co元素原子体积远大于B的原子体积.17,27在非负载型Co-B催化剂中,Co0的峰很明显,而负载后Co0的峰明显变小,这可能与Co-B均匀负载在载体上有关.从图4(b)中还可以看出,随着Co-B负载量的增加,Co2+的峰明显向高结合能偏移,这是由于Co2+离子与载体之间发生相互作用,导致一些Co活性物种不能被BH4-完全还原.28
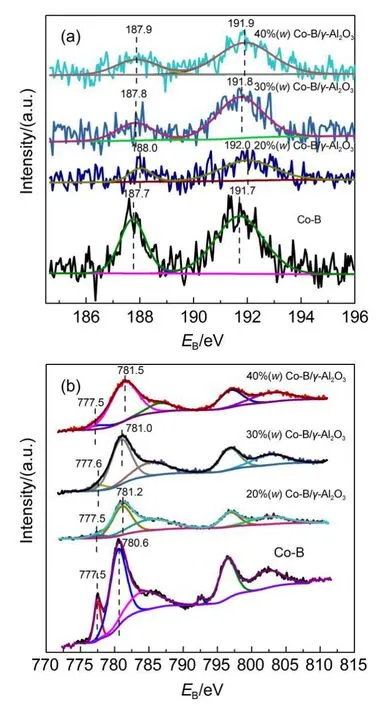
图4 催化剂样品的XPS谱图Fig.4 XPS patterns of the catalyst samples

表1 Co-B和Co-B/γ-Al2O3催化剂的体相和表面组成Table 1 Bulk and surface compositions of the Co-B and Co-B/γ-Al2O3catalysts
3.5 乳酸乙酯的加氢性能
图5为不同Co负载量的Co-B/γ-Al2O3催化剂对乳酸乙酯催化加氢反应性能的影响.由图5可见,随着Co负载量增加,乳酸乙酯的转化频率(TOF)、转化率和1,2-PDO选择性呈先增大后减小的趋势.20% (w)Co-B/γ-Al2O3和30%(w)Co-B/γ-Al2O3非晶态催化剂的TOF较为接近,分别为1.43和1.41 h-1,但30%(w)Co-B/γ-Al2O3催化剂的1,2-PDO选择性最高,为96.10%,这显著高于非负载型Co-B催化剂(与30%(w)Co-B/γ-Al2O3催化剂的Co质量相同),且高于Xue等11报道的结果.一方面,适宜的Co负载量能提高Co-B纳米粒子的分散性和热稳定性,使负载后的Co-B/γ-Al2O3催化剂表面富集Co,增加了表面活性中心位,提高催化剂的催化性能.26,29另一方面,根据XPS结果,Co-B/γ-Al2O3催化剂Co和B之间的电子效应,使Co呈富电子态,B为缺电子态.富电子Co活性位上的高电子密度有利于氢解离为活化氢,而缺电子态的B有利于乳酸乙酯分子中C=O的吸附和活化,从而有利于乳酸乙酯加氢反应的发生.6,16,27本研究中,虽然30%(w)Co-B/γ-Al2O3非晶态催化剂初次使用活性较高,但再次使用时催化剂迅速失活,乳酸乙酯的转化率降到30.0%左右,1,2-PDO选择性降为80%左右,关于催化剂的失活和再生问题还需进一步深入研究.
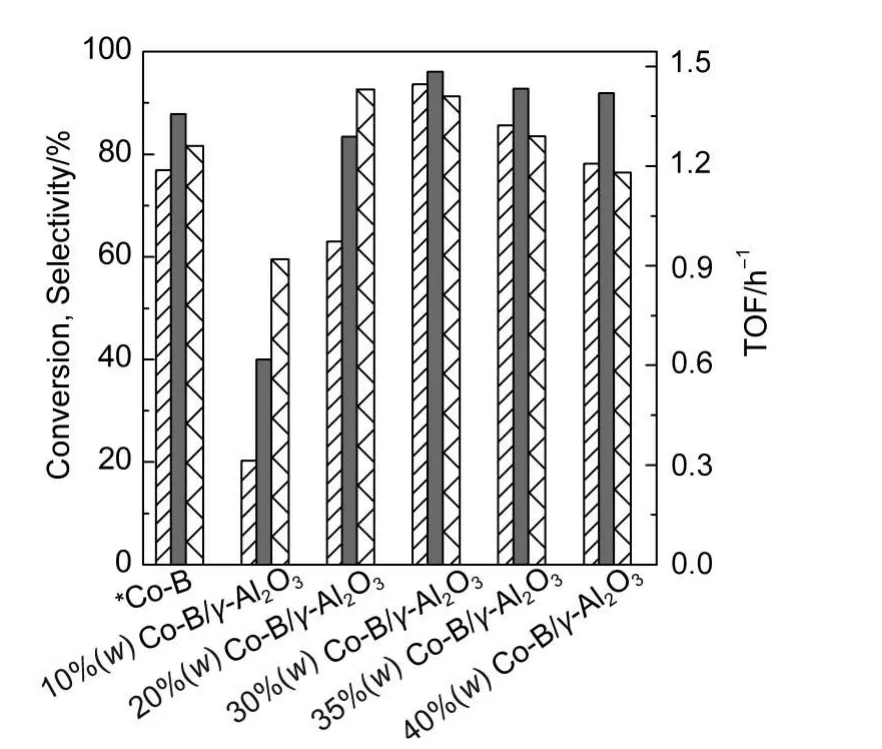
图5 Co-B/γ-Al2O3与非负载型Co-B催化剂的催化性能Fig.5 Catalytic performance of Co-B/γ-Al2O3catalyst and unsupported Co-B catalyst
4 结论
采用浸渍-还原法制备了负载型Co-B/γ-Al2O3非晶态合金催化剂.30%(w)Co-B/γ-Al2O3非晶态合金催化剂在乳酸乙酯液相加氢制备1,2-PDO反应中显示出较好的催化性能,在适宜反应条件下,乳酸乙酯的TOF为1.41 h-1,转化率为93.63%,1,2-PDO的选择性为96.10%.适宜的Co负载量可提高活性组分Co-B在载体上的分散性和热稳定性,较高的表面Co/B原子比以及非晶态合金中Co和B之间的电子转移效应是30%(w)Co-B/γ-Al2O3非晶态催化剂催化性能高的主要原因,催化剂的失活和再生问题还有待于进一步深入研究.
(1)Fan,Y.X.;Zhou,C.H.;Zhu,X.H.Catal.Rev.2009,51, 293.doi:10.1080/01614940903048513
(2)Chaminand,J.;Djakovitch,L.A.;Gallezot,P.;Marion,P.;Pinel, C.;Rosier,C.Green Chem.2004,6,359.doi:10.1039/b407378a
(3)Dusselier,M.;Van Wouwe,P.;Dewaele,A.;Makshina,E.;Sels, B.F.Energy&Environmental Science2013,6,1415.doi: 10.1039/c3ee00069a
(4)Corma,A.;Iborra,S.;Velty,A.Cat.Rev.2007,107,2411.
(5)Zhang,Z.G.;Jackson,J.E.;Miller,D.J.Appl.Catal.A2001,219,89.doi:10.1016/S0926-860X(01)00669-X
(6)Luo,G.;Yan,S.R.;Qiao,M.H.;Zhuang,J.H.;Fan,K.N. Appl.Catal.A2004,275,95.doi:10.1016/j.apcata.2004.07.024
(7)Yang,Q.;Zhang,J.;Zhang,L.;Fu,H.Y.;Zheng,X.L.;Yuan, M.L.;Chen,H.;Li,R.X.Catal.Commun.2013,40,37.doi: 10.1016/j.catcom.2013.05.023
(8)Fan,G.Y.;Zhang,Y.;Zhou,Y.F.;Li,R.X.;Chen,H.;Li,X.J.Chem.Lett.2008,37,852.doi:10.1246/cl.2008.852
(9)Simonov,M.N.;Zaikin,P.A.;Simakova,I.L.Appl.Catal.B2012,119,340.
(10)Kasinathan,P.;Yoon,J.W.;Hwang,D.W.;Lee,U.;Hwang,J. S.;Hwang,Y.K.;Chang,J.S.Appl.Catal.A2013,451,236. doi:10.1016/j.apcata.2012.10.027
(11)Xue,J.J.;Cui,F.;Huang,Z.W.;Zuo,J.L.;Chen,J.;Xia,C.G. Chin.J.Chem.2011,29,1319.doi:10.1002/cjoc.v29.7
(12)Huang,L.;Zhu,Y.L.;Zheng,H.Y.;Du,M.X.;Li,Y.W.Appl. Catal.A2008,349,204.doi:10.1016/j.apcata.2008.07.031
(13)Ji,W.R.;Tan,Y.B.;Zeng,Y.L.;Ying,H.J.;Hu,L.B.Journal of Zhejiang University of Technology2013,41,183.[计伟荣,谭冶斌,曾玉龙,应惠娟,胡凌波.浙江工业大学学报,2013,41,183.]
(14)Chen,Y.Catal.Today1998,44,3.doi:10.1016/S0920-5861(98) 00169-2
(15)Molnáar,Á.;Smith,G.V.;Bartók,M.Adv.Catal.1989,36,329.
(16)Wang,W.Y.;Zhang,X.Z.;Yang,Y.Q.;Yang,Y.S.;Peng,H. Z.;Luo,H.A.Acta Phys.-Chim.Sin.2012,28,1243.[王威燕,张小哲,杨运泉,杨彦松,彭会左,罗和安.物理化学学报,2012,28,1243.]doi:10.3866/PKU.WHXB201203081
(17)Li,H.;Liu,J.;Xie,S.H.;Qiao,M.H.;Dai,W.L.;Li,H.X. J.Catal.2008,259,104.doi:10.1016/j.jcat.2008.07.015
(18)Chen,Y.Z.;Liaw,B.J.;Chiang,S.J.Appl.Catal.A2005,284, 97.doi:10.1016/j.apcata.2005.01.023
(19)Ma,X.Y.;Zhao,F.W.;Sun,D.;Du,C.H.Fine Chemicals2014,31,452.[马晓雨,赵凤伟,孙 德,杜长海.精细化工,2014,31,452.]
(20)Li,H.X.;Li,H.;Wang,M.H.Appl.Catal.A2001,207,129. doi:10.1016/S0926-860X(00)00662-1
(21)Chiang,S.J.;Yang,C.H.;Chen,Y.Z.;Liaw,B.J.Appl.Catal. A2007,326,180.doi:10.1016/j.apcata.2007.04.019
(22)Xu,D.Y.;Zhao,L.;Dai,P.;Ji,S.F.J.Nat.Gas Chem.2012,21,488.doi:10.1016/S1003-9953(11)60395-2
(23)Wang,L.J.;Li,W.;Zhang,M.H.;Tao,K.Y.Appl.Catal.A2004,259,185.doi:10.1016/j.apcata.2003.09.037
(24)Yamashita,H.;Funabiki,T.;Yoshida,S.J.Chem.Soc.Chem. Commun.1984,868.
(25)Zhang,R.B.;Li,F.Y.;Shi,Q.J.;Luo,L.T.Appl.Catal.A2001,205,279.doi:10.1016/S0926-860X(00)00574-3
(26)Yang,C.C.;Chen,M.S.;Chen,Y.W.Int.J.Hydrog.Energy2011,36,1418.doi:10.1016/j.ijhydene.2010.11.006
(27)Li,H.X.;Li,H.;Zhang,J.;Dai,W.L.;Qiao,M.H.J.Catal.2007,246,301.doi:10.1016/j.jcat.2006.12.014
(28)Li,H.;Li,H,X.;Deng,J.F.Catal.Today2002,74,53.doi: 10.1016/S0920-5861(01)00530-2
(29)Long,J.Y.;Ma,L.;He,D.H.Acta Phys.-Chim.Sin.2010,26, 2719.[龙俊英,马 兰,贺德华.物理化学学报,2010,26, 2719.]doi:10.3866/PKU.WHXB20101022
Preparation of Amorphous Co-B/γ-Al2O3Catalyst and Its Performance in Catalytic Liquid Phase Hydrogenation of Ethyl Lactate
ZHAO Feng-Wei SHEN Mei-Yu WANG Lin DU Chang-Hai*
(School of Chemical Engineering,Changchun University of Technology,Changchun 130012,P.R.China)
Supported cobalt amorphous catalysts Co-B/γ-Al2O3were prepared using an impregnation-chemical reduction method for liquid phase hydrogenation of ethyl lactate to 1,2-propanediol(1,2-PDO).The Co-B/γ-Al2O3catalysts were characterized using inductively coupled plasma(ICP)optical emission spectrometry,X-ray diffraction(XRD),transmission electron microscopy(TEM),differential scanning calorimetry(DSC),and X-ray photoelectron spectroscopy(XPS).The effects of the catalyst preparation conditions on the hydrogenation of ethyl lactate were investigated.All the fresh catalysts showed an amorphous structure and Co-B particles were dispersed uniformly on the γ-Al2O3support.The thermal stability of the amorphous catalyst and the Co/B atomic ratio of surface composition increased with increasing the Co content.The Co-B/γ-Al2O3amorphous catalyst showed the highest catalytic activity when the theoretical loading of metal Co was 30%(mass fraction,w).The ethyl lactate turnover frequency(TOF),conversion,and selectivity to 1,2-PDO reached 1.41 h-1,93.63%,and 96.10%,respectively at a reaction temperature of 160°C and hydrogen pressure of 6.0 MPa for 9 h.The higher catalytic performance of the 30%(w)Co-B/γ-Al2O3supported amorphous catalyst is attributed to its highly dispersing Co-B particles,higher Co/B atomic ratio of surface composition,and electron transfer effect between Co and B.
Amorphous catalyst;Co-B/γ-Al2O3;Ethyl lactate;1,2-Propanediol;Catalytic hydrogenation
O643
10.3866/PKU.WHXB201501052www.whxb.pku.edu.cn
Received:November 5,2014;Revised:January 2,2015;Published on Web:January 5,2015.
∗Corresponding author.Email:du661123@163.com;Tel:+86-431-85717215.
The project was supported by the Natural Science Foundation of Jilin Provincial Science&Technology Department,China(201215117).吉林省科技厅自然科学基金(201215117)资助项目
