吡啶离子液体[BPy][BF4]与乙腈混合体系中杜醌的光化学反应动力学
2015-12-29朱光来张良伟刘艳成吴国忠
朱光来 王 玉 张良伟 刘艳成 吴国忠,*
(1安徽师范大学原子与分子物理研究所,安徽芜湖241000;2中国科学院上海应用物理研究所,上海201800)
吡啶离子液体[BPy][BF4]与乙腈混合体系中杜醌的光化学反应动力学
朱光来1,*王 玉1张良伟1刘艳成2吴国忠2,*
(1安徽师范大学原子与分子物理研究所,安徽芜湖241000;2中国科学院上海应用物理研究所,上海201800)
用激光闪光光解方法研究了杜醌(DQ)在吡啶型离子液体N-丁基吡啶四氟硼酸盐([BPy][BF4])与乙腈(MeCN)组成的共混溶剂中的光化学反应机理与动力学.实验结果表明,离子液体[BPy][BF4]对混合体系中杜醌激发三线态(3DQ*)的瞬态吸收峰位置和吸光度大小都没有产生明显影响.在N2饱和条件下,无论是在乙腈溶液中还是在[BPy][BF4]/MeCN混合溶液中3DQ*的衰减都遵循一级反应动力学规律.而[BPy][BF4]的存在对3DQ*与三乙胺(TEA)之间的电子转移影响显著.随着[BPy][BF4]/MeCN体系中离子液体比例的增加,杜醌三线态3DQ*与TEA间的瞬态反应机理没有改变,但它们之间的光诱导电子转移反应速率和生成自由基的量子产额逐渐降低,通过改变离子液体的比例可以调节该体系中光诱导电子转移反应的速率和效率.
N-丁基吡啶四氟硼酸盐;离子液体;杜醌;瞬态吸收光谱;光诱导电子转移
1 引言
室温离子液体是指在室温或接近室温下呈液态,由有机阳离子和无机阴离子所组成的离子化合物,简称为离子液体(ILs).1,2离子液体具有良好的热稳定性和化学稳定性、极低的蒸汽压、可循环利用等优点.1-3由不对称的阴、阳离子组成的结构特点,决定了离子液体具有独特的性质.目前人们对离子液体的研究主要集中在有机反应和绿色分离方面,而对离子液体内发生的化学反应的机理,特别是其结构和物性对反应影响的机理研究还有待深入,需要化学、物理和其他学科的交融来探索离子液体结构与性能的关系.4,5
©Editorial office ofActa Physico-Chimica Sinica
尽管离子液体在宏观尺度上呈现均匀液态,但实验与理论研究已经证实在一些离子液体中存在着不同形态聚集体.5-7离子液体与分子溶剂的混合体系中,组分比例不同会引起溶剂的热力学性质和局部微观结构的变化,从而对溶质分子的扩散、迁移等输运性质产生重要影响.近十年以来,离子液体以其独特的性能也逐渐引起了光化学研究者们的兴趣,开展了大量的光谱学研究以揭示其结构、物理和化学性质.8-10研究表明离子液体可作为产生和光谱表征自由基的优良介质.11,12然而,目前有关离子液体中的瞬态光化学反应尤其是光诱导电子转移反应方面的研究主要集中于咪唑离子液体.13-15如Samanta13结合瞬态吸收光谱和荧光手段研究了不同粘度的ILs中的电子转移反应,发现体系的粘度对电子转移反应的速率和量子产额有很大的影响.美国马里兰大学Vieira和Falvey10比较研究了咪唑和吡啶离子液体作为溶剂对电子传递过程的调控作用.国内相关研究机构也相继开展了离子液体中的脉冲辐解与激光光解研究,16-19着重考查离子液体本身的激发行为.16,17由于吡啶及其衍生物在染料敏化太阳能电池领域中的潜在应用价值,20,21深入研究吡啶离子液体对一些光化学过程尤其是光诱导电子转移过程的影响是非常必要的.
本文选择355 nm激光作为光源,以杜醌(四甲基对苯醌)作为探针分子,利用激光闪光光解方法研究了吡啶型离子液体[BPy][BF4]与MeCN混合体系中杜醌的瞬态吸收光谱.实验结果表明离子液体[BPy][BF4]作为溶剂对杜醌激发三线态无明显影响,而对杜醌/三乙胺体系的光诱导电子转移过程影响较大,随着[BPy][BF4]比例的增加,光诱导电子转移反应的速率和效率都明显降低.但相比较咪唑离子液体而言,吡啶离子液体更适合作为研究光诱导电子转移的介质,即使在[BPy][BF4]的比例足够大的情况下,杜醌三线态与三乙胺之间的电子转移也不会完全被抑制.
2 实验部分
2.1 实验材料
乙腈和三乙胺分别为购自上海百灵威公司的HPLC级试剂,杜醌购自日本TCI公司,纯度大于98%.以上试剂均未进一步处理直接使用.光解实验用离子液体[BPy][BF4]为高纯级试剂(>99%),由中国科学院兰州化学物理研究所绿色化学与催化中心提供,使用前在60°C条件下真空干燥12 h,以除去水分及挥发性有机物,最后将纯化后的离子液体存储于干燥器中备用.
2.2 仪器和方法
瞬态吸收光谱实验采用Nd:YAG激光器(NL303HT,立陶宛EKSPLA公司)产生的355 nm波长激光作为激励光源,脉冲宽度约6 ns,单脉冲能量约为20 mJ,采用300 W氙灯作为分析光源,在氙灯脉冲发生后(亮度增加100倍),于合适的延迟时间后,触发激光脉冲.激光与分析光垂直透过1 cm× 1 cm石英样品池,分析光经单色仪分光后使用有效检测范围为280-750 nm的R955光电倍增管(Hamamatsu)检测,输出信号由HP 54510B数字示波器转换成数字信号,并用动力学数据处理软件在计算机上进行分析.22实验前对所用样品溶液采用99.99%的高纯氮气鼓泡15 min以除去氧气.所有实验均在约25°C的室温下进行.
3 结果与讨论
3.1 杜醌在[BPy][BF4]/MeCN体系中的激光光解
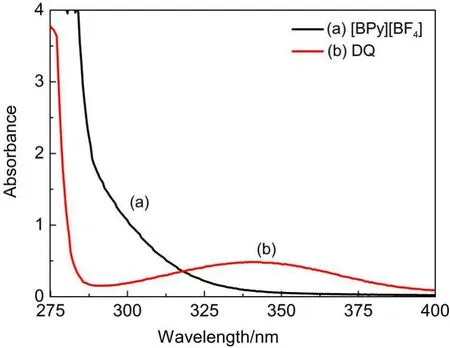
图1 纯[BPy][BF4](a)与含2×10-3mol·dm-3杜醌的乙腈溶液(b)的紫外-可见吸收光谱Fig.1 UV-Vis absorption spectra of pure[BPy][BF4](a) and 2×10-3mol·dm-3duroquinone(DQ)in acetonitrile(MeCN)solution(b)
如图1(a)所示,离子液体[BPy][BF4]及其乙腈溶液在紫外区域有强烈吸收,而在近紫外区尤其是350 nm以后无明显吸收.在355 nm光激发条件下,未观察到[BPy][BF4]有明显的瞬态吸收存在.而DQ在355 nm附近有较强吸收(图1(b)),是常用的光敏探针.因此,[BPy][BF4]是适合的光诱导反应介质.
在N2饱和条件下,2×10-3mol·dm-3杜醌乙腈溶液,经355 nm激光激发后得到一系列的瞬态吸收光谱.在未加[BPy][BF4]的DQ/MeCN中观察到最大吸收峰位于470-480 nm处宽的吸收带,如图2所示,可以归属为杜醌激发三线态(3DQ*)的瞬态吸收光谱.23在N2饱和条件下,3DQ*的衰减主要通过碰撞和系间窜越(ISC)等非辐射跃迁完成,如方程(1)和(2)所示.

保持杜醌浓度为2×10-3mol·dm-3,通过改变混合溶剂中[BPy][BF4]与MeCN的比例,平行做若干组实验.观测的结果与咪唑离子液体对杜醌的影响明显不同,24随着溶液中[BPy][BF4]体积分数(VIL)的增加,杜醌溶液的瞬态吸收带和最大吸收峰位置几乎没有发生变化,如图2所示,说明3DQ*不会直接与[BPy][BF4]发生化学反应.经过拟合发现,无论是以乙腈还是[BPy][BF4]/MeCN为溶剂,3DQ*时间谱均按照准一级动力学衰减.3DQ*在[BPy][BF4]比例不同的混合溶液中的衰减曲线变化不大,随着[BPy] [BF4]比例的增大,3DQ*的寿命略微延长,如图3所示,这可能是由于体系的黏度增大,扩散变慢,导致三线态因碰撞猝灭的几率变小.
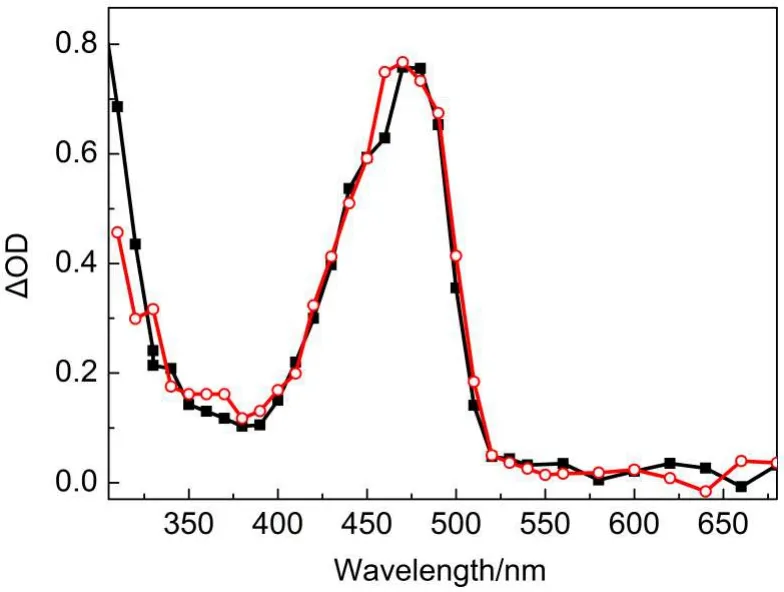
图2 N2饱和下DQ的[BPy][BF4]/MeCN溶液在355 nm激光激发后0.1 μs的瞬态吸收光谱Fig.2 Transient absorption spectra of DQ in N2-saturated [BPy][BF4]/MeCN solution recorded at 0.1 μs after 355 nm laser excitation
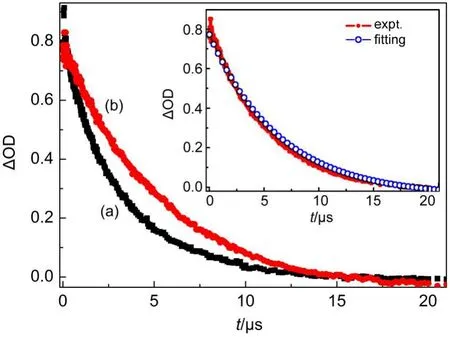
图3 N2饱和下DQ的[BPy][BF4]/MeCN溶液在激光激发后位于480 nm处的时间曲线Fig.3 Time profiles observed at 480 nm of DQ in N2-saturated[BPy][BF4]/MeCN solution
3.2 [BPy][BF4]对DQ/TEA体系电子转移反应的影响
3.2.1 3DQ*与TEA在乙腈溶液中的电子转移反应
醌类物质是一种良好的电子受体,它可以与胺之间发生电子转移反应.三乙胺与蒽醌、杜醌等受体之间的电子转移反应已经被广泛研究.25-27TEA的乙腈溶液在355 nm光激发下没有明显的瞬态吸收.图4所示的是在DQ/MeCN的溶液中加入2.9×10-3mol·dm-3TEA,经355 nm激光光解后得到的瞬态吸收峰,与图2中DQ在乙腈溶液的瞬态吸收明显不同.对比不同延时下的瞬态吸收发现,在光激发0.1 μs以后,3DQ*在480 nm的特征吸收逐渐减弱,而430 nm处新出现的吸收峰逐渐增强,此吸收峰主要归属为杜醌负离子自由基DQ-•的特征吸收.27说明

图4 N2饱和下DQ/TEA的乙腈溶液在激光激发后不同延时下测得的瞬态吸收光谱Fig.4 Transient absorption spectra of DQ/TEAin N2-saturated MeCN solution recorded at different delay time after laser excitation
3DQ*与TEA两者之间发生了电子转移,生成三乙胺阳离子自由基TEA+•和DQ-•.到1 μs时,3DQ*的吸收峰基本消失,而DQ-•的特征吸收峰则达到最大值.其主要反应机理在文献27中已有详述,概括如下:

选取DQ-•在430 nm处吸收作动力学分析,可以看到有明显的快速生成过程,根据数据分析系统的拟合,其生成符合准一级动力学规律.为定量研究反应动力学,我们用DQ-•的表观生成速率常数kgr与对应的TEA摩尔浓度作图,得到了TEA浓度变化与kgr之间的关系,如图5所示,经线性拟合得到DQ与TEA之间的光诱导电子转移反应速率为2.87× 108mol-1·dm3·s-1.

图5 N2饱和下乙腈溶液中DQ-•在430 nm处的表观生成速率常数(kgr)与三乙胺浓度的关系Fig.5 Dependence of first-order growth constant(kgr) rate of DQ-•at 430 nm on concentrations of TEAin N2-saturated MeCN solution
3.2.2 [BPy][BF4]对3DQ*/TEA电子转移的影响
在相同的温度和气氛条件下,进一步研究了[BPy][BF4]的体积分数VIL不同对3DQ*与TEA之间电子转移过程的影响.图6显示的是VIL为0.85时该体系的瞬态吸收光谱.与图4比较,DQ-•的特征吸收峰在激光激发0.1 μs后不是很明显,直到3 μs时430 nm处才显示一个宽的吸收带,而此时3DQ*在480 nm处的吸收峰也衰减变弱,在3 μs以后逐步消失.这表明在一定比例[BPy][BF4]/MeCN的混合体系中电子转移过程变慢.

图6 N2饱和下DQ/TEA在VIL=0.85的[BPy][BF4]/MeCN混合溶剂中,在激光激发后0.1,3,5 μs的瞬态吸收光谱Fig.6 Transient absorption spectra of DQ/TEArecorded at 0.1,3,and 5 μs after laser excitation in N2-saturated [BPy][BF4]/MeCN solution with VIL=0.85
选取430 nm处吸收进行动力学分析.由于3DQ*在430 nm处有较弱的吸收叠加,因此选取没有添加TEA时430 nm处的吸收峰与添加TEA后430 nm的叠加峰作减谱处理.28按照这种方法对图7(a)所示的不同TEA浓度下的时间曲线进行处理,得到DQ-•在430 nm处的表观生成速率与TEA浓度的关系(如图7(b)所示),经拟合得到DQ与TEA之间的光电子转移反应速率为1.09×108mol-1·dm3·s-1,约为纯乙腈溶液中的三分之一左右,但仍然处在相同数量级.经过对430 nm处时间曲线拟合可知,DQ-•的生成和衰减仍然符合准一级反应动力学(如图7插图所示),由此推断离子液体的存在只是影响了反应速率和效率,并不会改变反应机理.
为了定量研究离子液体对DQ/TEA系统发生的光诱导电子转移反应的调控,对DQ/TEA在不同比例离子液体的溶剂中的瞬态吸收进行了系统研究.在N2饱和条件下,保持DQ(2×10-3mol·dm-3)和TEA(3.6×10-3mol·dm-3)浓度不变,通过改变[BPy] [BF4]/MeCN共混溶剂的比例,平行做九组实验,经355 nm激光激发后得到一系列的瞬态吸收光谱和特征峰的时间曲线.图8给出了430 nm处DQ-•的特征吸收随离子液体比例的变化趋势,在离子液体比例较高的情况下,电子转移反应受到抑制.随着离子液体比例的增加,最大吸收峰的吸光度逐渐降低.研究表明瞬态产物的量子产额基本与特征峰的最大瞬态吸收成正比.将Ф0和ΔOD0记为DQ-•在乙腈溶液中的量子产额和最大吸光度,Ф与ΔODmax表明DQ-•在混合溶液中的量子产额和最大吸光度,则DQ-•在混合体系中的相对量子产额则可通过公式Ф/Ф0=ΔODmax/ΔOD0估算得到.24,29根据图8中430 nm处的最大吸光度计算得到的DQ-•的相对量子产额列在表1中.当VIL足够大时,DQ-•的量子产额明显低于乙腈中的值,且随着离子液体比例的增加而减小.但与我们以前研究咪唑离子液体中的情形相比,在吡啶离子液体中的相对量子产额要高得多,在VIL高达0.85时,电子转移的量子产额和反应速率仍然比较高.可能的原因在于相同阴离子的吡啶离子液体的黏度一般比咪唑离子液体的相对小一些,溶质在其中扩散稍快,所以吡啶离子液体更有利于电子转移的进行.

图7 (a)VIL=0.85时不同TEA浓度值下430 nm处的时间曲线;(b)DQ-•的表观一级生成速率常数与三乙胺浓度的关系Fig.7 (a)Time profiles observed at 430 nm in the solutions with different concentrations of TEA,VIL=0.85; (b)first-order growth rate constant of DQ-•at 430 nm plotted as a function of TEAconcentration
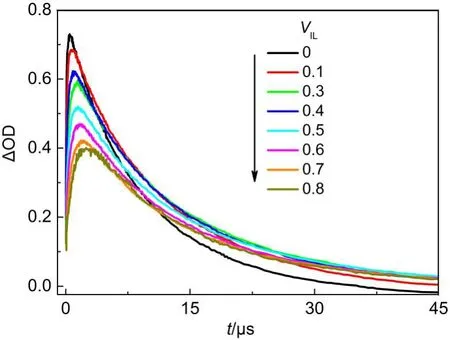
图8 N2饱和下DQ/TEA在不同VIL值下430 nm处的时间曲线Fig.8 Time profiles of DQ/TEAat 430 nm in the N2-saturated DQ/TEAsolutions with different VILvalues

表1 通过Φ/Φ0=ΔODmax/ΔOD0方程估算得到DQ-•的相对量子产额Table 1 Relative quantum yields of DQ-•estimated byΦ/Φ0=ΔODmax/ΔOD0equation
4 结论
瞬态吸收光谱研究表明:杜醌激发三线态3DQ*的瞬态吸收受吡啶离子液体[BPy][BF4]的影响很小,其吸光度和吸收峰位置都没有出现明显变化,说明3DQ*与[BPy][BF4]之间的相互作用不强.而[BPy][BF4]对DQ/TEA体系的光诱导电子转移过程影响很大,随着[BPy][BF4]/乙腈混合体系中离子液体比例的增加,杜醌三线态3DQ*与TEA间的电子转移速率和效率逐渐降低,但降低的程度远小于咪唑类离子液体中降低的趋势.与咪唑离子液体比较而言,[BPy][BF4]更适合作为光诱导电子转移的介质.适当改变离子液体比例,可以对一些光诱导反应的速率和效率进行调节,这对于吡啶离子液体在染料敏化太阳能电池中的潜在应用可能具有一定参考价值.
(1)Rogers,R.D.;Seddon,K.R.Science2003,302,792.doi: 10.1126/science.1090313
(2)Gu,Y.L.;Shi,F.;Deng,Y.Q.Chin.Sci.Bull.2004,49,515. [顾彦龙,石 峰,邓友全.科学通报,2004,49,515.]
(3)Endres,F.;ElAbedin,S.Z.Phys.Chem.Chem.Phys.2006,8, 2101.doi:10.1039/b600519p
(4)Zhang,P.;Gong,Y.;Lv,Y.;Guo,Y.;Wang,Y.;Wang,C.;Li,H. Chem.Commun.2012,48,2334.doi:10.1039/c2cc16906a
(5)Dupont,J.J.Braz.Chem.Soc.2004,15,341.doi:10.1590/ S0103-50532004000300002
(6)Bardak,F.;Xiao,D.;Hines,L.G.;Son,P.;Bartsch,R.A.; Quitevis,E.L.;Voth,G.A.ChemPhysChem2012,13, 1687.doi:10.1002/cphc.201200026
(7)Wang,J.;Zhang,L.;Wang,H.;Wu,C.J.Phys.Chem.B2011,115,4955.doi:10.1021/jp201604u
(8)Paul,A.;Samanta,A.J.Phys.Chem.B2007,111,1957.doi: 10.1021/jp067481e
(9)Yuan,S.;Zhang,Y.;Lu,R.;Yu,A.J.Photochem.Photobiol.A: Chem.2013,260,39.doi:10.1016/j.jphotochem.2013.03.013
(10)Vieira,R.C.;Falvey,D.E.J.Am.Chem.Soc.2008,130, 1552.doi:10.1021/ja077797f
(11)Gordon,C.M.;McLean,A.J.Chem.Commun.2000,1395.
(12)Alvaro,M.;Garcıa,H.Chem.Phys.Lett.2002,362,435.doi: 10.1016/S0009-2614(02)01138-7
(13)Samanta,A.J.Phys.Chem.B2005,109,9148.doi:10.1021/ jp0503967
(14)Yago,T.;Ishii,Y.;Wakasa,M.J.Phys.Chem.C2014,118, 22356.doi:10.1021/jp5069544
(15)Li,X.;Liang,M.;Chakraborty,A.;Kondo,M.;Maroncelli,M. J.Phys.Chem.B2011,115,6592.doi:10.1021/jp200339e
(16)Fu,H.;Xing,Z.;Wu,G.;Yao,S.Res.Chem.Intermed.2011,37,79.doi:10.1007/s11164-010-0226-2
(17)Fu,H.;Xing,Z.;Cao,X.;Wu,G.Chin.Sci.Bull.2013,58, 1882.doi:10.1007/s11434-013-5684-7
(18)Zhu,X.;Li,W.;Yan,H.;Zhong,R.J.Photochem.Photobiol.A: Chem.2012,241,13.doi:10.1016/j.jphotochem.2012.05.013
(19)Zhu,G.L.;Wu,G.Z.;Cui,Z.F.;Xu,X.S.Acta Phys.-Chim. Sin.2011,27,971.[朱光来,吴国忠,崔执凤,许新胜.物理化学学报,2011,27,971.]doi:10.3866/PKU.WHXB20110421
(20)Dürr,M.;Yasuda,A.;Nelles,G.Appl.Phys.Lett.2006,89, 061110.doi:10.1063/1.2266386
(21)Bai,Y.;Zhang,J.;Wang,Y.;Zhang,M.;Wang,P.Langmuir2011,27,4749.doi:10.1021/la200156m
(22)Zuo,Z.;Yao,S.;Luo,J.;Wang,W.;Zhang,J.;Lin,N. J.Photochem.Photobiol.B:Biol.1992,15,215.doi:10.1016/ 1011-1344(92)85125-E
(23)Scheerer,R.;Grätzel,M.J.Am.Chem.Soc.1977,99,865.doi: 10.1021/ja00445a032
(24)Zhu,G.;Wu,G.;Sha,M.;Long,D.;Yao,S.J.Phys.Chem.A2008,112,3079.doi:10.1021/jp077112y
(25)Scaiano,J.C.;Neta,P.J.Am.Chem.Soc.1980,102,1608.doi: 10.1021/ja00525a024
(26)Görner,H.Photochem.Photobiol.2003,77,171.doi:10.1562/ 0031-8655(2003)077<0171:POADTS>2.0.CO;2
(27)Görner,H.Photochem.Photobiol.2003,78,440.doi:10.1562/ 0031-8655(2003)078<0440:POPEOA>2.0.CO;2
(28)Ma,J.;Lin,W.;Du,F.;Han,Z.;Yao,S.;Lin,N.Sci.China Ser. B:Chem.2005,48,233.doi:10.1360/04ye0251
(29)Moan,J.Photochem.Photobiol.1984,39,445.
Photochemical Reaction Kinetics of Duroquinone in a Mixture of Ionic Liquid[BPy][BF4]and Acetonitrile
ZHU Guang-Lai1,*WANG Yu1ZHANG Liang-Wei1LIU Yan-Cheng2WU Guo-Zhong2,*
(1Institute of Atomic and Molecular Physics,Anhui Normal University,Wuhu 241000,Anhui Province,P.R.China;2Shanghai Institute of Applied Physics,Chinese Academy of Sciences,Shanghai 201800,P.R.China)
Photochemical reactions of duroquinone(DQ)in solutions consisting of mixtures of the ionic liquid N-butylpyridinium tetrafluoroborate([BPy][BF4])and acetonitrile(MeCN)were studied using the 355 nm laser flash photolysis technique.Increasing the ratio of[BPy][BF4]had no obvious impact on the absorption peak of the triplet excited state of DQ(3DQ*),which followed monoexponential kinetics in the N2-saturated solution. However,increasing the ratio of[BPy][BF4]did affect the photoinduced electron transfer process from triethylamine to3DQ*in the mixture by decreasing the reaction rate and the quantum yield of the transient radical. The results highlight the ability to tune the efficiency and the rate of the photoinduced electron transfer by changing the proportion of[BPy][BF4]in the mixture.
N-butylpyridinium tetrafluoroborate;Ionic liquid;Duroquinone;Transient absorption spectroscopy;Photoinduced electron transfer
O644
10.3866/PKU.WHXB201501222www.whxb.pku.edu.cn
Received:November 19,2014;Revised:January 22,2015;Published on Web:January 22,2015.
∗Corresponding authors.ZHU Guang-Lai,Email:zhglai@mail.ahnu.edu.cn.WU Guo-Zhong,Email:wuguozhong@sinap.ac.cn.
The project was supported by the National Natural Science Foundation of China(21173002)and Natural Science Foundation ofAnhui Province, China(1308085MB20).
国家自然科学基金(21173002)和安徽省自然科学基金(1308085MB20)资助项目
