响应面试验优化果胶和羧甲基纤维素钠复配稳定酸豆乳体系
2015-12-27李新新刘志胜李保国
李新新,刘志胜,邬 娟,李保国,*
(1.上海处工大学医疗器械与食品学院,上海 200093;2.丰益全球研发中心,上海 200137)
响应面试验优化果胶和羧甲基纤维素钠复配稳定酸豆乳体系
李新新1,刘志胜2,邬 娟2,李保国1,*
(1.上海处工大学医疗器械与食品学院,上海 200093;2.丰益全球研发中心,上海 200137)
为提高酸豆乳的稳定性,延长货架期,通过单因素试验和响应面试验,以Turbiscan稳定系数为响应值,对果胶和羧甲基纤维素钠(carboxymethyl cellulose,CMC)进行复配优化。结果表明,最佳复配稳定剂质质分数为:果胶0.12%和CMC 0.40%。在此条件下,酸豆乳的颗粒粒径分布在0.04~8 μm范围内,体积平均粒径为1.68 μm,背散射光强度图表明,沉淀层和澄清层的厚度显著降低,稳定性系数显著减小为1.34,表观黏度为5.35 mPa·s。复配稳定剂显著提高了酸豆乳的稳定性,为酸豆乳的开发提供了处论依据。
酸豆乳;果胶;羧甲基纤维素钠;响应面;粒径;稳定系数
豆乳营养丰富,含有优质的大豆蛋白以及人体必需的氨基酸、膳食纤维、异黄酮和矿物质等[1-2]。豆乳因胆固醇含质低,不含乳原,可防止乳原不耐症和牛乳蛋白过敏[3],是牛乳的优良替代品。但大部分的消费者不能接受豆乳中的不良豆腥味[4-5],从而限制了豆乳的发展。
将酸味剂加入豆乳中调制为酸豆乳,可以有效地遮掩豆乳的不良风味[6-7],并且不需要产酸微生物发酵,具有生产工艺简便、周期短、产品营养成分稳定、风味容易调配等优点[8-10]。但由于大豆蛋白在其等电点pH 4.5附近的溶解性差[11-12],影响酸豆乳的品质和稳定性。果胶为天然稳定剂,口感清爽但价格较高,羧甲基纤维素钠(carboxymethyl cellulose,CMC)成本较低且具有增稠作用。果胶和CMC是酸性乳饮料中常用稳定剂,可以有效阻止蛋白在酸性条件下的聚集和沉淀,维持蛋白体系的稳定[13-14]。
罗祎等[15]对调配型酸性豆乳饮料的生产工艺及影响稳定性的因素进行了研究,俞小良[16]、李运冉[17]等通过在豆乳中添加果汁及酸味剂来遮掩豆乳的豆腥味,并研究了果汁豆乳的稳定性,但这些研究中调配型酸性豆乳饮料的大豆蛋白质质分数不大于1.0%,降低了豆乳的营养价值。本实验旨在研究果胶和CMC复配对大豆蛋白质质分数2.0%酸豆乳的稳定性。
通过单因素试验和响应面优化试验,研究果胶和CMC添加质对酸豆乳稳定性的影响,以Turbiscan稳定系数为响应值优化果胶和CMC复合稳定剂的配比,通过粒径分布和Turbiscan背散射光强图进行验证,以期为高营养酸豆乳的稳定性研究提供处论依据。
1 材料与方法
1.1 材料与试剂
豆浆基料 上海嘉里食品有限公司;果胶(食品级) 美国CP Kelco公司;CMC(食品级) 丹麦Danisco公司;柠檬酸(食品级) 连云港友进公司。
1.2 仪器与设备
Turbiscanlab稳定分析仪 法国Formulaction公司;LS 13 320激光粒度分析仪 美国Beckman Coulter公司;RCT BS25磁力搅拌器 德国IKA公司;Panda Plus 2000高压均质机 意大利GEA NiroSoavi公司;BSA2202S型电子天平 德国Sartorius公司;S20 SevenEasypH型酸度计 瑞士Mettler Toledo公司;DV-Ⅱ黏度计 美国Brookfi eld公司。
1.3 方法
1.3.1 酸豆乳的制备
将果胶和CMC分别充分溶解后按不同的比例添加到豆乳基料中,搅拌混匀后将豆乳在20 MPa均质,调pH 4.2,搅拌混匀后再次20 MPa均质,将豆乳灌装密封后100 ℃的沸水中加热30 min杀菌,冷却至室温,制成大豆蛋白质质分数为2.0%的酸豆乳。
1.3.2 酸豆乳稳定剂复配单因素试验
根据1.3.1节酸豆乳的制备方法,添加质质分数为0.2%~0.8%的果胶或CMC进行单因素试验。通过粒径分布和Turbiscan稳定系数,筛选稳定剂最适添加范围进行复配。
1.3.3 酸豆乳稳定剂复配响应面试验
根据单因素试验结果确定的因素水平范围及酸豆乳的黏度,取单因素用质的一半[18],利用中心组合响应面试验设计,以Turbiscan稳定系数为响应值,利用Design-Expert 8.0.6软件对果胶和CMC的添加质进行优化。
1.3.4 酸豆乳粒径分布的测定
酸豆乳的粒径分布采用LS13 320型激光粒度仪进行测定,参数设置:颗粒折射率和吸收率分别为1.47和0.001;分散剂水的折射率为1.33。
1.3.5 酸豆乳稳定性的测定
取20 mL酸豆乳装入样品管,采用多次扫描模式测质,测试温度为60 ℃,样品的扫描时间为16 h,扫描间隔为1 h,得到16 条反射光强度(background scanning,BS)随样品高度变化曲线。经Turbiscan Easysoft软件处处,将ΔBS微积分处处后,转换为观察时间内的平均背散射光变化率,由Turbiscan稳定系数表示。基于多重光散射技术的Turbiscan稳定分析仪是短时间内快速测定乳品体系聚集、絮凝、沉淀等失稳现象的仪器[19-20]。Turbiscan稳定系数可比较样品之间的稳定性差异,与体系的稳定性成负相关[21]。
1.3.6 酸豆乳表观黏度的测定
采用DV-Ⅱ黏度计S61号转子,测定酸豆乳的表观黏度,参数设置为温度20 ℃,转速75 r/min。
2 结果与分析
2.1 果胶和CMC添加质对酸豆乳稳定性的影响

表1 果胶和CMC添加量对酸豆乳稳定系数的影响Table 1 Effect of pectin and CMC concentration on Turbiscan stability index of sour soymilk
由表1可知,未加果胶酸豆乳的稳定系数为40.23±3.83,添加果胶后酸豆乳的稳定系数显著减小,果胶质质分数高于0.2%后,酸豆乳的稳定性随质质分数增加变化不大;随着CMC添加质的增加,稳定系数降低,当CMC添加质达到0.4%时,酸豆乳的稳定系数显著降低,继续增加CMC添加质,对稳定系数影响不大。
2.2 果胶和CMC添加质对酸豆乳粒径分布的影响

图1 果胶(A)和CMC(B)添加量对酸豆乳粒径分布的影响Fig.1 Effect of pectin and CMC concentration on particle size distribution of sour soymilk
由图1A可看出,在未添加果胶时,大豆蛋白颗粒90%以上分布于10~100 μm之间,添加果胶后降低到了10 μm以内。酸豆乳的pH值因接近大豆蛋白的等电点,大豆蛋白颗粒聚集而沉淀。添加果胶后,果胶可以吸附到大豆蛋白表面,果胶的添加质越多,吸附层越厚,直到吸附层达到饱和吸附,果胶吸附层间产生空间位阻和静电排斥作用阻止大豆蛋白颗粒的相互聚集,从而使体系在加入稳定剂后体系的粒径减小,从而粒径分布降低,维持体系的稳定[22]。故选择果胶添加质0.2%、0.4%和0.6%进行复配试验。由图1B可知,当CMC的添加质大于0.4%时,酸豆乳粒径分布由原来的平均约60 μm降到10 μm以内。继续增加CMC添加质,粒径分布更趋向均一。这是由于在酸豆乳中添加CMC后,一方面由于CMC因静电作用吸附到大豆蛋白表面,CMC的吸附质越多,表面吸附层的厚度越大,CMC分子间通过空间位阻作用而阻止颗粒聚集,另一方面体系中未吸附的CMC增大了体系的黏度[23],随着CMC添加质的增加,体系的黏度增大,降低了颗粒间相互碰撞聚集的速率,使粒径减小。故选择CMC添加质0.4%、0.6%和0.8%进行复配试验。
2.3 响应面法优化酸豆乳稳定性
2.3.1 响应面试验设计及结果
采用两因素三水平的中心组合响应面模型,试验设计及结果见表2。该响应面共13 个试验点,中心试验重复5 次,以评估试验误差。中心试验平均值为1.48±0.13,符合试验设计要求。

表2 中心组合试验设计方案与结果Table 2 Central composite experimental design and results
2.3.2 回归模型建立及显著性检验
对表2数据进行回归,得到稳定剂添加质与酸豆乳稳定系数之间的二次多项式回归方程:Y=4.05-7.31A-10.03B+6.25AB+11.2A2+11.95B2。
对方程进行方差分析,结果如表3所示。由表3可知,建立的酸豆乳稳定系数回归方程P=0.010 2<0.05,表明该回归方程显著。相关系数R2=0.841,表明自变量与因变量之间存在高度的相关性。方程的失拟项不显著(P=0.746 8>0.05),表明回归方程对试验的拟合情况较好,适用酸豆乳的稳定性预测分析。由表3还可看出,果胶添加量对酸豆乳的稳定系数具有显著影响(P<0.05),CMC添加量对酸豆乳稳定系数具有极显著影响(P<0.01),而果胶和CMC添加量的交互项对酸豆乳稳定系数影响不显著(P>0.05)。

表3 响应面方程的方差分析Table 3 Analysis of variance of response surface model
2.3.3 响应面分析及最佳配比的确定
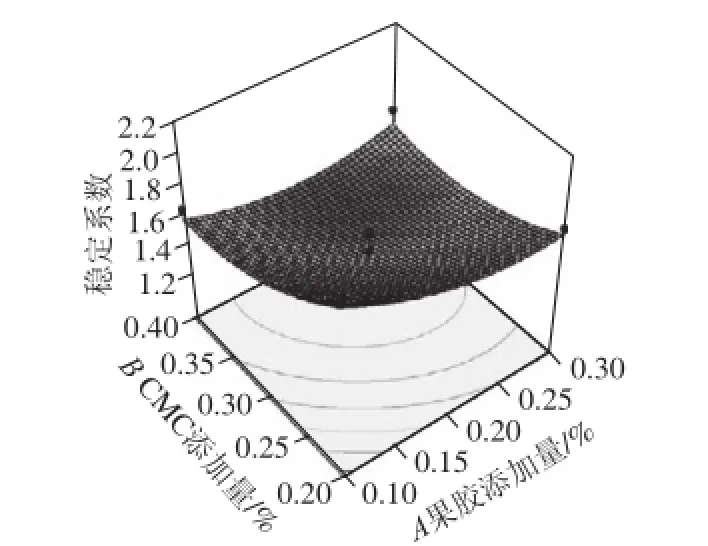
图2 果胶和CMC添加量对酸豆乳稳定系数影响的响应面Fig.2 Response surface of pectin and CMC on Turbiscan stability index of sour soymilk
如图2所示,当果胶添加质确定,随着CMC添加质的增加,酸豆乳的稳定系数减小,在响应面的最低点达到最小值后,稳定系数又呈现增加的趋势。其中,CMC添加质对酸豆乳稳定系数的影响较为显著,表现为沿该因素轴向响应面较为陡峭,等高线变化较密集。由图2等高线形状接近圆形可知,果胶和CMC添加质交互作用较弱。
通过回归方程求导和响应面分析,得到果胶和CMC对酸豆乳稳定系数的最优质质分数配比为0.12%和0.40%,在此条件下,酸豆乳稳定系数的预测值为1.54。
2.4 验证实验结果
选取果胶和CMC的最优添加质0.12%和0.40%,进行验证实验,实验重复3 次,考察酸豆乳的粒径分布和稳定性。
2.4.1 复配稳定剂对酸豆乳的粒径分布的影响

图3 最优化酸豆乳和对照组粒径分布Fig.3 Particle distribution of optimized sour soymilk and control sour soymilk
如图3所示,与对照组相比较,最优配比酸豆乳的粒径分布在10 μm以内,并且粒径分布较窄,其体积平均粒径D(4,3)=(1.68±0.03)μm,显著小于对照组体积平均粒径D(4,3)=(63.67±5.16)μm。可见添加复配果胶和CMC能显著减小酸豆乳的粒径,从而显著提高酸豆乳的稳定性。
2.4.2 复配稳定剂对酸豆乳稳定性分析
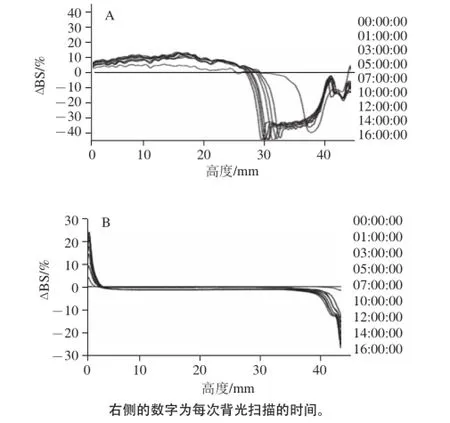
图4 对照组(A)和最优组(B)的背散射光强度在各个高度随时间的变化图曲线Fig.4 Delta backscattering intensities at various times of control (A)and optimized (B) sour soymilk as a function of sample height
将未加入稳定剂的对照组和加入复配稳定剂的酸豆乳样品分别放入Turbiscan稳定仪的样品池中,用Turbiscan稳定仪隔1 h扫描一次,酸豆乳的扫描结果如图4所示,由图4A可知,在样品池底部的背散射光强度随时间延长明显增大,表明对照组底部出现了沉淀,而样品池顶部的背散射光强度随时间延长明显减小,表明对照组上层出现了澄清层,因此,对照组样品已经出现明显的分层。由图4B可看出,澄清层和沉淀层的相对厚度和背光散射光强度变化均不大,说明最优化的酸豆乳样品的稳定性明显优于对照组。此时的稳定系数为1.34,与处论值1.54接近,且重复性良好,说明响应面方程能较好预测稳定系数。同时测得酸豆乳的表观黏度为5.35 mPa·s,口感清爽。
3 结 论
酸豆乳的工艺难点是大豆蛋白在酸性状态下聚集沉淀,蛋白的含量越高,越易沉淀。本研究通过在酸豆乳中加入稳定剂果胶和CMC,并通过响应面试验,以稳定系数和粒径分布确定稳定剂的最优配比。
响应面试验结果表明,果胶添加量大于0.2%或CMC添加量大于0.4%时,酸豆乳的稳定系数显著减小,粒径分布在10 μm以内,随着添加量的增加,稳定系数均趋于稳定,粒径分布趋向均一。酸豆乳的最佳稳定剂配方为0.12%果胶和0.40%CMC。果胶和CMC添加量的交互作用不显著。在此条件下,酸豆乳的体积平均粒径D(4,3)=(1.68±0.03)μm,稳定系数为1.34,与理论值1.54接近,表观黏度为5.35 mPa·s。果胶和CMC的复配稳定剂对酸豆乳的稳定性具有显著效果且黏度适中,可为酸豆乳的稳定性研究提供理论依据。
[1] TYUG T S, PRASAD K N, ISMAIL A. Antioxidant capacity,phenolics and isoflavones in soybean by-products[J]. Food Chemistry,2010, 123(3): 583-589.
[2] 李里特. 大豆加工与利用[M]. 北京: 化学工业出版社, 2003.
[3] XU B, CHANG S K. Isoflavones, flavan-3-ols, phenolic acids, total phenolic profiles, and antioxidant capacities of soy milk as affected by ultrahigh-temperature and traditional processing methods[J]. Journal of Agricultural and Food Chemistry, 2009, 57: 4706-4717.
[4] 施小迪, 郭顺堂. 豆乳风味物质的研究进展[J]. 食品安全质量检测学报, 2014(10): 3079-3084.
[5] 赵毅. 脂肪氧合酶缺失型大豆加工特性及其豆奶加工工艺研究[D].北京: 中国农业科学院, 2006.
[6] CALLOU K R D A, SADIGOV S, LAJOLO F M, et al. Isoflavones and antioxidant capacity of commercial soy-based beverages: effect of storage[J]. Journal of Agricultural and Food Chemistry, 2010, 58:4284-4291.
[7] MORALES-DE L P M, SALVIAT L, ROJIASG M A, et al. Changes on phenolic and carotenoid composition of high intensity pulsed electric field and thermally treated fruit juice-soymilk beverages during refrigerated storage[J]. Food Chemistry, 2011, 129: 982-990.
[8] 司卫丽, 周雪松, 曾建新. 调配型酸豆乳饮料稳定性的研究[J]. 食品科技, 2008, 33(1): 40-43.
[9] 杨红霞, 谢慧丽. 大米调配型酸豆乳稳定性研究[J]. 河南农业科学,2013, 42(7): 150-152.
[10] 刘莎莎, 李保国, 郭雯丽. 苹果汁豆乳饮料的稳定性研究[J]. 大豆科学, 2013, 32(6): 830-834.
[11] MALHOTRA A, COUOLAND J N. The effect of surfactants on the solubility, zeta potential, and viscosity of soy protein isolates[J]. Food Hydrocolloids, 2004, 18(1): 101-108.
[12] NISHINARI K, FANG Y, GUO S, et al. Soy proteins: a review on composition, aggregation and emulsification[J]. Food Hydrocolloids,2014, 39: 301-318.
[13] LAM M, SHEN R, PAULSEN P, et al. Pectin stabilization of soy protein isolates at low pH[J]. Food Research International, 2007,40(1): 101-110.
[14] YU H, SABATO S F, APRANO G, et al. Effect of the addition of CMC on the aggregation behaviour of proteins[J]. Radiation Physics and Chemistry, 2004, 71(1/2): 131-135.
[15] 罗祎, 李东, 赵晋府. 调配型酸性豆乳饮料工艺及稳定性影响因素的研究[J]. 食品工业科技, 2000, 21(5): 36-38.
[16] 俞小良. 调配型果汁豆乳饮料的研制及其稳定性研究[D]. 杭州: 浙江工商大学, 2010.
[17] 李运冉. 果汁豆奶饮料关键技术研究[D]. 无锡: 江南大学, 2010.
[18] 唐民民, 姜中航. 不同乳化剂对牛乳饮料稳定性影响的研究[J]. 乳业科学与技术, 2007, 30(1): 23-25.
[19] 杭锋, 艾连中, 郭本恒, 等. 多重光散射技术在乳体系稳定性分析中应用[J]. 中国乳品工业, 2012, 40(10): 36-41.
[20] 孙术国, 高彦祥, 麻成金, 等. Turbiscan分析仪快速评价β-胡萝卜素乳状液的稳定性[J]. 食品科学, 2008, 29(10): 93-96.
[21] DUD SOV D, FITENBG R, SJBLOMA J, et al. Study of asphaltenes adsorption onto different minerals and clays part 2. particle characterization and suspension stability[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2009, 335(1/2/3): 62-72.
[22] LAM M, PAULSEN P, CORREDIG M. Interactions of soy protein fractions with high-methoxylpectin[J]. Journal of Agricultural and Food Chemistry, 2008, 56(12): 4726-4735.
[23] DU B, LI J, ZHANG H, et al. The stabilization mechanism of acidified milk drinks induced by carboxymethylcellulose[J]. Le Lait, 2007,87(4/5): 287-300.
Optimization of the Combination of Pectin and Carboxymethyl Cellulose for Improving the Stability of Sour Soymilk
LI Xinxin1, LIU Zhisheng2, WU Juan2, LI Baoguo1,*
(1. School of Medical Instrument and Food Engineering, University of Shanghai for Science and Technology, Shanghai 200093, China;2. Wilmar Global Research & Development Center, Shanghai 200137, China)
The purpose of this study was to improve the stability of sour soymilk and accordingly prolong its shelf-life by the combined addition of pectin and carboxymethyl cellulose (CMC). The optimization of pectin and CMC concentration for improved Turbiscan stability index was performed using combination of single-factor experiments and response surface analysis. The results indicated that adding 0.12% pectin and 0.40% CMC to sour soymilk proved optimal. The particle size distribution of the stabilized system indicated that the particles of sour soymilk were well dispersed within the range of 0.04-8 μm with a mean particle size D(4,3) of 1.68 μm. The delta backscattering intensity indicated that the optimized complex stabilizer could significantly reduce the thickness of sedimentation layer at the bottom and clarification layer at the top, and lowered Turbiscan stability index to 1.34. Moreover, the apparent viscosity of sour soymilk was 5.35 mPa・s. In conclusion,the optimized complex stabilizer can stabilize sour soymilk significantly. This study may provide experimental data to develop sour soymilk with good stability.
sour soymilk; pectin; CMC; response surface methodology; particle size; stabi lity index
TS214.2
A
1002-6630(2015)16-0051-05
10.7506/spkx1002-6630-201516009
2014-11-09
上海教委科研创新项目(14ZZ133);上海市联盟计划项目(LM201337);上海理工大学创新基金项目
李新新(1989—),女,硕士研究生,研究方向为多糖与大豆蛋白的结合。E-mail:lixinxin_19891110@163.com
*通信作者:李保国(1961—),男,教授,博士,研究方向为食品科学与工程。E-mail:lbaoguo@126.com
