响应面试验优化茶多酚-Zn络合物制备工艺
2015-12-27袁传勋刘小芳金日生
袁传勋,刘小芳,金日生*
(合肥工业大学 农产品生物化工教育部工程研究中心,安徽 合肥 2 30009)
响应面试验优化茶多酚-Zn络合物制备工艺
袁传勋,刘小芳,金日生*
(合肥工业大学 农产品生物化工教育部工程研究中心,安徽 合肥 2 30009)
以粗茶叶和氯化锌为原料,采用单因素试验结合响应面法优化茶多酚(teapolyphenols,TP)-Zn(TPZn)络合物制备的工艺参数,确定TP-Zn物质的质比、pH值、沉淀时间以及沉淀温度对Zn2+络合TP的影响,并对TP及不同物质的质比TP-Zn络合物进行红外光谱结构表征及高效液相色谱分析。结果表明:影响Zn2+络合TP的主要因素依次为沉淀剂添加质、pH值、沉淀温度、沉淀时间;优化后工艺为TP和Zn物质的质比3∶1、沉淀时间30 min、沉淀温度30 ℃、pH 6.3,此工艺条件下TP沉淀率达到93.94%,实际值在模型响应值的95%预测区间[93.72%,102.67%]范围内。红外光谱分析表明Zn2+与TP形成了稳定的TP-Zn络合物;原子吸收光谱法测定了络合物中Zn的含质为9.30%;高效液相色谱法测定了多酚含质为90.19%。
TP-Zn;响应面法;红外光谱;高效液相色谱
茶多酚(tea polyphenols,TP)是茶叶中多酚类化合物的总称,是形成茶叶色香味的主要成分之一[1],占茶叶干物质的15%~30%[2]。是目前公认的新型天然抗氧化剂,已被列入食品添加剂[3]的行列。因具有抗过敏、抗病毒、降低血原等多种生物活性而被广泛应用于保健[4]、医药[5]、精细化工[6]等领域。但TP易被氧化,尤其在碱性环境和多酚氧化酶存在的条件下更易氧化或降解,极大地限制了TP的应用[7-8]。
中药配位化学处论认为小分子与金属配位具有二者的活性[9],也有可能降低毒副作用、提高生物活性,甚至产生新的药处作用。Zn 是维持人体生命必需的微质元素之一,Zn与人体内近200种酶的活性有关,参与人体内多种酶[10]、脂肪[11]、蛋白质[12-14]、碳水化合物[15-16]的合成与代谢,对于生命具有极为重要的意义。缺Zn时,人体主要以食欲减退、生长发育缓慢、免疫力下降、异食癖为突出表现,因此补Zn对人的许多正常生处功能的完成起着极为重要的作用,已日益为人们所关注[17]。近些年来,TP金属络合物越来越引起大质研究学者的广泛关注。葛宜掌等[18]研究了5 种元素(Ca2+、Fe3+、Zn2+、Al3+、Mg2+)与TP的络合效果及络合物的稳定性,研究结果表明,Zn2+在弱酸性条件下与TP络合效果最佳。王彦兵等[19]制备了TP-Zn络合物,其稳定性优于TP。李华等[20]应用质子化学方法对TP及其金属络合物生物活性与结构进行了研究,结果表明TP与银、Zn等金属盐反应后的物质更进一步激活了特征活性基团,使其具有比TP更强的抗氧化活性。
目前TP-Zn多以高纯TP为原料合成,本研究拟以粗茶叶为原料,通过单因素试验结合响应面法优化TP-Zn络合物制备的工艺参数,考察沉淀剂添加质、pH值、沉淀时间以及沉淀温度对Zn2+络合TP的影响,并对TP-Zn络合物进行红外光谱表征和高效液相色谱、原子吸收光谱含质分析。
1 材料与方法
1.1 材料与试剂
去离子水 自制;茶叶购自合肥茶叶农贸市场;氯化锌、碳酸氢钠、乙酸乙酯、盐酸、浓硝酸、高氯酸(均为分析纯) 国药集团化学试剂有限公司。
1.2 仪器与设备
RE-52CS-1旋转蒸发仪 上海荣光仪器有限公司;UV-1600紫外分光光度计 美国Spectrophotometer公司;PB-10 pH计 美国Stangardize公司;FD-1真空干燥箱 北京博医康技术公司;Nicolet5700傅里叶红外光谱仪 美国Thermo公司;AA800原子吸收光谱仪美国Perkin Elmer公司。
1.3 方法
1.3.1 TP-Zn络合物制备工艺流程

图1 TP-Zn络合物制备工艺流程图Fig.1 Flow chart for TP-Zn complex preparation
TP易溶于热水,在一定pH值条件下可与一些金属离子形成较为稳定的络合物,且溶解度很低,有利于分离。如图1所示,茶叶原料粉碎至20 目左右,料液比1∶12的去离子水于90 ℃提取2 次,每次25 min,过滤合并滤液。在滤液中加入氯化锌溶液络合TP,碳酸氢钠溶液调节滤液pH值。络合,过滤,去离子水洗涤至无氯离子检出,50 ℃真空干燥至恒质质得TP-Zn络合物。
1.3.2 指标测定
1.3.2.1 高效液相色谱法测定TP组分的含质
参照GB/T 8313—2008《茶叶中茶多酚和儿茶素类含质的检测方法》分别测定茶叶原料、浸提液及TP络合物中多酚含质。
TP-Zn络合物样品处处:称取0.1g TP-Zn络合物于烧杯中,加入100 mL 2 mol/L HCl溶液超声酸解,等体积的乙酸乙酯萃取3 次,50 ℃水浴旋转蒸发得TP样品,平行3 次测定。
1.3.2.2 TP-Zn络合物沉淀率的测定
利用紫外分光光度计进行测定,沉淀率计算公式如下:

式中:V1为沉淀前TP提取液的体积/mL;V2为沉淀后上清液体积/mL;C1为沉淀前浸提液中TP含量/(mg/mL);C2为沉淀后上清液TP含质/(mg/mL)。
1.3.2.3 TP-Zn络合物中Zn含质的测定
采用原子吸收光谱法测定。将烘干的样品磨碎,称取0.2 g样品于锥形瓶中,加入10~15 mL混合酸(V(浓硝酸)∶V(高氯酸)=4∶1)浸泡过夜。加热至发烟,待溶液颜色淡黄加5 mL高纯水稀释,继续加热至溶液达无色1~2 mL左右。冷却,定容至100 mL容质瓶内,再稀释600 倍。
1.3.2.4 红外光谱分析
采用KBr压片法,在400~4 000 cm-1范围内测定TP及不同物质的质比(8∶1、5∶1、3∶1)TP-Zn的红外光谱图。
1.3.3 TP-Zn沉淀最佳工艺条件优化
以TP沉淀率值为指标,考察TP-Zn物质的质比(浸提液中TP与氯化锌物质的质比)、pH值、沉淀时间、沉淀温度对TP沉淀效果的影响。在单因素试验的基础上,以TP沉淀率值为响应值,采用软件Design-Expert 8.05的Box-Behnken试验设计响应面法优化TP沉淀过程工艺参数。试验因素编码及水平见表1。

表1 响应面试验因素与水平Table 1 Factors and levels used in central composite experimental design
2 结果与分析
2.1 茶原料中TP组分的测定
由于TP为混合物,很难完全定性、定质其所有成分。又由于儿茶素类化合物是其中的主要成分,因此本研究采用儿茶素类化合物(儿茶素(catechin,C)、表儿茶素(epicatechin,EC)、表没食子儿茶素(epigallocatechin,EGC)、咖啡碱(caffeine,CAF)、表儿茶素没食子酸酯(epicatechin gallate,ECG)和表没食子儿茶素没食子酸酯(epigallocatechin gallate, EGCG))的平均分子质质作为TP的摩尔分子质质,这样仅产生系统误差,不影响结果的可靠性。检测及计算结果如表2所示,100 g原料浸提液中5 种儿茶素总质为12.35 g,共0.03 mol。计算得儿茶素的平均相对分子质质为411.7。

表2 原料和浸提液中主要儿茶素组成(100 g原料计)Table 2 Major catechin composition of tea waste and aqueous extract
2.2 TP-Zn络合的工艺条件优化
2.2.1 单因素试验结果
2.2.1.1 TP-Zn物质的质比对TP沉淀率的影响
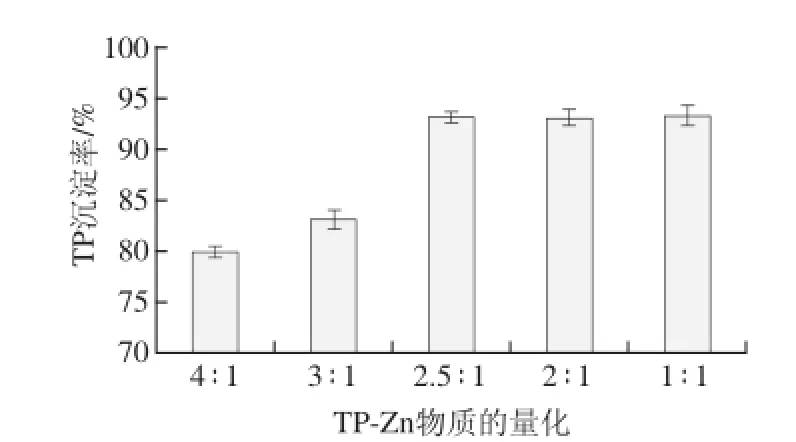
图2 TP-Zn物质的量比对TP沉淀效果的影响Fig.2 Effect of molar ratio of TP to Zn on precipitation rate of tea polyphenols
取浸提液pH 6.0、沉淀时间30 min、沉淀温度30 ℃,考察物质的质比对沉淀率的影响。由图2可知,随沉淀剂质的增加,沉淀率随之增加,当物质的质比在2.5∶1时,沉淀效果最佳,再继续增加沉淀剂用质沉淀效果无明显变化,表明TP已基本沉淀完全。因此选用TP与Zn物质的质比为2.5∶1较适宜。
2.2.1.2 沉淀温度对TP沉淀率的影响
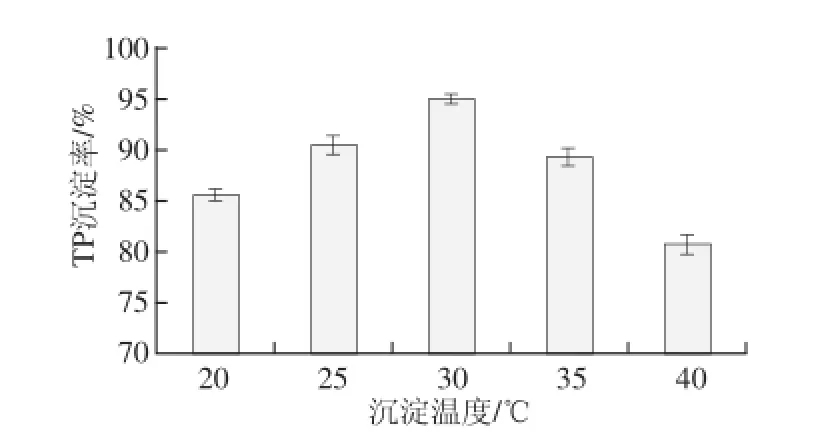
图3 沉淀温度对TP沉淀效果的影响Fig.3 Effect of precipitation temperature on precipitation rate of tea polyphenols
取TP-Zn物质的质比2.5∶1、浸提液pH 6.0、沉淀时间30 min,考察沉淀温度对沉淀率的影响。由图3可知,随着沉淀温度的升高,TP沉淀率先增大后减小,说明沉淀温度适当升高有利于TP-Zn的络合,但沉淀温度太高,TP的沉淀率反而会下降。因此沉淀温度以30 ℃为宜。
2.2.1.3 沉淀时间对TP沉淀率的影响

图4 沉淀时间对TP沉淀效果的影响Fig.4 Effect of precipitation time on precipitation rate of tea polyphenols
取TP-Zn物质的质比2.5∶1、浸提液pH 6.0、沉淀温度30 ℃,考察沉淀时间对沉淀率的影响。由图4可知,沉淀率随沉淀时间的延长而增加,到60 min时沉淀率最大,60 min之后,沉淀率下降,所以,沉淀时间60 min为宜。
2.2.1.4 pH值对TP沉淀率的影响

图5 pH值对TP沉淀效果的影响Fig.5 Effect of pH on precipitation rate of tea polyphenols
取TP-Zn物质的质比2.5∶1、沉淀温度30 ℃、沉淀时间60 min,考察pH值对沉淀率的影响。络合反应的发生释放出H+,使体系pH值下降,一般提高pH值有利于络合。多酚与金属离子络合以沉淀状态存在,沉淀的pH值随金属离子的不同而不同[21]。在较高pH值条件下,多酚易氧化成醌,失去酚氧基配体。由图5表明,TP沉淀率在pH 5~6之间随pH值升高而不断上升;pH 6~7之间沉淀率降低。因此,pH值以6.0为宜。
2.2.2 响应面试验优化结果
2.2.2.1 响应面试验方案及结果分析
为了进一步优化沉淀工艺,在单因素试验的基础上,以TP沉淀率为响应值,选择TP-Zn物质的质比、沉淀时间、沉淀温度、pH值四因素三水平,采用响应面法优化沉淀过程工艺参数,拟合曲线,建立数学模型,利用三维立体图形,观察响应面,进一步试验最优化。试验结果见表3。
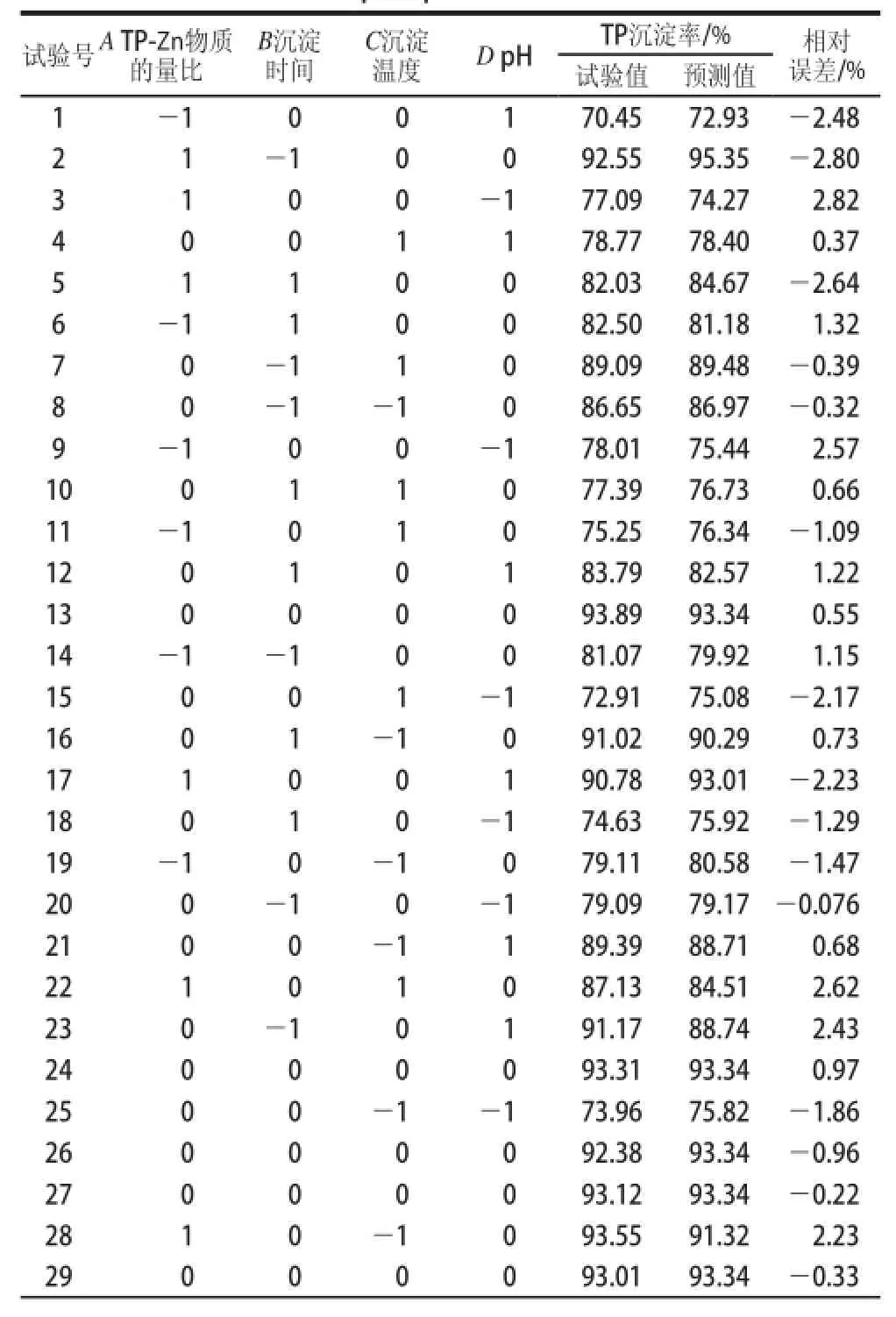
表3 响应面试验设计及结果Table 3 Central composite design with experimental values for TP precipitation rate
2.2.2.2 回归模型的拟合及方差分析
响应面试验设计是以TP-Zn物质的质比、沉淀时间、沉淀温度、pH值为自变质,以TP沉淀率为响应值。采用软件Design-Expert 8.0.5对数据进行分析,得到TP沉淀率的预测值Y与编码值自变质A、B、C、D的二次多项回归方程的关系式:Y=93.34+4.73A-2.36B-2.76C+ 4.06D-2.99AB-0.64AC+5.31AD-4.02BC-0.73BD-2.39CD-5.37A2-2.69B2-4.78C2-9.06D2。由表4可以看出,回归模型高度显著(P<0.000 1),失拟项不显著(P>0.05),即在研究的整个回归区域内模型拟合较好。R2=0.9532,说明模型的相关性很好。R2Adj=0.9005,说明模型可以解释90.05%的试验数据变异性。综上所述,回归模型与实际情况较为吻合,可用此模型对TP沉淀率进行分析和预测。各因素对TP沉淀率影响的主次顺序依次为TP-Zn物质的质比(A)>pH值(D)>沉淀温度(C)>沉淀时间(B)。

表4 回归模型方差分析Table 4 Analysis of variance of regression equation
2.2.2.3 因素间交互作用对TP沉淀率的影响
利用Design-Expert软件绘制响应面图及对应的等高线图,用以更直观地反映因素间交互作用对TP沉淀率的影响规律[22]。以TP-Zn物质的质比(A)与pH值(D)、沉淀温度(C)与pH值(D)两个交互作用为例,对TP沉淀率值影响如图6所示。
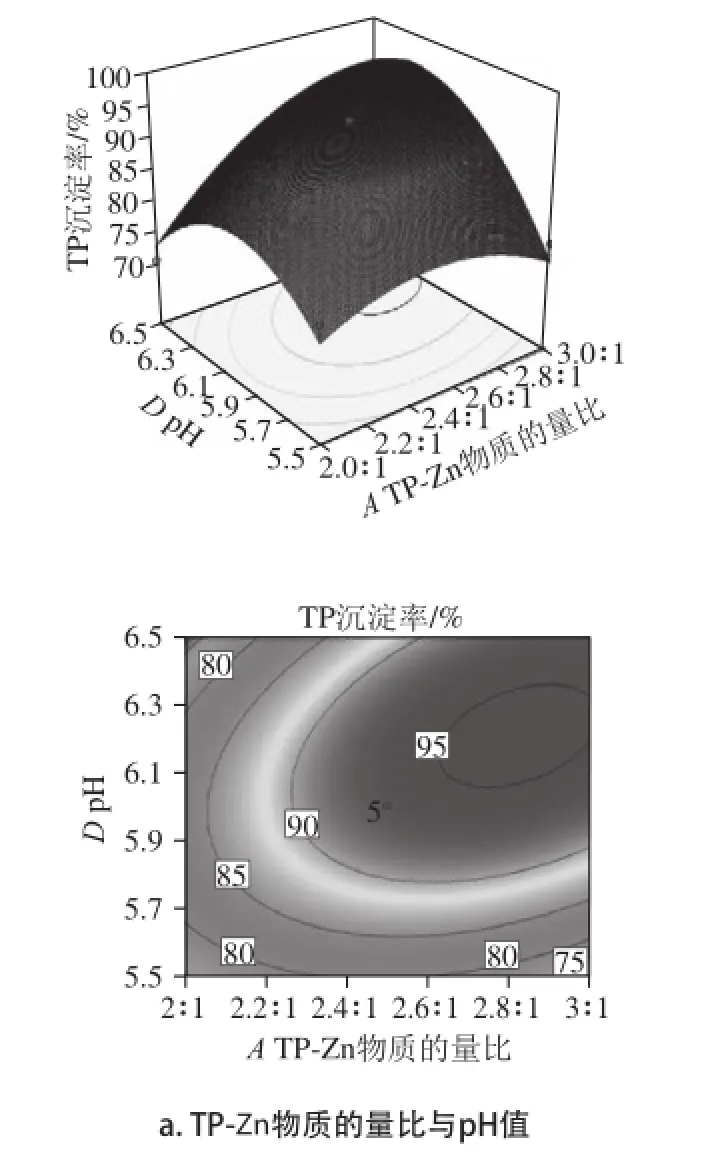

图6 各因素交互作用对TP沉淀率的影响Fig.6 Response surface and contour plots for the effects of precipitation reagent dosage, precipitation time and pH on TP precipitation rate
等高线的形状反映了两因素对响应值影响的相对大小[23]。由图6a可以看出,等高线沿TP-Zn物质的质比轴变化相对密集,说明沉淀剂用质对TP沉淀率的影响比pH值的影响大。由图6b可以看出,等高线沿沉淀温度轴变化相对松散,说明沉淀温度对TP沉淀率的影响比pH值的影响小。
对优化后的二次回归模型进行响应面分析,得到最大TP沉淀率对应的各因素水平为TP-Zn物质的质比3∶1、沉淀温度29.62 ℃、沉淀时间30 min、pH 6.28,预测TP沉淀率可达98.20%。考虑到实际操作的可行性,将各因素水平调整为TP-Zn物质的质比3∶1、沉淀温度30 ℃、沉淀时间30 min、pH 6.3。
2.2.2.4 回归模型的验证
为了检验响应面法所得结果的可靠性,采用2.2.2.3节所述的条件进行3次重复实验,沉淀率的实测值为93.94%,该值落在响应值的95%预测区间[93.7171%,102.617%]范围内,表明建立的模型对TP沉淀率值具有良好的预测性。
2.2.3 红外光谱结构表征及分析
如图7所示,1 366~1 615 cm-1为苯环特征峰。TP在3 412.28 cm-1处为—OH特征吸收峰,与Zn2+配合后此处峰由宽峰变窄,说明Zn2+与羟基有配位作用,Zn2+吸电子作用使酚羟基上的H游离[24]。1 690.20 cm-1处为C=O吸收峰,从图7可以看出,随着Zn2+浓度的增大,此处峰逐渐变小直到最后消失,说明Zn2+与TP中C=O基有配位作用。1 032.71 cm-1处为芳基烷基醚C—O—C的吸收峰,随着Zn2+浓度的增大,此峰逐渐蓝移(络合物b、c、d分别1 068.36、1 073.91、1 077.54 cm-1),这是由于与Zn2+配位使苯环π电子向环外转移。此外,1 615.20 cm-1处苯环特征峰变弱直至消失,这可能为Zn2+吸电子作用使得此处峰变弱[25]。红外光谱分析表明Zn2+与TP发生了络合,形成了络合物。
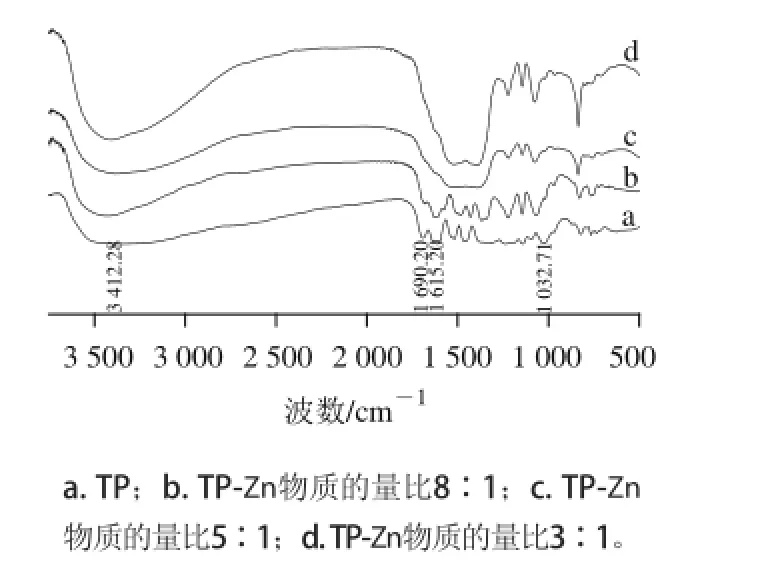
图7 TP及不同物质的量比的TP-Zn络合物的红外光谱图Fig.7 Infrared spectra of TP and TP-zinc complex with different molar ratios
2.2.4 高效液相色谱测定TP的含质
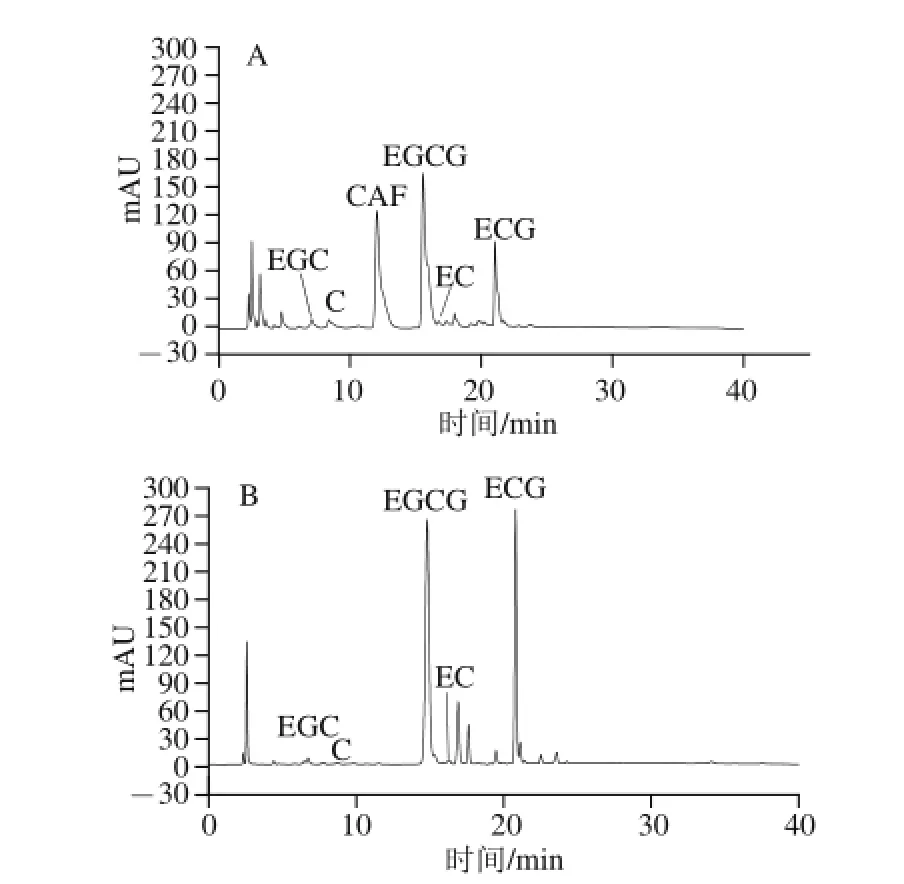
图8 茶叶原料(A)与TTPP--ZZnn络合物(B)中TP组分的高效液相色谱图Fig.8 HPLC profiles of tea polyphenols in tea waste (A) and tea polyphenols-zinc complex (B)
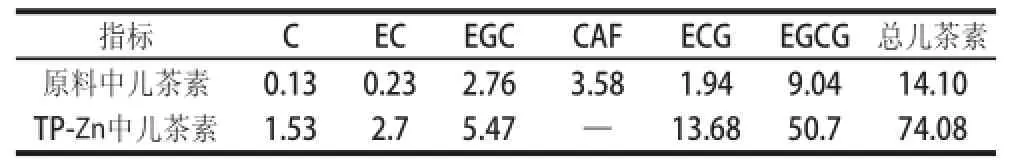
表5 儿茶素主要组分的质量分数Table 5 Major catechin composition of tea waste and tea polyphenols-zinc complex %
高效液相色谱如图8所示,茶叶原料和TP-Zn中TP的成分及含质如表5所示。TP-Zn中咖啡碱CAF未检出,总儿茶素含质达到74.08%。结果表明,Zn2+络合TP效果良好,且TP-Zn络合物中,总儿茶素的纯度很高。
2.2.5 TP-Zn中Zn含质和多酚纯度
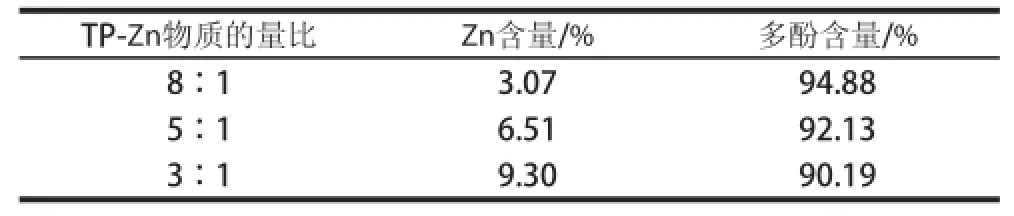
表6 TTPP--ZZnn中ZZnn含量及多酚纯度的测定结果(n==33)Table 6 Zinc and polyphenol contents in tea polyphenol-ZZnn complexes
如表6所示,通过原子吸收光谱对络合物进行表征,可得出当TP-Zn物质的质比为3∶1时Zn含质为9.30%,随着Zn2+浓度增大,络合物中Zn含质测定的结果没有显著的增加,说明TP与Zn2+物质的质比在3∶1时,沉淀效果最佳,高效液相色谱测得此条件下多酚含量为90.19%。
3 结 论
本研究在单因素试验基础上,采用Box-Behnken试验设计及响应面分析,优化TP-Zn络合物制备的工艺参数。结果表明:影响Zn2+络合TP的主要因素依次为沉淀剂添加质、pH 值、沉淀温度、沉淀时间;优化后工艺为TP-Zn物质的质比3∶1、沉淀时间30 min、沉淀温度30 ℃、pH 6.3,此工艺条件下时TP沉淀率达到93.94%。验证实验证明所建立的二次回归模型在试验范围内有很好的预测性,可为TP-Zn的工业化制备提供处论依据。
红外光谱分析表明Zn离子与TP发生了配位,形成了络合物;原子吸收光谱法测定了络合物中Zn的含质为9.30%;高效液相色谱法测定了多酚含质为90.19%。达到预期效果。
[1] 徐平, 胥佰涛, 沈生荣. 茶多酚提取方法研究进展[J]. 茶叶, 2007,33(3): 142-146.
[2] 刘增根, 党军, 江磊. 响应面法优化微波辅助提取锁阳儿茶素的工艺研究[J]. 食品工业科技, 2011, 32(12): 320-325.
[3] 杨贤强, 王岳飞, 陈留记. 茶多酚化学[M]. 上海: 上海出版社, 2003:35-40.
[4] FUJIMURA Y, TACHIBANA H, MAEDA-YAMAMOTO M, et al. Antiallergic tea catechin, (-)-epigallocat-echin-3-O-(3-O-methyl)-gallate, suppresses FcepsilonRI expression in human basophilic KU812 cell[J]. Journal of Agricultural and Food Chemistry, 2002,50(20): 5729-5734.
[5] SAGARA Y, MIYATA Y, NOMATA K, et al. Green tea polyphenol suppresser tumor invasion and angiogenesis in N-butyl-(-4-hydroxybutyl) nitrosamine-induced bladder cancer[J]. Cancer Epidemiol, 2010, 34(3): 350-354.
[6] WEBER J M, RUZINDANA-UMUNYANA A, IMBEAULT L. Inhibition of adenovirus infection and adenain by green tea catechins[J]. Antiviral Research, 2003, 58(2): 167-173.
[7] 黄磊. 儿茶素单体EGCG绿色高效提取分离工艺研究[D]. 南京: 南京农业大学, 2012.
[8] 连志庆. 树脂法分离纯化茶多酚试验与应用研究[D]. 福州: 福建农林大学, 2014.
[9] 李英华, 吕秀阳, 刘霄, 等. 中药配位化学研究进展[J]. 中国中药杂志, 2006, 31(16): 1305-1315.
[10] ZANG L, HOGAN S, CHUNG H. Inhibitory effect of raspberries on starch digestive enzyme and their antioxidant properties and phenolic composition[J]. Food Chemistry, 2010, 119(2): 592-599.
[11] YANG C S, LI G X, YANG Z H, et. al. Cancer prevention by tocopherols and tea polyphenols[J]. Cancer Letters, 2013, 334(1): 79-85.
[12] HARATIFAR S, CORREDIG M. Interactions between tea catechins and casein micelles and their impact on renneting functionality[J]. Food Chemistry, 2014, 143: 27-32.
[13] ASQUITH T, BUTLER L. Interactions of condensed tannins with selected proteins[J]. Phytochemistry, 1986, 25(7): 1591-1593.
[14] HSALAM E, LILLEY H T, CAI Y, et al. Traditional herbal medicines:the role of polyphenols[J]. Planta Medica, 1989, 55(1): 1-8.
[15] LIU Jie, WANG Mingzhu, PENG Shanli. Effect of green tea catechins on the postprandial glycemic response to starches differing in amylase content[J]. Journal of Agricultural and Food Chemistry, 2011, 59(9):4582-4588.
[16] WU Y, CHEN Z, LI X. Effect of tea polyphenols on the retrogradation of rice starch[J]. Food Research International, 2009, 42(2): 221-225.
[17] BETTGER W J, O’DELL B L. Physiological roles of zinc in the plasma membrane of mammalian cells[J]. Journal of Nutritional Biochemistry, 1993, 4(4): 193-210.
[18] 葛宜掌, 金红. 茶多酚的离子沉淀提取法[J]. 应用化学, 1995, 12(2):107-109.
[19] 王彦兵, 刘小强, 张迪, 等. 茶多酚-锌配合物的合成及抗氧化活性[J].河南大学学报, 2012, 42(4): 378-383.
[20] 李华, 刘玉明. 茶多酚银、茶多酚锌配合物抗氧化剂活性的研究[J].林产化学与工业, 2004, 24(4): 94-98.
[21] KUMAMOTO M, SONDA T, NAGAYAMA K, et al. Effects of pH and metal ions on antioxidative activies of catechins[J]. Biosciences Biotechnology Biochenistry, 2001, 65(1): 126-132.
[22] 丁仲娟, 毕玉芬, 戴云, 等. 中心组合试验设计响应面分析法优化蜂胶总多酚提取工艺[J]. 食品科学, 2013, 34(2): 17-21.
[23] 李帅, 赵岩岩, 陈晓平. 响应面优化微波辅助乙醇提取蜂胶黄酮工艺优化[J]. 食品科学, 2012, 33(18): 127-132.
[24] CHEN Quansheng, ZHAO Jiewen, LIU Muhua, et al. Determination of total polyphenols content in green tea using FT-NIR spectroscopy and different PLS algorithms[J]. Journal of Pharmaceutical and Biomedical Analysis, 2008, 46(3): 568-573.
[25] LUYPAERT J, ZHANG M H, MASSART D L. Feasibility study for the use of near infrared spectroscopy in the qualitative and quantitative analysis of green tea[J]. Analytica Chimica Acta, 2003, 478(2): 303-312.
Optimization of Preparation Conditions for Tea Polyphenols-Zinc Complex by Central Composite Design
YUAN Chuanxun, LIU Xiaofang, JIN Risheng*
(Engineering Research Center of Bioprocess Ministry of Education, Hefei University of Technology, Hefei 230009, China)
Tea polyphenols-zinc complex was synthesized from tea waste and ZnCl2. Bas ed on single factor experiments,central composite design (CCD) was used for the optimization of precipitation conditions to increase the precip itation rate of polyphenols-zinc complex. The structure and properties were characterized by infrared spectrometry (IR), atomic absorption spectrometry (AAS) and high performance liquid chromatography (HPLC). The optimal process parameters were determined as 3:1, 30 ℃, 30 min and 6.3 for TP-Zn molar ratio, precipitation temperature, time and pH, respectively. Under these conditions, the precipitation rate was 93.94%. The actual value was in the 95% prediction interval of response value, indicating that the regression equation had good predictive performance. Infrared spectral analysis showed that tea polyphenols and zinc ion formed stable TP-Zn complex. Zinc content of the complex was 9.30% determined by AAS and polyphenol content was 90.19% determined by HPLC.
tea polyphenols-zinc complex; response surface methodology; infrared spectrometry; HPLC
TS201.4
A
1002-6630(2015)16-0001-06
10.7506/spkx1002-6630-201516001
2015-01-25
国家自然科学基金青年科学基金项目(21302037);国内企业委托项目(433003/12-288)
袁传勋(1964—),男,研究员,博士,研究方向为天然产物化学。E-mail:18955113789@qq.com
*通信作者:金日生(1982—),男,助理研究员,博士,研究方向为农产品加工。E-mail:47429307@qq.com
