胃肝样腺癌1例报道
2015-12-25魁国菊杨立民孟加榕中国人民解放军第一七五医院病理科厦门大学附属东南医院病理科漳州363000通讯作者mailmengjiarongsinacom
魁国菊,杨立民,孟加榕(中国人民解放军第一七五医院病理科,厦门大学附属东南医院病理科,漳州 363000;通讯作者,E-mail:mengjiarong@sina.com)
胃肝样腺癌(hepatoid adenocarcinoma of stomach,HAS)是一种少见的原发于胃的特殊类型腺癌,其病理组织形态具有腺癌和肝细胞癌样分化特征,常伴血清甲胎蛋白(AFP)升高。临床上容易误诊、漏诊。现报道我院胃肝样腺癌1例,以提高对本病的认识,提高诊断水平。
1 病例资料
患者,男性,43岁,因“反复上腹部隐痛伴解黑便半月余”入院。半月前开始无明显诱因出现上腹部间歇性隐痛,伴解黑便,无畏寒、发热及呕血。查体未见明显异常。实验室检查:潜血弱阳性,肿瘤标记物甲胎蛋白(AFP-3)153.31 ng/ml(参考范围:0-8.78 ng/ml)。全腹部螺旋CT(SCT)平扫+增强检查示胃体大弯侧胃壁增厚,并见软组织结节突向腔内,胃周见一大小约16 mm×10 mm肿大淋巴结,符合胃体癌,并胃周肿大淋巴结。行电子胃镜检查示:胃体大弯近后壁可见约2.0 cm×2.5 cm大小不规则隆起型肿物,表面充血糜烂,周围黏膜充血水肿,考虑血肿?肿瘤?并予以活检,活检结果为胃体腺癌。拟行胃癌根治术,术中探查见胃体小弯侧上部可触及一质硬肿块,大小约2.5 cm×2.0 cm×1.0 cm,未侵出浆膜层;肝总动脉旁(No.8 组)、脾动脉旁(No.11组)淋巴结肿大,余胃周淋巴结未触及明显肿大,遂行根治性全胃切除术。术后切除病理示:肿物位于胃体,由两种肿瘤成分构成,相互有移行(见图1),浸润至胃壁黏膜下层,中-低分化的普通腺癌占30%,肝样分化区占70%,腺癌细胞呈不规则腺样或梁索状排列,细胞核大深染偏位,核分裂相易见,胞质嗜碱,肝样分化区域呈巢片状、梁状排列,细胞胖大,核大深染,核仁明显,核分裂相多见,胞质嗜酸(见图2),局部细胞质内或细胞外见红染的嗜酸性小体(见图3),间质血窦丰富,胃小弯侧淋巴结(3/11)见癌转移;贲门、胃大弯侧及幽门淋巴结(0/12)未见癌转移;免疫组织化学(IHS)示:肝样区域AFP(+)(见图 4)、Hep(+)、Villin(+),腺样区域 Villin(+)、CDX-2(+)(见图 5)、CK20(+),P53(+++)、Ki67 >80%;特殊染色PAS示细胞质内或细胞外嗜酸性小体阳性(见图6)。术后以“奥沙利铂、替吉奥(SOX)”方案化疗一个疗程,患者出现胃肠道不良反应,要求终止化疗,现于门诊随访半年,患者一般情况良好,无复发及转移。
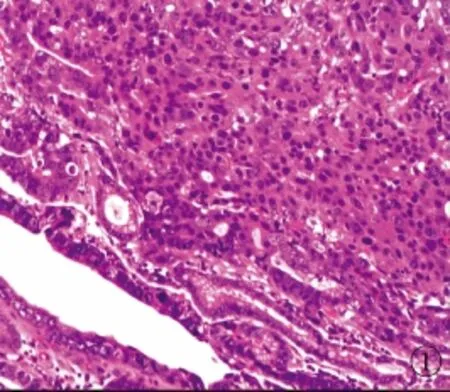
图1 普通腺癌与肝样腺癌两种肿瘤细胞的移行带(HE,×100)
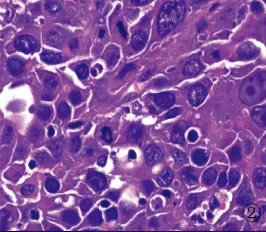
图2 片状分布的肝样分化区域,细胞核不规则,异型明显 (HE,×400)
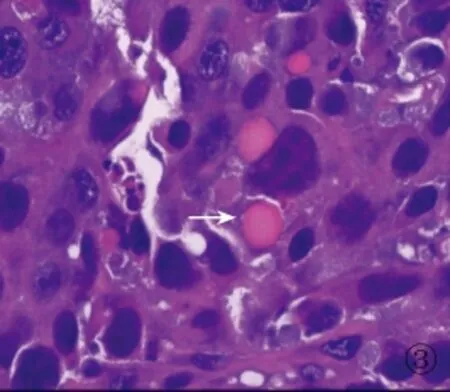
图3 肝样分化区域的肿瘤细胞内外见红染的嗜酸性小体(箭头所示)(HE,×400)
2 讨论
肝样腺癌(HAS)是一种原发于肝外的特殊类型的肿瘤,HAS多见于老年患者,可发生于多种器官,但胃最常见,约占63%[1],在胃癌中,HAS的发生率很低,占所有胃腺癌的 0.3%-1%[2,3]。在胚胎发育过程中,胃与肝均起源于内胚层的前肠,因此,如果胃癌分化失常,可向肝细胞分化,从而形成HAS[3]。有报道 80%的患者伴有血清 AFP 升高[4],本例患者术前查AFP也升高。
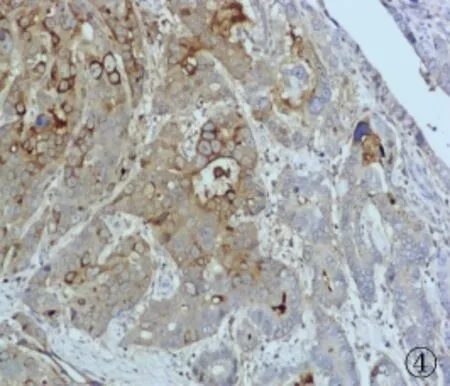
图4 肝样分化区域AFP(+),普通腺癌区域AFP(-)(Max-VisionTM法,×100)
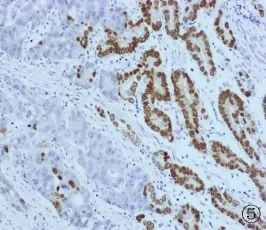
图5 普通腺癌区域CDX-2(+),肝样腺 癌 区 域 CDX-2(-)(MaxVisionTM法,×100)
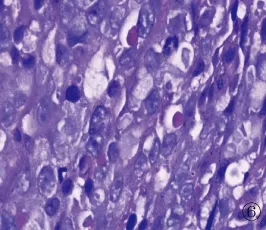
图6 PAS染色示肝样分化区域肿瘤细胞内及细胞外嗜酸性小体被染成紫红色(PAS,×400)
2.1 病理特点
典型的HAS常由腺癌区域和肝样分化区域构成,两者之间移行过渡,或在典型的腺癌区域中出现岛状分布的肝细胞癌样区域,可有高、中、低分化程度的差异,大部分病例腺癌区域为乳头状腺癌或管状腺癌;肝样分化区域癌细胞呈实性巢状或梁索状分布,间质血窦丰富,癌细胞体积大,核大小不一,可见巨核或多核瘤巨细胞,胞质嗜酸或透明,部分细胞质内或细胞外可见嗜酸性小体。免疫组化染色时,85%-95%的病例 AFP 阳性[5],30%-83.3%的病例Hep阳性[6]。该病例肝样区域AFP、Hep均为阳性。
2.2 诊断与鉴别诊断
因胃镜活检取材比较表浅,HAS术前诊断较为困难,而肝样区域范围常较小却又位于癌组织深层,故诊断为HAS的阳性率较低,本例胃镜活检结果显示腺癌。大部分病例均需手术切除病理得以确诊,无论AFP是否升高,腺癌中出现肝样分化区域均可作为诊断HAS的金标准。胃HAS要与非特殊性胃癌相鉴别,如胃腺癌、神经内分泌癌等,这些肿瘤无肝样分化区域,无血清AFP升高或免疫组化中AFP的阳性表达;HAS的侵袭性很强,极易发生肝内及其他腹腔脏器的转移,很容易误诊,当胃的HAS合并肝转移时,要与原发性肝癌(HCC)相鉴别,一般情况下,后者常有肝炎及肝硬化的病史,单发结节多见,转移至胃内的极为少见,且先侵犯胃壁浆膜层,形态学上一般无腺癌成分。
2.3 治疗及预后
HAS的治疗原则是以手术切除为主,辅以全身化疗及局部介入的综合治疗方案。术后检测AFP以了解治疗效果。手术切除的彻底性是预后的关键,故胃癌根治术为首选,如果无法完整切除或由其他脏器转移的肝样腺癌,在行胃癌根治性切除后行姑息治疗,可以提高生存率。目前尚无针对HAS的标准化疗方案,综合国内外文献报道,现比较推崇首选5-FU、MMC为主的化疗方案[7]。该病例中癌细胞浸润黏膜下层,属于早期癌,在手术治疗后,以“SOX”方案化疗一个疗程,患者出现副反应,终止化疗,于门诊随访半年,情况良好。HAS的预后差,容易转移及术后复发,临床生存期为10-18个月,第1,3,5年的生存率分别为 37.5%,12.5%和 8.3%[8]。
总之,肝样腺癌比较少见,易误诊,又易转移,预后差,在临床上,对胃腺癌患者应常规行血清AFP的检查,如有升高,应当引起注意。早发现、早治疗是提高生存率的关键。
[1]曲文书,王琳.胃肝样腺癌的病理与临床研究现状[J].现代肿瘤医学,2012,19(7):1429-1431.
[2]Kumashiro Y,Yao T,Aishima S,et al.Hepatoid adenocarcinoma of the stomach:histogenesis and progression in association with intestinal phenotype[J].Hum Pathol,2007,38(6):857- 863.
[3]Liu X,Cheng Y,Sheng W,et al.Analysis of clinicopathologic features and prognostic factors in hepatoid adenocarcinoma of the stomach[J].Am J Surg Pathol,2010,34(10):1465-1471.
[4]李晨,夏绍友,张勇.胃肝样腺癌血清甲胎蛋白阳性的临床意义[J].中国医药导报,2012,9(6):43-45.
[5]张迎东,许腾,宋军,徐为.胃肝样腺癌1例报道并文献复习[J].中国肿瘤外科杂志,2014,6(1):61-62.
[6]Metzgeroth G,Strobel P,Baumbusch T,et al.Hepatoid adenocarcinoma-review of the literature illustrated by a rare case originating in the peritoneal cavity[J].Onkologie,2010,33:263-269.
[7]罗庆伟,刘黎明,田小林.胃肝样腺癌的研究进展[J].中国癌症防治杂志,2014,6(4):414-417
[8]宋志远,孔棣.胃肝样腺癌的诊治研究进展[J].山西医药杂志,2012,41(8):802-803.
