固定化磷脂酶A1催化制备DHA型磷脂
2015-12-18马彦庆陈斌斌修志龙杨天奎
马彦庆 陈斌斌 郑 妍 修志龙 杨天奎 牟 英
(大连理工大学生命科学与技术学院1,大连 116000)(丰益(上海)生物技术研发中心有限公司2,上海 200000)
固定化磷脂酶A1催化制备DHA型磷脂
马彦庆1陈斌斌2郑 妍2修志龙1杨天奎2牟 英1
(大连理工大学生命科学与技术学院1,大连 116000)(丰益(上海)生物技术研发中心有限公司2,上海 200000)
以磷脂酰胆碱(PC)富集物和二十二碳六烯酸(DHA)浓缩液为底物,正己烷为反应介质,在固定化磷脂酶A1(PLA1)的催化作用下,制备DHA型磷脂(PL-DHA)。研究了底物摩尔比、加酶量、溶剂用量、反应温度、水活度、反应时间对PL-DHA制备的影响。通过条件优化,确定最佳条件为:DHA浓缩液和PC的摩尔比为4∶1,加酶量为2种底物总质量的20%,溶剂用量为4 mL,反应温度为40℃,反应时间为2 h。经气相色谱定量分析,得到的磷脂中DHA的含量为17.7mg/g PL,并用棒状薄层色谱火焰离子检测器(TLC-FID)分析了PC含量随反应的变化。
磷脂酰胆碱 二十二碳六烯酸 固定化磷脂酶A1
磷脂(PL)是生物膜重要组成部分,而且在细胞各种活性上起着重要作用,作为常用乳化剂和抗氧化剂,磷脂在食品、化妆品及医药行业也有广泛应用[1]。近年来,DHA因其具有促进婴幼儿智力发育,提高认知力及免疫力[2]等特性成为研究热点。研究表明,DHA生理功能因其载体分子形式不同而有所差异,因此人们开始重视DHA与磷脂的双重作用。大量试验表明磷脂型DHA比甘三酯型DHA更有利于DHA吸收[3],可以更快速地为大脑皮层提供所需DHA[4]等。
由于从海产品中分离、富集DHA型磷脂比较复杂,且有产地及原料限制,其产量无法满足人们需求,需要利用其他方法进行制备[5]。DHA型磷脂的制备方法有化学法与酶法,化学法因催化剂非专一性和试剂毒性,会造成副产物多且影响产品安全性。酶法则具备较多优势:首先,酶具有位置特异性,既可以选择磷脂特定位点进行催化反应,也可以选择性地催化特定底物,副产物少,产品安全性好;其次,酶法反应条件温和,具有环境友好的优点[6]。近些年来不断有研究者尝试采用酶法制备DHA型磷脂[7-8]。本研究报道固定化PLA1催化酸解反应制备DHA型磷脂。
1 材料和方法
1.1 材料与方法
1.1.1 原料与试剂
浓缩磷脂:秦皇岛金海食品工业有限公司,主要组分质量分数为:磷脂酰乙醇胺(PE)11.96%、磷脂酰肌醇(PI)8.86%、磷脂酰胆碱(PC)11.34%、溶血磷脂酰乙醇胺(LPE)2.71%;藻油:厦门汇盛生物有限公司,其中DHA质量分数≥35%;磷脂酶A1酶液:诺维信公司。
1.1.2 仪器
Agilent7820A气相色谱仪:美国Agilent Technologies有限公司;IATROSCAN MK-6S TLC-FID:日本三菱雅特隆(IATRON)公司。
1.2 试验方法
1.2.1 PC的富集
参考张秀青等[9]的方法,对浓缩磷脂中的PC进行富集,得到PC提取物经高效液相色谱定量检测,其中PC 59.4%、PE 19.91%、溶血磷脂酰胆碱(LPC)1.62%。经由气相色谱检测PC脂肪酸组成,计算其平均分子质量约为773 u。
1.2.2 DHA的富集
参考Domart等[10]的方法,富集DHA经气相色谱检测纯度为95.49%。平均分子质量约为320 u。
1.2.3 固定化PLA1的制备
按照2∶1∶1(g∶mL∶mL)比例分别添加牌号为D380的碱性离子交换树脂、磷脂酶A1酶液及20 mmol/L(pH 5.5)磷酸盐缓冲液,在30℃摇床中以100 r/min的转速振荡6 h,然后于30℃真空干燥箱内干燥至水分为2.5%。
1.2.4 酸解反应
取200mg PC,按比例加入DHA浓缩液,然后按照设定加入正己烷,底物溶解后,加入定量固定化PLA1,充氮保护,反应完成后分离固定化酶,终止反应。
反应过程中摇床的转速均为250 r/min。
1.2.5 产物的分离
反应完成后回收反应液,并以正己烷洗涤固定化酶3次,将洗涤液与反应液合并,低温旋蒸除去溶剂得粗产品。然后用冷丙酮将粗产品脱油3次,离心后收集沉淀层,然后低温真空干燥。
1.2.6 磷脂中DHA含量的分析
1.2.6.1 磷脂的甲酯化
称取一定质量样品,溶于正己烷,以C13∶0甲酯为内标物,参考Seung等[11]方法进行甲酯化后,备气相色谱定量分析。以下数据中DHA含量均为磷脂产物中含有DHA的质量含量。
1.2.6.2 气相色谱的条件
检测器:氢火焰离子化检测器。色谱柱型号为:CP-Sil 88 50 m×0.25 mm(0.2μm)。毛细管柱柱压:14.84 psi。进样量:1μL。分流比:20∶1。进样口温度:250℃。柱温箱升温程序为:80℃保持2 min,以10℃/min的速率升高至120℃,然后以5℃/min的速率升高至180℃后保持2 min,再以2℃/min的速率升高至206℃,之后以25℃/min的速率升高至230℃后保持5 min,最后运行2 min。
1.2.7 磷脂中PC含量检测
1.2.7.1 TLC-FID扫描条件
称取一定质量的样品,加入甲醇∶乙醇(体积比)=1∶1溶液溶解。色谱柱型号为:CHROMAROD-SIII。扫描速度:30 s/根。展开剂配比(体积比)为:氯仿∶甲醇∶水=72∶31∶3.2。检测器为FID检测器,氢气流速为160 mL/min,空气流量为2 L/min。
1.2.7.2 PC浓度与TLC-FID中PC出峰面积的标准曲线的建立
取PC标样,溶解于氯仿中,然后进行梯度稀释,分别配制成不同浓度标准溶液。分别将标准溶液上样,得到标准曲线为:
Y=0.000 2-1.022 9,其中R2=0.990 4。
式中:Y为PC浓度/mg/mL;为峰面积。
1.2.7.3 PC含量的计算
由1.2.7.1所述条件对样品进行扫描,然后根据1.2.7.2公式得到溶液的浓度,最后根据如下公式计算得到样品中PC含量:
PC=VY/M×100%
式中:V为溶液体积/mL;Y为样品浓度/mg/mL;M为称样质量/mg。
2 结果与讨论
在预试验中,分别选取正己烷、甲苯、叔丁醇作为反应溶剂,以商品NOVOZYM 435酶、TL IM酶、固定化PLA1作为催化剂,发现固定化PLA1在正己烷体系中的反应较优,磷脂产物中DHA含量较高,所以采用固定化PLA1作为催化剂,正己烷为溶剂进行反应优化。
2.1 底物比对反应的影响
在反应温度为40℃、加酶量为底物总质量15%、溶剂用量为5 mL、反应时间为2 h条件下,考察DHA∶PC/mol∶mol对反应的影响,结果见图1。
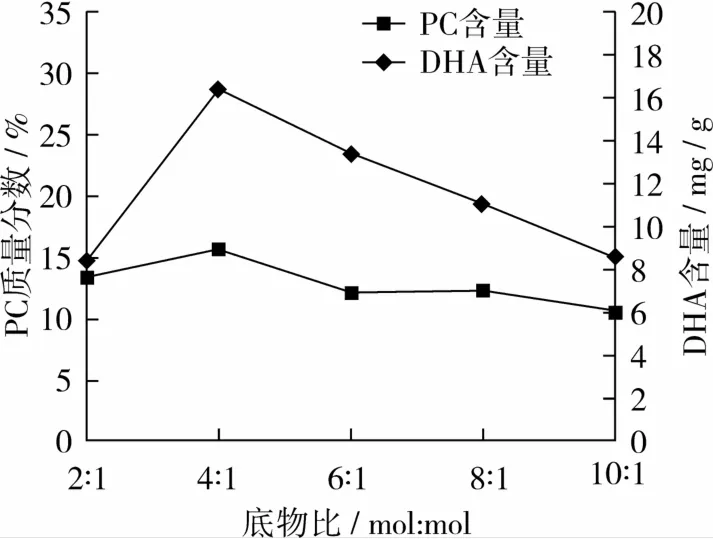
图1 底物比对反应的影响
由图1可知,随着底物比由2∶1升高至4∶1,DHA含量有所增加,但是随着底物比继续增加,DHA含量开始减少,同时PC水解也逐渐严重,原因可能是DHA浓缩液中含有一定水分,随着DHA添加量增加,累积的水分造成PC水解。在此条件优化中,DHA含量在底物比4∶1处达到最大值,所以选择底物比为4∶1继续优化反应温度。
2.2 反应温度对反应的影响
在底物比为4∶1、加酶量为底物总质量15%、溶剂用量为5 mL、反应时间为2 h条件下,考察反应温度对反应的影响,结果见图2。

图2 反应温度对反应的影响
由图2可知,随着温度由35℃升高至40℃,DHA含量有所增加,当温度继续升高时,DHA含量开始减少,这是因为,一定范围内提高反应温度虽然可提高底物传导速率,增强酶活力,加快反应速度,但是高温会使酶发生热变性[13]。在温度低于40℃时,酶活力增强,底物传导速率加快,有利于反应进行。然而超过这一温度时,温度过高引起酶的热变性。另一方面,随着温度升高,PC水解逐渐变得严重,可知在考察温度范围内,温度升高不利于产物回收。DHA含量在温度为40℃时处于最大值,所以选择此温度继续优化加酶量。
2.3 加酶量对反应的影响
在反应温度为40℃、底物比为4∶1、溶剂用量为5 mL、反应时间为2 h条件下,考察加酶量对反应的影响,结果见图3。

图3 加酶量对反应的影响
由图3可知,当加酶量由10%增加至25%时,DHA含量逐渐增加,但是当加酶量继续增加时,DHA含量却开始减少。原因可能是当加酶量较少时,反应开始底物未被酶饱和,随着加酶量增加,底物逐渐被酶饱和,反应速度随之加快,但加酶量过多,会对底物传导产生阻碍作用,使反应速度降低。当加酶量为20%与25%时,DHA含量最高,考虑20%的加酶量更适合实际生产需要,所以选择此加酶量继续优化溶剂用量。
2.4 溶剂用量对反应的影响
在反应温度为40℃、底物比为4∶1、加酶量为底物总质量20%、反应时间2 h条件下,考察溶剂用量对反应的影响,结果见图4。由图4可知,当正己烷用量由7 mL减少至6 mL时,DHA含量有所增加,溶剂用量继续减少,DHA含量基本不再变化。这是因为根据酶反应动力学的米氏方程,当底物浓度较小时,底物浓度越大,反应速度越快,而当底物浓度继续增加时,反应速度则不会出现明显变化。在溶剂用量为4 mL时,DHA含量相对较高,而且与6 mL相比,需要溶剂量较少,更适合实际生产需要,所以选此溶剂用量继续优化水活度。
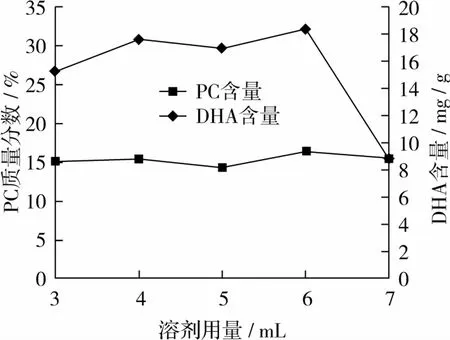
图4 溶剂用量对反应的影响
2.5 水活度对反应的影响
在反应温度为40℃、底物比为4∶1、溶剂用量为4 mL、加酶量为底物总质量20%、反应时间2 h条件下,考察水活度对反应的影响。水活度的控制按照Ducret等[14]描述的方法。

图5 水活度对反应的影响
由图5可知,当水活度为0.11时,DHA含量较小,这是因为酶活力需要一定的水活度来保持[15],而此水活度过低,酶活力较差。随着水活度增加至0.33,酶活力增加,DHA含量随之有所升高,但当水活度继续增大,DHA含量开始减少,而且PC的水解也变得更为严重。当体系水分较高时,作为副反应的水解反应将成为主要反应。所选用4个水活度的反应结果与未平衡水活度的反应结果作比较发现,未平衡水活度的反应较优,推测此时水活度应该在0.11与0.33之间,选择此水活度继续优化反应时间。
2.6 反应时间对反应的影响
在反应温度为40℃、底物比为4∶1、溶剂用量为4 mL、加酶量为底物总质量20%条件下,考察反应时间对反应的影响。

图6 反应时间对反应的影响
由图6可以看出,当反应时间由1.0 h增加至2.0 h时,DHA含量有所增加,反应时间继续增加,DHA含量基本不变。这是因为在反应进行至2.0 h时,已达到平衡点,随着反应时间继续增加,反应体系中各种物质的质量不会发生变化。
3 结论
本试验研究了利用固定化PLA1催化富含PC的磷脂进行酸解反应从而得到DHA型磷脂的方法。由试验的优化,当磷脂用量为200mg时,得到的最优酸解反应条件为:DHA浓缩液和PC的摩尔比为4∶1,加酶量为2种底物总质量的20%,溶剂用量为4 mL,反应温度为40℃,反应时间为2.0 h。
[1]James F M,Roslyn B A,David R H,et al.Lipids.In:Chemistry,biochemistry and nutrition[M].New York:Plenum Press,1986:369-428
[2]Tapiero H,Nguyen B G,Couvreur P,et al.Polyunsaturated fatty acids(PUFA)and eicosanoids in human health and pathologies[J].Biomed Pharmacother,2002,56(5):215-222
[3]Ulven SM,Kirkhus B,Larnglsit A,et al.Metabolic effects of Krill oil are essentially to those of fish oil butat lower dose of EPA and DHA,in healthy volunteers[J].Lipids,2011,46(1):37-46
[4]Picq M,Chen P,Perez M,et al.DHA metabolism:targeting the brain and lipoxygenation[J].Molecular Neurobiology 2010,42(1):48-51
[5]孙兆敏,李金章,丛海花,等.酶法制备n-3多不饱和脂肪酸型磷脂的工艺[J].中国油脂,2010,35(4):33-36
[6]Hong S I,Kim Y,Kim C,et al.Enzymatic synthesis of lysophosphatidylcholine containing CLA from sn-glycero-3-phosphatidylcholine(GPC)under vacuum[J].Food Chemistry,2011,129(1):1-6
[7]潘丽,谷克仁,杨壮.制备富含n-3多不饱和脂肪酸的磷脂[J].粮油加工,2006,12:57-60,68
[8]Garc IA H S,Kim I-H,Lope I-HernandeiA,etal.Enrichment of lecithin with n-3 fatty acids by acidolysis using immobilized phospholipase A1[J].Grasas Y Aceites,2008,59(4):368-374
[9]张秀青,于才渊.高纯卵磷脂的分离提纯方法[J].粮油加工,2006,4(4):45-49
[10]Domart C,MiyauchiD T,SumerwellW N.The fractionation ofmarine-oil fatty acid with urea[J].The Journal of the A-merican Oil Chemists'Society,1995,32(9):481-483
[11]Seung IH,Yangha K,Chong-Tai K,et al.Enzymatic synthesis of lysophatidylcholine containing CLA from snglycero-3-phosphatidylchoine under vacuum[J].Food Chemistry,2011,129(1):1-6
[12]GB/T 17377—2008,动植物油脂脂肪酸甲酯的气相色谱分析[S]
[13]陈惠晴,杨基础.超临界CO2中脂肪酶催化反应的研究[J].清华大学学报,1999(6):28-30
[14]Ducret A,TraniM,Lortie R.Lipase-catalyzed enantioselective esterification of ibuprofen in organic solvents under controlled water activity[J].Enzyme and Microbial Technology,1998,22(4):212-216
[15]Rao H V,Peter JH,Alasdair RM.Reaction ratewith suspended lipase catalyst shows similar dependence on water activity in different organic solvents[J].Biochimica et Biophysica Acta,1992,1118(3):218-222.
Preparation of Phospholipid-Docosahexaenoic Acid Catalyzed by Immobilized Phospholipase A1
Ma Yanqing1Chen Binbin2Zheng Yan2Xiu Zhilong1Yang Tiankui2Mu Ying1
(School of Life Science and Biotechnology,Dalian University of Technology1,Dalian 116000)
(Functional Food Technology Department,Wilmar(Shanghai)Biotechnology Research and Development Center Company Limited2,Shanghai 200000)
A facile enzymatic synthesis approaching to prepare phospholipid-docosahexaenoic acid(PLDHA)has been investigated through the phospholipase A1(PLA1)-catalyzed reaction of docosahexaenoic acid(DHA)aswell as phospholipid enriched in phosphatidylcholine(PC).The alteration elements of different parameters such asmolar ratio of substrates,reaction temperature,enzyme dosage,solvent dosage,water activity and reaction time have been researched systematically.The ratio of DHA and PCwas4∶1(mol/mol),the enzyme dosagewas the 20%of two substrates,the solvent dosagewas4mL and the reaction temperature and reaction time were 40℃and 2 h. By the quantitative analysis of GC,the content of DHA was detected to be 17.7mg/g PL on the optimal condition. The variation of PC content before and after the reaction was also analyzed by The Thin Layer Chromatography-Flame Ion Detector(TLC-FID).
phosphatidylcholine,docosahexaenoic acid,immobilized phospholipase A1
TS229
A
1003-0174(2015)03-0075-05
2013-11-28
马彦庆,男,1988年出生,硕士,生物化工
修志龙,男,1965年出生,教授,生物化工
