RP-HPLC法测定黑顺片中6种酯型生物碱的含量
2015-12-17王超群翟宏焱王晓华
王超群,翟宏焱,王晓华
(1.安徽省医学科学研究院,合肥 230061; 2.安徽省食品药品检验研究院,合肥 230051)
RP-HPLC法测定黑顺片中6种酯型生物碱的含量
王超群1,翟宏焱2,王晓华1
(1.安徽省医学科学研究院,合肥 230061; 2.安徽省食品药品检验研究院,合肥 230051)
建立黑顺片中6种酯型生物碱含量的高效液相测定方法。采用岛津C18色谱柱(250 mm×4.6 mm,5 μm),以乙腈-四氢呋喃(体积比为25∶15)为流动相A,以0.1 mol/L乙酸铵溶液(每1 000 mL加冰乙酸0.5 mL)为流动相B梯度洗脱,流量为1.0 ml/min,检测波长为235 nm,柱温为35℃。苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱进样量分别在0.222~4.430,0.060~1.119,0.144~2.878,0.015~0.297,0.025~0.496,0.011~0.229 μg范围内与色谱峰面积线性呈良好的线性关系,相关系数r均大于0.999 5,检出限分别为2.10,2.70,2.20,2.60,1.60,3.10 ng,样品在12 h内稳定。苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱的加标回收率分别为98.7%~102.2%,98.6%~102.3%,99.0%~101.9%,102.0%~97.3%,102.1%~98.3%,95.7%~103.5%,测定结果的相对标准偏差分别为2.5%,2.5%,2.2%,2.3%,2.2%,1.7%(n=6)。该方法简便,测定结果准确、可靠,可为黑顺片的质量评价和质量控制提供参考。
黑顺片;酯型生物碱;RP-HPLC
附子为毛茛科植物乌头(Aconitum earm ichaeli Debx)的子根,具有回阳救逆、补火助阳、逐风寒湿邪的功效[1],为最具特色的临床治疗阳虚里寒症的首选药物。附子主要毒、效成分为乌头碱类双酯型生物碱(即新乌头碱、乌头碱、次乌头碱),通过炮制可使既是有效成分又是有毒成分的乌头碱类双酯型生物碱转化成活性及毒性都降低的乌头碱类单酯型生物碱(即苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱)[2]。附子在炮制加工过程中,双酯型生物碱分子结构中的乙酰基被水解脱去,生成毒性相对较低的单酯型生物碱,单酯型生物碱含量保证安全性,而双酯型生物碱含量保证药效[3-4]。为控制附子的毒性,必须测定其中双酯型乌头碱的含量,为保证附子提取物的药效,有必要同时测定其中单酯型生物碱的含量,所以最终选择其中含量较高的3个单酯型乌头碱(苯甲酰新乌头碱、苯甲酰乌头原碱、苯甲酰乌头次碱)和3个双酯型乌头碱(新乌头碱、次乌头碱、乌头碱)进行含量测定。
附子炮制品主要有黑顺片、白附片,其中黑顺片为临床常用中药之一,目前并没有能够同时控制毒性和保证疗效的炮制工艺规范,也无能够表明附子安全性和有效性的科学、量化的质量标准,由于炮制工艺不尽相同,使得其生物碱的含量差异高达10倍[5],难以保障临床用药的安全有效。为保证疗效及控制药物的毒性,建立能够同时兼顾黑顺片安全和有效量化的质量标准非常有必要。近年来,有关附子的生物碱含量测定研究较多[6-8],但对黑顺片中生物碱类成分测定的高效液相检测方法未见报道。
笔者建立了反相高效液相色谱法可以同时测定黑顺片中3种双酯型和3种单酯型生物碱成分的检测方法,为有效的评价和控制黑顺片炮制品质量,规范炮制工艺提供依据。
1 实验部分
1.1 主要仪器与试剂
液相色谱仪:LC-20AD型,日本岛津公司;
紫外检测器:SPD-M20A型,日本岛津公司;
色谱数据工作站:LC solution型,日本岛津公司;
柱温箱:CTO-20A型,日本岛津公司;
自动进样阀:SIL-20AC型,日本岛津公司;
电子天平:(1)XP56型,瑞士Mettler Toledo公司,(2)BP210S型,德国Sartorius公司;
超声波清洗器:SB2200-T型,上海奥特赛恩斯仪器公司;
乌头碱(批号110720-2004104,纯度为100%),新乌头碱(批号799-9403,纯度为100%),次乌头碱(批号0798-9403,纯度为100%),苯甲酰新乌头原碱(批号111795-200901,纯度为99.6%),苯甲酰乌头原碱(批号111794-201102,纯度为96.5%),苯甲酰次乌头原碱(批号111796-201002,纯度为97.3%),中国食品药品检定院;
乙腈:色谱纯;
异丙醇-乙酸乙酯混合溶液:体积比为1∶1;
黑顺片饮片:市售;
实验所用其它试剂均为分析纯;
实验用水为去离子水。
1.2 色谱条件
色谱柱:Shimadzu C18柱(250 mm×4.6 mm,5 μm);流动相:以乙腈-四氢呋喃(体积比为25∶15)为流动相A,以0.1 mol/L乙酸铵溶液(每1 000 mL加冰乙酸0.5 mL)为流动相B,按表1进行梯度洗脱,流速为1.0 mL/min;检测波长:235 nm;柱温:35℃。

表1 流动相梯度洗脱参数
1.3 对照品溶液制备
精密称取6种酯型生物碱对照品适量,分别以0.05%盐酸-甲醇溶液溶解并定容至2 mL容量瓶中,配制成苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱质量浓度分别为2.215,0.559 7,1.439,0.494 4,0.496 1,0.573 7 mg/mL的对照品溶液。精密吸取上述苯甲酰新乌头原碱对照品溶液1 mL,苯甲酰乌头原碱对照品溶液1 mL,苯甲酰次乌头原碱对照品溶液1 mL,新乌头碱0.3 mL,次乌头碱0.7 mL和乌头碱0.2 mL置于10 mL量瓶中,加0.05%盐酸-甲醇溶液至标线,摇匀,配制成苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱质量浓度分别为221.5,55.97,143.9,14.83,24.81,11.47 μg/mL的混合对照品溶液。
1.4 样品处理
精密称取黑顺片粉末(过3号筛)2 g,置于具塞锥形瓶中,加氨试液3 mL,精密加异丙醇-乙酸乙酯混合溶液50 mL,称量,2 h充分润湿后超声处理(300 W,40 kHz,水温25℃以下)30 min,放冷,再称量,用异丙醇-乙酸乙酯混合溶液补足减失的质量,摇匀,滤过。精密量取续滤液25 mL,在40℃以下减压回收溶剂至干,残渣用0.05%盐酸-甲醇溶解并定容至2 mL量瓶中,用0.45μm的微孔滤膜过滤,即得供试品溶液。
2 结果与讨论
2.1 样品提取条件的优化
对附子中生物碱提取方法的优化,考察了异丙醇-乙酸乙酯(1∶1)与乙醚两种溶媒的提取率,结果见表2。

表2 不同提取溶媒的结果 μg/g
表2结果表明,异丙醇-乙酸乙酯(1∶1)的提取率优于乙醚。
2.2 色谱条件的选择
查阅相关文献[1,9],高效液相色谱法测定乌头类生物碱成分多采用含二乙胺和三乙胺的碱性流动相或者酸性乙酸铵为流动相,这些流动相对同时测定单酯型和双酯型生物碱不能达到满意的分离效果。比较了多种流动相,最终选定以乙腈-四氢呋喃(体积比为25∶15)与0.1 mol/L乙酸铵溶液为流动相,并进行梯度洗脱,6种生物碱分离度较好,且可在60 min内完成1次进样测定。
2.3 供试液配制溶液的选择
2010版药典及其它文献中供试液的配制大多数最后是用异丙醇-二氯甲烷(1∶1)溶液定容,考虑到二氯甲烷沸点较低(39.75℃),易挥发,毒性较大,且酯型生物碱在碱性条件下易水解,在酸性条件下相对稳定,本实验改用加0.05%盐酸-甲醇溶液配制对照品和供试品溶液[10]。
2.4 色谱图
供试品溶液色谱图见图1。
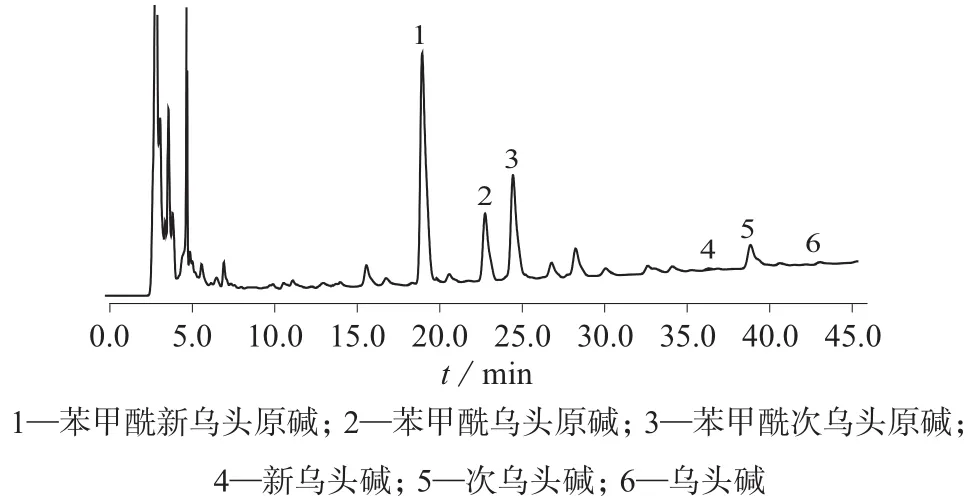
图1 供试品溶液色谱图
2.5 线性方程与检出限
分别精密吸取混合对照品溶液1,2,5,10,15,20 μL,按1.2色谱条件测定色谱峰面积。以进样量X(μg)为横坐标、色谱峰面积Y为纵坐标进行线性回归,建立6种生物碱线性回归方程,将对照品溶液以0.05%盐酸-甲醇溶液不断稀释并进行HPLC分析,以信噪比为3倍时的进样量为检出限,结果见表3。
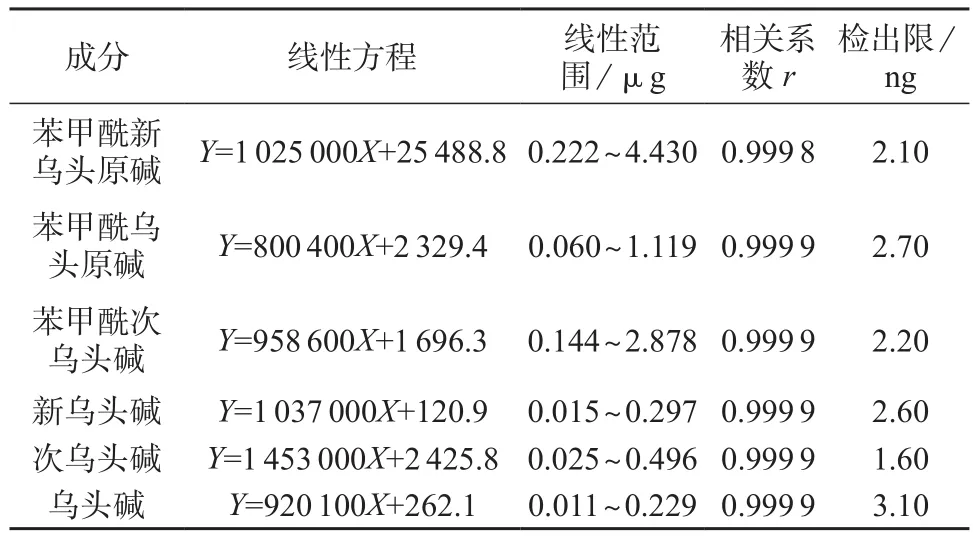
表3 6种生物碱成分的线性关系
2.6 重复性试验
取同一批黑顺片粉末,按1.4方法平行制备6份供试品溶液,并在1.2色谱条件下进样10μL,测定苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱的含量,结果见表4。由表4可知,该法重复性较好。
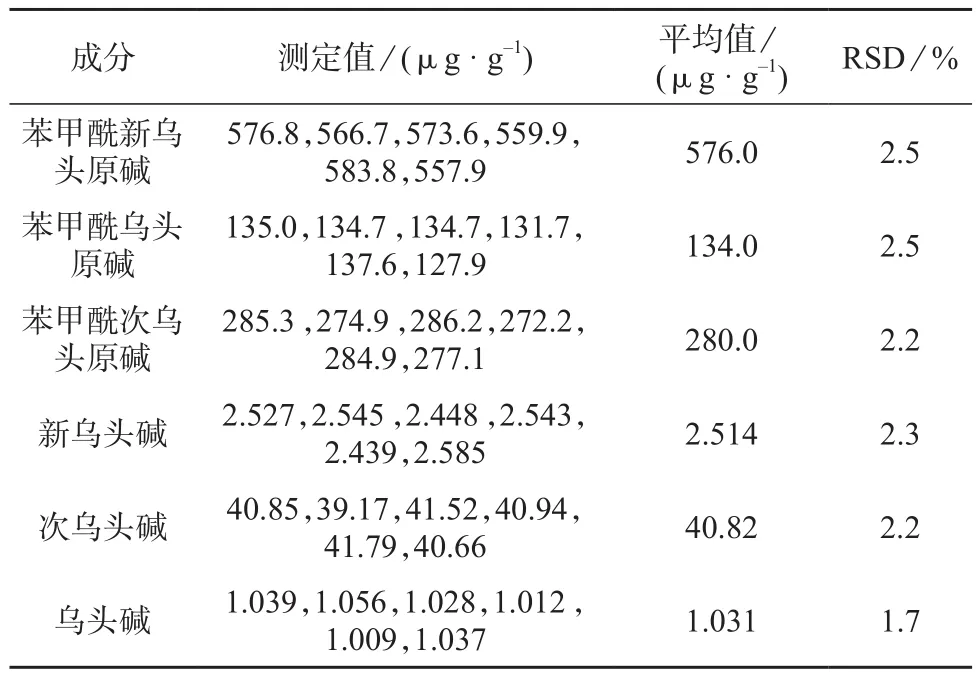
表4 6种生物碱重复性考察结果
2.7 稳定性考察
精密吸取同一供试品溶液,按实验方法分别在第0,2,4,6,8,12 h 间隔进样10 μL,测定苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱峰面积,结果见表5。由表5可知,苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱测定结果的相对标准偏差分别为1.52%,1.49%,1.64%,1.38%,0.94%,1.22%,表明样品在12 h内稳定。
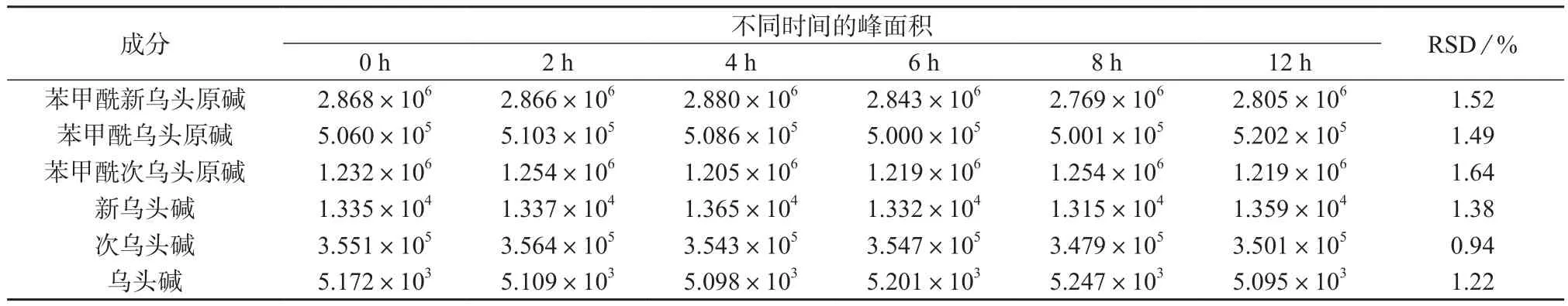
表5 6种生物碱稳定性考察
2.8 加标回收试验
精密称取已知苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱含量的黑顺片6份,每份1 g,分别精密加入适量的对照品苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱,按1.4制备供试品溶液,在1.2色谱条件下进样10 μL,进行加标回收试验,结果见表6。由表6可知,样品加标回收率较好,说明该方法具有较高的准确度。
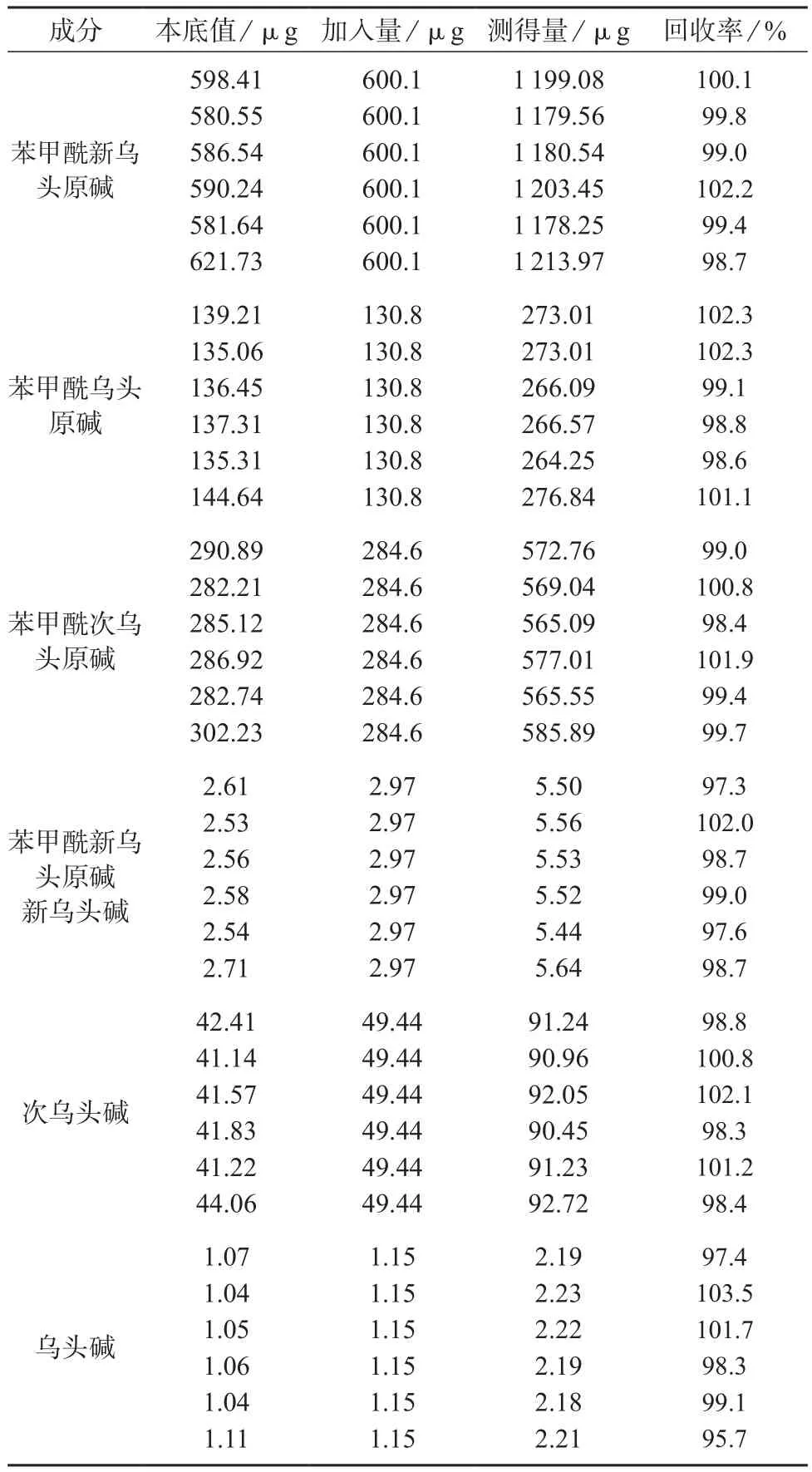
表6 回收试验结果
2.9 样品测定
取4个批号的黑顺片饮片,按1.4制备供试品溶液,并在1.2色谱条件下进样10μL,测定苯甲酰新乌头原碱、苯甲酰乌头原碱、苯甲酰次乌头原碱、新乌头碱、次乌头碱、乌头碱色谱峰面积,并计算以上6种酯型生物碱的含量,结果见表7。
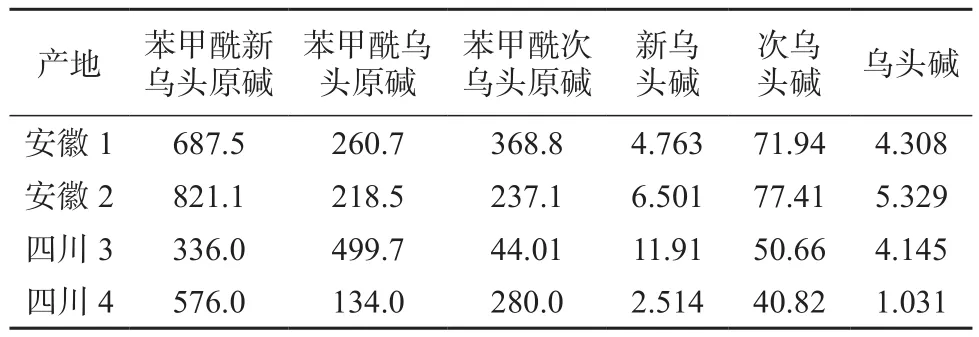
表7 种酯型生物碱含量测定结果 μg/g
从不同产地来源的黑顺片6种生物碱含量来看,4个批次的单酯型生物碱的总量在0.088%~0.13%之间,双酯型生物碱的总量在0.004 4%~0.008 9%之间。单酯型含量均明显高于双酯型生物碱含量。
3 结语
建立了同时测定3种单酯型和3种双酯型乌头生物碱的HPLC方法。通过异丙醇-乙酸乙酯(1∶1)与乙醚两种不同溶剂对样品中生物碱类成分提取率的比较,选择异丙醇-乙酸乙酯(1∶1)作为样品提取溶媒比较合适,通过查阅文献考察了较多的色谱条件系统,最后选择乙腈-四氢呋喃(体积比为25∶15)与0.1 mol/L乙酸铵溶液为流动相,并进行梯度洗脱,结果6种不同生物碱分离度较好,且可在60 min内完成1次进样测定。本方法线性范围宽,稳定性好,重现性及成本较低,对黑顺片的质量控制和优化炮制工艺具有重要的意义。
[1]药典委员会.中华人民共和国药典:一部[M].北京:中国医药科技出版社,2010: 177.
[2]邵峰,俞瑜,任刚. HPLC法同时测定附子理中丸中三种单酯型生物碱含量[J].中国实验方剂学杂志,2012,18(16): 57-62.
[3]黄勤安,张聿梅,何轶,等.乌头碱水解转化规律的研究[J].中国中药杂志,2007,32(20): 2 143-2 145.
[4]周林,任玉珍,李飞,等.不同炮制方法对附子生物碱成分的影响[J].安徽中医学院学报,2012,31(5): 71-73.
[5]陈彦琳,杜杰,梁焕,等.道地药材附子炮制加工规范化探讨[J].中国现代中药,2009,11(7): 42.
[6]陈东安,刘云华,陈燕,等. RP-HPLC测定附片中的总酯型生物碱[J].华西药学杂志,2010,25(5): 585-586.
[7]聂黎行,张聿梅,鲁静,等.附子和附片质量标准研究[J].中国药学杂志,2010,45(15): 1 182-1 186.
[8]孙兰,周海燕,赵润怀,等. HPLC法同时测定附子中6种单酯和双酯型生物碱[J].中草药,2009,40(1): 131-134.
[9]张聿梅,鲁静,蒋渝,等.川乌和制川乌中单酯及双酯型生物碱的含量测定[J].药物分析杂志,2005,25(7): 807.
[10]刘玉兰,刘世坤,裴奇,等.高效液相色谱法测定附子中3组分的含量[J].中国药房,2006,17(5): 1 255-1 256.
Determination of Six Kinds of Ester-Type Alkaloids in Aconiti Lateralis Praeparata by RP-HPLC
Wang Chaoqun1, Zhai Hongyan2, Wang Xiaohua1
(1. Anhui Academy of Medical Sciences, Hefei 230061, China; 2. Anhui Institute for Food and Drug Control, Hefei 230051, China)
The method for simultaneously determining six kinds of ester-type alkaloids in Aconiti Lateralis Praeparata was devolped by HPLC. The column was Shimadzu C18column(250 mm×4.6 mm, 5μm), the mobile phase consisting of acetonitrile-tetrahydrofuran (the wolume ratio was 25∶15, phase A) and 0.1 mol/L ammonium acetate (0.5 mL glacial acetic acid per 1 000 mL, phase B) were used as gradient elution solution with the flow of rate of 1.0 mL/min. The detection wavelength was set at 235 nm with column temperature of 35℃. The linear range of benzoylmesaconitine, benzoylaconitine, benzoylhypaconitine, mesaconitine, hypaconitine and aconitine were 0.222-4.430, 0.060-1.119, 0.060-2.878, 0.015-0.297, 0.025-0.496, 0.011-0.229 μg, respectively, and the correlation coefficients were more than 0.999 5, the sample was steady within 12 h. The detection limits were 2.10, 2.70, 2.20, 2.60, 1.60,3.10 ng, and the average recoveries were 98.7%-102.2%, 98.6%-102.3%, 99.0%-101.9%, 102.0%-97.3%, 102.1%-98.3%, 95.7%-103.5% with RSD of 2.5%, 2.5%, 2.2%, 2.3%, 2.2%, 1.7%(n=6) for benzoylmesaconitine, benzoylaconitine, benzoylhypaconitine, mesaconitine, hypaconitine and aconitine, respectively. This method is simple, accurate, reliable and provides reference for quality evaluation and quality control in Aconiti Lateralis Praeparata.
Aconiti Lateralis Praeparata; ester-type alkaloids; RP-HPLC
O657.7
A
1008-6145(2015)02-0062-04
10.3969/j.issn.1008-6145.2015.02.018
联系人:王晓华;Email: 1210wxh@sina.com
2015-12-08
