新风胶囊肝肾亚急性毒性实验研究
2015-12-13成遥,张贺,孟楣,刘健
成 遥,张 贺,孟 楣,刘 健
(1.安徽中医药大学第一附属医院药学部,国家中医药管理局中药制剂三级实验室,安徽合肥 230031;2.安徽中医药大学,安徽合肥 230012)
新风胶囊(XFC)为安徽中医药大学第一附属医院(以下简称我院)刘健教授自创的经验方,并由我院药学部进一步研发为医院制剂,于2005年取得了安徽省医院制剂的批准文号(皖药制字20050062),该方由黄芪、薏苡仁、雷公藤、蜈蚣等4味中药组成,具有益气健脾,化湿通络之功效。临床主要用于治疗风湿类疾病,如类风湿性关节炎,强直性脊椎炎,系统性红斑狼疮等,疗效确切安全。该制剂中雷公藤(Tripterygium wilfordii Hook.f.)系卫矛科雷公藤属植物,味苦、性寒,有大毒,归肝、肾经,药用部位为根,是祖国医学中一种常见草药,应用历史悠久,具有祛风除湿、通络止痛、消肿止痛、解毒杀虫等功效[1],1960年代以来应用于治疗类风湿性关节炎(RA),起效快而疗效好,逐渐受到世界范围内的认可[2]。与此同时,现代药理学证实,雷公藤对人体的肝、肾、生殖等功能有一定影响,是近年来发生中毒事件最多的草药之一,其中肝肾损害屡见不鲜,柯坤宇[3]报道,因类风湿性关节炎服用雷公藤多苷片(40 mg·d-1)30 d致急性肝损害1例。黄光照等[4]报道了4例雷公藤中毒的尸检病理报告,其中2例死于急性肾功能衰竭。雷公藤为XFC主要构成药物,XFC安全性的临床循证医学证据较多,刘健等[5-7]均做过深入的研究,但关于XFC安全性的实验数据较匮乏,为进一步验证XFC的安全性及其是否具有雷公藤样的肝肾毒性,本实验研究了XFC对大鼠的肝肾亚急性毒性,为临床安全用药提供依据。现报道如下。
1 材料与方法
1.1 动物和仪器 SD大鼠60只,雌雄各半,体重180~220 g,由安徽长临河科技有限公司提供,SPF级,准字号为scxk(皖)2014-002。我院SPF级动物房内饲养,温度20℃,相对湿度55% ~65%。动物食用全营养颗粒饲料,灭菌注射用水。ZN17-UX/UW型动物天平。DM0421E型低速离心机。日立CA7600全自动生化分析仪。奥林巴斯CKX31-C11BF型光学显微镜。
1.2 药品及试剂 新风胶囊(安徽中医药大学第一附属医院制剂,批号20140521);雷公藤饮片(购自我院中草药房,由我院李立华主任药师鉴定);10%水合氯醛;10%甲醛溶液。
1.3 方法
1.3.1 分组及给药 取60只SD大鼠常规饲养适应1周后,随机分为5组:雷公藤组、XFC组(低、中、高)和空白对照组(CON组),每组12只。雷公藤组剂量为原生药 1.92 g·kg-1·d-1、XFC 组(低、中、高)大鼠分别灌胃给予相应XFC胶囊内容物溶解药液 0.6 、1.2 、2.4 g·kg-1·d-1。相当于临床成人(体重以 60 kg计)用量0.06 g·kg-1·d-1的10、20、40倍。连续给药30 d。空白组每日灌服等量灭菌注射用水。给药体积为15 mL·kg-1。给药期间正常供给饲料与灭菌注射用水。
1.3.2 观察指标和检测方法 实验期间,考察大鼠的一般状态:包括毛色变化、精神状态、活动情况、饮食饮水量等,称取大鼠逐日体重。于第31天给药后,10%水合氯醛轻度麻醉后腹主动脉取血,留取的血样静置后,于4 500 r·min-1离心15 min,分离血清,-20℃保存,用全自动生化分析仪测定血清谷丙转氨酸(ALT)、谷草转氨酸(AST)、尿素氮(BUN)、血肌酐(SCr)。解剖大鼠,留肝、肾组织,称质量,计算脏器系数,留取肝、肾组织于10%甲醛中保存,制作组织切片(取材、固定、脱水、浸蜡、包埋、切片、脱蜡、HE染色),显微镜下观察。
1.4 统计学分析 使用SPSS 19统计软件处理,各组数据以(±s)表示,多组之间比较采用单因素方差分析(one way-ANOVA)表示,方差齐性检验采用t检验,多组之间两两比较采用LSD-t检验的方法,P<0.05表示差异有统计学意义。
2 实验结果
2.1 动物一般状况 给药期间无大鼠死亡,与空白组比较,其余各组大鼠毛色、精神、活动等一般状况均未见明显异常,体重增长差异无统计学意义(P>0.05);各组大鼠肝、肾脏器官均未见明显肿胀,其肝肾指数也无明显差异(P>0.05),见表1。
表1 新风胶囊对大鼠肝肾功能体质量及肝肾指数的影响(±s,n=12)
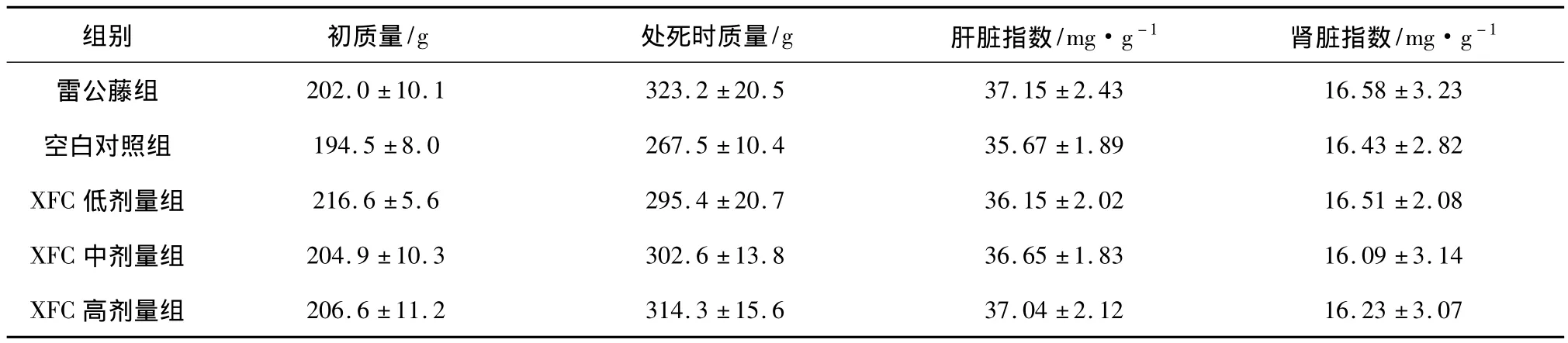
表1 新风胶囊对大鼠肝肾功能体质量及肝肾指数的影响(±s,n=12)
组别 初质量/g 处死时质量/g 肝脏指数/mg·g-1 肾脏指数/mg·g -1雷公藤组 202.0 ±10.1 323.2 ±20.5 37.15 ±2.43 16.58 ±3.23空白对照组 194.5 ±8.0 267.5 ±10.4 35.67 ±1.89 16.43 ±2.82 XFC 低剂量组 216.6 ±5.6 295.4 ±20.7 36.15 ±2.02 16.51 ±2.08 XFC 中剂量组 204.9 ±10.3 302.6 ±13.8 36.65 ±1.83 16.09 ±3.14 XFC 高剂量组 206.6 ±11.2 314.3 ±15.6 37.04 ±2.12 16.23 ±3.07
2.2 血清生化指标检测结果 给药30 d后,与空白组比较,雷公藤组各肝肾功能指标水平均明显升高(P<0.05),见表2。由表2可知,XFC的低、中、高三个剂量组测得的ALT、AST值与空白组比较P>0.05,雷公藤组 P <0.05,由此可见雷公藤组的转氨酶指标显著升高,提示肝功能有所恶化,而XFC各个剂量组对肝功能无明显影响;XFC的低、中、高三个剂量组测得的BUN、SCr值与空白组比较P>0.05,与雷公藤组比较 P <0.05,由此可见雷公藤组的BUN、SCr水平显著升高,提示肾功能有所恶化,而XFC各个剂量组对肾功能无明显影响。
2.3 新风胶囊对大鼠肝、肾组织学的影响
2.3.1 对肝组织学的影响 结果见图1,空白对照组大鼠的肝切片可见,肝组织结构完整,汇管区及小叶内无炎细胞浸润,肝细胞无变性(图1A)。雷公藤组可见,肝组织结构完整,少量汇管区可见炎细胞(以中性粒细胞为主)浸润,小叶内少量炎性细胞浸润,中央静脉周围肝细胞胞浆疏松水肿,其余肝细胞变性不显著(图1B)。XFC各组可见肝组织结构完整,汇管区及小叶内未见炎细胞浸润,肝细胞胞浆略微疏松水肿,其余肝细胞变性不显著(图1C,1D,1E)。
表2 新风胶囊对大鼠肝肾功能血液学指标的影响(±s,n=12)

表2 新风胶囊对大鼠肝肾功能血液学指标的影响(±s,n=12)
注:与空白对照组相比▲P<0.05。
组别 ALT/IU·L-1 AST/IU·L-1 BUN/mmol·L-1 SCr/μmol·L -1雷公藤组 55.00±12.13▲ 121.17 ±20.15▲ 8.45±1.21▲ 34.43 ±6.37▲空白对照组 44.50 ±8.06 102.50 ±8.09 7.76 ±0.87 31.83 ±5.23 XFC 低剂量组 46.63 ±7.34 106.25 ±7.39 8.15 ±1.00 30.15 ±3.31 XFC 中剂量组 47.04 ±9.11 116.80 ±6.75 6.65 ±0.76 29.18 ±4.36 XFC 高剂量组 46.60 ±8.24 104.32 ±8.65 8.04 ±0.98 30.23 ±5.09
2.3.2 对肾组织学的影响 结果见图2。空白组肾小球和肾皮质、髓质未见充血,未见炎细胞浸润,近曲小管及远曲小管上皮细胞无变性(图2A)。雷公藤组肾小球和肾皮质、髓质现充血,近曲小管上皮细胞略肿胀,可见粉染细颗粒,皮、髓质交界处偶见灶状炎细胞浸润(图2B)。XFC低、中、高组肾皮质、髓质未见充血,高剂量组皮质内肾小球略现充血,近曲小管及远曲小管无显著改变(图2C、2D、2E)。
3 讨论
本实验着重考察新风胶囊对大鼠肝肾的亚急性毒性,以相当于XFC临床成人用量(2.4 g·d-1)的10、20、40倍剂量给药,以常规的肝肾功能检测指标血清ALT、AST和血清BUN、SCr作为指标,方法简便,结果易得。结果显示,雷公藤组所测肝肾功能指标水平显著升高,肝、肾功能减退,产生一定的病理损伤,但损伤程度较轻,大鼠的体重和肝肾指数未现显著异常,主要表现为细胞肿胀和少量炎性细胞浸润。这进一步验证了雷公藤对肝肾的毒副作用,而新风胶囊各剂量组肝肾指标水平与空白对照组相比未见明显异常,肝肾功能正常,组织病理学改变亦十分轻微,这提示在人40倍耐受剂量下XFC仍未见雷公藤样肝肾毒性。
新风胶囊为我院刘健教授在“脾虚致痹”理论启发下,与临床实践相结合而自创的验方,君药为黄芪、薏苡仁,臣药为雷公藤、蜈蚣。作为新风胶囊臣药的雷公藤临床应用广泛,对多种疾病尤其是风湿类疾病疗效好、见效快,几乎没有可以完全替代的药物,与此同时,据临床观察,雷公藤的肝肾毒副作用发生率为58.1%[8],肝脏与肾脏是人体重要的代谢器官,体内产生的毒物与废物必须依靠肝、肾排出,但其自身非常脆弱。如何降低雷公藤的肝肾毒副作用,已成为现今中药领域的研究热点,关于雷公藤配伍减毒的研究已有显著进展,与雷公藤配伍减毒的药物有甘草、女贞子、凤尾草、白芍总苷、阿魏酸钠、茶多酚、番茄红素等[9-17],但雷公藤与黄芪、薏苡仁配伍减毒的用法仍不多见。我院刘健教授独创性的提出让黄芪和薏苡仁来和雷公藤配伍来降低它的毒副作用,本实验验证了这一成果。黄芪和薏苡仁的现代药理学研究表明,这两味药物内不同成分对肝细胞、肾细胞有保护作用,对肝癌细胞有抑制作用。黄芪多糖可保护肝细胞化学性损伤,并对CYP1A和CYP3A的表达有积极作用。黄芪注射液能抵抗自由基介导的脂质过氧化,对大鼠的肾脏有保护作用[18-21]。薏苡仁脂肪酸和薏苡仁油对人肝癌细胞具有抑制作用并可诱导其凋亡,从而抑制肿瘤生长[22-23]。以薏苡仁油为主要成分的康莱特注射液已成为抗肿瘤治疗辅助药物广泛应用于临床[24]。关于本制剂中单味药黄芪、薏苡仁对大鼠肝、肾等重要器官的保护作用机制,将在后面的研究中做更深一步的探讨。
[1]郭艳红,谭 垦.雷公藤的毒性及其研究概况[J].中药材,2007,30(1):112-117.
[2]Chen BJ.Triptolide,a novel immunosuppressive and anti- inflammatory agentpurified from aChinese herbTripterygium wilfordiiHook f[J].Leuk Lymphoma,2001,42(3):253-265.
[3]柯坤宇.雷公藤多苷片引起肝损害一例报告[J].实用临床医学,2009,10(7):40-42.
[4]黄光照,李 玲,刘 良,等.雷公藤中毒的尸检病理变化-附4例尸检报告[J].中国中西医结合杂志,2009,29(2):165-168.
[5]刘 健,徐桂琴.新风胶囊治疗类风湿性关节炎临床疗效的系统评价[J].中医药临床,2011,23(6):502-508.
[6]黄传兵,谌 曦,汪 元,等.新风胶囊联合来氟米特治疗强直性脊柱炎临床研究[J].中医药临床,2011,23(5):405-408.
[7]黄传兵,刘 健,谌 曦,等.新风胶囊治疗类风湿性关节炎疗效观察[J].中医药临床,2013,33(12):1399-1403.
[8]Chen BH.In vitro propagation of a medicinal plant:Tripterygium wilfordii Hook f[J].Forestry Stud China,2009,11(3):174-178.
[9]张 静,江 莹,王 芳,等.基于“异类相制”理论探讨雷公藤肝毒性配伍减毒的作用[J].中草药,2014,45(18):2711-2715.
[10]李涯松,童培建,马红珍,等.甘草对雷公藤治疗类风湿关节炎的减毒增效作用[J].中国中西医结合杂志,2006,26(12):1117-1119.
[11]吕娟涛,汤 浩.女贞子多糖对肝损伤保护作用的实验研究[J].中国医院药学杂志,2010,30(12):1024-1025.
[12]刘建群,洪 沁,张 维,等.凤尾草对雷公藤甲素的减毒作用[J].中国医院药学杂志,2010,30(6):443-446.
[13]李振彬,王志强,宫彩霞,等.白芍总苷对雷公藤多苷治疗狼疮性肾炎减毒增效作用的实验研究[J].中药新药与临床药理,2009,20(6):513-516.
[14]刘 伟,曹 勇,王凤娟,等.阿魏酸钠干预雷公藤多苷致小鼠肝损伤[J].武汉大学学报(医学版),2006,27(4):468-470.
[15]李钦民,韩 真.茶多酚对雷公藤内酯醇致小鼠肝损害的保护作用[J].世界华人消化杂志,2006,14(9):908-911.
[16]何 军,赵春景,廖昌军,等.番茄红素对雷公藤多苷致小鼠肝损害的保护作用[J].中国临床药理学与治疗学,2010,10(15):1096-1098.
[17]冯 哲,周学平.中药性味相制配伍减毒的方法探要[J].中华中医药杂志,2013,28(3):595-598.
[18]贾 睿,杜金梁,曹丽萍,等.黄芪多糖对鲤化学性肝细胞损伤的抑制作用[J].华中农业大学学报,2014,33(2):103-110.
[19]陈瑾歆,何 军,张娟娟,等.黄芪多糖对人肝癌细胞HepG2凋亡相关基因表达的影响[J].中国老年学杂志,2014,34(1):124-126.
[20]马 丹,谢晓娜,邹敬涛,等.黄芪注射液对糖尿病大鼠肾脏的保护作用及其机制[J].吉林大学学报(医学版),2014,40(2):267-269.
[21]邓海鸥,林 凯,黎映兰,等.黄芪多糖对老年早期糖尿病肾病者TNF-α、IL-6和免疫功能的影响[J].中药材,2014,37(4):713-716.
[22]包永睿,王 帅,孟宪生,等.薏苡仁脂肪酸类成分对人肝癌细胞株SMMC-7721细胞周期及细胞凋亡的影响[J].中成药,2014,36(2):235-239.
[23]张明发,沈雅琴.薏苡仁油抗肝癌的药理作用与临床应用[J].现代药物与临床,2010,25(6):422-426.
[24]赵为武,李 俊,郭晓关,等.薏苡仁提取油的成分分析[J].安徽农业科学,2014,42(1):257-258.
