多重增敏环保型痕量铅电化学传感器研制
2015-12-10何卫东窦文超赵广英
何卫东,窦文超,赵广英*
(浙江工商大学食品与生物工程学院,浙江省食品安全重点实验室,浙江 杭州 310000)
多重增敏环保型痕量铅电化学传感器研制
何卫东,窦文超,赵广英*
(浙江工商大学食品与生物工程学院,浙江省食品安全重点实验室,浙江 杭州 310000)
为改进铅电化学传感器的敏感性、稳定性、准确性和安全性,用碳酸羟基磷灰石高效富集Pb2+,用离子液体([BMIM]PF6)增加其导电性,加覆Nafion膜增加其敏感性与稳定性,共同修饰丝网印刷碳电极,构建一种多重增敏环保型快速检测痕量铅电化学传感器;优化检测条件后用方波溶出伏安法进行测定的结果为:Pb2+质量浓度在3~600 μg/L范围内呈现良好的线性关系,检出限为0.37 μg/L(RSN=3),连续8 次测定的相对标准偏差为3.4%。茶叶样品检测结果与电感耦合等离子体质谱测定结果无显著性差异。本研究研制出一种环保、敏感、准确、经济、简便且可用于茶叶中痕量铅检测的新型电化学传感器。
碳酸羟基磷灰石;电化学传感器;铅;茶叶
重金属是环境污染的重要来源,因其具有持久性、非生物降解性、毒性等特点,对环境和人类健康都构成了重大威胁[1]。重金属的毒性表现主要归因于氧化应激,即体内产生自由基等氧化剂与抗氧化剂之间的不平衡,这种不平衡会引起生物分子和组织损伤[2]。重金属还是引起癌症的一个重要因素,长期低剂量接触重金属在肿瘤发生中发挥关键作用[3]。铅是一种常见的重金属,会在人体内积累,对神经系统等造成严重的损害[4]。因此,对铅进行及时准确地监控与检测是十分有必要的。现在常用的铅检测方法有原子吸收光谱法[5]、分光光度法[6]、电感耦合等离子体质谱法[7]、电化学法[8]等。相较于其他方法,电化学方法操作相对简便、不需要昂贵的仪器。在多种电化学分析技术中,方波溶出伏安(square wave stripping voltammetry,SWV)法由于具有很高的灵敏度和选择性等优点而常被用于重金属离子检测。但传统的测定痕量铅的电化学传感器采用汞作为电极修饰物以保证检测的灵敏度[9],但是汞本身有毒,易造成环境再污染和对操作者安全的威胁。为克服此弊端,近期有报道用多壁碳纳米管[10]、石墨烯[11]、羟基磷灰石[12]等无毒材料替代汞修饰电极,但其灵敏度有待提升,因此研究选用更好的材料对电化学传感器进行改进已成为研究趋势和发展方向。
已有研究表明,碳酸羟基磷灰石(carbonated hydroxyapatite,CHA)对重金属离子(Pb2+、Cd2+、Cu2+、Hg2+等)的吸附强于标准羟基磷灰石(hydroxyapatite,HAP)[13-14],但是CHA应用于电化学方法检测重金属方面的效果未见有报道。
本研究采用CHA富集待测Pb2+,增加检测灵敏度和准确性;以十二烷基苯磺酸钠(sodium dodecylbenzenesulfonate,SDBS)分散CHA,加入离子液体1-丁基-3-甲基咪唑六氟磷酸盐([BMIM]PF6)增加其导电性,并用Nafion膜增加稳定性和信号再放大,制成痕量铅电化学传感器,将上述材料共同修饰丝网印刷碳电极(screen-printed carbon electrode,SPCE),用方波溶出伏安法进行测定,构建具有环保、敏感、稳定、准确、经济、操作简便等优点并可以批量生产的快速检测痕量Pb2+电化学传感器,易于提高样品抽检率,应用潜力大。
1 材料与方法
1.1 材料与试剂
1 mg/mL铅标准溶液 国药集团化学试剂有限公司;1-丁基-3-甲基咪唑六氟磷酸盐 中国科学院兰州化学物理研究所;十二烷基苯磺酸钠 杭州蓝博实业有限公司;5% Nafi on117 瑞士Fluka公司。
其他试剂均为分析纯,实验用水为双蒸馏水。
1.2 仪器与设备
丝网印刷碳电极 嵘斌生物科技有限公司;LK2006型电化学工作站 兰力科化学电子高技术有限公司;BHW-09A恒温加热赶酸仪 上海博通化学科技有限公司;KQ3200E型超声波清洗器 昆山市超声仪器有限公司;Multiwave 3000微波消解仪 奥地利安东帕(中国)有限公司;SevenMulti pH计 梅特勒-托利多仪器(上海)有限公司;使用的玻璃器皿在使用前要浸泡在硝酸溶液(20%~30%)中8 h以上,使用时要用双蒸水冲洗干净,晾干。
1.3 方法
1.3.1 CHA的应用机理与制备
制备方法:首先将300 mL 0.5 mol/L Na2HPO4溶液逐滴滴入500 mL 0.5 mol/L Ca(NO3)2溶液中,用1 mol/L NaOH溶液调节pH值至10,搅拌4 h后加入13 g Na2CO3,再用1 mol/L NaOH溶液调节pH值保持至10,搅拌4 h后陈化48 h。将陈化物过滤后,用双蒸水洗涤至中性。然后在100 ℃条件下烘干,研磨后保存备用。
1.3.2 电极的修饰原理与方法
CHA无毒且对Pb2+的富集和吸附力更强于HAP,用其替代汞和HAP修饰SPCE,既环保又能增强检测灵敏度,以SDBS作分散剂分散CHA后制成悬液使用。[BMIM]PF6有较高的电导率和离子迁移率、高稳定性和宽电化学窗口,能提高导电性,放大检测信号[16-19]。将用SDBS分散的CHA与[BMIM]PF6混均、滴涂修饰SPCE,能够提高检测灵敏度,起双重放大信号的作用,既环保又简便。Nafion是非电活性离子交换聚合物[20],它的—RSO3基团赋予Nafion重要的吸水特性,吸附的水为质子提供传输介质,使之具有离子导电性[21-22]。Nafion膜还能增强对Pb2+的富集、电催化和对阳离子的选择透过性,并能抵抗干扰杂质,增加电极稳定性[23]。CHA/ SDBS/[BMIM]PF6/Nafi on共同修饰SPCE。
修饰方法:准确称取20 mg CHA,溶于3.9 mL 0.35 mg/mL SDBS(SDBS的溶剂为V(乙醇)∶V(水)= 1∶10),再加入0.1 mL [BMIM]PF6,超声30 min后摇匀制成修饰液备用。取1.5 μL该修饰液,滴加于工作电极表面,室温干燥40 min;再取1 μL 0.5% Nafi on(Nafi on溶剂为V(乙醇)∶V(水)=1∶2)滴加于电极表面,室温干燥20 min。制成CHA/[BMIM]PF6/SDBS/Nafi on SPCE,避光保存。
1.3.3 方波溶出伏安法检测痕量铅
以25 mL 0.1 mol/L HAc-NaAc为电解质溶液,充氮5~10 min,以除去溶液中溶解氧的干扰。加入25 μL 100 μg/mL铅标准溶液,用方波溶出伏安法进行测定。测定条件为:初始电位—1.0 V、电沉积电位—1.1 V、终止电位—0.2 V、电位增量0.004 V、方波频率15 Hz、方波幅度0.04 V、电沉积时间180 s、平衡时间20 s、清洗电位0.2 V、清洗时间40 s、搅拌速率400 r/min。
1.3.4 循环伏安法表征三重修饰对Pb2+响应的方法
先将修饰电极在300 μg/L Pb2+溶液中开路富集5 min,用循环伏安法对Pb2+在不用修饰电极上的响应进行研究(循环伏安法参数为初始电位—1.1 V、扫描范围—1.1~—0.2 V、扫描速率0.1 V/s)。
1.3.5 茶叶样品预处理及测定方法
称取0.5 g左右的茶叶样品加入消化罐内,加入5 mL HNO3溶液和2 mL H2O2,然后将其置于微波消解仪内进行消解。消解完毕后,将消化罐放入赶酸仪,在150 ℃赶酸40 min,冷却备用。每个茶叶样品消解3份。
方波溶出伏安法测定:用少量0.1 mol/L pH 5.0的HAc-NaAc溶液冲洗样品消化罐,将消化好的样品转移到小烧杯中。然后用NaOH将样品pH值调节至5左右。再用0.1 mol/L pH 5.0的HAc-NaAc溶液将样品液定容至25 mL。然后在最优条件下用方波溶出伏安法进行测定。
电感耦合等离子体质谱(inductively coupled plasma mass spectrometry,ICP-MS)法测定:用超纯水冲洗消化罐,将样品转移到25 mL容量瓶中,用超纯水定容至25 mL。用孔径为0.45 μm的微孔滤膜过滤大约5 mL该样品溶液,对过滤后的样品溶液进行ICP-MS测定。具体参数参考文献中的参数[24]。
1.3.6 样品铅含量计算
为了消除茶叶样品的基底干扰,本研究采用二次加标法进行检测,每次加标0.5 μg,然后将得到的数据带入二次加标法公式经过计算得到样品的铅含量。
二次加标法公式:假设二次加标的线性良好且斜率为K,茶叶样品Pb2+含量为X(mg/kg),称量样品质量为M(g),溶液中Pb2+质量为m(μg),每次加标量为A(μg),二次加标测得的溶出峰高分别为H1和H2,则:

1.3.7 检测结果比较
综上所述,本文主要通过结合绘本内容进行补写、扩写、续写三方面对写话训练的实施办法进行了论述。总的来说,读写联动训练是确保小学低年级学生的语文综合素养能得到提升的关键,因此,相关教师在实际教学过程中应充分结合学生特点、绘本内容、读写联动训练目标等展开教学,确保绘本能在小学低年级阶段发挥出预期作用。
为了比较本法测定结果与ICP-MS法测定结果的差异,以验证本法的准确性。采用t检验对本法与ICP-MS法的测定结果进行比较。
设样本平均数为,总体平均数为μ,样本容量为n,样本标准差为σx,则:

由自由度为n—1,α=0.05,查表可得临界值。将计算所得的t值与临界值比较,若t值小于临界值,则两者无明显差异,即本法测定结果与ICP-MS法测定结果无明显差异,准确性较好;反之亦然。
2 结果与分析
2.1 碳酸羟基磷灰石的红外图谱及修饰电极表面形态分析
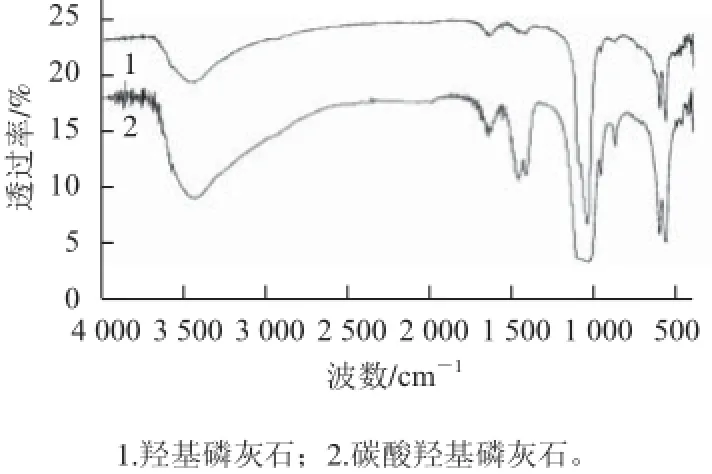
图 1 羟基磷灰石及碳酸羟基磷灰石的红外光谱图Fig.1 IR spectra of HAP and CHA
对标准羟基磷灰石和碳酸羟基磷灰石进行红外图谱表征,如图1所示。HAP(曲线1)和CHA(曲线2)的出峰位置相似,在500~700 cm—1附近都出现了P—O的弯曲振动吸收峰,在1 000~1 100 cm—1附近都出现了P—O的反对称伸缩振动吸收峰。曲线1在850cm—1及1 500 cm—1附近出现的C的特征峰,说明HAP中也含有微量的C,类似于天然骨磷灰石组成。而曲线2在850cm—1及1500cm—1附近出现明显的C特征峰,说明CHA中C含量明显高于HAP。特别是1 500 cm—1附近的双峰,是C碳酸根进入磷灰石结构的重要标志。由此可见,此次合成的是具有典型羟基磷灰石结构的碳酸羟基磷灰石。

图 2 CHA/[BMIM]]PPFF6/SDBS/Nafi on SPCE的表面形态电镜图Fig.2 SEM image of surface morphology of CHA/[BMIM]PF6/SDBS/ Nafi on SPCE
对CHA/[BMIM]PF6/SDBS/Nafi on SPCE表面用扫描电镜进行表征,如图2所示。CHA均匀地分散于SPCE表面呈现一种多微孔结构,有利于Pb2+的吸附。[BMIM]PF6与CHA均匀混合,充盈于各微孔之间,有利于电子的传递。Nafi on膜覆于外层,既起阳离子传输信号放大作用,又对其余2 种修饰物起保护作用,使之不易掉落。
2.2 Pb2+在传感器上的电化学行为

图 3 Pb 3 Pb2+在修饰前后的SPCE上的方波溶出伏安曲线Fig.3 Square wave voltammograms of lead at unmodifi ed and modifi ed SPCE

图 4 Pb 4 Pb2+在不同修饰电极上的循环伏安曲线Fig.4 Cyclic voltammograms of lead at differently modifi ed SPCEs
由图4可知,3 种修饰电极对铅响应的循环伏安曲线的氧化峰和还原峰均在—0.7~—0.8 V附近。其中,当溶液中无Pb2+时(曲线1),循环伏安曲线不出峰。裸电极(曲线2),CHA/SDBS SPCE(曲线3),CHA/SDBS/ [BMIm]PF6SPCE(曲线4),CHA/SDBS/[BMIm]PF6/ Nafi on SPCE(曲线5)对Pb2+的电流峰依次增大,并且曲线3和曲线2的电流峰差距显著,说明CHA对Pb2+的富集作用是信号放大的关键。离子液体和Nafi on膜对响应信号也有一定的放大作用。
HAP吸附Pb2+的原理是Pb2+与HAP的≡POH位点络合,使HAP中的Ca2+溶解[25]。此时,在Ca2+的位置会产生吸引力,从而从溶液中吸附更多的Pb2+。
2.3 条件优化
为了使修饰电极对Pb2+的响应最佳,分别对电解质溶液类型、电解质溶液pH值、CHA质量浓度、富集时间进行了优化。
2.3.1 电解质溶液的选择
使用修饰电极分别在0.1 mol/L的HAc-NaAc、NH4Ac、KNO3、NaH2PO4-Na2HPO4溶液中对Pb2+进行测定,得出在HAc-NaAc溶液中Pb2+的响应信号最大。因此选用0.1 mol/L的HAc-NaAc溶液作为电解质溶液。
2.3.2 电解质溶液pH值

图 5 pH值对峰电流的影响Fig.5 Effect of pH on the peak current
将100 μg/L Pb2+在0.1 mol/L HAc-NaAc电解质溶液中进行测定,电极修饰物CHA质量浓度为2 mg/mL,富集时间为210 s。由图5可见:在pH 3.0~5.0时,峰电流呈增大趋势;在pH 5.0时,峰电流达到最大。可能是因为在pH值小于5.0时,由于溶液中H+浓度较高,占据Pb2+的结合位点,从而使之固定Pb2+能力较低。当pH值大于5.0时,溶液的pH值开始不利于Ca2+的溶出,使得对Pb2+的吸附能力下降。因此,选择pH 5.0为最佳的电解质溶液pH值。
2.3.3 CHA质量浓度

图 6 CHA质量浓度对峰电流的影响Fig.6 Infl uence of CHA concentrations on the peak current
将200 μg/L Pb2+在0.1 mol/L pH 5.0的HAc-NaAc电解质溶液中进行测定,富集时间为210 s。由图6可见,当CHA质量浓度在1~5 mg/mL时,峰电流呈上升趋势,因为随着CHA质量浓度的增加,吸附Pb2+的量也随之增加。当CHA质量浓度大于5 mg/mL后,峰电流开始下降,可能是因为修饰量过大而导致电极导电性减弱。因此,选择5 mg/mL作为最佳的CHA浓度。
2.3.4 富集时间
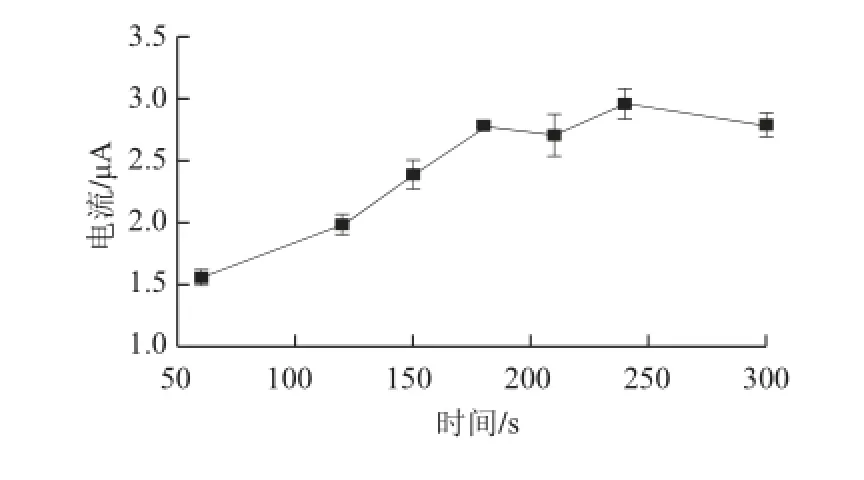
图 7 富集时间对峰电流的影响Fig.7 Effect of deposition time on the peak current
将100 μg/L Pb2+在0.1 mol/L pH 5.0的HAc-NaAc电解质溶液中进行测定,电极修饰物CHA浓度为5 mg/mL。由图7可见,电流峰在60~180 s呈明显的上升趋势,当富集时间超过180 s后,峰电流变化趋于平缓。可能是因为当富集时间超过180 s后,电极表面已经达到饱和,峰电流变化较小。因此,选择180 s为最佳富集时间。
2.4 工作曲线
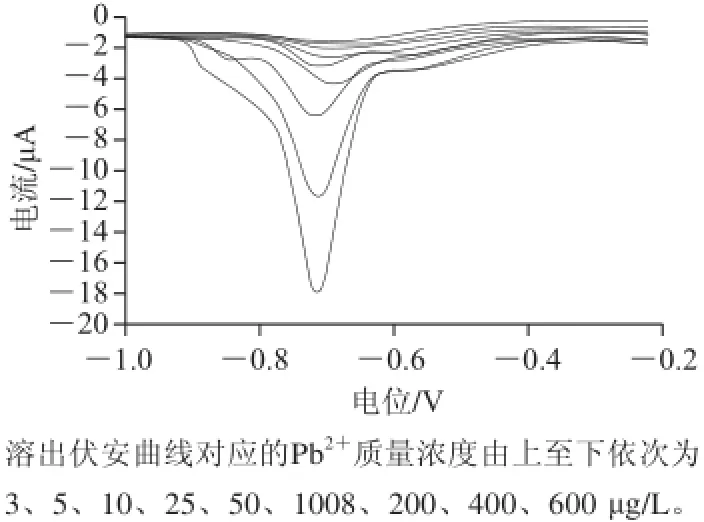
图 8 不同质量浓度Pb2+的溶出伏安图(3~600 μg/L)Fig.8 Striping voltammograms for different concentrations of Pb2+(3-600 μg/L)

图 9 优化条件下Pb2+的标准曲线Fig.9 Standard curves of lead under the optimized conditions
由图8和图9可知,溶出峰电流与Pb2+质量浓度在3~600 μg/L范围内呈现良好的线性关系。线性回归方程为y=0.025 69x+0.555 66(R2=0.996),其中y代表峰电流强度/μA;x代表Pb2+质量浓度(μg/L),检出限为0.37 μg/L(RSN=3)。用裸电极和修饰电极分别对100 μg/L Pb2+连续进行8 次平行测定,得到相对标准偏差分别为42.19%和3.4%。说明此电极具有良好的灵敏度和稳定性。此外,图8中不同质量浓度的Pb2+特征电化学峰位置有微小的差异,这可能是由于SPCE是一次性电极,不同SPCE之间存在微小的个体差异,使特征电化学峰位置有微小的差异。
2.5 茶叶样品检测

表 1 CHA/[BMIM]PF6/SDBS/Nafifi on SPCE和ICP-MS检测茶叶样品中Pb2+含量比较Table 1 Comparison of CHA/[BMIM]PF6/SDBS/Nafifi on SPCE and ICP-MS for determination of Pb2+in tea samples
用方波溶出伏安法和ICP-MS法对茶叶样品中的Pb2+含量进行检测,并将2种方法的检测结果进行比较。由表1可见:本法与ICP-MS的测定结果相近,且5 份茶叶样品的Pb2+含量均符合国家标准(国家标准规定茶叶中Pb2+含量不超过5 mg/kg[26])。对检测结果进行t检验,自由度(n—1)为2,α=0.05,查表得临界值为4.303,经过t检验发现,本法与ICP-MS的检测结果并无明显差别。由表1还可知,相对标准偏差不超过10%,可见本法对茶叶中铅的检测不仅具有良好的准确性,还具有良好的稳定性。
为了解样品中其他物质对Pb2+响应信号的影响,随机选取了样品2和样品5进行了回收率测定实验,结果如表2所示。样品2和样品5的回收率均较好。因此,此法在实际样品分析中也具有较好的表现。

表 2 回收率实验结果Table 2 Results of recovery tests
3 结 论
本研究将CHA分散于SDBS中,并且结合离子液体和Nafion,制成一种三重增敏的痕量Pb2+电化学传感器,与未修饰电极相比在敏感性、准确性和稳定性方面有明显提升。优化检测条件后测得Pb2+质量浓度在3~600 μg/L范围内与峰电流呈现良好的线性,检出限为0.37 μg/L(RSN=3),对100 μg/L Pb2+连续测定的相对标准偏差为3.4%(n=8),且适用于茶叶样品的检测。
综上所述,CHA/[BMIM]PF6/SDBS/Nafion SPCE是一种敏感、环保、准确、稳定的新型Pb2+电化学传感器。
[1] LIU Jinling, WU Hao, FENG Jianxiang, et al. Heavy metal contamination and ecological risk assessments in the sediments and zoobenthos of selected mangrove ecosystems, South China[J]. Catena, 2014, 119: 136-142.
[2] WYLLY R G N, JOSE P C. Protective effect of curcumin against heavy metals-induced liver damage[J]. Food and Chemical Toxicology, 2014, 69: 182-201.
[3] ZHAO Qihong, HUANG Ying, CAO Ye, et al. Potential health risks of heavy metals in cultivated topsoil and grain, including correlations with human primary liver, lung and gastric cancer, in Anhui province, Eastern China[J]. Science of the Total Environment, 2014, 470-471: 340-347.
[4] FRANCE W, JEAN M T. Handbook of clinical neurology[M]. Elsevier Besloten Vennootschap, 2014: 851-864.
[5] de RAFAEL A S, CEPHORA M S, GUSTAVO L P P, et al. Lead biomonitoring in different organs of lead intoxicated rats employing GF AAS and different sample preparations[J]. Talanta, 2013, 104: 90-96.
[6] 田久英, 卢菊生, 吴宏. 阻抑过氧化氢氧化偶氮胂&褪色动力学光度法测定痕量铅和镉[J]. 冶金分析, 2008, 28(3): 64-67.
[7] 罗雯, 马金晶, 张龙旺, 等. 微波消解-ICP-MS测定傣药嘎哩啰树皮中的11 种无机元素[J]. 光谱学与光谱分析, 2012, 32(9): 2562-2565.
[8] ALFREDO S, SONIA M Z, ISABEL S, et al. Development of screen-printed carbon electrodes modified with functionalized mesoporous silica nanoparticles: application to voltammetric stripping determination of Pb(Ⅱ) in non-pretreated natural waters[J]. Electrochimica Acta, 2010, 55: 6983-6990.
[9] ALI A E, T KHAYAMIAN, SHOKOOH S K. Application of adsorptive cathodic differential pulse stripping method for simultaneous determination of copper and molybdenum using pyrogallol red[J]. Analytica Chimica Acta, 2004, 505(2): 201-207.
[10] CÉSAR R T T, VIVIAN S S, BRUNO E L B, et al. Simultaneous determination of zinc, cadmium and lead in environmental watersamples by potentiometric stripping analysis (PSA) using multiwalled carbon nanotube electrode[J]. Journal of Hazardous Materials, 2009, 169(1/2/3): 256-262.
[11] 许春萱, 吴志伟, 曹凤枝, 等. 羧基化石墨烯修饰玻碳电极测定水样中的痕量铅和镉[J]. 冶金分析, 2010, 30(8): 30-34.
[12] MHAMMEDIA M, ACHAK M, NAJIH R, et al. Microextraction and trace determination of cadmium by square wave voltammetry at the carbon paste electrode impregnated with Ca10(PO4)6(OH)2[J]. Materials Chemistry and Physics, 2009, 115: 567-571.
[13] 刘羽, 胥焕岩. 磷块岩对二价镉离子的吸附性能研究[J]. 矿物学报, 2001(3): 406-408.
[14] ELENA M, ALEXANDRE M R, ANDEA M C. Studies on the mechanisms of lead immobilization by hydroxyapatite[J]. Environmental Science and Technology, 2002, 36: 1625-1629.
[15] 张爱娟, 王卫伟, 李成峰. 不同条件下碳酸羟基磷灰石的合成及吸附性能研究[J]. 硅酸盐通报, 2012, 31(6): 1371-1375.
[16] OPALLO M, LESNIEWSKI A. A review on electrodes modified with ionic liquids[J]. Journal of Electroanalytical Chemistry, 2011, 656(1/2): 2-16.
[17] LI Yonghong, LIU Xiaoying, ZENG Xiandong, et al. Simultaneous determination of ultra-trace lead and cadmium at a hydroxyapatitemodified carbon ionicliquidelectrode by square-wave stripping voltammetry[J]. Sensors and Actuators B, 2009, 139(2): 604-610.
[18] LIN Zhenyu, CHEN Xiaoping, CHEN Hongqin, et al. Electrochemiluminescent behavior of N6-isopentenyl-adenine/ Ru(bpy)system on an electrically heated ionic liquid/carbon paste electrode[J]. Electrochemistry Communications, 2009, 11(10): 2056-2059.
[19] WARDAK C. Ionic liquids as new lipophilic additives to the membrane of leadionselective electrodes with solid contact[J]. International Journal of Environmental and Analytical Chemistry, 2009, 89(8): 735-748.
[20] PAN Dawei, WANG Yuane, CHEN Zhaopeng. Nanomaterial/ ionophore-based electrode for anodic stripping voltammetric determination of lead: an electrochemical sensing platform toward heavy metals[J]. Analytical Chemistry, 2009, 81(12): 5088-5094.
[21] PAGE K A, CABLE K M, MOORE R B. Molecular origins of the thermal transitionsand dynamic mechanical relaxations in perfluoro sulfonate ionomers[J]. Macromolecules, 2005, 38(15): 6472-6484.
[22] IJERI V, CAPPELLETTO L, BIANCO S, et al. Nafion and carbon nanotube nanocomposites for mixed proton and electron conduction[J]. Journal of Membrane Science, 2010, 363(1/2): 265-270.
[23] XU Maotian, WU Yihui, WANG Jianxiu. Electrochemistry of and redox-induced metal release from metallothioneins at a nafion-coated bismuth film electrod[J]. Electroanalysis, 2006, 18(21): 2099-2105.
[24] 周学忠, 谢华林. ICP-MS法测定西洋参中的微量元素[J]. 食品科学, 2013, 34(10): 207-210.
[25] BAILLEZ S, NZIHOU A, BERNACHE A D. Removal of aqueous lead ions by hydroxyapatites: equilibria and kinetic processes[J]. Journal of Hazardous Materal, 2007, 139(39): 443-446.
[26] 农业部. NY 5244—2004 无公害食品: 茶叶[S].
Development of Environmental-Friendly and Multiple Sensitive Electrochemical Sensor for the Detection of Trace Lead
HE Weidong, DOU Wenchao, ZHAO Guangying*
(Key Laboratory of Food Safety of Zhejiang Province, College of Food Science and Biotechnology Engineering, Zhejiang Gongshang University, Hangzhou 310000, China)
This study aimed to improve the sensitivity, stability, accuracy and safety of the electrochemical sensor for lead (Pb2+). The screen-printed carbon electrode (SPCE) was modified with carbonated hydroxyapatite to accumulate Pb2+efficiently, ionic liquid [BMIM]PF6to improve electrical conductivity, and Nafion membrane to increase the sensitivity and stability. Thus, we established an environmental-friendly and multiple sensitive electrochemical sensor for rapid determination of trace lead. Under optimized experimental conditions, the signal peaks of square-wave stripping voltammetry had a linear relationship with Pb2+concentrations in the range from 3 to 600 μg/L, with a detection limit of 0.37 μg/L (RSN= 3). The relative standard deviation (RSD) of the sensor was 3.4% (n = 8). The results determined by this method were similar to those determined by ICP-MS. The electrochemical sensor developed in this study proved environmental-friendly, sensitive, accurate, economic and convenient.
carbonated hydroxyapatite (CHA); elecrtrochemical sensor; lead; tea
TS272.7;O657.1
A
1002-6630(2015)02-0168-06
10.7506/spkx1002-6630-201502032
2014-04-28
国家自然科学基金面上项目(30571623)
何卫东(1989—),男,硕士研究生,研究方向为重金属电化学传感器改进研究。E-mail:zhaogy-user@163.com
*通信作者:赵广英(1960—),女,教授,硕士,研究方向为食品质量与安全快速检测技术研究。E-mail:zhaogy-user@163.com
