甘精胰岛素联合吡格列酮治疗磺脲类继发失效2型糖尿病疗效观察
2015-12-05李翔
李 翔
甘精胰岛素联合吡格列酮治疗磺脲类继发失效2型糖尿病疗效观察
李 翔①
目的:探讨甘精胰岛素联合吡格列酮治疗磺脲类继发性失效的2型糖尿病的疗效。方法:60例患者随机数字表法分为A组和B组各30例;A组给予甘精胰岛素联合吡格列酮治疗,B组给予门冬胰岛素30R皮下注射,两组均治疗12周。测定治疗前后空腹血糖(FBG)、餐后2 h血糖(2 h PG)、糖化血红蛋白(HbA1c)、空腹C肽(FCP)、餐后2 h C肽(2 h CP)及低血糖发生率。结果:治疗12周后,两组FBG、2 h PG和HbA1c均明显下降,FCP和2hCP均明显升高,与治疗前比较差异有统计学意义(P<O.05),但组间比较差异无统计学意义。A组发生低血糖1例(3.3%),B组发生7例(23.3%),两组比较差异有统计学意义(P<O.05)。结论:甘精胰岛素联合吡格列酮治疗磺脲类继发性失效的2型糖尿病有较好疗效,治疗方便且易于掌握。
甘精胰岛素; 吡格列酮; 磺脲类继发性失效; 2型糖尿病
磺脲类药物继发性失效(SFS)是2型糖尿病(T2DM)患者治疗中常见问题,胰岛素强化治疗是对SFS糖尿病患者的主要治疗措施[1],但部分患者拒绝每天多次胰岛素注射的强化治疗方法。为寻找方便、有效的恢复部分胰岛B细胞功能的治疗方案,笔者采取了每日睡前皮下注射甘精胰岛素联合餐时口服吡格列酮方案,治疗门诊SFS T2DM患者,现报告如下。
1 资料与方法
1.1 一般资料 选择2011年9月-2013年9月本院2型糖尿病患者60例,男33例,女27例,平均年龄(57.2±14.3)岁,病程2~15年。符合1999年WHO诊断标准,已服用足量磺脲类药物持续≥3个月,空腹血糖(FBG)≥8.0 mmol/L,餐后血糖(2 h PG)≥14 mmol/L,糖化血红蛋白(HbA1c)≥8.0%且均未使用过胰岛素治疗的患者,除外饮食、应激,可能服用皮质激素类药物,严重肝、肾功能损害,心血管疾病及DKA,高渗性昏迷等急性并发症因素影响。60例患者随机数字表法分为A组和B组各30例,两组患者性别、年龄、体重指数等方面比较,差异无统计学意义(P>O.05),具有可比性。见表1。
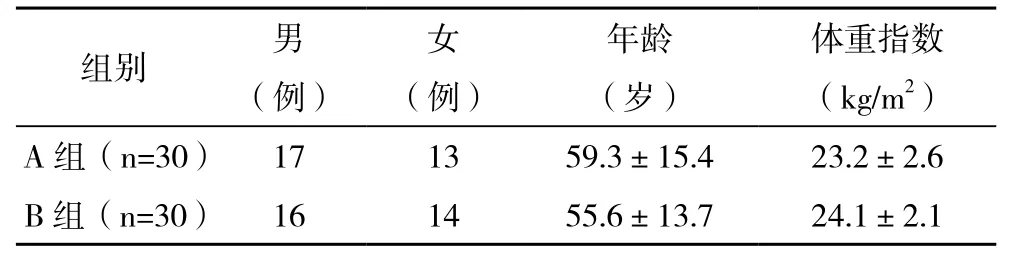
表1 两组患者一般资料比较
1.2 方法 研究对象均行糖尿病教育,饮食和运动治疗。两组均停用原口服降糖药物,伴高血压和(或)高血脂者继续应用降压和(或)降脂药物。A组每日清晨口服服吡格列酮15~30 mg,睡前注射甘精胰岛素,起始剂量0.2 U/(kg·d)。B组改为早、晚餐前皮下注射门冬胰岛素30R,起始剂量0.3 U/(kg·d)。根据血糖值调整胰岛素用量,控制目标为FBG 4.5~6.5 mmol/L,2hPG 5.0~8.0 mmol/L,若没有达标,每2~3天增加胰岛素剂量2 U;若出现低血糖,则减少胰岛素剂量2~6 U。分别于第2、4、8、12周复诊。治疗前和第12周测空腹血糖(FBG)、餐后2 h血糖(2 h PG)、糖化血红蛋白(HbA1c)、空腹C肽(FCP)、餐后2hC肽(2 h CP)。有典型低血糖症或血糖小于3 mmol/L定义为低血糖。
1.3 统计学处理 使用PEMS 3.1统计学软件进行分析,计量资料用(±s)表示,组间比较采用t检验,计数资料以率(%)表示,组间比较用 χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 两组患者FBG、2 h PG、HbA1c、FCP和2 h CP改善情况比较 治疗12周后,A组和B组FBG、2hPG、HbA1c均明显下降,FCP和2 h CP均明显升高,比较差异有统计学意义(P<0.05);但治疗后组间比较,差异无统计学意义。见表2。
表2 两组患者FBG、2 h PG、HbA1c、FCP和2 h CP改善情况比较(±s)

表2 两组患者FBG、2 h PG、HbA1c、FCP和2 h CP改善情况比较(±s)
*与治疗前比较,P<0.05
组别FBG(mmol/L)2 h PG(mmol/L)HbA1c(%)FCP(ng/mL)2 h CP(ng/mL)A组(n=30)治疗前12.70±2.5217.83±4.1410.52±2.211.30±0.632.41±1.25治疗后 6.01±1.46*7.93±1.53*6.48±2.42*1.61±0.52*5.53±1.73*A组(n=30)治疗前12.53±2.7118.49±3.8710.21±2.191.34±0.572.46±1.27治疗后 6.21±1.34*7.76±1.41*6.31±2.64*1.65±0.59*5.41±1.81*
2.2 不良反应 A组发生低血糖反应1例(3.3%),B组发生7例(23.3%),两组比较差异有统计学意义(P<0.05)。两组患者观察期间均未出现肝肾功能下降,低血糖昏迷等严重药物不良反应。
3 讨论
磺脲类继发性失效是2型糖尿病治疗中常见问题,每年发生率为5%~10%,连续5年后可达40%~50%[2]。其机制尚不明确,可能是磺脲类降糖药物(SU)主要作用于B细胞上的SU受体,促进胰岛素的释放。若长期大量使用SU,可引起胰岛B细胞上SU受体数量减少和亲和力下降,对SU的敏感性也降低,且长期慢性的高胰岛素血症,使胰岛B细胞长期过度负荷而逐渐衰竭。也有人认为是长期过量使用磺脲类药物,引起内质网应激和B细胞凋亡,导致胰岛细胞处于疲劳状态,引起胰岛细胞敏感性下降,出现胰岛素抵抗及胰岛细胞分泌下降,从而导致磺脲类药物继发性治疗失效[3]。磺脲类药物控制血糖是以牺牲胰岛功能为代价的,胰岛素的强化治疗能消除高血糖毒性作用,使胰岛细胞得到充分休息,胰岛素抵抗也得到相应改善。
门冬胰岛素30是一种双时相胰岛素类似物,它含有30%可溶性门冬氨酸胰岛素可以满足餐时胰岛素需求;而其余70%精蛋白结晶门冬氨酸胰岛素可以满足基础胰岛素需求。每天注射两次控制空腹及餐后血糖,具有明显的作用高峰,易出现夜间低血糖等不足,从而影响血糖平稳控制和长期达标[4]。
糖尿病治疗的血糖控制目标是在不发生低血糖的前提下,使HbAlc、FBG和2 h PG尽可能接近正常[5]。本实验结果显示,两种治疗方案均能较理想的控制血糖,使HbAlc达标。但A组FBG、2 h PG及HbAlc的控制效果均更为优越,而且低血糖发生率更低。因为甘精胰岛素是长效胰岛素类似物,它能模拟生理性基础胰岛素分泌,补充基础胰岛素,可控制空腹和两餐之间的血糖,皮下注射后形成微沉淀,持续稳定地释放胰岛素单体,无峰值作用[6-7]。每天只需注射1次,注射时间与进餐无相关性。陈莉等[8]研究表明,甘精胰岛素和门冬胰岛素均能有效降低血糖和糖化血红蛋白,但血糖达标时甘精胰岛素用量少于门冬30胰岛素(P<0.05)。同时门冬胰岛素30可能增加受试者发生夜间低血糖的风险[9]。本研究结果表明,治疗后治疗组低血糖事件发生率明显低于对照组,说明在相同血糖水平控制条件下,甘精胰岛素能更持久且平稳的降低血糖,能够控制夜间高血糖和黎明现象而不增加夜间低血糖的危险性,且减少了胰岛素注射次数,患者满意度也更高[10-12]。
本研究结果显示,联合用药组能更好地控制血糖且低血糖发生率低,也与应用吡格列酮治疗有关,吡格列酮通过激活脂肪、骨骼肌、肝细胞内过氧化物酶增殖活化受体γ(PPAR-γ),PPAR-γ被激活后诱导脂肪生成酶和与糖代谢调节相关蛋白的表达,促进脂肪细胞和其他细胞的分化,提高靶细胞对胰岛素的反应,从而改善胰岛素敏感性,减轻胰岛素抵抗,保护残存的胰岛β细胞功能[13-14],使HbA1c下降1%~1.5%。随着骨骼肌对胰岛素敏感性的增加而使葡萄糖摄取增多,故餐后血糖明显下降;而在肝脏可增加胰岛素对肝糖输出的抑制作用而降低空腹血糖,改善肝脏和外周组织的胰岛素抵抗,而不增加胰岛素分泌[15]。所以,加用吡格列酮治疗后胰岛素用量明显减少,使2型糖尿病患者胰岛β细胞负荷减轻,功能得到部分改善。
本研究所采用“一次服药,一次注射”的治疗方案,每天早晨服用吡格列酮片,睡前注射1次胰岛素,结果有显著疗效。血糖和HbA1c明显降低,β细胞功能得到恢复,故对于磺脲类继发性失效2型糖尿病患者选用甘精胰岛素加吡格列酮联合治疗优于预混胰岛素治疗,且治疗方式简单、方便,易于掌握,患者依从性更好。
[1]曾龙驿,穆攀伟,张国超,等.加用甘精胰岛素或中效胰岛素的2型糖尿病患者血糖波动的比较[J].中华内分泌代谢杂志,2009,16(25):39-41.
[2]王毅飞,伊娜,张松,等.胰岛素加罗列酮治疗血糖控制不良的2型糖尿病患者疗效观察[J].中国实用内科杂志,2004,24(7):434.
[3] Qian L, Zhang S, Xu L, et al. Endoplasmic reticulum Stress in beta cells: latent mechanism of secondary sulfonylurea failure in type 2 diabetes[J]. Med Hypotheses,2008,71(6):889-891.
[4]俞海燕,郭晓珍,孙军卫,等.甘精胰岛素联合罗格列酮在2型糖尿病初始胰岛素治疗中的疗效观察[J].临床内科杂志,2009,15(2):419-420.
[5]徐迎侠,刘洪英.甘精胰岛素联合口服降糖药物对血糖控制不佳的2型糖尿病患者的疗效观察[J].国际内分泌代谢杂志,2011,12(31):155-156.
[6]中华医学会糖尿病学分会.2007年版中国2型糖尿病防治指南[J].中华内分泌代谢杂志,2008,24(增录Za):1-2a-23.
[7]吕朝辉,潘长玉,陈家伦,等.甘精胰岛素与格列美脲联合应用治疗口服降糖药控制不佳2型糖尿病的有效性和安全性[J].中华内分泌代谢杂志,2009,16(25):617-621.
[8]陈莉,韩萍.甘精胰岛素和门冬胰岛素30治疗2型糖尿病的疗效比较[J].实用药物与临床,2011,14(4):344-345.
[9] Strojek K, Bebakar W M, Khutsoane D T, el al. Once-daily initiation with biphasic insulin as part 30 versus insulin glargine in patients with type 2 diabetes inadequately controlled with oral drugs: an openlabel, multinational RCT[J]. Curr Med Res Opin,2009,25(12):2887-2894.
[10]聂晓亚,盂晓军.初诊2型糖尿病应用甘精胰岛素与门冬胰岛素30治疗的临床观察[J].中国实用医药,2010,5(24):161-162.
[11] Nathan D M, Buse J B, Davidson M B, et al. Medical managementof hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy[J]. Diabetes Care,2009,34(32):193-203.
[12] Davies M, Lavalle-Gonzalez F, Storms F, et al. Initiation of insulin glargine therapy in type 2 diabetes subjects suboptimally controlled on oralantidiabetic agents:results from the AT. LANTUS trial[J]. Diabetes Obes Metab,2008,80(10):387-399.
[13] Kipnes M S, Krosnick A, Rendell M S, et al. Piog-litazone hydrochloride in combination with type 2 diabetes mellitus:arandomized, placebo-controlled study[J]. Am J Med,2009,91(111):10-17.
[14]司广新,卢学勉.2型糖尿病患者噻唑烷二酮类药物疗效差异性分析[J].国际内分泌代谢杂志,2013,51(2):89.
[15]刘英敏.吡格列酮的临床合理应用与再评价[J].实用糖尿病杂志,2009,6(2):20-21.
The Effect of Glargine Combined with Pioglitazone in the Treatment of Secondary Failure of Sulfonylurea in Type 2 Diabetes
LI Xiang.//Medical Innovation of China,2015,12(01):057-060
Objective: To explore the effect of insulin glarage combined with pioglitazone in the treatment of type 2 diabetes. Method: 60 cases were randomly divided into group A and group B, 30 cases in each group. Group A was treated with insulin glargine combined with pioglitazone, while group B was given subcutaneous injection of insulin aspart 30R. Both groups were treated for 12 weeks. To compare the fasting plasma glucose (FBG), 2-hour postprandial plasma glucose (2 h PG), glycosylated hemeglobi (HbA1c), fasting C-peptide (FCP), 2-hour postprandial C-peptide (2 h CP)and incidence of low blood glucose before and after treatment. Result:After treatment for 12 weeks, the FBG, 2hPG and HbA1c of the two groups remarkably decreased, but the FCP and 2 h CP of the two groups significantly increased, andthe differences were statistically significant (P<O.05). But there were no statistical significant between the two groups(P>0.05). The low blood glucose reaction was noticed in 1 case (3.3%) in group A, but 7 cases (23.3%)in group B,and the differences were statistically significant (P<O.05). Conclusion: Treating secondary failure of sulfonylurea in type 2 diabetes with insulin glargine combined with pioglitazone has good effect, and the method is simple, convenient and easy to master, which is worth clinical popularizing and application.
Insulin glargine; Pioglitazone; Secondary failure of sulfonylurea; Type 2 diabetes
10.3969/j.issn.1674-4985.2015.01.020
2014-06-23) (本文编辑:王宇)
①辽宁省大连市第五人民医院 辽宁 大连 116021
李翔
First-author’s address: The Fifth People’s Hospital of Dalian City, Dalian 116021, China
