右美托咪定复合罗哌卡因骶管麻醉在小儿手术中的应用
2015-12-02邹振宇杨小霖李兰洋任江宋仕钦
邹振宇,杨小霖,李兰洋,任江,宋仕钦
(1攀枝花市第二人民医院,四川 攀枝花 617023;2川北医学院附属医院)
术后疼痛是手术创伤引起的主观不愉快的感觉和情绪体验,小儿虽能感受疼痛,但对疼痛表述不清,造成疼痛评估困难,术后往往因疼痛治疗不充分,带来日后痛觉异常。同时由于部分镇痛物在小儿中使用受到限制或对药物不良反应的过渡担心,小儿术后疼痛往往被忽视,从而给患儿带来痛苦并影响康复过程。在小儿下腹及下肢手术中,骶管麻醉是一种可供选择的简单、相对安全的麻醉技术,骶管麻醉可以减少静脉和吸入全麻药的应用,降低术中对手术创伤的应激反应,有利于术后患儿平稳复苏,并且能提供早期有效的术后镇痛。由于单次骶管阻滞局麻药作用时间有限,因此临床上常复合其他辅助药物以延长镇痛时间。2012年11月~2015年1月,我们将右美托咪定复合罗哌卡因应用于小儿手术中,取得良好效果。现将结果报告如下。
1 资料与方法
1.1 临床资料 选择攀枝花市第二人民医院收治的择期手术患儿60例,均为男性;年龄1~5岁,体质量10~20 kg,ASA分级Ⅰ~Ⅱ级。其中腹股沟疝36例,包皮环切20例,下肢外伤4例。排除标准:对所用药物有过敏史,凝血功能障碍,穿刺部位感染,发育不良,骨骼畸形,神经系统疾病。所有患儿随机分为观察组和对照组各30例。本实验经攀枝花市第二人民医院临床研究伦理委员会批准,并取得患者家属知情同意。
1.2 麻醉方法 所有患儿术前常规禁食禁饮,入手术室后采用多功能监护仪(Dash 4000,美国通用公司)监测心电图、SpO2、HR、BP、平均动脉压(MAP)。面罩吸入8%七氟烷,氧流量2 L/min,待患儿入睡后七氟烷调至3%,肌注阿托品0.01 mg/kg同时建立静脉通道,静注乳酸钠林格注射液10 mL/(kg·h),静脉注射芬太尼 2 μg/kg,维库溴铵0.1 mg/kg,气管插管后机械通气,监测呼气末二氧化碳。取左侧卧位下以23G头皮针行骶管穿刺阻滞,穿刺成功后随机注入对照组(0.25%罗哌卡因1 mL/kg+0.9%NS 1 mL)或观察组(0.25%罗哌卡因1 mL/kg+右美托咪定1 μg/kg,生理盐水稀释至1 mL)预先配好的药液。术中根据血压调整吸入七氟烷0.5% ~2.0%维持麻醉,使MAP下降不超过术前MAP的30%,手术结束缝合完皮肤同时停用七氟烷。患儿完全清醒后拔除气管导管送入PACU呼吸室内空气。
1.3 观察方法 MAP、HR:记录麻醉诱导前和骶管注药以后每 5 min的 MAP、HR、SpO2,直至送入PACU。在PACU由护理人员监测记录HR、MAP、SpO2,每30 min记录一次,直至术后6 h。若术中、术后MAP降低幅度≥基础值的30%时(定义为低血压),加快补液或给予麻黄碱0.2 mg/kg。若出现心动过缓≤60次/min者,静脉给予阿托品0.01~0.02 mg/kg。其他不良反应如恶心、呕吐、呼吸抑制(持续SpO2<95%,需要氧气吸入)、尿潴留等也被记录。镇痛评分、时间:术后患儿送入 PACU,由PACU护理人员采用儿童疼痛评价行为量表(FLACC)评分评价患儿镇痛效果,前6 h每30 min记录1次,随后1 h记录1次,直至骶管阻滞后24 h。若FLACC评分≥4分则认为患儿疼痛,给予芬太尼0.5 ~1.0 μg/kg,同时记录镇痛时间(从骶管阻滞至FLACC评分≥4分)。镇静评分:在术后30 min及1、2 h进行。1分:对刺激较迟钝或无反应;2分:睡眠,对移动或刺激有反应;3分:清醒,可安慰;4分:无法安慰的哭闹;5分:行为激烈需要约束限制。麻醉时间:从麻醉诱导开始到手术结束停七氟烷时间。苏醒时间:即手术结束到唤醒睁眼时间,苏醒延迟定义为手术结束后30 min患儿仍不能唤醒睁眼。
1.4 统计学方法 采用SPSS21.0统计软件。计量资料以±s表示,组间比较采用成组t检验。计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
两组不同时点MAP、HR水平比较见表1,由表1可知,两组不同时点MAP、HR水平比较P均>0.05。两组麻醉时间、苏醒时间、镇静评分、镇痛时间比较见表 2。观察组术后 2、4、6、8、12、16、20 h FLACC≥4 分者分别为 0、0、0、3、6、26、30 例,对照组分别为0、4、22、30、30、30、30 例,两组比较,P均<0.05。观察组术后发生恶心、呕吐1例,心动过缓3例;对照组发生恶心、呕吐3例,心动过缓0例;两组比较,P均 >0.05。
表1 两组麻醉诱导前、术中、术后MAP和HR水平比较( ±s)
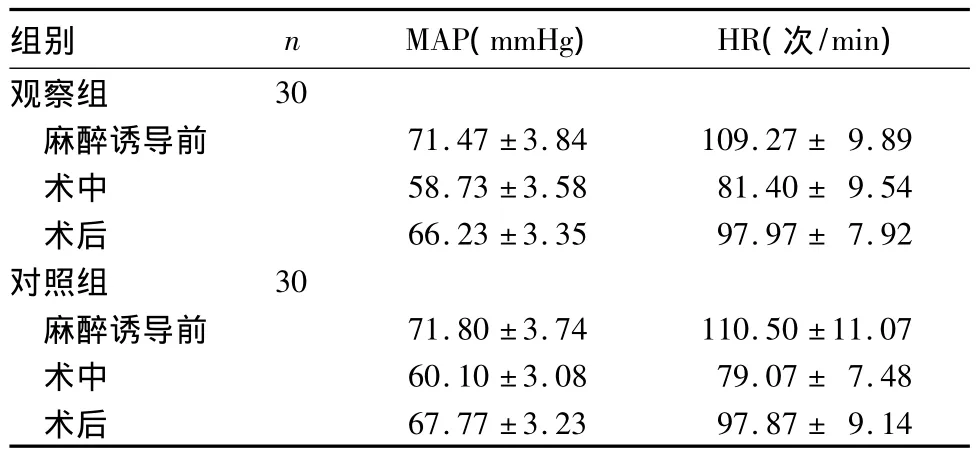
表1 两组麻醉诱导前、术中、术后MAP和HR水平比较( ±s)
组别 n MAP(mmHg) HR(次/min)观察组30麻醉诱导前 71.47 ±3.84 109.27 ± 9.89术中 58.73 ±3.58 81.40 ± 9.54术后 66.23 ±3.35 97.97 ± 7.92对照组 30麻醉诱导前 71.80 ±3.74 110.50 ±11.07术中 60.10 ±3.08 79.07 ± 7.48术后67.77 ±3.23 97.87 ± 9.14
3 讨论
当前,国内外用于椎管内镇痛的α2-肾上腺素能受体激动剂主要为可乐定。国外EI-Hennawy等[1]在小儿进行下腹部手术时将新型α2-肾上腺素能受体激动剂右美托咪定2 μg/kg混合0.25%布比卡因用于骶管麻醉及镇痛,发现右美托咪定能显著延长镇痛时间,且无心动过缓、低血压及呼吸抑制等不良反应;Kanazi等[2]发现,右美托咪定在蛛网膜下腔混合局麻药使用也能显著延长感觉、运动阻滞时间和镇痛时间;而且以上两个研究均未发现右美托咪定对脊髓神经有毒性损伤作用。与可乐定一样,右美托咪定在不增加不良反应发生率的情况下且能增加局麻药的药效;相对于可乐定来说,右美托咪定是高选择性的α2-肾上腺素能受体激动剂,这种高选择性能使其在较高剂量下具有镇静和镇痛效应,而较少导致心血管不良反应。另外,相对于阿片类镇痛剂,右美托咪定最大的优点就是对呼吸影响较小。
表2 两组麻醉时间、苏醒时间、镇静评分、镇痛时间比较( ± s)

表2 两组麻醉时间、苏醒时间、镇静评分、镇痛时间比较( ± s)
注:与对照组比较,*P <0.05。
组别 n 麻醉时间(min)苏醒时间(min)镇静评分(分)镇痛时间(h)观察组 30 69.67 ±5.49 12.27 ±2.88*2.11 ±0.48*14.23 ±3.07*对照组30 67.67 ±4.08 8.90 ±2.37 3.18 ±0.74 5.70 ±1.32
罗哌卡因属于长效酰胺类局麻药,麻醉效能与布比卡因相似,但相对于布比卡因安全范围更宽,其心血管和神经毒性更小,对运动神经阻滞没有布比卡因深,浓度适中时能产生运动神经阻滞与感觉神经阻滞分离,但两者镇痛时间相差不大,它能够安全的用于区域阻滞麻醉和小儿椎管内镇痛。
Anand等[3]发现,在小儿骶管阻滞麻醉中使用0.25%罗哌卡因复合右美托咪定2 μg/kg时,其镇痛持续时间(平均14.5 h)明显比单独应用0.25%罗哌卡因长(平均5.5 h),且患儿血流动力学稳定,无明显不良反应发生。虽然 EI-Hennawy等[1]和Anand等[3]所作的研究中没有发现右美托咪定(2 μg/kg)骶管应用会导致血流动力学明显改变,但临床正常剂量的右美托咪定使用时,最常见的不良反应就是可能导致低血压或心动过缓[4]。因此,本研究把右美托咪定剂量减少到1 μg/kg,发现同样能达到理想的镇痛效果,其镇痛时间比单独应用0.25%罗哌卡因明显延长,并且降低了因使用右美托咪定导致不良反应的潜在风险。本研究观察组有3例患儿出现心动过缓,虽经静脉使用阿托品0.02 mg/kg后迅速好转,但提示对于原本存在心动过缓的患者,椎管内应用右美托咪定时应谨慎。
全麻苏醒期躁动(EA)是麻醉苏醒期的行为混乱,常出现在麻醉后苏醒的早期阶段,主要表现为哭闹、兴奋、躁动和定向障碍[5]。EA在小儿七氟烷吸入麻醉后发生率较高,虽然在镇静、镇痛药物的应用下这种兴奋性行为的发生有所减少,但其仍然没有较好的预防及治疗方法。国外研究[6]显示,在小儿麻醉中α2-肾上腺素能受体激动剂可乐定不管是静脉还是骶管应用(3 μg/kg)均能预防EA发生,右美托咪定由于其镇静、镇痛特点也能够有效预防EA的发生[7~9]。本研究亦发现,观察组患儿苏醒时安静、合作,而与之相对应的对照组患儿苏醒时更多表现为躁动、不安,观察组术后镇静评分低于对照组,提示骶管给予右美托咪定能有效预防七氟烷麻醉后EA发生,且观察组患儿均处于轻度睡眠的镇静状态,容易被唤醒。
[1]El-Hennawy AM,Abd-Elwahb AM,Abd-Elmaksoud AM,et al.Addition of clonidine or dexmedetomidine to bupivacaine prolongs caudal analgesia in children[J].Br J Anaesth,2009,103(2):268-274.
[2]Kanazi GE,Aouad MT,Jabbour-Khoury SI,et al.Effect of lowdose dexmedetomidine or clonidine on the characteristics of bupivacaine spinal block[J].Acta Anaesthesiol Scand,2006,50(2):222-227.
[3]Anand VG,Kannan M,Thavamani A,et al.Effects of dexmedetomidine added to caudal ropivacaine in paediatric lower abdominal surgeries[J].Indian J Anaesth,2011,55(4):340-346.
[4]李志鹏,柳垂亮.右美托咪定的临床应用进展[J].实用医学杂志,2013,29(19):3254-3256.
[5]鲍杨,史东平,封卫征.全麻苏醒期患者躁动的研究进展[J].临床麻醉学杂志,2010,26(2):183-184.
[6]Bock M,Kunz P,Schreckenberger R,et al.Comparison of caudal and intravenous clonidine in the prevention of agitation after sevoflurane in children[J].Br J Anaesth,2002,88(6):790-796.
[7]Patel A,Davidson M,Tran MC,et al.Dexmedetomidine infusion for analgesia and prevention of emergence agitation in children with obstructive sleep apnea syndrome undergoing tonsillectomy and adenoidectomy[J].Anesth Analg,2010,111(4):1004-1010.
[8]Isik B,Arslan M,Tunga AD,et al.Dexmedetomidine decreases emergence agitation in pediatric patients after sevoflurane anesthesia without surgery[J].Paediatr Anaesth,2006,16(7):748-753.
[9]Saadawy I,Boker A,Elshahawy MA,et al.Effect of dexmedetomidine on the characteristics of bupivacaine in a caudal block in pediatrics[J].Acta Anaesthesiol Scand,2009,53(2):251-256.
